INTRODUCCIÓN
La detección de microdeleciones en el brazo largo del cromosoma Y ha supuesto un avance significativo en la comprensión de la infertilidad masculina.
En el ámbito mundial, el 15% de todas las parejas presenta infertilidad. El varón es responsable del 20-40% de estos casos y comparte la responsabilidad con la mujer en un 20-30% adicional. Por tanto, de manera aproximada, se podría afirmar que en el varón se encuentra la causa de la esterilidad de la pareja en un tercio de los casos como factor aislado y en otro tercio junto a un factor femenino también alterado.
Dentro del factor masculino resultan de gran interés las alteraciones de origen genético. En primer lugar, porque la prevalencia de estas alteraciones es muy elevada, sobre todo entre los casos de factor masculino severo. Además, en un elevado porcentaje de estos casos va a ser posible la descendencia recurriendo a procedimientos de fecundación in vitro-intra-cytoplasmatic sperm injection (FIV-ICSI), y se pueden transmitir a los hijos estas anomalías genéticas o condicionar el éxito de las técnicas de reproducción asistida.
El conocimiento de estas situaciones tiene, por tanto, un gran interés desde el punto de vista clínico, pronóstico e incluso legal. Las posibles anomalías que hay que destacar son numerosas, pero un resumen de las más importantes se pueden encontrar en la tabla 1, incluyendo las microdeleciones del cromosoma Y, que se tratarán a continuación de manera más detallada.
Muchas de las azoospermias u oligozoospermias severas, de carácter secretor, se deben a la presencia de microdeleciones en el brazo largo del cromosoma Y (Yq) que explicarían por sí mismas el 10-20% de estos cuadros. Una deleción es la pérdida de parte de un cromosoma. Si estas pérdidas afectan a genes independientes pero contiguos en el mismo cromosoma, y sólo son detectables por técnicas microgenéticas, se les denominan microdeleciones1.
CROMOSOMA Y
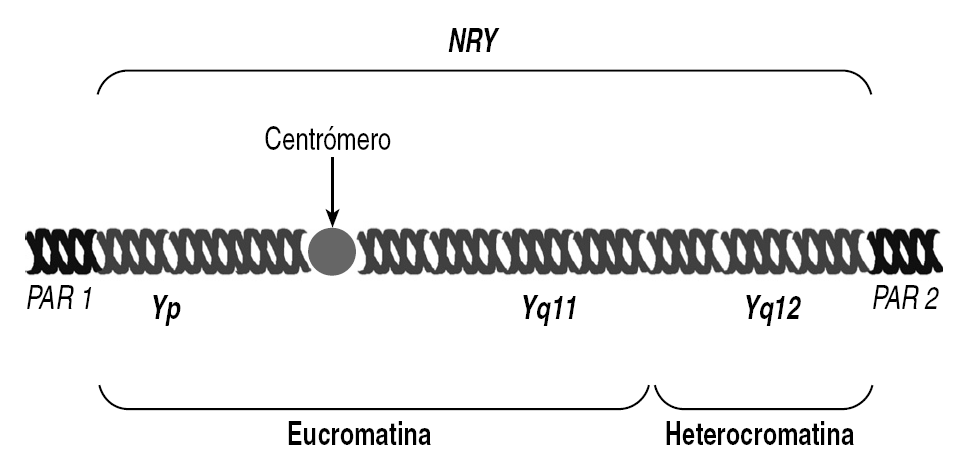
Este cromosoma no sólo es el principal determinante de la diferenciación sexual masculina, sino que contiene genes importantes para la producción de espermatozoides (espermatogénesis). El cromosoma Y es pequeño, muy repetitivo y tiene relativamente pocos genes (fig. 1). Sin embargo, hoy se sabe que los genes que se encuentran en él son de gran interés porque son responsables de funciones importantes. En total se han estudiado 78 genes, y la combinación de ellos produce 27 proteínas.
Figura 1. Organización genómica del cromosoma Y. Las microdeleciones que se asocian a esterilidad suelen encontrarse en el brazo largo del cromosoma Y, principalmente en la región Yq11. NRY: región no recombinante del cromosoma Y.
Los cromosomas sexuales X e Y están relativamente aislados entre sí, de manera que el 95% del cromosoma Y no se recombina con el X (la recombinación es el cambio de ADN que tiene lugar entre parejas de cromosomas). Desde que quedó aislado del X (que sigue intercambiando ADN con su homólogo X en las células femeninas) el cromosoma Y ha ido degenerando, acumulando mutaciones, lo que ha provocado, por una parte, la pérdida de gran parte de su material genético y, por otra, la adquisición de secuencias relativamente nuevas.
En la evolución, el cromosoma Y ha ido acumulando genes externos de fertilidad masculina. Estos genes se repiten muchas veces, lo que podría servir para evitar que se pierdan genes importantes debido a las mutaciones.
Pero estos genes están presentes en distintas cantidades y organizaciones en diferentes varones y esta variación significa que, por ejemplo, el mapa del cromosoma Y publicado, que se basa en un varón, puede no ser suficiente para explicar las anomalías funcionales dependientes de estos genes en la totalidad de los varones. Por tanto, aunque el hallazgo de la secuenciación completa y el mecanismo de reparación y duplicación del cromosoma sexual Y abre nuevas líneas de investigación para conocer por qué se produce la infertilidad masculina, será necesario todavía esperar unos años para que estos resultados repercutan en un tratamiento efectivo. Ahora, lo que se debe investigar es el mecanismo por el que se producen las proteínas, tanto las normales como las anormales, ya que estas últimas son una de las causantes de la infertilidad.
Se sospecha que entre un 10 y un 25% de los casos de infertilidad masculina podría deberse a defectos del cromosoma Y. Entre las anomalías que se encuentran en este cromosoma hay que destacar las microdeleciones del cromosoma Y. Este trastorno aparece por unos defectos en el gen que impiden que llegue la información necesaria para producir el espermatozoide en el testículo2.
MICRODELECIONES DEL CROMOSOMA Y
Las microdeleciones del cromosoma Y pueden ser responsables del 15% de las causas de azoospermias no obstructivas y del 6% de las oligozoospermias severas. Se localizan en el brazo largo del cromosoma Y (Yq11), en la denominada azoospermic zone factor (AZF). A través de técnicas de análisis molecular basadas en la reacción en cadena de la polimerasa (PCR) fue posible subdividir en el cromosoma Y 3 regiones: AZFa, AZFb y AZFc, así como una cuarta región denominada AZFd, localizada entre AZFb y AZFc. En cada una de ellas se presentan diferentes genes candidatos que intervienen en la esterilidad masculina:
AZFa: abarca 1 millón de pares de bases, sus genes presentan copias homólogas en el cromosoma X y su expresión es ubicua. Se ha identificado el gen DFFRY (Drosophila fat facets related Y) DBY (dead box polipeptid Y)
AZFb: 3 millones de pares de bases. Presencia principalmente del gen RBMY (RNA binding motif). Hay copias de RBMY repartidas a lo largo de todo el cromosoma Y.
AZFc: 1,4 millones de pares de bases. Se encuentra el gen DAZ (deleted in azoospermia) que tiene una copia en el brazo corto del cromosoma 3.
La región AZFc es la involucrada más frecuentemente en los casos de esterilidad, con más del 80% de casos referidos de microdeleción del cromosoma Y.
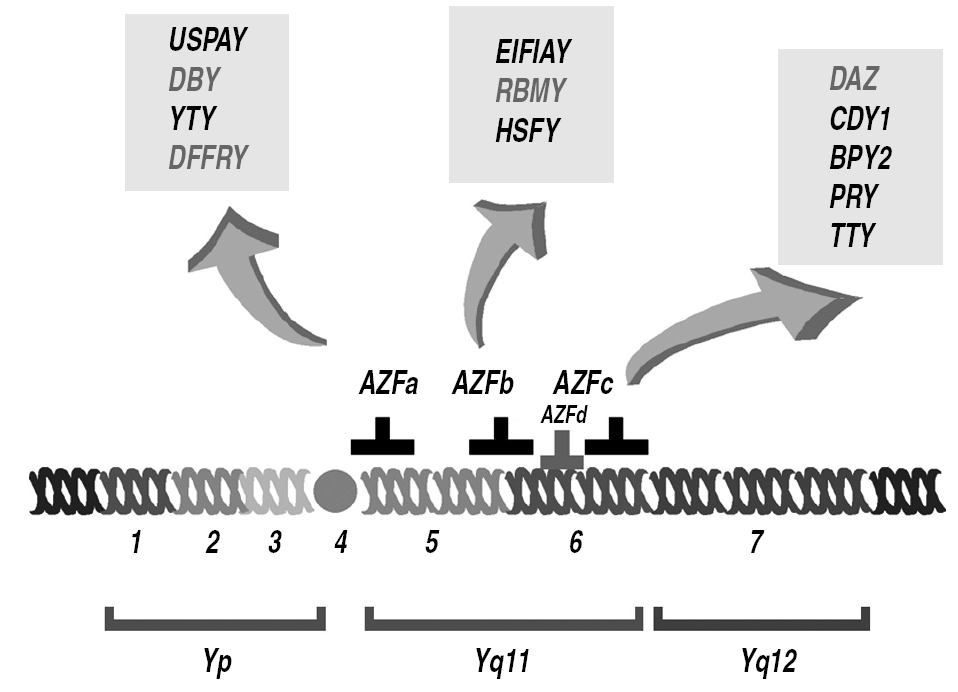
No hay una estrecha correlación entre el lugar de la deleción y el fenotipo histológico encontrado en la biopsia testicular. Sin embargo, la presencia de deleciones AZFa y AZFb proximales suele relacionarse con graves defectos en la espermatogénesis (síndrome de sólo células de Sertoli), mientras que las deleciones de AZFb distal y AZFc presentan diferentes grados de fallo en la espermatogénesis3,4. Esta relación que hay entre las formas histopatológicas y el tipo de deleción, que ha sido observada empíricamente, necesita de estudios más amplios para que se pueda sustentar científicamente (fig. 2).
Figura 2. Genes y regiones asociadas a esterilidad en el cromosoma Y. Se conocen diversas regiones del cromosoma Y que se asocian a esterilidad. Actualmente se está profundizando en el estudio de la funcionalidad de estas zonas para tratar de definirlas con cuadros clínicos e histopatológicos específicos.
CAUSA DE LAS MICRODELECIONES
La presencia de microdeleciones en el cromosoma Y pueden deberse a 2 situaciones diferentes. Por una parte es posible su aparición de novo en un sujeto porque el cromosoma Y es susceptible de pérdidas espontáneas por la presencia en él de una alta frecuencia de elementos repetitivos. También se han involucrado ciertos haplotipos en este cromosoma que podrían predisponer.
La segunda posibilidad es que la microdeleción se transmita a la descendencia, bien de forma espontánea donde la elevada edad del padre podría ser un factor predisponente, o bien tras un tratamiento por esterilidad. Por tanto, parece evidente la importancia del consejo genético en estos casos2,5.
INDICACIONES DE ESTUDIO DE MICRODELECIONES DEL CROMOSOMA Y
En principio estaría indicado el estudio en todos los casos de azoospermia idiopática u oligospermia severa (< 5 x 106 espermatozoides/ml). Sin embargo, no debería hacerse rutinariamente en los casos de infertilidad no idiopática. El problema es que estas 2 situaciones representarían los extremos y entre ellas hay un gran número de casos en los que las indicaciones no son tan evidentes. Se va a necesitar un gran número de estudios hasta poder especificar sin duda qué casos deben estudiarse y los que no serían necesarios. Los pacientes oligozoospérmicos severos con microdeleción del cromosoma Y son estériles, pero actualmente a través de la técnica de ICSI es posible que tengan descendencia. Incluso en muchos de los pacientes azoospérmicos con microdeleción de Yq es posible recuperar quirúrgicamente espermatozoides del testículo mediante TESA (testicular sperm aspiration) o TESE (testicular sperm extraction) con los que proceder a ICSI. No obstante, también se han aportado casos de transmisión natural de esa deleción de padre a hijo. La deleción completa y simultánea de las 3 regiones (AZFa, AZFb y AZFc) parece comportar un valor pronóstico negativo ya que en todos los casos se asocia a una ausencia total de espermatozoides. Todos los pacientes (100%) con una microdeleción tratados con éxito a través de ICSI transmiten la microdeleción y la esterilidad a su descendencia masculina, pero no a su descendencia femenina. Tampoco se debe menospreciar la posibilidad de transmisión de otras anomalías genéticas. Por tanto no habría que olvidar las siguientes premisas:
"El estudio de las microdeleciones del cromosoma Y está indicado en todos los casos de infertilidad masculina o al menos con alteraciones seminales graves."
"El conocimiento de la existencia de microdeleciones del cromosoma Y es obligatorio antes de tomar la decisión del ICSI."
Estos estudios deben, además, indicarse de forma temprana ante cierto grado de sospecha por la posibilidad de anticiparnos a la progresión hacia azoospermia en varones oligozoospérmicos, lo que permitiría plantear la criopreservación antes de que ello ocurra. Por otra parte, se podría hacer previsiones e, incluso, hacer una valoración de la expectativa de obtener espermatozoides en la biopsia testicular que en el caso de pacientes que presenten deleciones en AZFa y además se acompañen de alteraciones en otros parámetros, como el perfil hormonal, sería muy reducida4,6.
Los grandes avances en cirugía y las técnicas de reproducción asistida permiten aplicar tratamientos exitosos en casos de infertilidad masculina. Sin embargo, por cada uno de estos éxitos se aumenta el riesgo de aparición de anomalías genéticas en su descendencia. Por tanto, el prescindir del diagnóstico andrológico previo a FIV-ICSI podría hacernos incurrir en responsabilidad legal, puesto que no se estudian posibles problemas genéticos transmisibles ni factores capaces de reducir las posibilidades de éxito de las técnicas de reproducción asistida.
CONSEJO GENÉTICO
Siempre se debería tener 2 situaciones presentes: por una parte, un cuadro de azoospermia no obstructiva u oligospermia severa más la presencia de microdeleciones del cromosoma Y nos indicaría que el origen es genético y, por tanto, transmisible a la descendencia masculina; por otra, también sería importante indicar la criopreservación a los hijos afectados, dada la posibilidad del paso de oligospermia a azoospermia con el paso de los años7.
Correspondencia: Dr. R.A. González Fernández.
Servicio de Inmunología. Hospital Reina Sofía.
Avda. Menéndez Pidal, s/n. 14004 Córdoba. España.
Correo electrónico: Rafael.gonzalez.sspa@juntadeandalucia.es