¿ Introducción
Virus Influenza A H1N1
Este virus se identificó a principios de abril de 2009 y la Organización Mundial de la Salud (OMS) elevó la alerta de pandemia a nivel cinco. En mayo de 2009, el Centro de Control y Prevención de Enfermedades (CDC) en los Estados Unidos informó sobre complicaciones severas de Influenza A H1N1 en mujeres embarazadas, incluidos 20 casos confirmados y una muerte. Las mujeres embarazadas fueron más propensas a señalar disnea pero en general informaron síntomas similares a los de la población no embarazada, como fiebre, tos, dolor faríngeo, rinorrea, cefalea, mialgias, vómito y diarrea. La muerte ocurrió en una paciente, por lo demás sana, con 35 semanas de gestación e inicio abrupto de distrés respiratorio severo que requirió intubación. Se le practicó cesárea de urgencia, por presentar falla respiratoria y se inició tratamiento con oseltamivir, ocho días después de la presentación inicial.
Para el 16 de junio de 2009, había un total de 45 muertes registradas de complicaciones relacionadas con H1N1, de las que seis (13%), fueron mujeres embarazadas: una en el primer trimestre, una en el segundo trimestre y cuatro en el tercer trimestre. Con excepción de asma y obesidad, todas las mujeres eran sanas previo a la infección por influenza. Ninguna tuvo evidencia de neumonía bacteriana secundaria y cada una recibió tratamiento con oseltamivir, un antiviral inhibidor de neuraminidasa. Cinco de las seis mujeres tuvieron embarazos viables y se atendieron por cesárea, ninguno de los productos tuvo evidencia de infección por influenza.1,2
En México, de los 16 442 casos confirmados hasta el 31 de julio, la mayor parte se dio en Chiapas, Yucatán, Distrito Federal, Jalisco, Tabasco, Veracruz y Guerrero. De ellos, la mitad correspondió a hombres y 69.1% a mujeres en el grupo de 20 a 54 años de edad. En nuestro país, la sintomatología de los 146 pacientes fallecidos hasta finales de julio fue: fiebre en 84.9%, tos en 84.2%, insuficiencia respiratoria en 76%, expectoración en 53.4% y ataque al estado general en 47.9%.3,4 En nuestra institución, durante el periodo comprendido entre el 17 de abril y el 9 de junio de 2009, se atendieron 6780 pacientes con infección respiratoria aguda, de ellos, 127 pacientes se catalogaron como sospechosos de padecer influenza, de los que 67 fueron positivos a la prueba serológica rápida y 22 fueron confirmados mediante RT-PCR. Se internaron 55 de los 127 enfermos sospechosos. La evolución fue satisfactoria en 49, que egresaron en buenas condiciones. Hubo seis defunciones confirmadas por virus de influenza A H1N1. Los seis enfermos fallecidos llegaron al HGM con insuficiencia respiratoria aguda grave que ameritó de intubación endotraqueal y respiración asistida; dos llegaron en estado agónico y fallecieron unos minutos después de haber ingresado al Servicio de Urgencias, a pesar de las medidas de reanimación.5
El diagnóstico de confirmación de influenza H1N1 es a través del estudio de PCR de una muestra nasal y de faringe y ante la sospecha de influenza tipo A H1N1 se deberá de ofrecer tratamiento antiviral sin esperar resultados de confirmación de caso.6,7
Durante la pandemia, las embarazadas de bajo riesgo con enfermedad leve no necesitan realizarse prueba diagnóstica o recibir tratamiento antiviral. Un estudio reciente reportó que no hubo retraso en el diagnóstico en mujeres embarazadas pero si un retraso significativo en ofrecer el tratamiento a causa de la preocupación de médicos y madres en la seguridad de medicamentos antivirales en el desarrollo del feto.
¿ Métodos
Diseño: Estudio retrospectivo y descriptivo de casos. Población: Pacientes embarazadas con síndrome febril respiratorio agudo y diagnóstico de Influenza A H1N1 mediante RT-PCR atendidos en el Servicio de Infectología del Hospital General de México en el periodo de abril a diciembre de 2009.
Tamaño y tipo de muestreo: Muestreo no probabilístico de casos consecutivos encontrados en expedientes que cumplan criterios de inclusión.
Criterios de inclusión: Diagnóstico de Influenza A H1N1 mediante prueba de RT-PCR y prueba positiva de embarazo además de confirmación de viabilidad del producto al ingreso con ultrasonido obstétrico.
Variables evaluadas: Características demográficas, clínicas, desenlaces obstétricos, complicaciones asociadas al tratamiento y la infección, desenlace clínico de la infección y supervivencia global.
Análisis estadístico: Estadística descriptiva de acuerdo al tipo de variables. Cálculo de frecuencias simples y proporciones así como medidas de tendencia central y de dispersión.
¿ Resultados
Se incluyeron cinco pacientes, sin vacunación previa ni riesgo aparente de exposición a contactos estrechos.
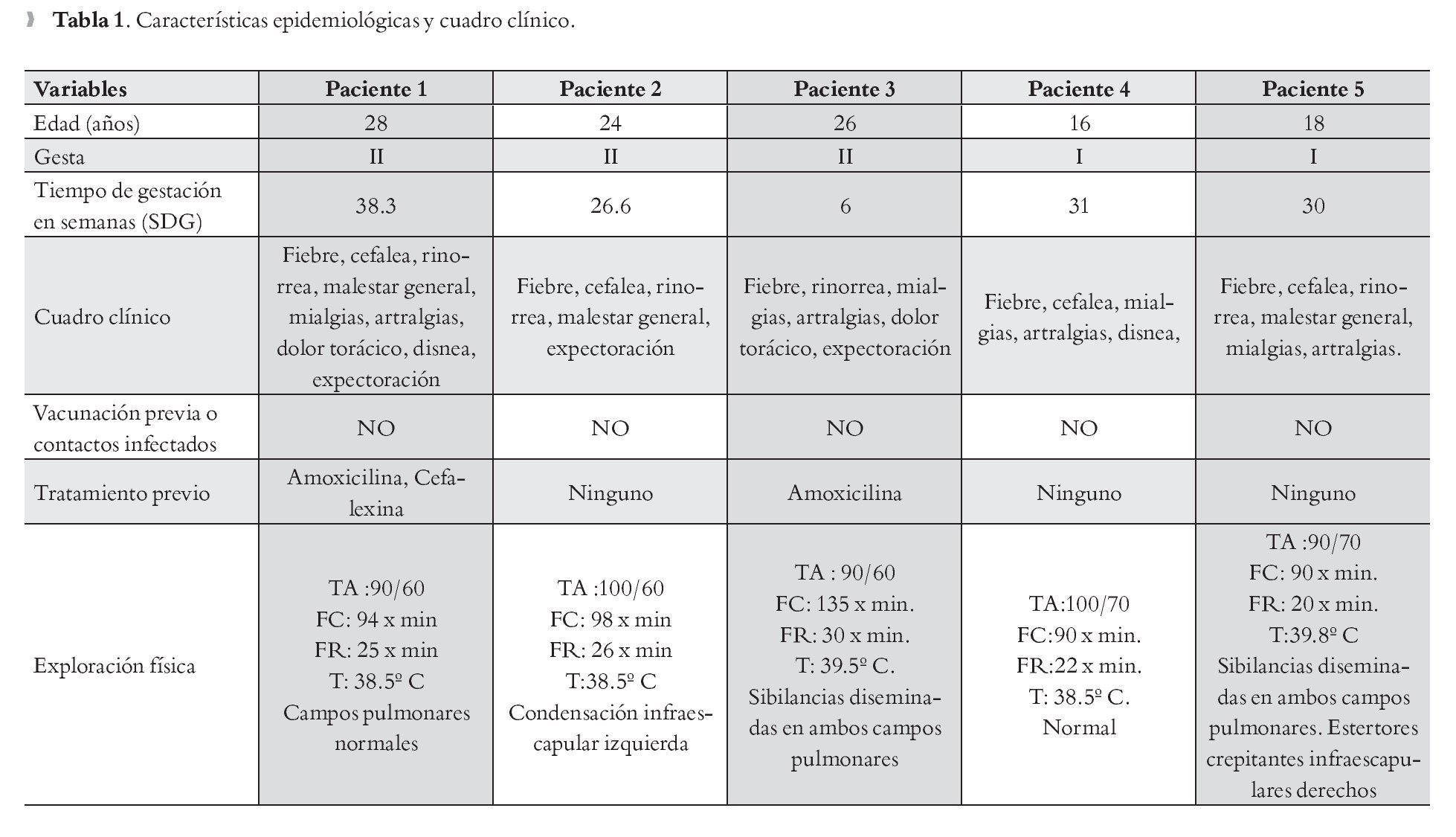
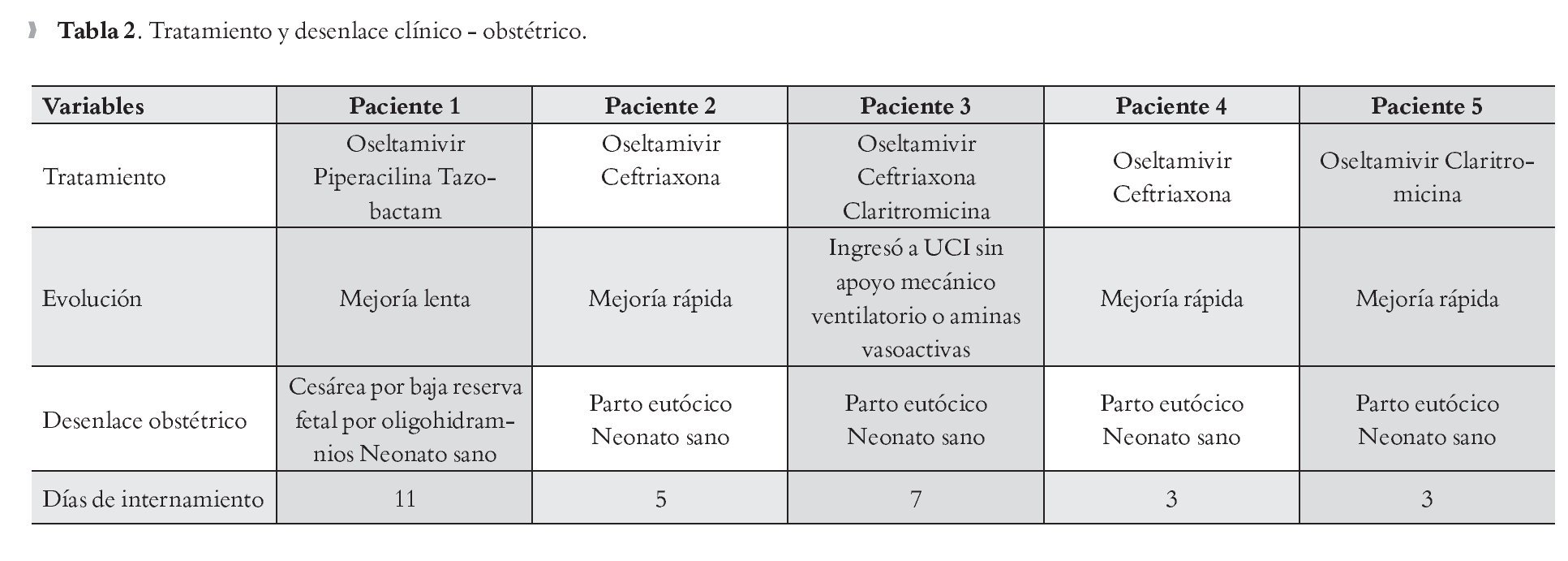
Paciente 1: 28 años de edad. G:II, con 38.3 semanas de gestación; internamiento de 11 días. Exploración física: Fiebre de 37.5ºC. Campos pulmonares normales. Radiografía de tórax: infiltrado reticulonodular basal derecho. Presentó hipoxemia severa con pO2 de 56.6% y SaO2 90%. Recibió tratamiento con oseltamivir, piperacilina y tazobactam. Su mejoría fue lenta. Desenlace obstétrico: Cesárea por baja reserva fetal por oligohidramnios. Neonato sano.
Paciente 2: 24 años de edad. G:II, con 26.6 semanas de gestación; internamiento de cinco días. Exploración física: Fiebre: 38.5ºC, taquipnéica con condensación infraescapular izquierda. Radiografía de tórax: opacidad de lóbulo basal izquierdo. Hipoxemia severa con una pO2 de 57.8% con SaO2 91%. Recibió tratamiento con oseltamivir y ceftriaxona. Mejoría rápida. Desenlace obstétrico: Parto eutócico. Neonato sano.
Paciente 3: 26 años de edad. G:II; con seis semanas de gestación; internamiento de siete días. Exploración física: Fiebre: 39.5ºC, disnea de pequeños esfuerzos y sibilancias en ambos hemitórax. Radiografía de tórax: Infiltrado intersticial bilateral. SaO2 91%. Recibió tratamiento con oseltamivir, ceftriaxona y claritromicina. Ingresó a UCI con oxigeno suplementario FiO2 60% y no requirió ventilación mecánica. Desenlace obstétrico: Parto eutócico. Neonato sano.
Paciente 4: 16 años de edad. G:I; con 31 semanas de gestación. Internamiento de tres días. Exploración física: fiebre de 38.5ºC, disnea de medianos esfuerzos, campos pulmonares normales. Radiografía de tórax: normal. SaO2 96%. Recibió tratamiento con oseltamivir y ceftriaxona. Mejoría rápida. Desenlace obstétrico: Parto eutócico. Neonato sano.
Paciente 5: 18 años de edad. G:I; 30 semanas de gestación. Internamiento de tres días. Exploración física: fiebre de 39.8ºC, estertores infraescapulares derecho. Radiografía de tórax: infiltrado reticular basal derecho. SaO2 92%. Recibió tratamiento con oseltamivir y claritromicina. Mejoría rápida. Desenlace obstétrico: Parto eutócico. Neonato sano (Tablas 1 y 2).
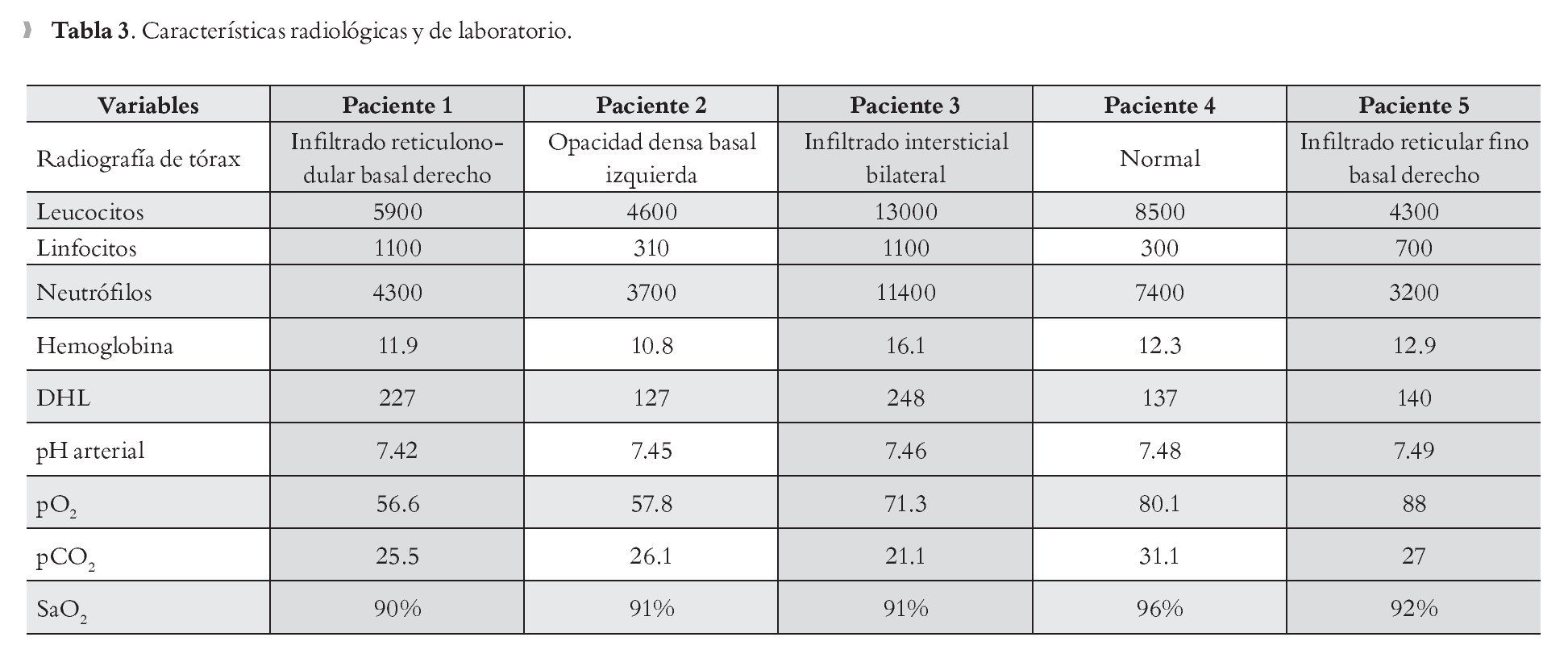
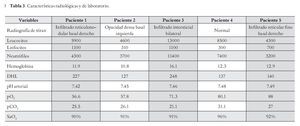
Hallazgos radiográficos: Cuatro pacientes tuvieron evidencia radiológica de pequeños exudados inflamatorios, no generalizados, como en los casos severos y en una paciente, su teleradiografía de tórax fue normal. Una paciente únicamente presentó leucocitosis con neutrofilia y que correspondió al proceso inflamatorio más severo tanto clínico como radiológico y además se acompañó de un proceso obstructivo de bronquioliar. Dos pacientes presentaron hipoxemia severa que se asociaron a un proceso inflamatorio localizado y la paciente número tres, infiltrados intersticiales con sibilancias, la hipoxemia no fue tan severa (Tabla 3).
¿ Discusión
Los pacientes con infección por el virus de la influenza A H1N1 presentan síndrome febril respiratorio agudo incluyendo tos, dolor faríngeo, rinorrea y fiebre. La presentación clínica puede estar complicada por el desarrollo de una infección bacteriana secundaria. Los síntomas comúnmente se desarrollan en una semana de exposición y los pacientes transmiten el contagio por aproximadamente ocho días posteriores al inicio de los síntomas. La mayor parte de las mujeres embarazadas tendrán un curso sin complicaciones, pero se han señalado desenlaces obstétricos adversos, incluida la muerte materna. El riesgo de morbilidad por influenza estacional es mayor para mujeres embarazadas, éste fenómeno también se ha observado durante el brote epidemiológico actual, ya que las mujeres embarazadas han tenido mayor frecuencia de internamiento que la población general.8,9 Las complicaciones asociadas a la influenza A H1N1 en embarazo incluyen alteraciones en monitoreo fetal (más frecuentemente taquicardia fetal) y morbilidad asociada a fiebre, la hipertermia en el embarazo temprano se ha asociado con defectos del tubo neural y otras anomalías congénitas y la fiebre durante el parto es un factor de riesgo de convulsiones en el recién nacido, encefalopatía, parálisis cerebral y muerte.
En los cinco casos presentados en este reporte, todas las pacientes tuvieron un síndrome febril respiratorio, cursando cuatro mujeres el tercer trimestre del embarazo y una paciente el primer trimestre de embarazo, como se reporta en la literatura, aunque en nuestras pacientes no hubo monitoreo fetal, la resolución de los partos fue satisfactoria.
Las pacientes presentadas tuvieron una infección de leve a moderada sin requerir apoyo ventilatorio mecánico y el motivo de internamiento fue el establecer una vigilancia estrecha para evitar complicaciones graves.
La mortalidad también parece ser mayor en las mujeres embarazadas, especialmente si la infección ocurre en el tercer trimestre. En una serie de 1350 mujeres embarazadas durante la epidemia de 1918, aproximadamente 50% desarrollaron neumonía con mortalidad de 27%; la mayor parte de las mujeres que fallecieron, cursaban el tercer trimestre.10 Nuestras cuatro pacientes en el tercer trimestre tuvieron una evolución satisfactoria; asimismo, la evolución de nuestras cinco pacientes fue satisfactoria y su egreso fue por recuperación.
En una serie de cinco mujeres recientemente hospitalizadas por la pandemia A H1N1, la CDC reportó a dos mujeres que desarrollaron aborto espontáneo (a las 13 semanas) y ruptura prematura de membranas (a las 35 semanas).11
El virus de influenza A H1N es resistente a adamantanos, como amantadina o rimantadina. El tratamiento de elección en mujeres embarazadas y no embarazadas, es oseltamivir 75 mg dos veces al día por cinco días o zanamivir, inhalación de 2 mg a 5 mg dos veces al día, por cinco días. Oseltamivir y zanamivir son fármacos categoría C en el embarazo, pero no se han señalado eventos adversos en las mujeres que recibieron estos agentes durante la gestación. Un estudio basado en un modelo placentario humano mostró que oseltamivir se metaboliza extensamente por la placenta con mínima acumulación en el lado fetal.12,13 En dos series de casos de mujeres expuestas a este fármaco durante el embarazo, la incidencia de malformaciones congénitas mayores fue similar a la población general. Hay pocos datos disponibles con zanamivir; en un informe de tres mujeres que fueron expuestas a éste durante su embarazo: una presentó aborto, otra terminación electiva de embarazo y otra parto transvaginal con producto sano. El tratamiento idealmente debe ser iniciado posterior al inicio de los síntomas, porque el beneficio de los antivirales es mejor si se administra dentro de las primeras 48 horas de aparición de sintomatología. Sin embargo, estudios en influenza estacional en pacientes hospitalizados, se ha demostrado beneficio aún si se inicia después de 48 horas.2 Además de medicamentos antivirales específicos, se debe administrar acetaminofén si la paciente se encuentra febril.
Las pacientes con sospecha de infección por la pandemia con H1N1, deben usar mascarilla protectora y aislarse en habitación lejos de proveedores de salud y otros pacientes hospitalizados. Si se confirma infección por H1N1 se deben agregar bata y guantes a las medidas de protección habituales, si es necesario nebulizar a la paciente existe el riesgo de aerolización de partículas, también se debe agregar lentes de protección. Debido a la naturaleza pandémica de la enfermedad las pacientes no necesitan ser colocadas en habitaciones con presión negativa. Si la paciente tiene su parto mientras se encuentra infectada con H1N1 debe ser separada del producto inmediatamente después del parto, la paciente debe evitar contacto cercano con el niño hasta haber suspendido el tratamiento antiviral por 48 horas, su fiebre haya remitido y pueda controlar su tos y secreciones. Después de éste periodo inicial de aislamiento, se deben mantener prácticas de higiene de manos y cuidados al toser además de utilizar mascarilla por los siguientes siete días.2 En nuestras pacientes, después del parto permanecieron aisladas de su bebé hasta pasar el periodo de contagio. La alimentación de los recién nacidos fue con fórmula láctea durante el internamiento.
Se debe considerar profilaxis posexposición en mujeres embarazadas en contacto estrecho con pacientes con sospecha o confirmación de infección por H1N1. Se recomiendan dos regímenes: oseltamivir (75 mg vía oral diaria) o zanamivir (10 mg inhalados al día). Aunque zanamivir puede ser el fármaco de elección por su limitada absorción sistémica, la vía inhalada puede no ser tolerada, especialmente en mujeres con alguna condición respiratoria subyacente, como enfermedad pulmonar obstructiva crónica o asma. En este contexto, oseltamivir es una alternativa razonable. La profilaxis debe continuarse por cinco días después de la exposición conocida pero puede extenderse a consideración del obstetra en escenarios donde pueden ocurrir múltiples exposiciones. Es necesario monitorear los síntomas de influenza de manera estrecha.2
El riesgo de transmisión de A H1N1 a través de leche materna se desconoce. Sin embargo, ya que los reportes de viremia con influenza estacional son raros, es poco probable que A H1N1 pueda cruzar a la leche materna. Por otro lado, la lactancia fortalece la respuesta inmune neonatal y los infantes que no reciben seno materno pueden ser más vulnerables a una infección viral. El uso de medicamentos antivirales para el tratamiento de H1N1 o quimioprofilaxis con los mismos, no es una contraindicación a la lactancia.2 La concentración de oseltamivir y zanamivir en leche materna se ha estimado en menos de la dosis pediátrica de cada uno.15 Si el neonato necesita ser aislado de su madre infectada, puede administrarse leche extraída de la madre hasta que puedan reunirse nuevamente el binomio madre-hijo, si no existe esta posibilidad de asistencia disponible, la madre puede alimentar al bebé directamente del seno y debe utilizar estrictamente mascarilla además de las medidas higiénicas de manos y protocolo de tos.
La Organización Mundial de la Salud recomienda que el orden de prioridad de vacunación deben ser: trabajadores de la salud, mujeres embarazadas, individuos con ciertas condiciones médicas, individuos sanos entre 15 y 49 años de edad, niños sanos y finalmente individuos sanos con edad entre 50 y 64 años.16 La vacuna estacional de influenza estará disponible de manera regular y debe ofrecerse a todas las mujeres embarazadas durante el periodo de riesgo (noviembre a marzo). Dichas vacunas son intervenciones de bajo costo que han mostrado que tienen beneficios sustanciales en madre e hijo.17,18 De las pacientes presentadas, ninguna tenia antecedente de vacunación previa para influenza estacional.
¿ Conclusiones
La mujer embarazada es más susceptible a infección por el virus de la Influenza A H1N1 y el tercer trimestre de embarazo es la mayor etapa de incidencia. Debido a esta mayor prevalencia en la mujer embarazada, los cuidados de atención y vigilancia temprana tienen que ser más estrechos. La sintomatología que las pacientes presentan es variable, desde casos leves, como se presentaron en nuestras pacientes como casos reportados de la literatura de mayor morbi-mortalidad. La incidencia de la infección por virus de la influenza también correspondió a la edad de la población general afectada, de la tercera a la cuarta década. En nuestra población de pacientes, la sintomatología presentada fue similar a la referida por la población general, en la mayoría de las pacientes presentaron un síndrome febril respiratorio, de leve a moderado y que coincidió con los hallazgos clínicos, radiológicos y una evolución favorable, se encontraron alteraciones en la radiografía de tórax. No se encontraron alteraciones relevantes en la gasometría o la biometría hemática, y la deshidrogenasa láctica no presentó elevaciones significativas. En ninguna de las pacientes se aislaron bacterias como complicación de neumonía bacteriana secundaria a influenza, sin embargo en dos pacientes se agregó tratamiento antimicrobiano además del tratamiento antiviral del tipo de oseltamivir por los datos clínicos y radiológicos y no se presentaron complicaciones asociadas. El cuadro más severo se presentó en la paciente con menor tiempo de gestación. En todos los casos el desenlace obstétrico y clínico fue bueno y el neonato se mostró sano al nacimiento, lo que al menos en estos casos sugiere cierta seguridad en el uso de tratamiento antiviral con oseltamivir durante el tercer trimestre de embarazo.
Es recomendable la aplicación preventiva a la población femenina embarazada de la vacuna para la influenza, tanto estacional como la epidémica A H1N1.
Correspondencia: Dr. Banda Lara Marco Isaac.
Unidad 405 Dr. Balmis 148
Col. Doctores 06720 México D.F.
Teléfono: 2789 2000. Extensión: 1365.
Correo electrónico:bandamarco@prodigy.net.mx