Comparar la eficacia del diclofenaco tópico 0.1% vs. nepafenaco tópico en reducir el dolor asociado a la fotocoagulación panretiniana con láser argón.
Material y métodosEnsayo clínico aleatorizado doble enmascarado, 132 pacientes (183 ojos) con diagnóstico de retinopatía diabética proliferativa tratados con fotocoagulación panretiniana. Aleatorización en 2 grupos: diclofenaco y nepafenaco tópicos. Se aplicaron 2 dosis de los analgésicos tópicos previas a la fotocoagulación panretiniana, se evaluó el dolor inmediatamente y 15min después. Se analizó nivel de dolor, efectos adversos y síntomas asociados al finalizar la fotocoagulación retiniana.
ResultadosLa mediana de la edad para ambos grupos fue de 55 años, relación H:M de 1:1.4. El nivel de dolor inmediato fue de 35.5 (RIC 14-72) para el nepafenaco y de 45 (RIC 14-70) para el diclofenaco (p=0.48). A los 15min fue de 30 (RIC 4-50) para el nepafenaco y de 20 (RIC 2-50) para el diclofenaco (p=0.48). No hubo diferencias significativas en síntomas asociados entre los grupos ni efectos adversos en la superficie ocular.
ConclusionesEl tratamiento previo con nepafenaco y diclofenaco tópicos es igualmente eficaz y seguro para reducir el dolor asociado a la fotocoagulación panretiniana en pacientes con retinopatía diabética proliferativa.
To compare the efficacy of topical diclofenac 0.1% vs topical nepafenac in reducing pain associated to argon laser retinal photocoagulation
Material and methodsDouble blinded, randomized clinical trial. One hundred thirty two patients with diagnosis of proliferative diabetic retinopathy treated with retinal photocoagulation. Randomization in to 2 groups: topical diclofenac and nepafenac. Before retinal photocoagulation 2 doses of topical non-steroidal anti-inflammatory drugs were applied, pain was assessed immediately and 15minutes after. Level of pain, adverse effects and associated symptoms at the end of retinal photocoagulation were analyzed.
ResultsThe median for age in both groups was 55 years, M:F ratio of 1:1.4. The immediate level of pain was 35.5 (ICR 14-72) for nepafenac and 45 (ICR 14-70) for diclofenac (P=.48). At 15minutes the pain level was 30 (ICR 4-50) for nepafenac and 20 (ICR 2-50) for diclofenac. There was no difference in associated symptoms or adverse effects among groups.
ConclusionsThe preventive treatment with topical nepafenac and diclofenac is equally effective and safe for reducing the pain associated with retinal photocoagulation in patients with proliferative diabetic retinopathy.
La fotocoagulación panretiniana (FCP) ha sido el estándar de oro en el manejo de la retinopatía diabética proliferativa desde finales de los años setenta e inicio de los ochenta, cuando el Estudio de la Retinopatía Diabética (Diabetic Retinopathy Study) y el Estudio para el Tratamiento Temprano de la Retinopatía Diabética (Early Treatment Diabetic Retinopathy Study) demostraron que el uso de esta terapia reducía el riesgo de pérdida visual severa hasta en un 50% a 5 años1,2.
Durante el procedimiento de FCP, los pacientes suelen referir dolor en el rango de intensidad moderado, de una calidad punzante o penetrante y de una duración breve3,4. Se ha reportado que hasta un 40% de los ojos con retinopatía diabética proliferativa reciben 30% menos disparos de los considerados como mínimo por el Estudio de la Retinopatía Diabética (Diabetic Retinopathy Study), siendo el dolor ocular asociado a la aplicación de la FCP la principal razón atribuida a esta falta de cumplimiento en el tratamiento5–8. Este «subtratamiento» en la FCP está asociado con un aumento en la incidencia de complicaciones asociadas a la retinopatía diabética proliferativa (hemorragias vítreas, desprendimiento traccional de retina) y a una pérdida acelerada de la visión8.
Se ha intentado reducir este tipo de dolor mediante el uso de diferentes agentes farmacológicos tópicos (mediante colirios oftálmicos)4,9, vía oral3,10 o local (inyecciones perioculares o retrobulbares de agentes anestésicos)11, siendo estos últimos los más efectivos en la reducción transprocedimiento del dolor pero también los más frecuentemente asociados a complicaciones oculares severas (perforación inadvertida del globo ocular, anestesia del tallo cerebral y arresto respiratorio)12–15. Dejando de lado los medicamentos perioculares, los agentes farmacológicos que han demostrado mayor efectividad en lograr una reducción en el dolor ocular relacionado con la FCP durante y después del procedimiento han sido los antiinflamatorios no esteroideos (AINE). Específicamente se ha demostrado que el diclofenaco, ya sea de forma tópica en colirio oftálmico o vía oral, es más efectivo que el placebo en la reducción del dolor asociado a la FCP con láser argón; y se ha recomendado su aplicación de manera regular antes de cada sesión16,17. Sin embargo, no existe evidencia contundente sobre el régimen óptimo para la aplicación de los AINE tópicos previo a la FCP con fin de lograr una mejor analgesia durante y después del procedimiento, evitando que su uso se haya convertido en estándar de oro en la práctica diaria. El surgimiento de nuevas generaciones de AINE con una mayor penetración y biodistribución intraocular ha planteado la posibilidad de mejorar el perfil analgésico y antiinflamatorio; tal es el caso del nepafenaco (inhibidor no selectivo de la ciclooxigenasa) que ha demostrado una alta efectividad clínica para reducir la actividad inflamatoria tanto en el segmento anterior como en el segmento posterior17,18.
El riesgo asociado al uso de medicamentos anestésicos perioculares y retrobulbares, así como la falta de consenso sobre la aplicación de AINE tópicos previo al procedimiento de FCP, nos plantea la importancia de buscar alternativas seguras y poco invasivas que permitan lograr una mejor analgesia durante y después del procedimiento para así reducir la tasa de subtratamiento con FCP y potencialmente el deterioro visual asociado a la progresión de la severidad de la retinopatía diabética proliferativa. El presente estudio tiene como objetivo comparar la eficacia del nepafenaco tópico contra la del diclofenaco sódico tópico en lograr analgesia durante y en el período inmediato posterior al procedimiento de FCP.
Materiales y métodosSe realizó un ensayo clínico, aleatorizado, doble enmascarado, para comparar la eficacia de 2 AINE tópicos (diclofenaco sódico 0.1% y nepafenaco 0.1%) en reducir el dolor asociado a la FCP en el período posterior inmediato al procedimiento. El estudio fue aprobado por el Comité de Ética de la institución correspondiente (Escuela de Medicina del Tecnológico de Monterrey) y se apegó a los principios establecidos en la Declaración de Helsinki, en todo caso se obtuvo el consentimiento informado de los participantes posterior a la explicación detallada de los procedimientos. Se incluyeron todos los pacientes mayores de 18 años diagnosticados con retinopatía diabética proliferativa a quienes se indicó FCP como tratamiento en la Clínica de Oftalmología Santos y de la Garza Evia del Tecnológico de Monterrey (Santa Catarina, Nuevo León, México) durante el período enero 2013 a agosto 2013.
Se excluyeron pacientes con antecedente de sesiones previas de FCP, hipersensibilidad o alergia previa a cualquier AINE tópico previamente utilizado, uso concomitante de cualquier tipo de narcótico o AINE, enfermedad corneal previa (denervación corneal o queratitis neurotrófica, queratitis infecciosa, herpes oftálmico, adelgazamiento, perforación o derretimiento corneal), antecedente de enfermedades autoinmunes o del tejido conectivo, antecedente de múltiples (más de 3) cirugías oculares, uso crónico de ácido acetilsalicílico y a pacientes que no tuvieran la capacidad para comprensión de los instrumentos de medición utilizados.
Para el cálculo del tamaño de la muestra se utilizó un análisis de comparación de medias (error tipo i=0.05; error tipo ii=0.2), considerando que el nivel medio de dolor reportado por las 2 series que utilizaron diclofenaco tópico al 0.1% fue de 33.8 (±20)4,16 y el nivel medio de dolor esperado para el grupo de estudio experimental, en este caso nepafenaco, será de 20 con una desviación estándar similar a la reportada en estudios previos10. El nivel medio esperado de dolor para el grupo con nepafenaco se proyecta a partir de que es necesaria una diferencia de 13 puntos en la escala análoga visual del dolor (EAV) para que esta diferencia sea clínicamente significativa19–21. De este cálculo se obtiene como necesaria una muestra poblacional de 66 pacientes por grupo para lograr un poder del estudio (1-beta) del 95%.
La variable principal a estudiar fue la severidad del dolor reportado justo al finalizar la FCP y 15min después, utilizando la EAV para dolor. Las variables secundarias fueron edad, género y síntomas sistémicos u oculares no percibidos al inicio del estudio (lagrimeo, fotofobia, prurito ocular, visión borrosa, sensación de cuerpo extraño, deslumbramiento, cefalea y mareo) así como las complicaciones o efectos adversos relacionados directamente con el uso de AINE tópicos (defecto corneal epitelial, erosión corneal epitelial).
Los participantes se aleatorizaron en 2 grupos: (1) diclofenaco sódico tópico 0.1% y (2) nepafenaco suspensión oftálmica 0.1%, mediante un programa en la Internet (http://www.randomization.com). Por principios éticos, no se incluyó un grupo placebo, ya que se ha demostrado que el diclofenaco sódico tópico es estadísticamente más efectivo que este (placebo, lágrimas artificiales) en la reducción del dolor asociado a la FCP4,16. Se tomó como grupo control, entonces, al grupo del diclofenaco sódico al 1%.
Los medicamentos tópicos se almacenaron en goteros con la misma capacidad y apariencia, y se colocó una etiqueta azul o verde para diferenciar los diferentes grupos. El medicamento tópico se asignó al gotero con la etiqueta de color por un tercer investigador, de manera que los investigadores principales y el paciente fueron enmascarados al colirio aplicado. El código de etiquetado para cada gotero se guardó y no se reveló hasta finalizar el estudio.
La midriasis pupilar se realizó de la misma manera en todos los pacientes, aplicando una gota de fenilefrina al 2.5% y tropicamida al 1% (TP ofteno; Laboratorios Sophia, Gdl, Mx) 30min previos al inicio de la FCP, pudiendo repetirse la dosis en caso de no lograr una midriasis pupilar adecuada. Se aplicó el colirio oftálmico con la etiqueta asignada, una gota 60min previos al inicio de la FCP seguida de una segunda dosis de una gota de 5-10min antes del inicio de la FCP. Se utilizó una gota de clorhidrato de tetracaína tópica (5mg/ml) en el ojo al que se aplicará la FCP justo previo al inicio del procedimiento, con la finalidad de facilitar la colocación del lente de contacto para fondo de ojo empleado en la administración del láser.
Se aplicó la FCP utilizando láser argón verde NIDEK GYC-1000 (Nidek Inc, Freemont, CA, EUA) y lente Ocular Mainster PRP 165 (Ocular Instruments, Bellevue, WA, EUA) con un máximo de 800 disparos por sesión, utilizando como parámetros un tamaño del spot de 200micras, una duración del disparo de 0.15seg y una intensidad variable dependiendo de las características propias del paciente (100-700mW). Se registró para cada paciente la energía utilizada en los disparos, así como el número total de disparos; pudiendo calcular la energía total aplicada (energía/intensidad disparo×número total de disparos) durante la sesión de FCP de cada paciente. Todas las sesiones de FCP fueron realizadas por el mismo oftalmólogo investigador (JCHC).
Inmediatamente después de la sesión de FCP se examinó al paciente bajo la lámpara de hendidura para evaluar la superficie ocular (córnea y conjuntiva) y evaluar efectos adversos (queratopatía epitelial, desepitelización o defectos epiteliales corneal o conjuntivales) y se pidió al paciente que evaluara el nivel de dolor experimentado durante la misma, utilizando la EAV, herramienta previamente validada como confiable y sensible para la medición del dolor22. Consiste en una línea de 100mm marcada en el extremo inicial con la leyenda no dolor y en el otro extremo el peor dolor que he sentido. Se le solicita al paciente marcar con una X sobre la línea, la intensidad del dolor experimentado. Posteriormente, un tercer investigador midió en milímetros (mm) la posición de la X y la registra, convirtiéndola en un puntaje del 0 al 100 (fig. 1).
Escala análoga visual de dolor, línea de 100mm marcada en el extremo inicial con la leyenda no dolor y en el otro extremo el peor dolor que he sentido. Adaptada de: Acute pain management: Operative or medical procedures and trauma, clinical practice guideline No. 1. AHCPR Publication No. 92-0032; February 1992. Agency for Healthcare Research & Quality, Rockville, MD; pages 116-117.
Se realizó exploración de los resultados mediante pruebas para normalidad, obteniéndose una distribución no normal para todas las variables a estudiar excepto para el total de energía aplicada. Se realizó el análisis estadístico mediante Chi cuadrada de Pearson para las variables nominales (género, ojos tratados y síntomas asociados al término del tratamiento) y mediante pruebas no paramétricas (Mann-Whitney) para muestras independientes en el caso de las variables continuas (edad, EAV inmediata y EAV a los 15min). Se utilizaron pruebas no paramétricas para muestras relacionadas (Wilcoxon) para el análisis de la EAV inmediata y a los 15min para género, para comparar la EAV inmediata y a los 15min para el grupo nepafenaco y para el grupo diclofenaco, y para comparar la EAV inmediata y a los 15min en el número de ojos tratados. Se utilizó la prueba T de Student no pareada para comparar el total de energía aplicada entre el grupo experimental y el control, entre género y entre número de ojos tratados. Se utilizó el método de Pearson para analizar correlaciones entre el total de energía aplicada y el dolor reportado en la EAV inmediata y a los 15min. La significación estadística se definió como un valor de p<0.05. Para los cálculos estadísticos se usó el programa de ordenador Excel®, NCSS® 2007 para Windows Vista® (Kaysville, Utah, EUA) y SPSS® versión 17.
ResultadosSe estudiaron un total de 132 pacientes (183 ojos) con diagnóstico de retinopatía diabética proliferativa, 77 pacientes (56.8%) del género femenino y 55 hombres (43.2%) con relación hombre:mujer de 1:1.4, distribuyéndose al azar 66 pacientes (90 ojos) en el grupo de estudio (nepafenaco) y 66 pacientes (93 ojos) en el grupo control (diclofenaco). La mediana de la edad para ambos grupos fue de 55 años (rango intercuartílico [RIC] 48-63 para el grupo del nepafenaco, y 49-63 para el grupo del diclofenaco). Treinta pacientes (45.5%) fueron mujeres en el grupo del nepafenaco y 27 (40.9%) fueron mujeres en el grupo diclofenaco. Se trataron 2 ojos en 24 pacientes (36.3%) del grupo nepafenaco y en 27 pacientes (40.9%) de grupo diclofenaco (tabla 1).
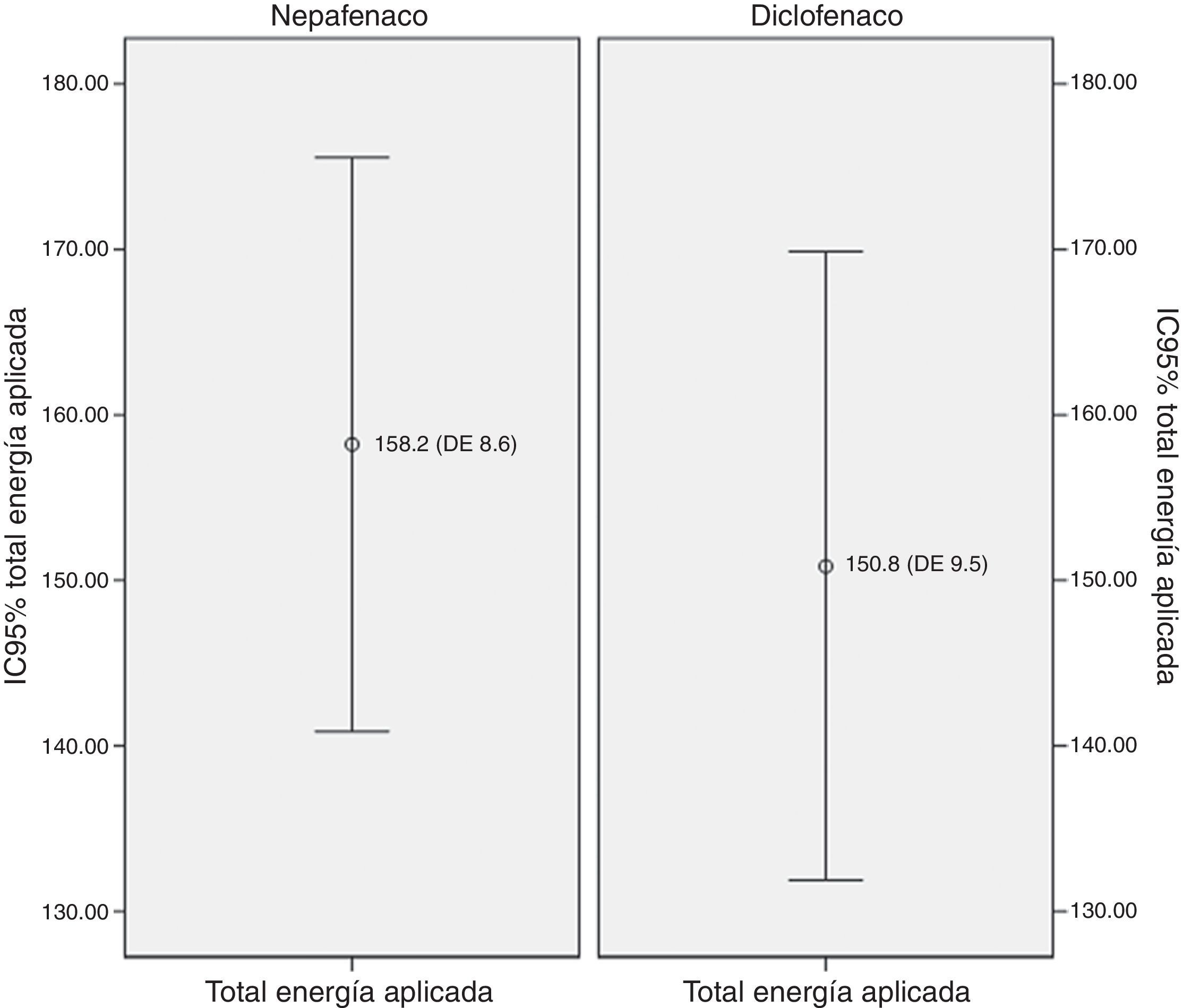
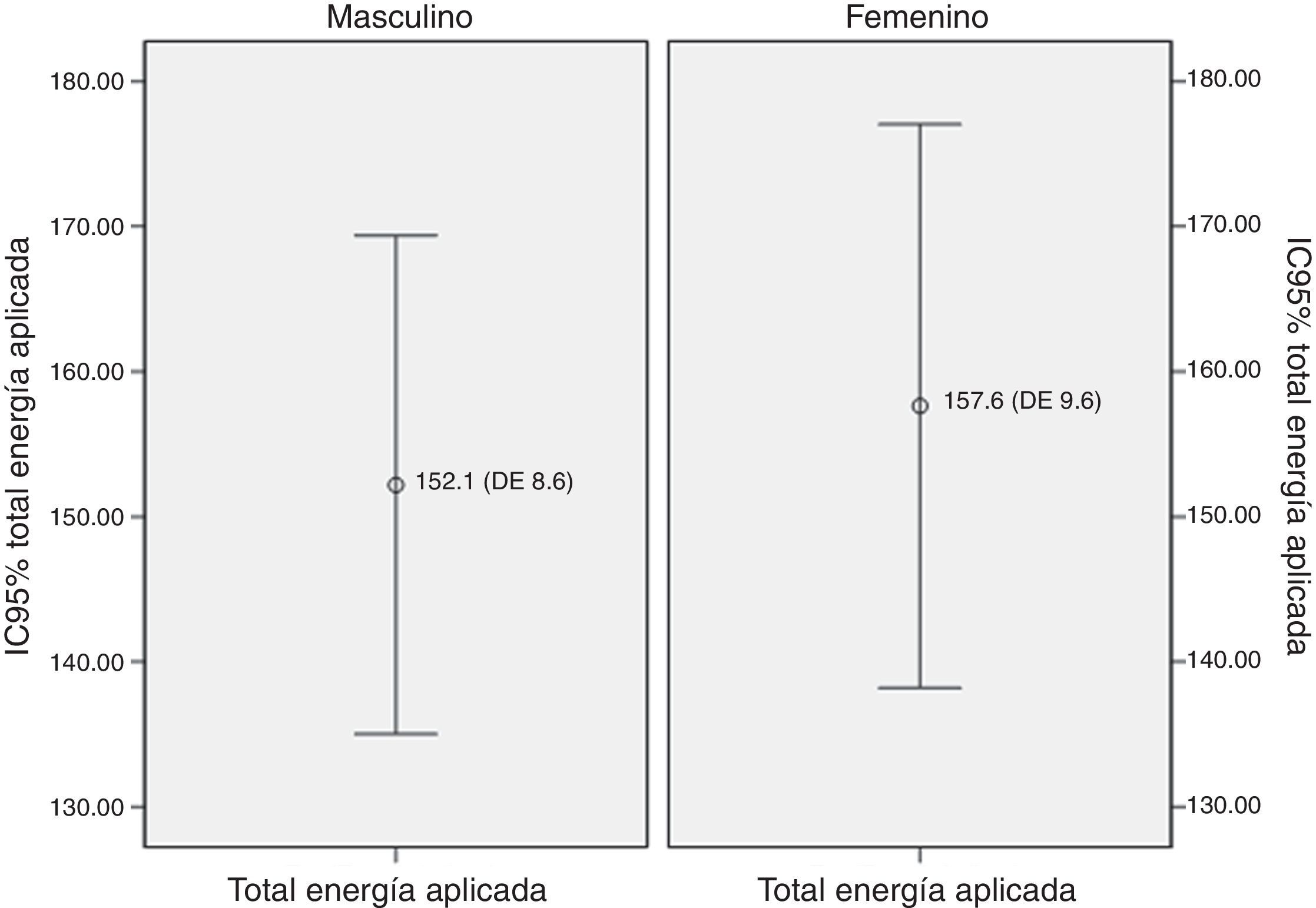
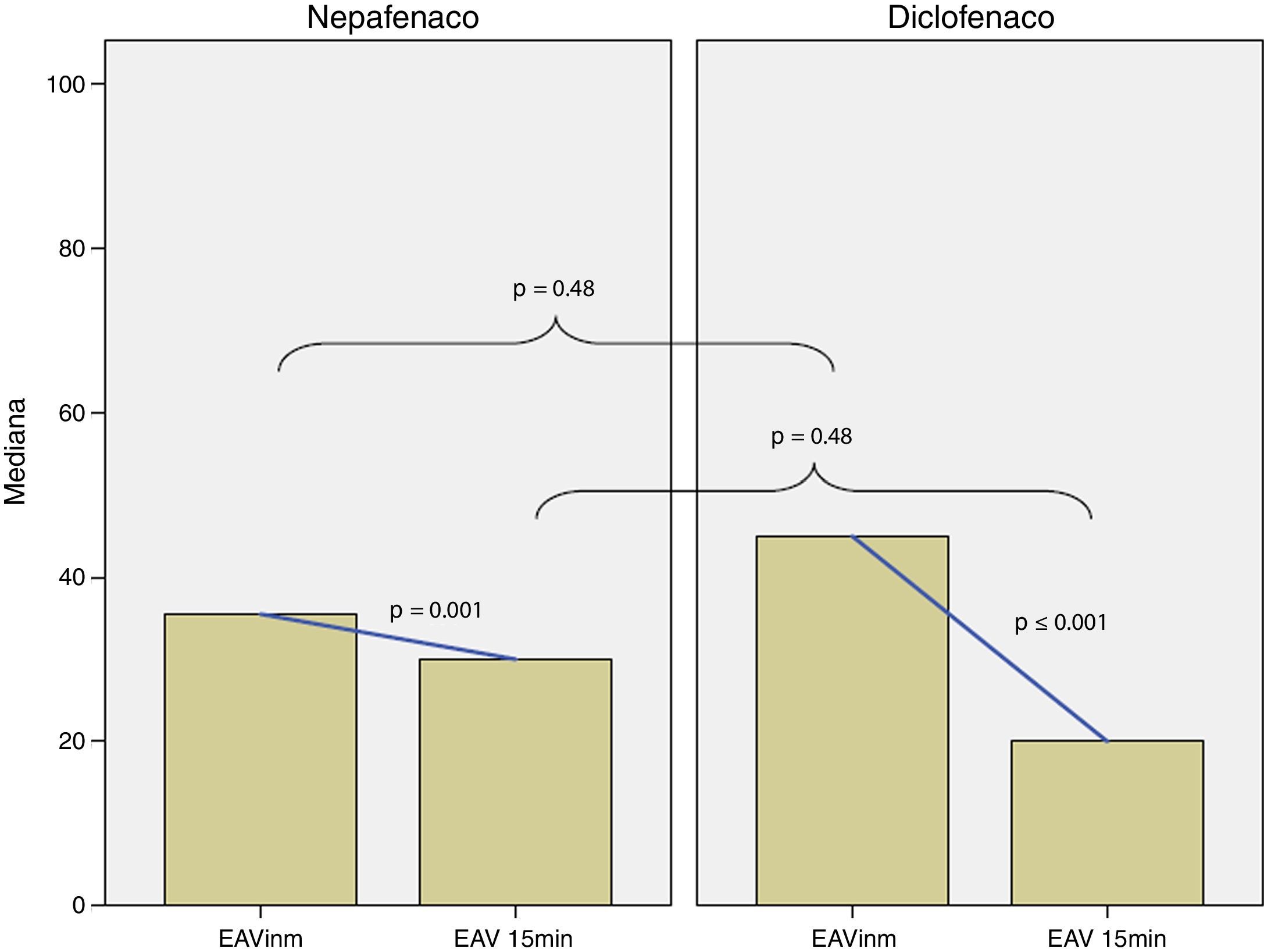
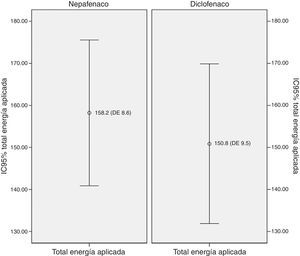
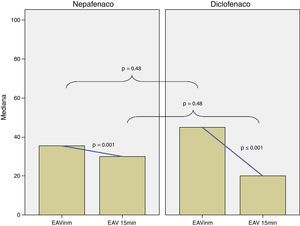
La diferencia en las medias para el total de energía aplicada en los grupos de nepafenaco y diclofenaco y entre géneros no fue estadísticamente significativa (figs. 2 y 3). No existió una correlación entre el total de energía y el nivel de dolor reportado en la EAV: diclofenaco 0.1% EAV inmediata r=0.07, p=0.52 y EAV 15min r=0.14, p=0.24; nepafenaco 0.1% EAV inmediata r=0.08, p=0.48 y EAV 15min r=0.18, p=0.14. La mediana en el nivel de dolor inmediatamente después de la sesión de FCP medido a través de la EAV de dolor fue de 35.5 con un RIC de 14-72 para el grupo del nepafenaco y de 45 con un RIC de 14-70 para el grupo del diclofenaco (p=0.48) (fig. 4). La misma escala de dolor a los 15min posteriores a la finalización del tratamiento de fotocoagulación mostró una mediana de dolor de 30 (RIC 4-50) para el grupo del nepafenaco y de 20 (RIC 2-50) para el grupo del diclofenaco (p=0.48) (fig. 3). El análisis del nivel de dolor inmediato posterior a la sesión de fotocoagulación para género fue de 34 (RIC 12-62) para género femenino y de 45 (RIC 17-50) para género masculino (p=0.59), mientras que el mismo análisis de dolor para los 15min posteriores al tratamiento mostró una mediana de dolor de 20 (RIC 2-50) para el género femenino y de 30 (RIC 10-55) para el género masculino (p=0.37).
Medianas para la EAV inmediata y a los 15min para los grupos nepafenaco y diclofenaco. Las líneas de interpolación representan el cambio entre EAV inmediata y a los 15min para cada grupo (cambios estadísticamente significativos). La diferencia entre las medianas de la EAV inmediata y a los 15min del grupo nepafenaco y diclofenaco no fueron estadísticamente significativas (p=0.48 para ambos tiempos).
El nivel de dolor inmediato posterior al tratamiento de fotocoagulación retiniana cuando se trató solamente un ojo fue de 47 (RIC 12.5-78.5) y cuando se trataron los 2 ojos fue de 34 (RIC 15-56) (p=0.12). El reporte del nivel de dolor a los 15min posteriores del tratamiento fue de 30 (RIC 3-59) para el grupo donde se trató un solo ojo y de 28 (RIC 3-48) para el grupo de 2 ojos tratados (p=0.22). La media del total de energía aplicada cuando se trató solamente un ojo fue de 131 (±73) y de 191.8 (±58.4) cuando se trataron 2 ojos.
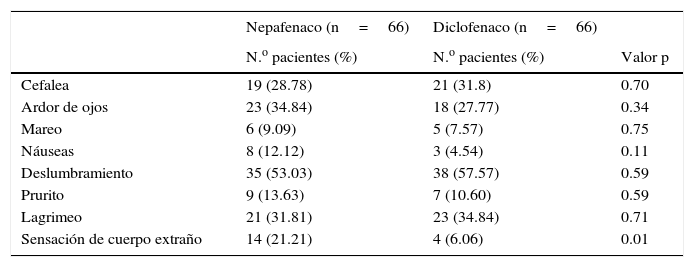
El 84.8% de los pacientes en el grupo nepafenaco y el 81.8% del grupo diclofenaco presentaron al menos un síntoma asociado posterior a la sesión de FCP. Los síntomas o molestias más comunes posteriores a la sesión de tratamiento fueron en ambos grupos el deslumbramiento, lagrimeo, cefalea y ardor de ojos. Sin embargo, la sensación de cuerpo extraño fue más frecuente en 14 pacientes (21%) del grupo del nepafenaco y en 4 pacientes (6%) del grupo diclofenaco (p=0.01) (tabla 2). No se reportaron efectos adversos en la superficie ocular asociados directamente al tratamiento tópico con los AINE.
Síntomas asociados al término de la sesión de fotocoagulación panretiniana
| Nepafenaco (n=66) | Diclofenaco (n=66) | ||
|---|---|---|---|
| N.o pacientes (%) | N.o pacientes (%) | Valor p | |
| Cefalea | 19 (28.78) | 21 (31.8) | 0.70 |
| Ardor de ojos | 23 (34.84) | 18 (27.77) | 0.34 |
| Mareo | 6 (9.09) | 5 (7.57) | 0.75 |
| Náuseas | 8 (12.12) | 3 (4.54) | 0.11 |
| Deslumbramiento | 35 (53.03) | 38 (57.57) | 0.59 |
| Prurito | 9 (13.63) | 7 (10.60) | 0.59 |
| Lagrimeo | 21 (31.81) | 23 (34.84) | 0.71 |
| Sensación de cuerpo extraño | 14 (21.21) | 4 (6.06) | 0.01 |
El objetivo principal de este estudio fue evaluar y comparar el efecto analgésico del nepafenaco tópico contra el del diclofenaco tópico al 0.1% durante la FCP con láser argón. Las prostaglandinas producen miosis, aumento en la permeabilidad vascular de todas las barreras hematooculares y poseen actividad quimiocinética al tener un rol importante en mantener y amplificar las fases celulares y humorales en la respuesta inflamatoria, proceso durante el cual se producen mediadores que estimulan la fibras nerviosas productoras de dolor4. Se han utilizado AINE para inhibir la cascada del ácido araquidónico, específicamente de la ciclooxigenasa, para lograr una disminución en la producción de prostaglandinas y por ende de mediadores nociceptivos.
Weinberger et al. evaluaron la eficacia del diclofenaco de sodio al 1% tópico en reducir el dolor asociado a FCP en 87 pacientes. Utilizaron EVA para determinar el dolor durante y después de la FCP, reportando un dolor medio de dolor del 44.2% para el diclofenaco de sodio tópico al 1% y una media de dolor del 53.1% para el grupo de cloruro de sodio tópico (placebo), siendo esta diferencia estadísticamente significativa (p=0.01)4. Zakrzewski et al. compararon el uso de diclofenaco tópico 0.1% y de forma oral mediante tabletas de liberación prolongada contra placebo previo a la FCP 16. Sus resultados demostraron que solo el diclofenaco vía oral fue clínica y estadísticamente superior al placebo en la reducción del dolor inmediatamente después del tratamiento y a los 15min posteriores al mismo, opuesto a lo reportado por Weinberg et al. (diclofenaco sódico 0.1% superior a placebo clínica y estadísticamente).
El nepafenaco constituye una nueva clase de AINE, cuyo mecanismo de profármaco supone una mayor biodisponibilidad y penetración en segmento anterior y posterior del ojo, así como una reducción en el riesgo de complicaciones de superficie por su rápida absorción en córnea y superficie ocular18. El nepafenaco es hidrolizado a amfenaco por hidrolasas intraoculares, maximizando su bioactivación intraocular23. Estudios en modelos animales han mostrado un coeficiente de permeabilidad del nepafenaco 4 veces mayor al del diclofenaco, y en humanos se ha demostrado una bioactivación (hidrólisis) rápida en iris, cuerpo ciliar, retina y coroides que permite la inhibición de la síntesis de prostaglandinas de un 85-95% por 6h en cuerpo ciliar y de un 55% en retina/coroides por 4h23,24. Por su parte, el diclofenaco 0.1% mostró supresión de la síntesis de prostaglandinas en iris/cuerpo ciliar por 20min con una recuperación del 75% en la síntesis de prostaglandinas a las 6h. Además, la inhibición de la síntesis de prostaglandinas en retina/coroides fue mínima24.
Tomando en cuenta los antecedentes y la evidencia reportada en estudios previos de la eficacia y ventajas del nepafenaco sobre otros AINE para inhibir la síntesis intraocular de prostaglandinas y por consecuencia de la formación de mediadores de dolor, la hipótesis de nuestro estudio fue que el uso del nepafenaco suspensión oftálmica una dosis 60min previos al inicio de la FCP y una segunda dosis de 5-10min antes de la misma, es superior al uso de diclofenaco sódico tópico al 0.1% en la misma posología para disminuir el dolor durante y después de la FCP en pacientes con diagnóstico de retinopatía diabética proliferativa. Por principios éticos, se tomó como control al grupo de diclofenaco tópico en vista de la evidencia respecto a la superioridad del mismo sobre el placebo (lubricante ocular en colirio) en reducir el dolor asociado a la FCP con argón16.
En los resultados del presente estudio, el nivel de dolor reportado en la EAV inmediatamente después de la sesión de FCP en el grupo diclofenaco fue de 45, similar a lo reportando en otros estudios (44.2 Weinberger et al., 33.8 Zakrzewski et al.)4,16. El nivel de dolor inmediato reportado para el grupo nepafenaco fue 35.5, aunque menor que el del reportado para el grupo diclofenaco, la diferencia no fue estadísticamente significativa ni clínicamente significativa, teniendo en cuenta que es necesaria una diferencia mínima de 13 puntos en la EAV para ser considerada significativa de manera clínica19–21. A los 15min, el nivel de dolor reportado para el grupo diclofenaco fue de 20 (RIC 2-50), nuevamente similar a lo reportado por otros autores para ese tiempo de evaluación (10.1±13.9, Zakrzewski et al.)16; y de 30 (RIC 4-50) para el grupo nepafenaco. Aunque en la evaluación del dolor para este tiempo se observó una tendencia hacia un menor nivel de dolor en el grupo diclofenaco, la diferencia no fue significativa.
El nivel de dolor reportado en los 15min posteriores a la sesión de fotocoagulación mostró una disminución de 5 en el grupo del nepafenaco (p=0.001) y con una reducción de un 25 (p<0.001) en el grupo del diclofenaco. Los niveles de dolor reportados a los 15min posteriores al tratamiento disminuyeron de manera estadísticamente significativa para ambos grupos, siendo clínicamente significativo únicamente para el grupo de diclofenaco.
Se pudo observar que ambos medicamentos fueron eficaces en reducir el dolor asociado a la FCP de forma inmediata y a los 15min, con tendencia no significativa de manera estadística o clínica a una mayor disminución del dolor de forma inmediata en el grupo nepafenaco y una mayor disminución a la reducción del dolor a los 15min en el grupo del diclofenaco. Aunque se observó una tendencia hacia un mejor efecto analgésico inmediato del nepafenaco (atribuido a su alto coeficiente de permeabilidad intraocular) y una la tendencia hacia un menor nivel de de dolor a los 15min en el grupo diclofenaco (aunque con un coeficiente menor de penetración intraocular, lograría niveles de analgesia aceptables) las diferencias entre los 2 grupos en el inmediato posterior a la FCP y a los 15min no fueron estadística ni clínicamente significativas; por lo que en general podríamos decir que ninguno de los 2 AINE fue mejor que el otro en ningún tiempo de evaluación.
En el análisis del número de ojos tratados relacionado con el nivel de dolor inmediato y a los 15min posteriores al tratamiento con láser argón en retina, el nivel de dolor reportado fue en ambos tiempos mayor cuando se trató solamente un ojo, a pesar de que el total de energía aplicado fue, como era de esperarse, mayor cuando se trataron 2 ojos. No existió una diferencia significativa para el total de energía aplicada entre los grupos o para el nivel de dolor reportados entre género femenino o masculino (figs. 1 y 2). Asimismo, no hubo una correlación entre el total de energía aplicada y el dolor inmediato o a los 15min en ninguno de los 2 grupos. El dolor asociado a la FCP se atribuye a la estimulación de los nervios ciliares que corren por el espacio supracoroideo, así que la variación en la percepción de dolor la podríamos explicar no solo con la cantidad de energía aplicada (y por tanto con el tratamiento de uno o 2 ojos), sino también con el tratamiento de los meridianos horizontales (y por tanto del sitio anatómico de los nervios cililares) y con otras variables como el tamaño y duración del «spot» del láser25.
Los síntomas posteriores al tratamiento de fotocoagulación láser en retina más comunes para ambos grupos fueron, en orden de frecuencia, el deslumbramiento, lagrimeo, cefalea y ardor de ojos, sin haber diferencia significativa para cada uno de ellos entre los grupos. Así, aunque los síntomas fueron frecuentes hasta en el 80% de los pacientes en ambos grupos, solamente la sensación de cuerpo extraño fue de manera significativa más frecuente en el grupo del nepafenaco.
Una limitación del presente estudio es que no se estudió el nivel de dolor posterior a la sesión de fotocoagulación retiniana con láser argón más allá de los 15min posteriores al mismo. La farmacodinamia del nepafenaco presume un tiempo en inhibición de síntesis de prostaglandinas hasta por 4-6h contra un tiempo máximo de inhibición de prostaglandinas a los 20min posteriores a su aplicación. Estudios posteriores pudieran comparar la eficiencia en la reducción de dolor de ambos fármacos en tiempos ulteriores a los 15min del tratamiento de fotocoagulación retiniana. Igualmente, una limitación metodológica del estudio reside en la dificultad para establecer una correlación directa entre el uso del AINE tópico y la incidencia de síntomas asociados a la finalización del tratamiento con fotocoagulación retiniana, debido a la existencia de múltiples variables que podrían intervenir en la percepción de los mismos síntomas (p. ej. variación en el uso y manipulación de lente de contacto panfundoscópico, uso de solución viscosa para la adaptación del lente). El uso de anestésico tópico previo al procedimiento con la finalidad de adaptar el lente panfundoscópico pudiera ser una variable de confusión para la valoración objetiva del dolor asociado a la FCP. Sin embargo, la farmacodinamia del clorhidrato de tetracaína permite aplicar anestesia local y superficial de corta duración (10-15min)26 con una muy baja penetración en córnea y segmento anterior, sin una penetración significativa en segmento posterior y por tanto efecto sobre el sitio de inicio del estímulo doloroso en la FCP (nervios ciliares supracoroideos)26,27.
Asimismo, aunque éticamente debatible por la falta de evidencia conclusiva sobre la superioridad del diclofenaco sódico tópico 0.1% contra el placebo, la existencia de un grupo controlado con placebo proveería un mayor poder a los hallazgos de diferencia entre los 2 grupos de AINE tópico.
En conclusión, no existió una diferencia significativa en el nivel de dolor reportado de manera inmediata y a los 15min posteriores al tratamiento de fotocoagulación láser argón entre el grupo tratado con nepafenaco y el grupo tratado con diclofenaco. Se observó una tendencia no significativa (estadística o clínica) a un menor nivel de dolor justo al terminar el tratamiento en el grupo de nepafenaco y un menor nivel de dolor a los 15min posteriores al tratamiento en el grupo de diclofenaco. El tratamiento previo a la FCP utilizando AINE (nepafenaco y diclofenaco) mostró eficacia al reducir el dolor asociado a la FCP con láser argón. Con respecto a la seguridad, no existieron diferencias significativas para los efectos adversos o síntomas asociados entre los grupos a excepción de la sensación de cuerpo extraño (más común en el grupo del nepafenaco). A pesar de reportarse síntomas posteriores al tratamiento en una gran mayoría de los pacientes en ambos grupos, no se reportaron efectos adversos de consideración, resolviéndose todos sin complicaciones.
Responsabilidades éticasProtección de personas y animalesLos autores declaran que los procedimientos seguidos se conformaron a las normas éticas del comité de experimentación humana responsable y de acuerdo con la Asociación Médica Mundial y la Declaración de Helsinki.
Confidencialidad de los datosLos autores declaran que han seguido los protocolos de su centro de trabajo sobre la publicación de datos de pacientes.
Derecho a la privacidad y consentimiento informadoLos autores han obtenido el consentimiento informado de los pacientes y/o sujetos referidos en el artículo. Este documento obra en poder del autor de correspondencia.
FinanciamientoEsta investigación no recibió financiamiento o subsidio de ninguna agencia pública, comercial o derivada de sectores privados.
Conflicto de interesesLos autores declaran no tener conflicto de intereses con los materiales presentados en la investigación.