¿ INTRODUCCIÓN
De las patologías que afectan al retro peritoneo, excluyendo la patología intrínseca de órganos situados en ese espacio, se encuentran como los más frecuentes: la fibrosis retroperitoneal idiopática (FR), los abscesos retroperitoneales y la patología tumoral primaria. En 1905 Albarán y en 1948, John K. Ormond describen a la fibrosis retroperitoneal como un proceso fibrótico que tiende a atrapar los uréteres.1,2 La fibrosis retroperitoneal se divide en idiopática (FRI) o secundaria (FRS) a ciertos fármacos, malignidades, infecciones y otros factores desencadenantes.3 Las principales características epidemiológicas de la FRI fueron investigadas en un estudio realizado en el año 2004 en Finlandia, el cual reportó una incidencia anual de 0.1 por 100 000 habitantes y una prevalencia de 1.4 por 100 000 habitantes. El pico de incidencia es en pacientes de 40 a 60 años de edad, con un predominio masculino, una relación hombre: mujer entre 2:1 y 3:1.4,5 La fibrosis retroperitoneal secundaria representa menos de la tercera parte de la FR. Existen diferentes condiciones y causas potenciales de FRS, como son el uso de ciertos medicamentos (metisergida, alcaloides derivados de la ergotamina, agonistas de dopamina), cáncer retroperitoneal primario (linfoma, sarcoma), enfermedad metastásica retroperitoneal (carcinoides, carcinomas), trauma, radioterapia, cirugía abdominal mayor e infecciones.3,6 La FRI no tiene causas identificables, aunque ha sido reportada en pacientes que sufren de enfermedades inflamatorias y autoinmunes que involucran otros órganos o estructuras, tales como, la tiroiditis autoinmune, pancreatitis autoinmune y lupus eritematoso sistémico.7
La FRI es un raro proceso inflamatorio crónico, que desarrolla una placa fibrótica localizada en el retroperitoneo que se extiende desde los pedículos renales hasta el reborde pélvico caudalmente y lateralmente hasta el reborde externo de los músculos psoas, produciendo obstrucción ureteral como síntoma más llamativo. Se distribuye alrededor de la aorta, aunque sin rodearla del todo, pudiendo llegar hasta la bifurcación aórtica e incluso a las ilíacas comunes. Existen casos atípicos de FRI en los que la masa fibrótica no está centrada en la aorta, sino que suele situarse justo al lado de la aorta o rodeando una arteria o vena importante, como el eje celiaco o la vena cava.8 La fibrosis está asociada con un infiltrado inflamatorio con aspectos histopatológicos peculiares, rico en linfocitos, células plasmáticas y macrófagos, así como una asociación al sistema HLA (HLA-DRB1-03).9,10 Se ha postulado que el origen de este proceso, puede ser debido a una reacción autoinmune frente a un antígeno, situado en las placas ateromatosas de la aorta, principalmente de la infrarenal y las ilíacas comunes.10 Existe un lípido insoluble (ceroide) que pasa al tejido peri-aórtico induciendo una respuesta inmune mediada por IgG.
¿ PRESENTACIÓN DEL CASO
Se trata de paciente femenino de 71 años de edad sin antecedentes de interés el cual inicia su padecimiento en julio del 2004 en León, España, con cefalea frontoparietal y occipital, vértigo de 24 horas de evolución, fotofobia, nauseas y vómito. También se agrega diarrea con heces de color claro, dolor abdominal difuso en hemi-abdomen inferior y ataque al estado general.
Presión arterial de 220/110, FR: 18x', FC: 98x', temperatura de 36.8º C. Consciente, orientada, afebril, cardiopulmonar sin alteraciones. Abdomen blando, depresible, doloroso en forma difusa en hemi-abdomen inferior, sin datos de irritación peritoneal y con peristalsis normal. Los exámenes de laboratorio del 29 de julio de 2004 muestran los siguientes datos: Hb 11.7 g, leucocitos 5800/mm3, plaquetas de 228000/mm3, TPT 31.5 seg, glucosa 86 mg/dL, creatinina 6.17 mg/dL, urea 145 mg/dL, TGO 15, TGP 16, GGT 33, Na 147 mEg/L, K 5.8 mEq/L, colesterol 189 mg/dL, triglicéridos 88 mg/ dL, fosfatasa alcalina 165, proteínas totales 6.9. Electro-cardiograma sin alteraciones. Telerradiografía de tórax del 29 de julio de 2004: cardiomegalia, pinzamiento de ambos senos costo frénicos. Ecocardiograma del 06 de agosto de 2004: fracción de eyección 68%, esclerosis mitral ligera con insuficiencia tricuspídea ligera, leve aumento de presión pulmonar, derrame pericárdico leve.
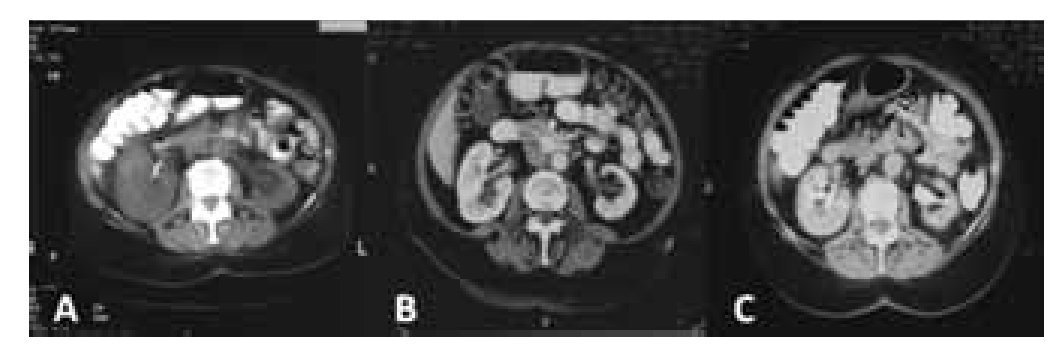
Tomografía axial computada (TAC) craneal del 30 de julio de 2004: normal. Ultrasonografía abdominal del 02 de agosto de 2004: ureteropielohidronefrosis bilateral, más importante del riñón derecho, vejiga de características normales. TAC de abdomen del 10 de agosto de 2004: ureteropielohidronefrosis bilateral, más acentuada en el sistema excretor derecho, en bifurcación de ilíaca, masa que rodea aorta y engloba a la vena cava inferior y ambos uréteres (Imagen 1). Se colocó catéter doble J derecho y se dio tratamiento con calcio antagonista.
Imagen 1. Tomografìa computada de abdomen: A) hidronefrosis bilateral (2004), B) ectasia moderada (2005), C) riñones normales (2006).
¿ MANEJO
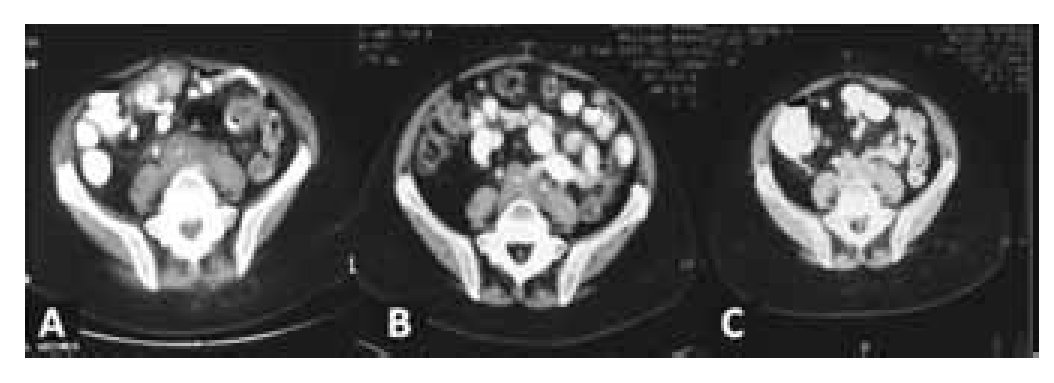
Se le realizó laparotomía exploratoria con toma de biopsia de masa retroperitoneal cuyo reporte en el trans operatorio fue: proceso linfoproliferativo con fibrosis, compatible con linfoma. Se colocó catéter doble J izquierdo. Se realizó estudio histopatológico definitivo, en el cual se observó tejido conectivo con zonas de fibrosis y bandas gruesas de colágeno; entre ésta es observaron células linfoides aisladas y agregadas, de las cuales son variable en forma y tamaño, con formación ocasional de centros germinales. Entre las mismas existen algunos macrófagos, así como agregados de células plasmáticas y eosinófilos. Focalmente se observó necrosis grasa con acúmulos focales de neutrófilos. Se determinó realizar estudio de inmunohistoquímica para confirmación de la policlonalidad del infiltrado linfoide, obteniendo tinciones positivas a linfocitos con CD45, CD20 y CD3. Con respecto a los eosinófilos y aislados neutrófilos, se obtuvo positividad a CD15; con los macrófagos fue positivo el CD68; para las células plasmáticas se presentaron positivos CD30, kappa y lambda. Resultado negativo a las pancitoqueratinas y el bcl-2, por lo que se descartó la posibilidad de linfoma, tanto Hodgkin como no Hodgkin, así como la posibilidad de carcinoma. Con los resultados obtenidos se decidió agregar al tratamiento prednisona, 20 mg diarios, la cual se disminuyó en forma gradual hasta alcanzar la dosis de 5 mg/día, con lo que se mostró mejoría en sus reportes de laboratorio: creatinina 1.31 mg/ml, BUN 24.3 mg/ml, ácido úrico 6.76 mg/ml, Hemoglobina 15 g, Hematocrito 44.2% y plaquetas de 179 000/mm3 del 11 de abril de 2007, con seguimiento a tres años sin reactivación de la fibrosis retroperitoneal (Imagen 2).
Imagen 2. Tomografía computada de pelvis. Comparación de la masa retroperitoneal a nivel de aorta e ilíacas comunes: A) 2004, B) 2005, C) 2006.
¿ DISCUSIÓN
La fibrosis retroperitoneal es una enfermedad poco común con la cual el proceso fibrótico involucra el retroperitoneo, rodeando la aorta por debajo del nivel de las arterias renales. La etiología de la FRI permanece dudosa, pero algunas drogas como la metisergida, hidralazina, betabloqueadores y los alcaloides derivados de la ergotamina, han sido asociados con esta enfermedad.11 Los hallazgos patológicos se presentan como un infiltrado inflamatorio que contiene macrófagos, linfocitos, células plasmáticas y ocasionalmente eosinófilos. Los macrófagos son a menudo una capa lipídica y la mayoría de las lesiones la contienen con áreas de infiltrado linfocítico perivascular compuesto por células tipo T y B. En este caso la demostración patológica de centros germinales de linfocitos, acompañados de macrófagos, así como de células plasmáticas y eosinófilos fueron determinantes en el diagnóstico de la fibrosis retroperitoneal, la cual se reforzó con estudio inmunohistoquímico para dichas células. Es posible que la periaortitis se desarrolle como una reacción inmune a los componentes de las placas ateroescleróticas.2,12 Estos compuestos pueden incluir oxidación de las lipoproteínas de baja densidad, material ceroide. La presencia de IgG en la ruptura de las placas ateroescleróticas puede dar sostén a esta posibilidad.12 El síntoma inicial más frecuente es el dolor hasta en el 90%, es dolor lumbar (40% a 60%) o abdominal (50%); es sordo e insidioso, además existen otras manifestaciones en el estadio temprano, tales como astenia, anorexia, pérdida de peso y fiebre. El cuadro clínico del estadio tardío es atribuible a la obstrucción ureteral progresiva, pudiendo llegar a la anuria. El deterioro general, la debilidad, la pérdida de peso y los trastornos gastrointestinales pueden constituir los primeros indicios de la enfermedad secundaria a uremia progresiva.13 En este caso de FRI, debutó con datos de uremia con elevación importante de azoados. Las alteraciones del laboratorio son inespecíficas, la elevación de la velocidad de sedimentación globular por encima de 30 mm/h, incremento de creatinina y urea. La ultrasonografía es la primera técnica diagnóstica realizada a estos pacientes, la cual posee gran sensibilidad para detectar dilatación pielocaliceal, como en nuestro reporte, pero poco sensible para detectar la placa fibrótica. La TC es la técnica más útil para el diagnóstico de confirmación, es variable, pudiendo localizarse en el medio, de forma simétrica o asimétrica, bien o mal definida o extensa; tras la administración de contraste intravenoso, la placa puede captarlo en mayor o menor medida, dependiendo de la vascularización. Varios medicamentos, tales como los corticoesteroides, tamoxifeno, azatioprina y ciclofosfamida, han sido recomendados para este propósito. Ross y Tinkler reportaron éxito con corticoesteroides basados en la presencia de células inflamatorias en la placa fibrosa.14 Actualmente, el tratamiento con corticoesteroides es la principal terapia para la FRI, pero la mayoría de los estudios son retrospectivos y no controlados.5 De cualquier forma, no hay un acuerdo en la literatura acerca de la dosis y duración de la terapia con esteroides. Varios esquemas usando esteroides con dosis de 20 a 60 mg, han sido propuestos, especialmente en el inicio del tratamiento. En una serie de 11 pacientes, se administró glucocorticoides con una dosis inicial de 60 mg diarios en días alternados durante los primeros dos meses, los cuales fueron disminuidos durante los siguientes dos meses a una dosis diaria de 5 mg. Este protocolo adicionaba alfa-bloqueadores y suplementos de calcio, con el intento de prevenir los efectos colaterales de las altas dosis de esteroides.11 En un estudio reciente en una cohorte grande de pacientes, los glucocorticoides se administraron en una dosis inicial de 60 mg diarios, durante 6 semanas y reducidos en los siguientes 2 a 3 meses a 10 mg diarios. La duración promedio del tratamiento fue de 1 año. Veintidós pacientes de los 24 seleccionados, reportaron reducción significativa de los síntomas y 19 experimentaron parcial o completa regresión de la masa. Se presentó recaída de la enfermedad en 13 pacientes después de la suspensión de los glucocorticoides.15 Nuestro esquema de tratamiento, aunque no tenemos un estudio de casos y controles, fue agregar prednisona 20 mg diarios por tres meses, dosis que se disminuyó gradualmente hasta 5 mg diarios en los siguientes 9 meses, obteniendo un resultado satisfactorio. Los glucocorticoides pueden ser usados como un modo de tratamiento primario para la FRI con respuesta satisfactoria en la mayoría de los pacientes. El seguimiento debe incluir tomografía a los 3 y 6 meses para evaluar la regresión de la masa. En un pequeño número de pacientes (8.3%), la masa retroperitoneal no remite y la ureterolisis quirúrgica podría ser requerida. Higgins y colaboradores sugieren dos grupos distintos: los pacientes seriamente enfermos que responden pobremente a la cirugía y la terapia de esteroides y un segundo grupo, en los que la obstrucción ureteral, a menudo unilateral, se desarrolla tempranamente y quienes podrían responder mejor al tratamiento con esteroides.16
¿ CONCLUSIÓN
La FRI es una enfermedad poco común de múltiples etiologías. Es una entidad generalmente diagnosticada en estadios avanzados, con una uropatía obstructiva importante (uni o bilateral) y en ocasiones con insuficiencia renal ya establecida. En fases iniciales puede ser útil el tratamiento médico, sin embargo, en etapas avanzadas está indicado el tratamiento quirúrgico apoyado con maniobras endourológicas. El esquema con esteroides puede ser usado como primera línea de tratamiento para la mayoría de los pacientes con mínimas complicaciones y su evaluación debe ser periódica por el resto de su vida.
Correspondencia:
Dr. Carlos Martínez Arroyo.
Servicio de Urología. Hospital Español de México.
Av. Ejército Nacional 613 - 702, Complejo Médico Antonino Fernández. Colonia Granada, 1520, México, D.F.
Teléfono y Fax: 5203-1779.
Correo electrónico: endouro@terra.com.mx