Revisar la concordancia entre patólogos en el diagnóstico de atipia epitelial plana de mama.
MétodosRevisión sistemática de artículos registrados en la base de datos de Pubmed, Scopus y Embase con los términos «pathologists» y «flat epithelial atypia», «flat epithelial atypia» e «interobserver variability», «interobserver agreement in flat epithelial atypia» (Scopus y Embase) y en la base de datos Lilacs con los términos en español «patólogos» y «atipia epitelial plana», buscando artículos con valoración de concordancia entre observadores en el diagnóstico de atipia epitelial plana mediante el coeficiente kappa. Se excluyeron artículos de revisión, resúmenes de congresos y comentarios.
ResultadosCon los términos de búsqueda se encontraron 140 publicaciones. De estas, se excluyeron 121 en el cribado por título y resumen. De la revisión restante de artículos completos, fueron seleccionados 5 para análisis cualitativo. Los valores kappa variaron desde un acuerdo regular, kappa=0,39 en residentes y patólogos en entrenamiento sin aplicación de tutorial hasta un acuerdo casi perfecto de 0,83 en patólogos con un interés especial en patología mamaria y tutorial previo.
ConclusionesEste estudio revisa la reproducibilidad entre observadores en el diagnóstico de atipia epitelial plana en biopsias de mama. Una baja concordancia puede darse principalmente en centros que no disponen de patólogos experimentados. Un proceso de enseñanza previo reduce la posibilidad de error, pero preferentemente se deberían remitir estos casos a centros especializados para revisión y diagnóstico.
To review the agreement between pathologists in the diagnosis of flat epithelial atypia of the breast.
MethodsWe performed a systematic review of articles with the terms “pathologists” and “flat epithelial atypia”, “flat epithelial atypia” and “interobserver variability” registered in the Pubmed, Scopus and Embase databases, those with the terms “interobserver agreement in flat epithelial atypia” in Scopus and Embase, and those with the terms “pathologists” and “flat epithelial atypia” in the Lilacs database. We sought articles with interobserver variability assessment in the diagnosis of flat epithelial atypia using the kappa coefficient. We excluded review articles, conference abstracts and comments.
ResultsA total of 140 publications were identified with the search terms. Of these, 121 were excluded in the screening after reading the title and abstract. Of the remaining review of full-text articles, 5 were selected for qualitative analysis. The kappa values ranged from fair agreement, Kappa=0.39 in residents and pathologists in training not receiving prior training, to near perfect agreement of 0.83 in pathologists with a special interest in breast pathology and prior training.
ConclusionsThis study reviews the interrater agreement in the diagnosis of flat epithelial atypia in breast biopsies. Low reproducibility occurs mainly in centres without experienced pathologists. A prior teaching process reduces the possibility of error, but these cases should preferably be referred to specialised centres for review and diagnosis.
En el año 2003 la Organización Mundial de la Salud1 determinó los aspectos diagnósticos de la atipia epitelial plana (FEA, por sus siglas en inglés [flat epithelial atypia]). La misma entidad, en 2019, caracteriza estas lesiones en el reemplazo de las células epiteliales nativas de las unidades ducto-lobulares por acinos dilatados, agrandados cuyos contornos son más redondeados y revestidos por una a varias capas de células de cuboidales a columnares levemente atípicas con núcleos que semejan los núcleos monomórficos del carcinoma ductal in situ de bajo grado2.
Es una lesión rara que se manifiesta esencialmente con microcalcificaciones en la mamografía3–7, se reporta en el 2,4% de las biopsias benignas de mama8 y coexiste frecuentemente con lesiones de alto riesgo especialmente con hiperplasia ductal atípica (27-53%)9–12, pero también se puede acompañar de neoplasia lobular e incluso de carcinoma in situ e invasivo12.
La biopsia percutánea con aguja gruesa (trucut) es un procedimiento muy utilizado para el diagnóstico de la patología mamaria13–15. En general, su rendimiento diagnóstico y baja tasa de complicaciones, mínima incisión, aceptación16 y facilidad de la técnica en un ámbito de atención ambulatorio inciden en su elección. Sin embargo, la FEA puede ser difícil de diagnosticar y se pueden pasar por alto lesiones de alto riesgo o cáncer lo cual soporta la recomendación tradicional de realizar posteriormente una biopsia por escisión que reduzca esta posibilidad7,13. De manera alterna, algunos servicios reemplazan las biopsias de aguja trucut por el uso de biopsias asistidas por vacío que permiten un mayor volumen de tejido para estudio patológico y después con el diagnóstico de FEA proceden, previo concepto del equipo multidisciplinario, a su escisión también asistida por vacío como alternativa a la biopsia abierta en casos sin atipia residual o baja sospecha de alteraciones en la arquitectura15. En cualquier opción, conocer la reproducibilidad del diagnóstico de FEA se hace importante para los cirujanos que confían en la interpretación que hace el patólogo para guiar sus recomendaciones de manejo7. Este estudio revisa los estudios que valoran la consistencia del diagnóstico histológico de FEA de mama mediante el coeficiente kappa.
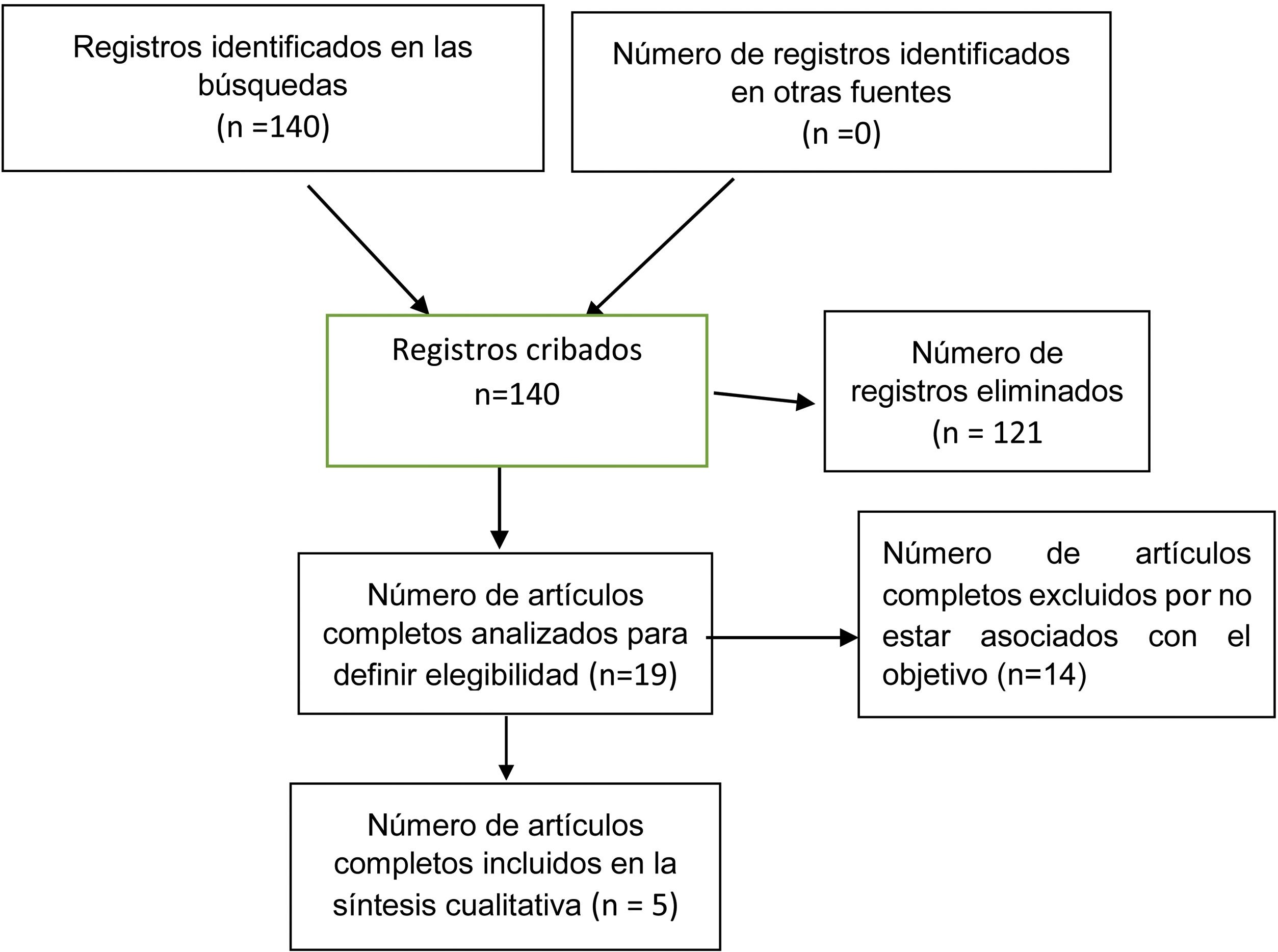
MétodosRevisión sistemática de artículos registrados en la base de datos de Pubmed, Scopus y Embase con los términos «pathologists» y «flat epithelial atypia», «flat epithelial atypia» e «interobserver variability», «interobserver agreement in flat epithelial atypia» (Scopus y Embase), y en la base de datos Lilacs con los términos en español «patólogos» y «atipia epitelial plana», sin uso de filtros, entre el 9/07/2020 y el 26/07/2020 buscando artículos con evaluación de variabilidad entre observadores mediante el coeficiente kappa en el diagnóstico de FEA. Se excluyeron artículos de revisión, resúmenes de congresos y comentarios. Los términos de búsqueda fueron aportados por el autor; con otro revisor se seleccionaron los artículos pertinentes al objetivo de la investigación, según el título, o por información adicional del resumen. Las discrepancias se solventaron con revisión del artículo completo y mutuo acuerdo. En los artículos que continuaron en evaluación el autor revisó el artículo completo para asegurarse de la pertinencia de los artículos con el objetivo de la investigación. En la figura 1 se muestra el flujo de información a través de las diferentes fases de la revisión sistemática.
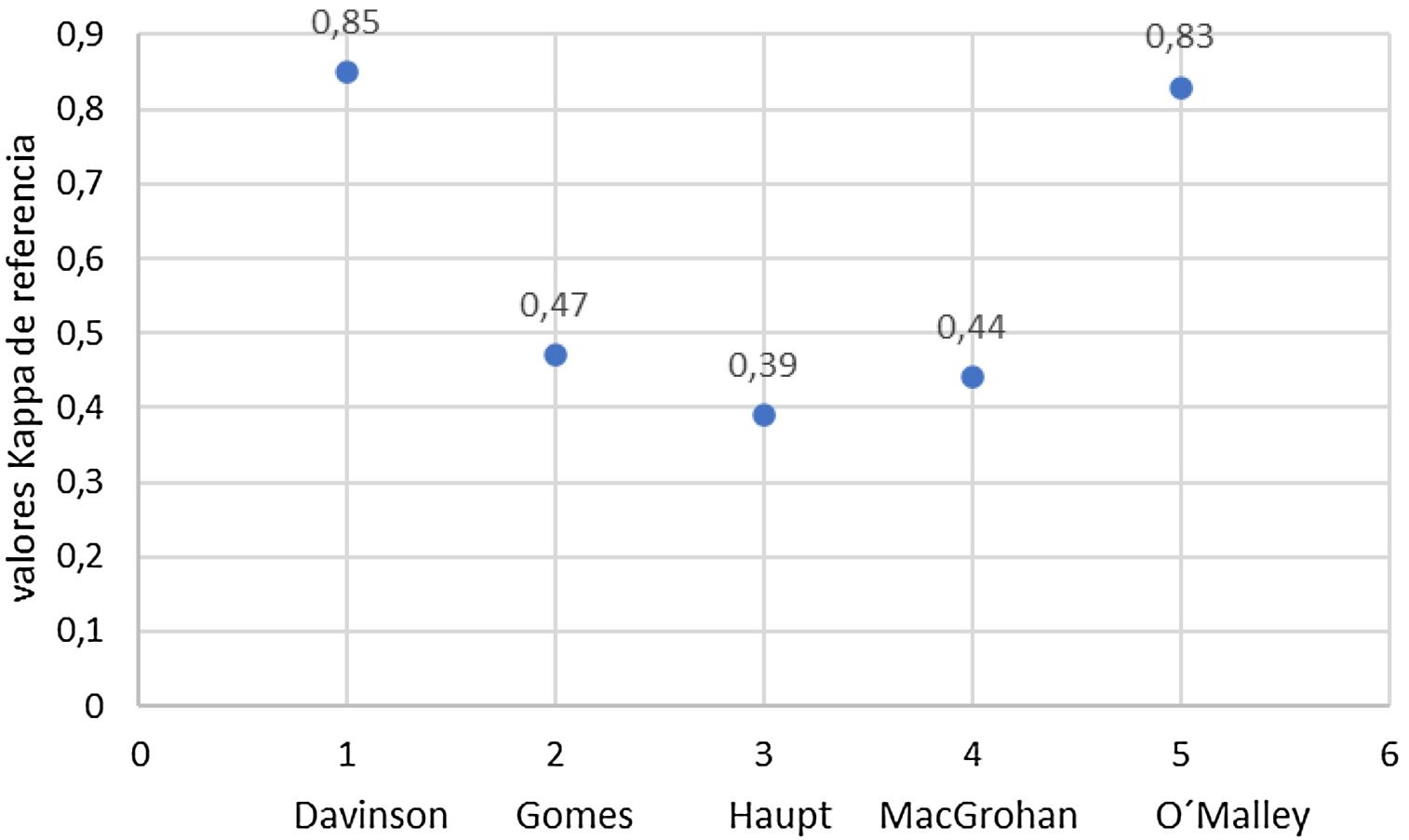
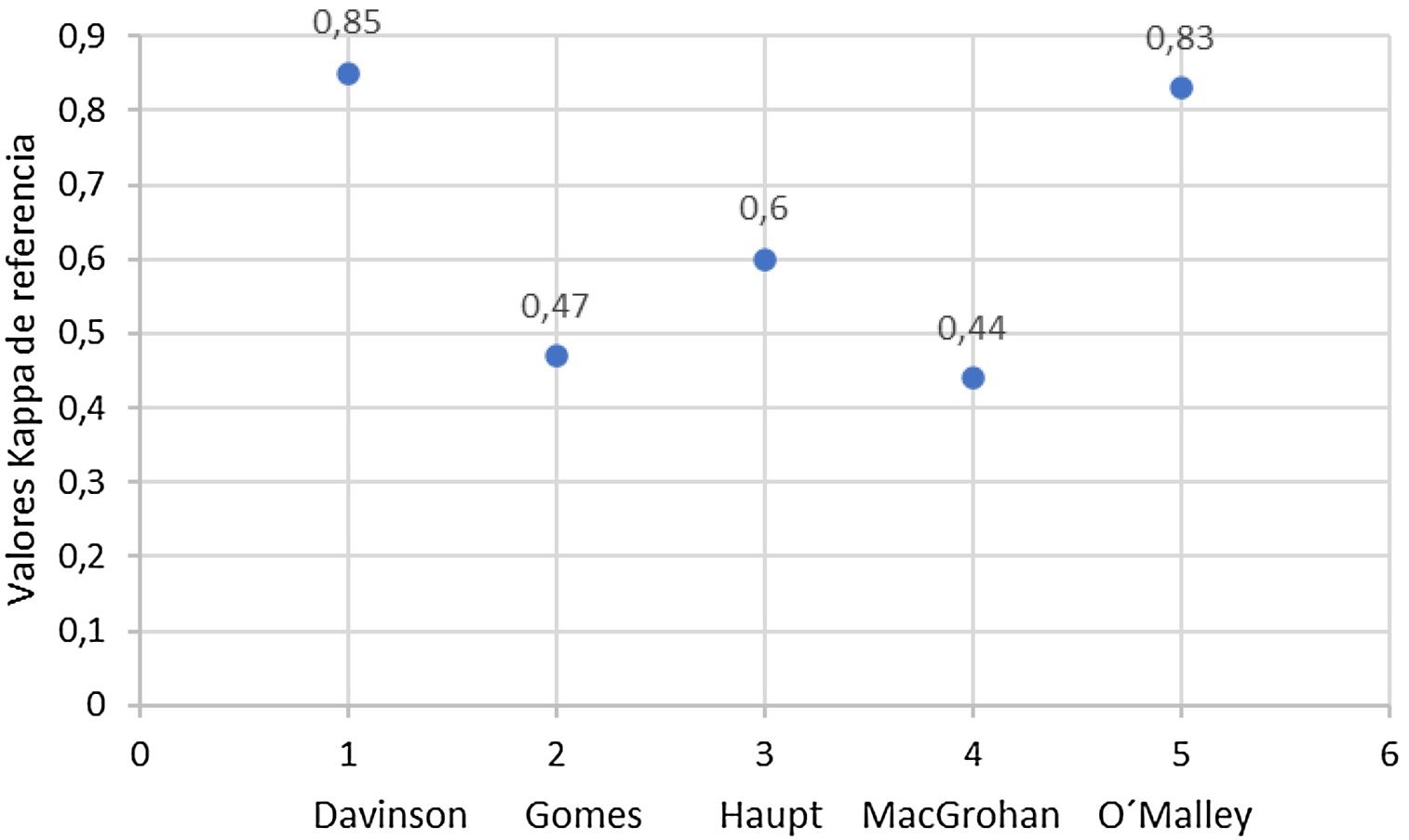
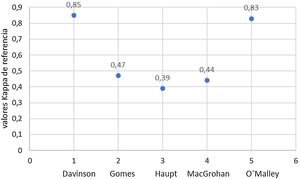
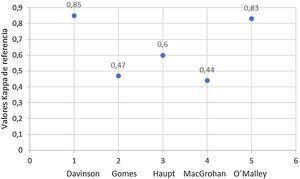
ResultadosCon los términos de búsqueda se encontraron 140 publicaciones. De estas, se excluyeron 121 en el cribado por título y resumen, 54 de ellas por tratarse de artículos repetidos en la búsqueda. Las demás se excluyeron por no corresponder al objetivo de la investigación o formar parte de los criterios de exclusión. De la revisión restante de artículos completos, fueron finalmente seleccionados 5 para análisis cualitativo los cuales se resumen en la tabla 1. Los valores kappa se calificaron de acuerdo con la tabla 2 y sus resultados iniciales se resumen en la figura 2 y en la figura 3 después del tutorial evaluado en el trabajo de Haupt et al.17y la evaluación de inmunohistoquímica CK5 / 6 y E-cadherina en el estudio de MacGrogan et al.18.
Características y valores del coeficiente kappa en los estudios seleccionados
| Autor | Casos | Material evaluado | Número de patólogos | Tipo | Kappa | Aspectos metodológicos |
|---|---|---|---|---|---|---|
| Haupt et al.17 | 8 | Casos de examen para lesiones de células columnares | 16 | Dos patólogos con experiencia en patología mamaria vs. 14 residentes y subespecialistas en entrenamiento de patología | 0,390,60 | Antes y después de tutorial del grupo en entrenamiento |
| MacGrogan et al.18 | 6 | Biopsias por escisión o biopsias asistidas por vacío | 20 | Patólogos de 16 hospitales de la red francesa contra el cáncer y 2 hospitales universitarios, un hospital belga y un laboratorio privado | 0,440,44 | Se evaluó concordancia con láminas de hematoxilina-eosina y con inmunohistoquímicaCK5/6 y E-cadherina |
| Darvishian et al.19 | 12 | Atipia en biopsia trucut | 4 | Patólogos dedicados o con experiencia en patología mamaria | 0,85 | Casos institucionalesSe hizo tutorial previo |
| O’Malley et al.20 | 14 | Imágenes con lesiones de células columnares | 8 | Patólogos con interés en patología mamaria, un patólogo de referencia | 0,83 | Se hizo tutorial previo. Imágenes en PowerPoint buscando distinguir FEA de lesiones celulares columnares no atípicas |
| Gomes et al.21 | 20 | Atipia en biopsia trucut | ND | Patólogo con experiencia y entrenamiento en patología mamaria vs. informes de patólogos generales | 0,47 | Casos recibidos para segunda opinión |
ND: no se define.
Interpretación de valores kappa de referencia
| Valores kappa | <0 | 0.00-0.19 | 0.20-0.39 | 0.40-0.59 | 0.60-0.79 | 0.80-1.00 |
| Interpretación | Sin acuerdo | Acuerdo bajo | Acuerdo regular | Acuerdo moderado | Acuerdo sustancial | Acuerdo casi perfecto |
Fuente: McGrogan et al.18.
En los artículos seleccionados las evaluaciones de concordancia se hicieron entre patólogos dedicados, con experiencia o interés en patología mamaria en 2 publicaciones19,20, con patólogos generales21 o en período de formación17 en una, y en una publicación no fue establecida18. Los casos estudiados fueron de pacientes institucionales en 3 publicaciones e imágenes docentes de referencia en 2.
DiscusiónLa FEA es un dilema para patólogos y clínicos5, las biopsias percutáneas con aguja 14G (aguja gruesa, trucut) generan dificultad en el diagnóstico por la pequeña cantidad de tejido que obtienen y la subjetividad inherente al diagnóstico de atipia19. La presencia frecuente de otras lesiones benignas proliferativas atípicas y en ocasiones incluso carcinomas in situ e invasivos de bajo grado como carcinomas tubulares20 derivaron en la recomendación de realizar biopsia por escisión después de la biopsia diagnóstica percutánea. Sin embargo, la baja asociación con carcinoma y la opción de biopsias asistidas por vacío que permiten mayor tejido para análisis han abierto la opción de plantear la escisión percutánea asistida por aspiración en casos seleccionados15. En cualquier opción se requiere de un diagnóstico patológico confiable, pero en un estudio lo que se observó fue una extensa y preocupante variabilidad en el uso del término FEA7. Para evaluar la confiabilidad de un diagnóstico una de las herramientas estadísticas es el valor kappa de concordancia entre observadores que busca medir que los diagnósticos realizados sean realmente los correctos22.
Al evaluar la concordancia para atipias epiteliales planas en los estudios seleccionados se encuentra que hay un acuerdo casi perfecto entre patólogos con dedicación o experiencia en patología mamaria cuando se incluye un tutorial previo sobre el tema como se valoró en los estudios de Darvishian et al.19, y en el de O’Malley et al.20; aunque entre ellos difieren en el tipo de material evaluado, en el primero son pacientes institucionales y en el segundo material docente, se puede asumir que con la definición de la patología incluida en el tutorial se puede identificar bien la lesión. Es de anotar, sin embargo, que a pesar del acuerdo diagnóstico en el material de la biopsia trucut presente en el estudio de Darvishian et al.19, la biopsia por escisión realizada posteriormente encontró 2 casos de carcinoma ductal in situ.
La inclusión de un tutorial también mejoró de la reproducibilidad diagnóstica en residentes y subespecialistas en entrenamiento, pasando de kappa 0,39(acuerdo regular) a conseguir un acuerdo sustancial (kappa 0,60)17.
El diagnóstico de FEA presenta dificultades diagnósticas, lo que puede resultar en la práctica clínica en que no se diagnostiquen estas lesiones cuando realmente existen, principalmente entre patólogos generales, pero también ocurren falsos diagnósticos ante la presencia de otras lesiones21 dado que la clasificación patológica de las proliferaciones epiteliales no invasivas en los análisis morfológicos es difícil incluso para patólogos experimentados en mama18 por lo que se sugiere que las diferencias entre FEA, hiperplasia de células columnares, hiperplasia ductal usual e hiperplasia ductal atípica se discutan ampliamente durante la revisión del caso clínico7.
ConclusionesLa reproducibilidad diagnostica para la FEA mejora con un proceso educativo previo en el cual se precisen los criterios histológicos. Las entidades proliferativas de mama en general se deben orientar a patólogos con dedicación o experiencia en mama con facilidad para llevar a cabo una discusión de estos casos.
Responsabilidades éticasProtección de personas y animalesEl autor declara que para esta investigación no se han realizado experimentos en seres humanos ni en animales.
Confidencialidad de los datosEl autor declara que han seguido los protocolos de su centro de trabajo sobre la publicación de datos de pacientes.
Derecho a la privacidad y consentimiento informadoEl autor declara que en este artículo no aparecen datos de pacientes.
FinanciaciónEl autor declara no haber recibido financiación para este trabajo.
Conflicto de interesesEl autor declara no tener ningún conflicto de intereses.