El diagnóstico de las lesiones mamarias se realiza de forma multidisciplinar entre clínicos, radiólogos y patólogos. La citología por punción-aspiración con aguja fina de la mama es un procedimiento técnicamente simple, barato, de resultados inmediatos, cuya efectividad ha sido probada en el manejo de pacientes con enfermedad mamaria. Desde la introducción del screening mamográfico, la mayoría de dichas lesiones se aspiran en estadios premalignos o preinvasivos. Su interpretación citológica puede ser muy difícil y requerir estudios posteriores, como la core-biopsia. A pesar de estas limitaciones, la citología mamaria sigue siendo la técnica de elección para el estudio de ganglios axilares, lesiones metastásicas y recidivas.
The diagnosis of breast lesions is multidisciplinary, with participation by clinicians, radiologists, and pathologists. Fine-needle aspiration cytology of the breast is a technically simple and inexpensive procedure and the results can be made available immediately. This procedure can improve the management of patients with breast disease. Since the introduction of mammographic screening, more breast lesions are being detected and aspirated at a premalignant or preinvasive stage. Cytological interpretation of the findings can be very difficult and requires further investigation such as core needle biopsy. Despite these limitations, breast cytology remains the technique of choice for the study of axillary lymph nodes, recurrences, and metastatic lesions.
El cáncer de mama es el más prevalente en la mujer en los países occidentales; la detección precoz y un diagnóstico adecuado son esenciales para un correcto manejo clínico.
La patología mamaria incluye un amplio espectro de lesiones: entidades no neoplásicas, tumores benignos y neoplasias malignas, hecho que implica que el diagnóstico citológico requiera un esfuerzo multidisciplinar entre radiólogos, patólogos y clínicos (triple test diagnóstico).
El estudio citológico de la mama se inició con la aspiración de células malignas por Sir James Paget en 1853. Desde entonces se ha extendido la popularidad de la técnica debido a la buena relación coste/efectividad, la calidad del procedimiento, el bajo índice de complicaciones, la rapidez y alta precisión diagnóstica, con una sensibilidad de entre el 80-100% y una especificidad de alrededor del 99%, según las series1,2.
En las 2 últimas décadas las campañas de screening radiológico poblacional detectan lesiones cada vez menores, premalignas o en estadios preinvasivos, que dificultan el diagnóstico citológico3. El problema que plantea la imposibilidad de diferenciar citológicamente entre carcinoma in situ o infiltrante, y los diagnósticos de atipia citológica, han mermado la utilización de esta técnica y potenciado el uso de la core-biopsia o biopsia con aguja gruesa (BAG), en el diagnóstico de la patología mamaria. La BAG permite valorar la estructura tisular, y en general tiene mayor sensibilidad y precisión diagnóstica, especialmente en lesiones sin claros criterios de benignidad o malignidad (zona gris o borderline) y lesiones no palpables y/o calcificadas, aunque en algún estudio comparativo la especificidad es menor en la BAG que en la punción-aspiración con aguja fina (PAAF)4,5.
A pesar de estos inconvenientes hay que tener en cuenta que la PAAF de lesiones mamarias es una técnica fácil de realizar y permite no solo el diagnóstico, sino también la indicación de tratamiento neoadyuvante preoperatorio mediante el estudio por punción de ganglios axilares, así como analizar el comportamiento biológico del tumor con biomarcadores como los receptores hormonales, el índice de proliferación o la expresión de Her2neu.
ProcedimientoLa PAAF no es difícil de realizar, pero requiere experiencia y correlación con la radiología y la clínica, de modo que es aconsejable que la punción se efectúe e interprete en el mismo lugar que dichos estudios. La técnica de la PAAF depende en gran parte de quién la efectúe, por lo que es muy importante la coordinación entre el diagnóstico clínico, el radiológico y el citológico, aplicando un triple test diagnóstico1. En lesiones no palpables la punción debe realizarse bajo control radiológico; en general, la celularidad aspirada es mayor en punciones guiadas por ecografía que en las estereotácticas. Los resultados del estudio por técnicas de imagen y del diagnóstico citológico han de ser concordantes; en caso contrario, debe proseguirse el estudio.
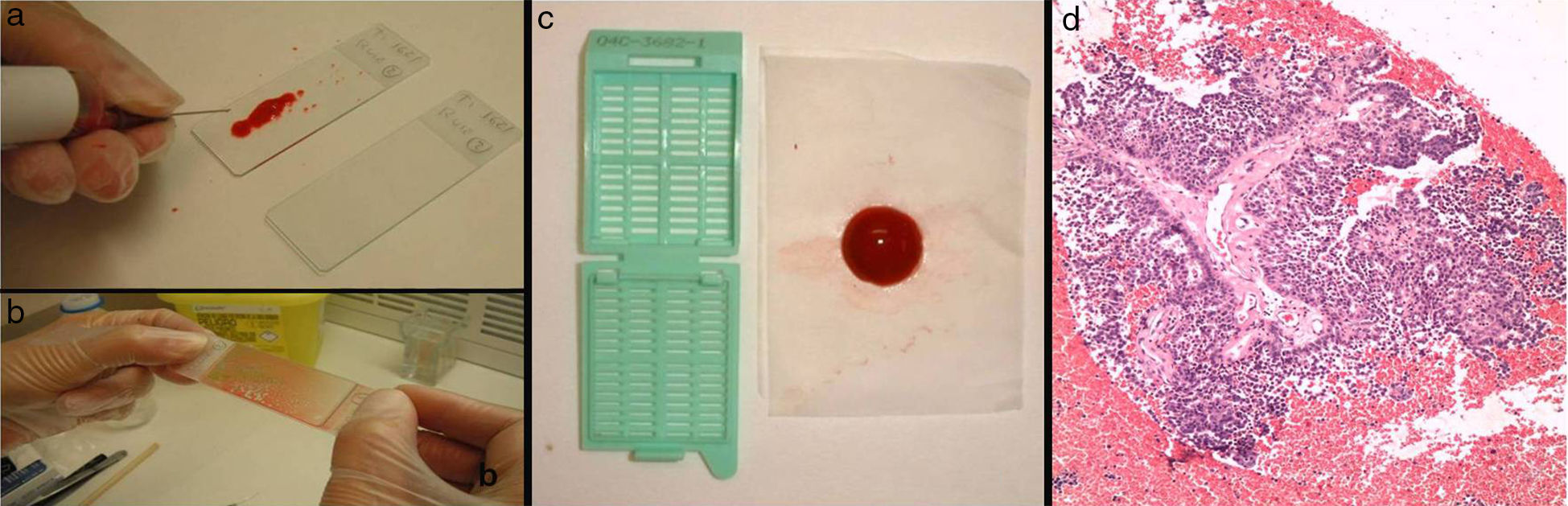
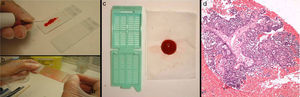
Para la punción se utilizan agujas de 23 o 25G y jeringuillas de 10-20mL. Una vez puncionada la lesión se realiza el vacío aspirando la jeringa y se moviliza la aguja dentro de la lesión. Antes de retirar la aguja de la lesión es importante dejar de hacer el vacío para que el material no se pierda en el interior de la jeringa. Para extraer el material, una vez retirada la aguja, se vuelve a hacer el vacío retirando el émbolo, se recoloca la aguja en la jeringa y se inyecta el aire aspirado de manera que el contenido quede depositado sobre un portaobjetos. El material se extiende y se puede fijar en alcohol de 96° para teñir con Papanicolaou, o dejar secar al aire para realizar tinción de Giemsa. Posteriormente se efectúa un lavado de la aguja con suero fisiológico que se centrifuga, y del sedimento se realiza un bloque celular que se fija en formol al 10% y se procesa como una biopsia (fig. 1). El bloque celular es útil para efectuar estudios complementarios y una reserva de material para posibles estudios futuros.
El líquido que se obtiene en las punciones de lesiones quísticas suele ser poco celular, y debe procesarse con citocentrífuga para recuperar el máximo número posible de células.
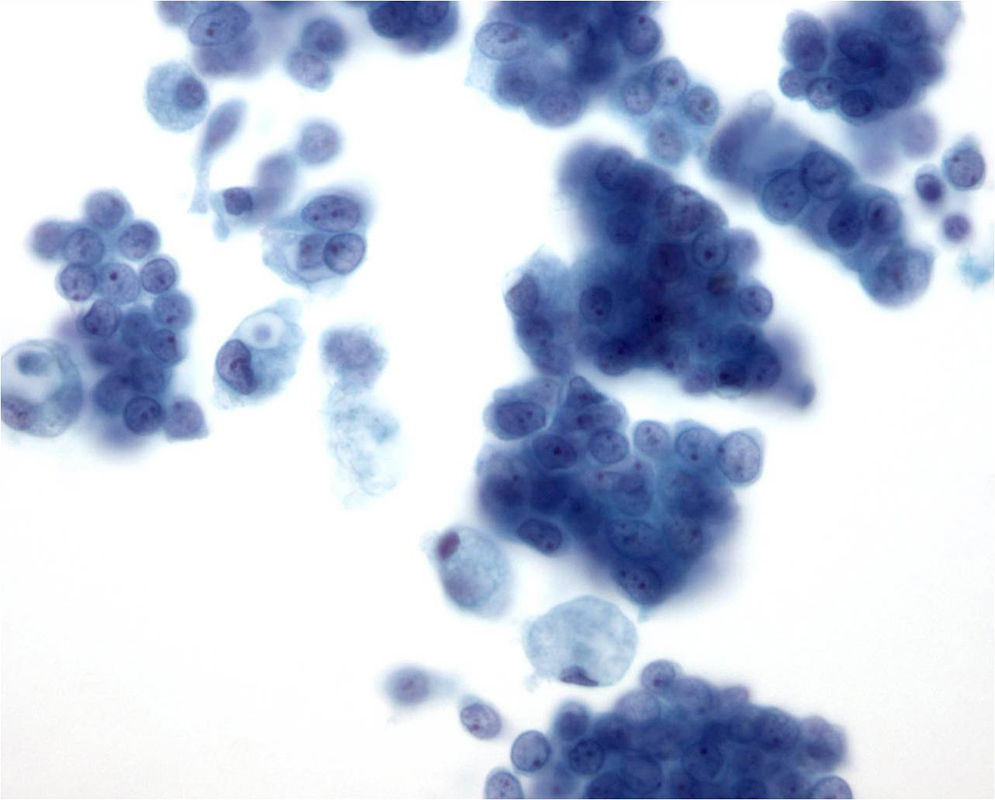
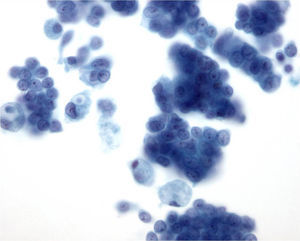
Últimamente ha aumentado la utilización de la citología líquida6, en la que el material aspirado se deposita en un recipiente con un medio líquido fijador, y posteriormente, por medio de unos filtros, se dispone sobre un portaobjetos, se fija en alcohol y se tiñe con Papanicolaou. Con este método los rasgos citológicos pueden ser diferentes a los de las extensiones convencionales7, pero el material se conserva bien para realizar estudios inmunocitoquímicos o moleculares. Una de las características de la citología líquida es que limpia el fondo de la preparación y dispone las células en monocapa8, lo que permite una mejor valoración de la morfología celular, aunque se pierde información del fondo, y las placas y fragmentos tisulares pueden quedar menos preservados que en las extensiones directas (fig. 2).
Otros estudios en patología mamaria incluyen la secreción del pezón, el lavado ductal9,10 y las improntas celulares, que pueden realizarse como estudio peroperatorio de los márgenes de resección de las tumorectomías y de los ganglios centinelas. Algunos autores postulan el beneficio de realizar improntas de las BAG11; en estos casos el estudio citológico da un diagnóstico rápido de benignidad o malignidad, o confirma si la muestra es adecuada o no para el diagnóstico, permitiendo una repetición inmediata en caso de discorrelación clínico/radiológica.
DiagnósticoEn 1996 el Instituto Nacional del Cáncer en Bethesda recomendó el uso de 5 categorías diagnósticas: benigno, atipia, sospechoso, maligno e insatisfactorio3.
En el informe citológico debería constar la idoneidad del material, tanto la cantidad del aspirado como la calidad de las extensiones y tinción. Se considera que el material es adecuado para diagnóstico cuando se observan 6 placas de células epiteliales con unas 15 células por placa1, aunque en general se necesitan más células para hacer un diagnóstico de benignidad que de malignidad. La presencia de abundante sangre o células inflamatorias en las extensiones también puede dificultar la valoración de la muestra.
La nomenclatura que suele utilizarse en el diagnóstico citológico, y que se corresponde con las categorías diagnósticas, es:
- -
Negativo para células malignas en lesiones benignas, si es posible añadiendo el tipo de lesión (quiste, fibroadenoma, inflamación, etc.).
- -
Células atípicas, indica que el material aspirado corresponde a un tipo de lesión que no puede tipificarse, en la que los hallazgos celulares son probablemente, pero no definitivamente, benignos, y que requiere estudios adicionales.
- -
Sospechoso para células malignas cuando faltan criterios de certeza para un diagnóstico de malignidad, ya sea por escasa representación celular o bien porque la celularidad está mal preservada u oculta por material hemático o inflamación, pero los hallazgos son altamente indicativos de malignidad.
- -
Positivo para células malignas cuando hay certeza de malignidad; en algunos casos se puede tipificar correctamente el tipo de neoplasia.
La terminología de lesión proliferativa, con o sin atipia, se utiliza en un espectro de lesiones que incluyen hiperplasia epitelial, adenosis, papilomas, cicatriz radial e hiperplasia ductal atípica12. El término zona gris o borderline13 hace referencia a este grupo de lesiones, que son difíciles de diferenciar de algunas variantes de carcinoma in situ.
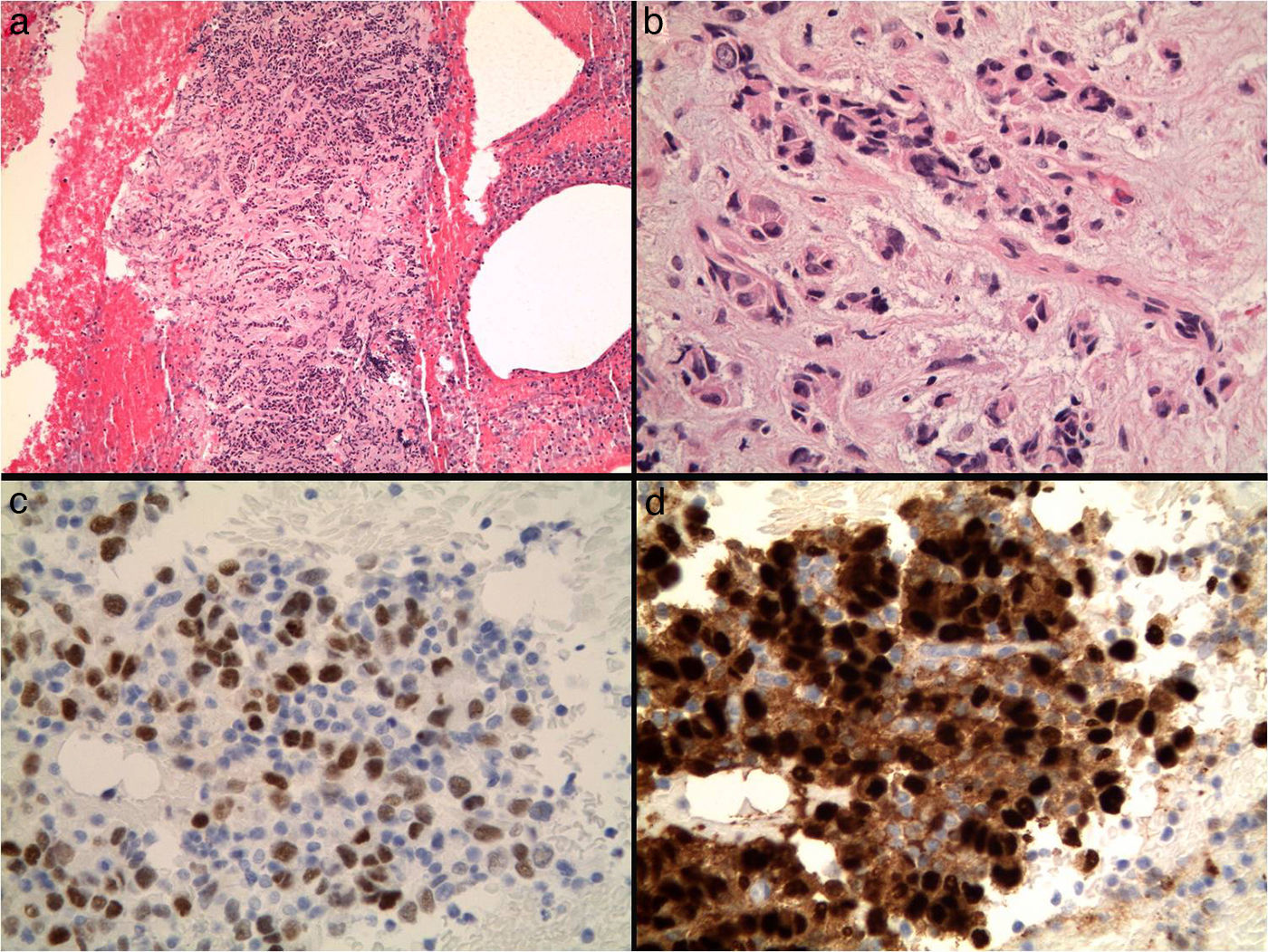
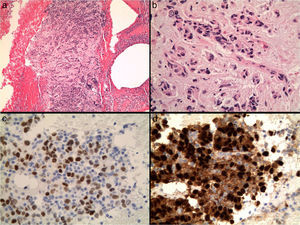
VentajasLa PAAF permite un diagnóstico rápido (en minutos), de bajo coste, con un procedimiento mínimamente invasivo que las pacientes aceptan fácilmente, tanto física como psicológicamente, con una alta sensibilidad y fiabilidad diagnóstica14. Evita la cirugía en lesiones benignas, permite planificar el tratamiento en cada paciente, evaluar las lesiones múltiples, diferenciar entre lesiones mamarias y ganglios linfáticos intramamarios, tomar muestras del tumor para realizar biomarcadores tumorales1,15, como receptores hormonales (fig. 3), índice de proliferación o expresión de Her2neu, o para estudios moleculares, como inestabilidad de microsatélites por técnicas de FISH en pacientes con alto riesgo de cáncer de mama16.
La PAAF está indicada en casi todas las lesiones mamarias, ya sean palpables o hallazgos radiológicos, con finalidad tanto diagnóstica como terapéutica. Permite el diagnóstico de neoplasias primarias benignas y malignas, tumores metastásicos, linfomas, lesiones epiteliales atípicas y procesos inflamatorios1.
En las lesiones quísticas, a la vez que diagnóstica, la PAAF se considera también terapéutica al evacuar el quiste. Si después de la evacuación del quiste persiste una masa residual, esta debe de ser nuevamente puncionada.
También está indicada en el diagnóstico de recidivas o para realizar una mejor estadificación en cáncer localmente avanzado17.
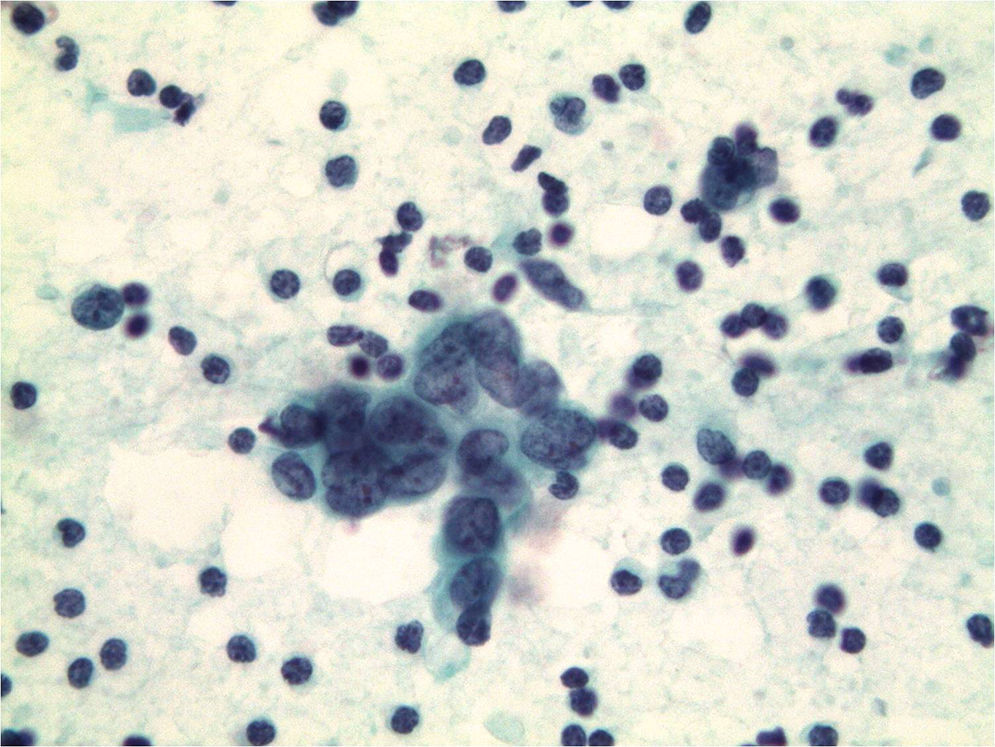
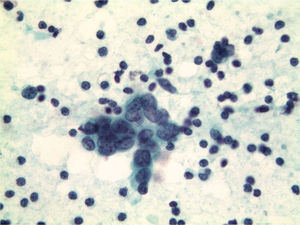
Otra importante indicación es la valoración de la afectación de los ganglios axilares (fig. 4) en el momento del diagnóstico, para planificar la conducta a seguir en cada caso, quimioterapia neoadyuvante en caso de afectación ganglionar o estudio de ganglio centinela en los casos negativos para malignidad11.
Asimismo, permite estudiar lesiones que no pueden explicarse desde un punto de vista fisiológico, sobre todo en pacientes jóvenes, y lesiones persistentes o sospechosas en pacientes con historia familiar.
La interpretación inmediata del resultado permite una rápida planificación del tratamiento, y en los casos de benignidad, reduce la ansiedad de la paciente.
LimitacionesUna de las principales limitaciones de la PAAF de mama es la imposibilidad de diferenciar el carcinoma in situ del infiltrante, importante para determinar el manejo clínico de la paciente. Algunos autores18,19 postulan que la infiltración estromal que puede verse en las extensiones, o sobre todo en secciones del bloque celular, podrían predecir la invasión tumoral (fig. 3).
Otra de las limitaciones es la dificultad diagnóstica de las lesiones proliferativas con atipia20, también conocidas como de la zona gris o borderline, principalmente la hiperplasia ductal atípica, difícil de diferenciar de carcinomas de bajo grado, ya que el diagnóstico específico se basa en el patrón arquitectural, que no puede apreciarse en las extensiones. También puede ser problemático el diagnóstico de lesiones como cicatrices radiales, adenosis esclerosante o atipia del epitelio plano. El diagnóstico de lesión proliferativa puede llegar a representar hasta un 10% de todos los diagnósticos1. Otras limitaciones son la tipificación de las lesiones papilares21, las lesiones mucinosas y la falta de un diagnóstico específico en las lesiones benignas.
Los diagnósticos erróneos «pitfalls»22 pueden ser debidos a que la lesión no está representada en el material aspirado, a un mal procesamiento de la muestra (artefacto de extensión, fijación o tinción), o por falta de comunicación entre la persona que realiza la punción y la que interpreta la citología12.
Las principales causas de diagnósticos falsos negativos son:
- -
Pequeños focos de carcinoma en el contexto de una lesión predominantemente benigna, como cambios fibroquísticos con metaplasia apocrina.
- -
Carcinoma originado en una lesión proliferativa compleja.
- -
Carcinomas bien diferenciados, algunos subtipos histológicos específicos, como carcinoma tubular o coloide, o algunos tipos de tumores poco frecuentes, tales como carcinoma metaplásico o apocrino.
- -
Carcinomas extensamente necróticos o quísticos.
- -
Errores de muestreo, sobre todo en lesiones pequeñas, profundas o con estroma desmoplásico
- -
Extensiones inadecuadas.
Las principales causas de falsos positivos son:
- -
Preparaciones subóptimas por artefacto de extensión o fijación que pueden exagerar los cambios celulares dando lugar a diagnósticos de atipia. La valoración de la muestra está limitada cuando las extensiones son poco celulares.
- -
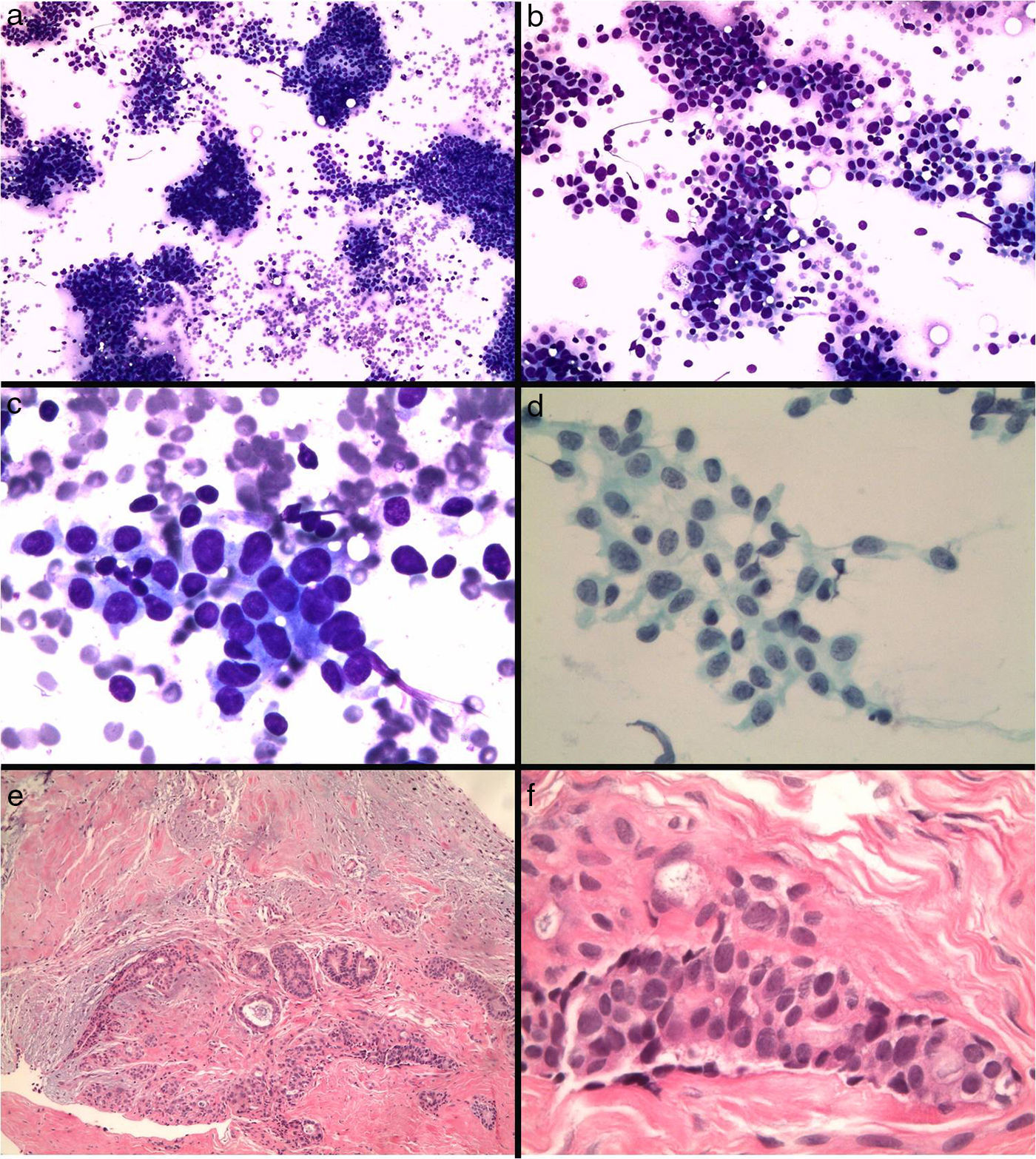
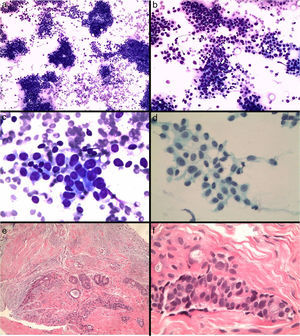
El fibroadenoma es la causa más frecuente de falsos positivos3,14,22 por la atipia que pueden presentar las células epiteliales, que pueden ser dominantes en las extensiones (fig. 5).
Figura 5.Fibroadenoma diagnosticado erróneamente de carcinoma. a y b) Extensiones citológicas muy celulares con células epiteliales que se disponen en placas y aisladas (Diff-Quick, ×10 y ×20). c) Células de núcleo grande, con nucléolo y alteración de la relación núcleo/citoplasma (Diff-Quick, ×40). d) Placa de células epiteliales con tendencia a la dehiscencia (Papanicolaou, ×40). e) El estudio histológico de la lesión muestra un fibroadenoma (hematoxilina-eosina, ×4), f) con marcada atipia del componente epitelial (hematoxilina-eosina, ×40).
(0.58MB). - -
Lesiones papilares.
- -
Cambios asociados a la lactancia o el embarazo22.
- -
Atipia reactiva14 por cambios epiteliales regenerativos asociados a mastitis, necrosis grasa, intervención quirúrgica o posradioterapia; en estos casos la información clínica es fundamental.
- -
Metaplasia apocrina.
- -
Tumores de anejos cutáneos.
El índice de falsos negativos es generalmente inferior al 5% en la punción de lesiones palpables, y de entre un 5-10% en las no palpables, índice mucho mayor que el de falsos positivos. La experiencia de quien realiza la punción y del citopatólogo disminuye los falsos positivos y negativos, y aumenta la precisión diagnóstica23. Todos los resultados falsos positivos o negativos deben seguirse con BAG guiada por radiología14,24.
La sensibilidad de la PAAF disminuye en lesiones pequeñas25, menores de 5mm, cada día más frecuentes, dada la mayor precisión de las técnicas de imagen, así como en los tumores que son predominantemente quísticos, necróticos o hemorrágicos. La desmoplasia de la lesión también dificulta la aspiración de células tumorales, que quedan atrapadas por la fibrosis. Asimismo, son difíciles de aspirar las lesiones que se localizan en planos profundos de la mama.
La incidencia de diagnósticos no concluyentes en citología mamaria varía entre un 4 y un 18% según las series, siendo los fibroadenomas y los cambios fibroquísticos las causas más frecuentes3.
ComplicacionesEl índice de complicaciones es generalmente mínimo, y cuando se producen son de índole menor. El más frecuente es el dolor, sobre todo en las punciones de la zona subareolar. La siembra de células tumorales en el trayecto de punción de la aguja es excepcional. Otras complicaciones incluyen hemorragia, hematomas, infección y reacción vagal en el momento de la punción. No se han descrito contraindicaciones de la técnica.
ConclusiónLa PAAF es una técnica simple, de bajo coste, que permite un diagnóstico rápido de alta efectividad, aunque la interpretación citológica de algunas lesiones mamarias puede ser difícil. Desde la introducción de programas de screening mamográfico ha aumentado la dificultad del diagnóstico citológico por la mayor proporción de carcinomas de bajo grado y lesiones proliferativas de pequeño tamaño detectadas. Debido a la menor efectividad de la PAAF en lesiones no palpables, esta suele reemplazarse por la BAG en el estudio de lesiones detectadas por screening, aunque precisa de más tiempo para poder emitir el diagnóstico y el coste es mayor en esta última. A pesar de la menor utilización de la PAAF, esta continúa siendo la técnica de elección para evaluar lesiones metastásicas, recidivas y realizar estudio de ganglios axilares.
Responsabilidades éticasProtección de personas y animalesLa autora declara que para esta investigación no se han realizado experimentos en seres humanos ni en animales.
Confidencialidad de los datosLa autora declara que en este artículo no aparecen datos de pacientes.
Derecho a la privacidad y consentimiento informadoLa autora declara que en este artículo no aparecen datos de pacientes.
Conflicto de interesesLa autora declara no tener ningún conflicto de intereses.