Introducción
Aproximadamente, 6,35 millones de nuevos casos de cáncer se diagnostican anualmente1. En nuestro país, a partir de la década de 1990, los tumores malignos son la segunda causa de muerte después de las enfermedades cardiovasculares. Hoy día, se estima que hay entre 60 y 80 casos por cada 100.0002. La prevalencia de dolor por cáncer es del 30% al momento de ser diagnosticadο, del 50% en pacientes que están siendo sometidos a tratamiento, y del 90% en pacientes que se encuentran con cáncer avanzado3. El 65% del dolor oncológico es causado por compromiso de estructuras orgánicas, provocado por el crecimiento tumoral. El 25% del dolor es causado por los diferentes tratamientos, como radioterapia, quimioterapia y cirugía. El resto presenta dolor atribuible a síndromes dolorosos crónicos comunes, como lumbalgias y cefaleas4.
El objetivo en el tratamiento del dolor oncológico es aliviar el dolor, interrumpiendo la transmisión o modulándolo a nivel cerebral o espinal. Se puede lograr con monoterapia o con combinaciones de diferentes tipos de fármacos5. La Organización Mundial de la Salud (OMS) desarrolló una escala de tres escalones para manejar el dolor oncológico, basada exclusivamente en la administración de agentes por la vía oral. En el escalón I se incluyen analgésicos no opiáceos + coadyuvantes; en el escalón II se incluyen opiáceos leves + coadyuvantes y en el escalón III se incluyen opiáceos potentes + coadyuvantes6. Los opiáceos son el patrón de oro para el manejo de dolor nociceptivo.
Los opioides endógenos naturales incluyen betaendorfinas, encefalinas y dinorfinas. En 1973 se descubrieron receptores opioides en el sistema nervioso central (SNC). Los receptores opioides tienen papeles integrales en el sistema antinociceptivo endógeno y están localizados a lo largo del SNC y los nervios periféricos7,8. Los tres receptores opioides mejor descritos son los receptores mu, kappa y delta. Estos se encuentran en el SNC, particularmente en el asta dorsal de la médula espinal, y en los nervios periféricos9. Un agonista opioide, al unirse al receptor, produce analgesia, así como efectos indeseables, como estreñimiento, somnolencia, náuseas y depresión respiratoria10.
La hidromorfona es un opiáceo semisintético, derivado de la morfina. Tiene una alta afinidad por el receptor mu. La hidromorfona es similar a la morfina: es hidrofílica y la vida media es similar. Es diferente en cuanto a los efectos adversos, ya que el prurito, la sedación, las náuseas y el vómito son menos frecuentes11. La dosis equianalgésica de la morfina con la hidromorfona va en un rango de 3:1 a 9:1, dependiendo de la vía de administración12. La latencia es de 30 min posterior a la administración oral del fármaco y 5 min después de la administración por vía intravenosa11. La hidromorfona se metaboliza en el hígado a hidromorfona 3-glucurónido (H3G) y es excretada por el riñón. Este metabolito H3G carece de efectos analgésicos y puede tener efectos neurotóxicos, como alodinia, mioclonías y convulsiones. La producción de este metabolito es relativamente baja, por lo que el riesgo de efectos secundarios neurotóxicos es muy baja13.
Nuestro objetivo fue reportar la dosis promedio efectiva de la hidromorfona en pacientes con dolor crónico oncológico en nuestra experiencia de 4 años en el Centro Médico Nacional "20 de Noviembre".
Material y métodos
Se trata de un estudio observacional, descriptivo, longitudinal y retrospectivo. Se revisaron 72 expedientes, en un total de 4 años, de todos los pacientes con dolor crónico oncológico que hayan estado en tratamiento con hidromorfona.
Los criterios de inclusión fueron: todos los pacientes con dolor oncológico tratados con hidromorfona en el servicio de clínica del dolor del Centro Médico Nacional "20 de Noviembre".
En este trabajo calculamos la dosis promedio en la que se logró un buen control del dolor (escala analógica visual [EVA] < 4). También se reportan los efectos adversos con mayor incidencia, así como si algún paciente abandonó el tratamiento y sus causas. En este estudio también se reportó el tipo de cáncer de cada paciente y el tiempo de tratamiento con hidromorfona.
El análisis estadístico se realizó con los programas Statistica 7, Epi Info 6.04 y Mini Tab 14. Para el análisis estadístico descriptivo se utilizaron: medidas de tendencia central: media, mediana, moda; medidas de dispersión: rango, desviación estándar, medidas de posición (percentiles 10, 25, 50, 75 y 90); gráficas de barras, box plots y circulares. Para el análisis estadístico inferencial se utilizaron intervalos de confianza (IC) del 95% para la proporción poblacional e IC del 95% para la media aritmética poblacional.
Resultados
En este estudio se revisaron 72 expedientes de pacientes con dolor oncológico que estuvieron en tratamiento con hidromorfona en los últimos 4 años: 30 varones y 42 mujeres.
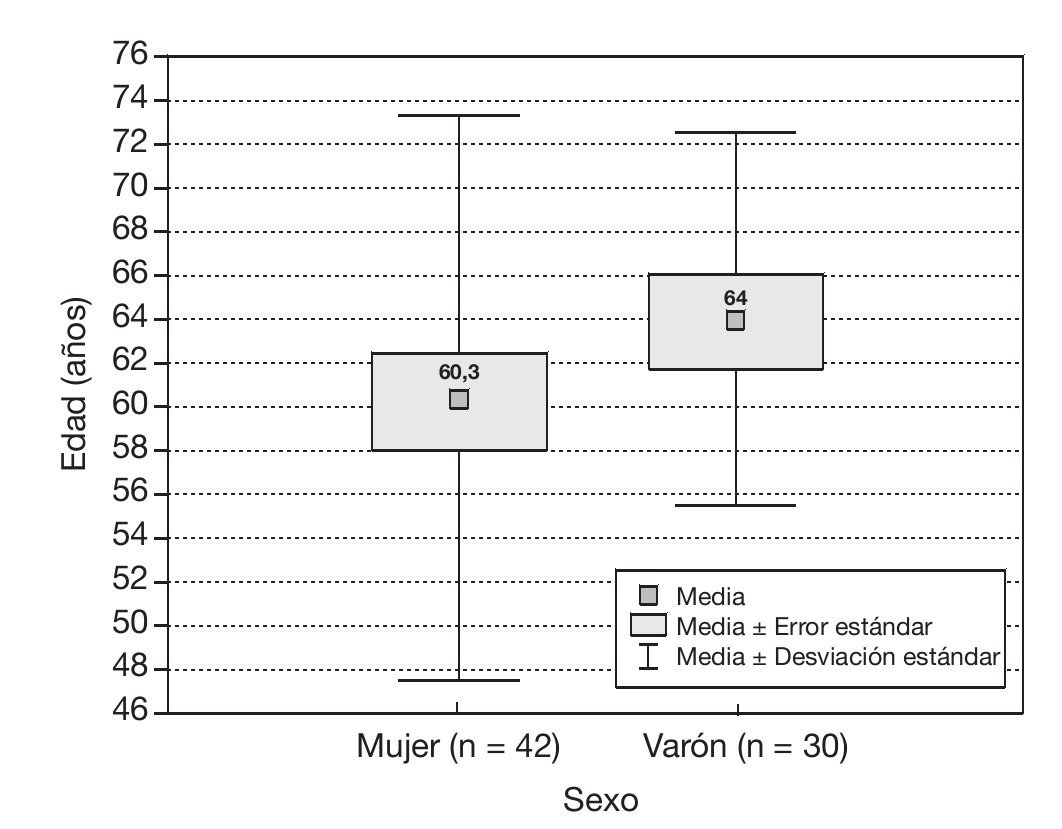
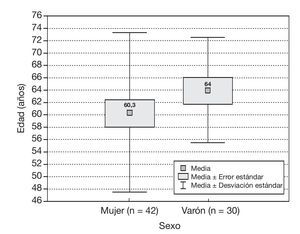
El rango de edad fue de 43 a 84 años, con una media de 62,23 + 11,3. La media de edad para las mujeres fue de 60,3 y para los varones de 64,0 años.
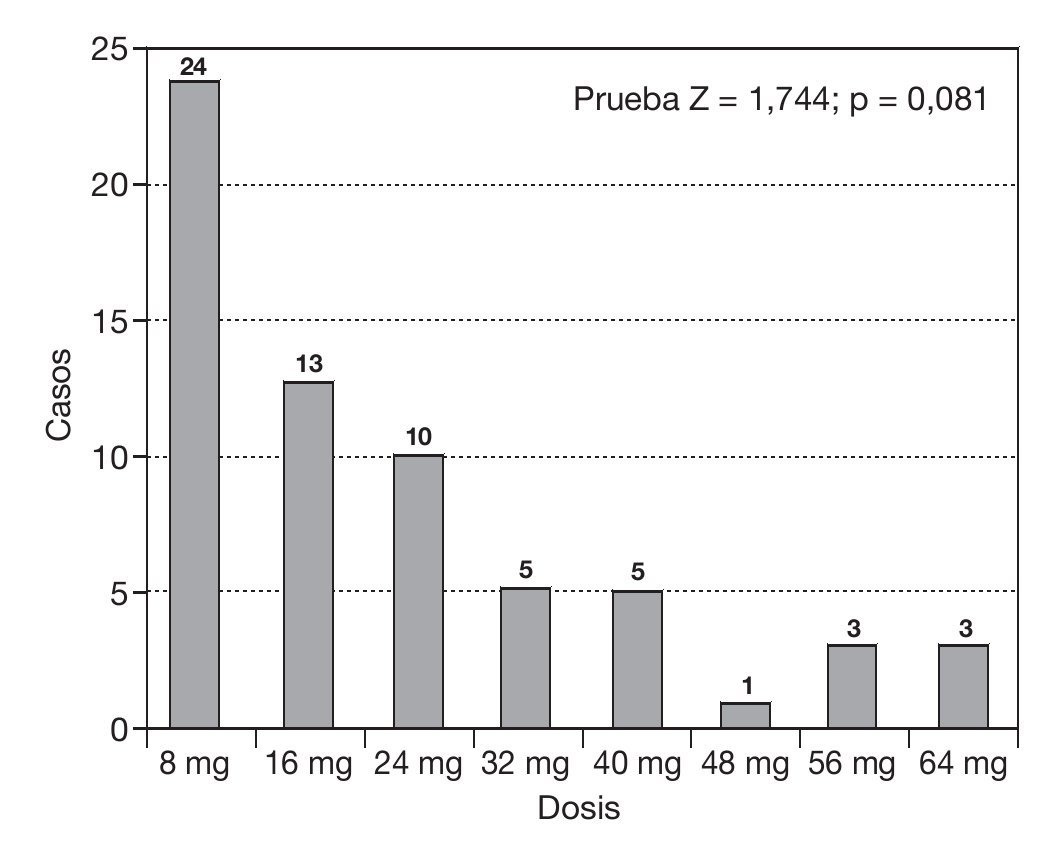
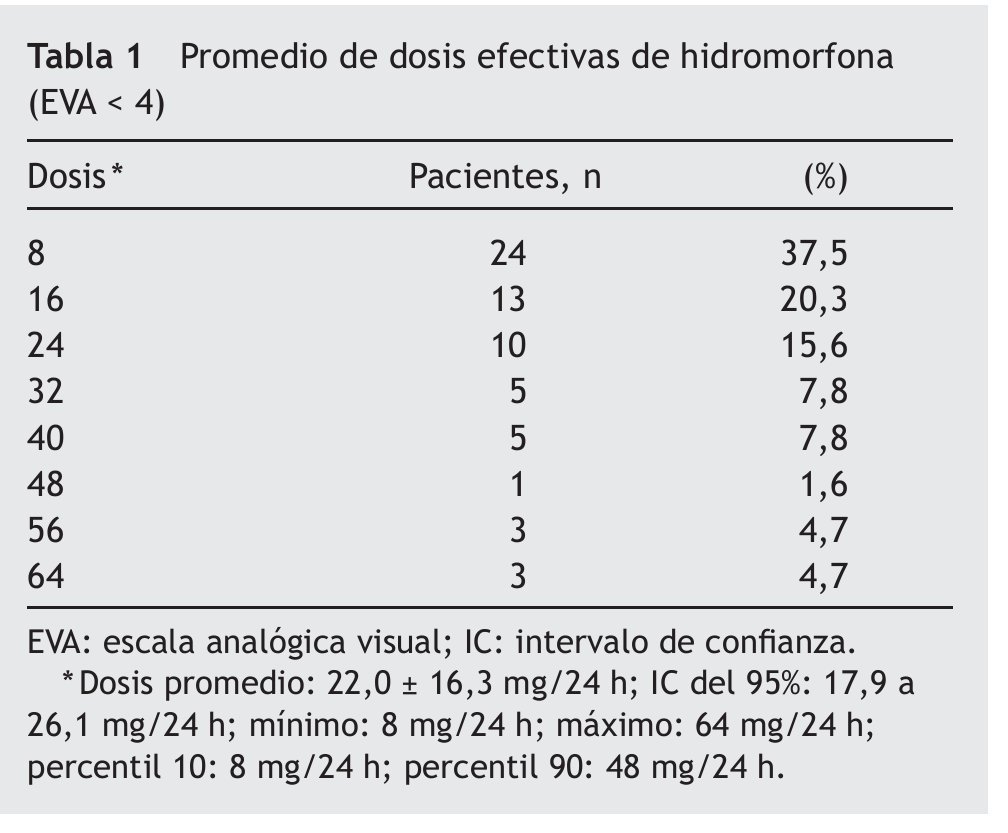
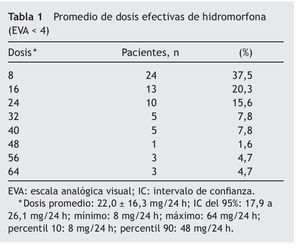
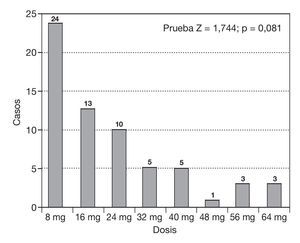
En cada paciente, la dosis se consideró efectiva cuando esta disminuía la EVA a < 4. De los 72 pacientes estudiados, 64 pacientes refirieron una EVA < 4 (88,88%), un paciente abandonó el tratamiento debido a intolerancia a los efectos adversos y 7 pacientes nunca llegaron a tener una EVA < 4. En la tabla 1 podemos observar el promedio de las dosis efectivas que se utilizó en los restantes 64 pacientes, que fue de 22,0 + 16,3 mg. En la figura 1 se observan sólo datos demográficos en los que se observa y se compara la edad de acuerdo con el sexo de cada paciente. En la figura 2, podemos observar la distribución de las dosis utilizadas para obtener una EVA < 4, el número de pacientes que utilizaron cada dosis y el porcentaje de cada uno. La dosis está expresada en mg/día.
Figura 1 Comparación de la edad según el sexo.
Figura 2 Distribución de la dosis efectica (mg/día).
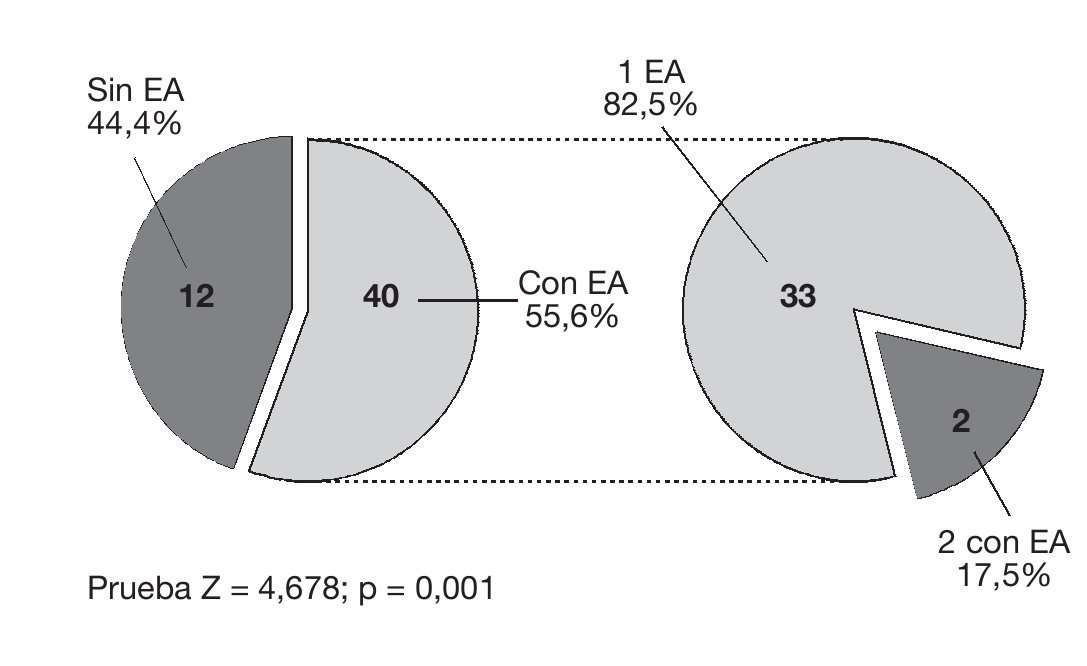
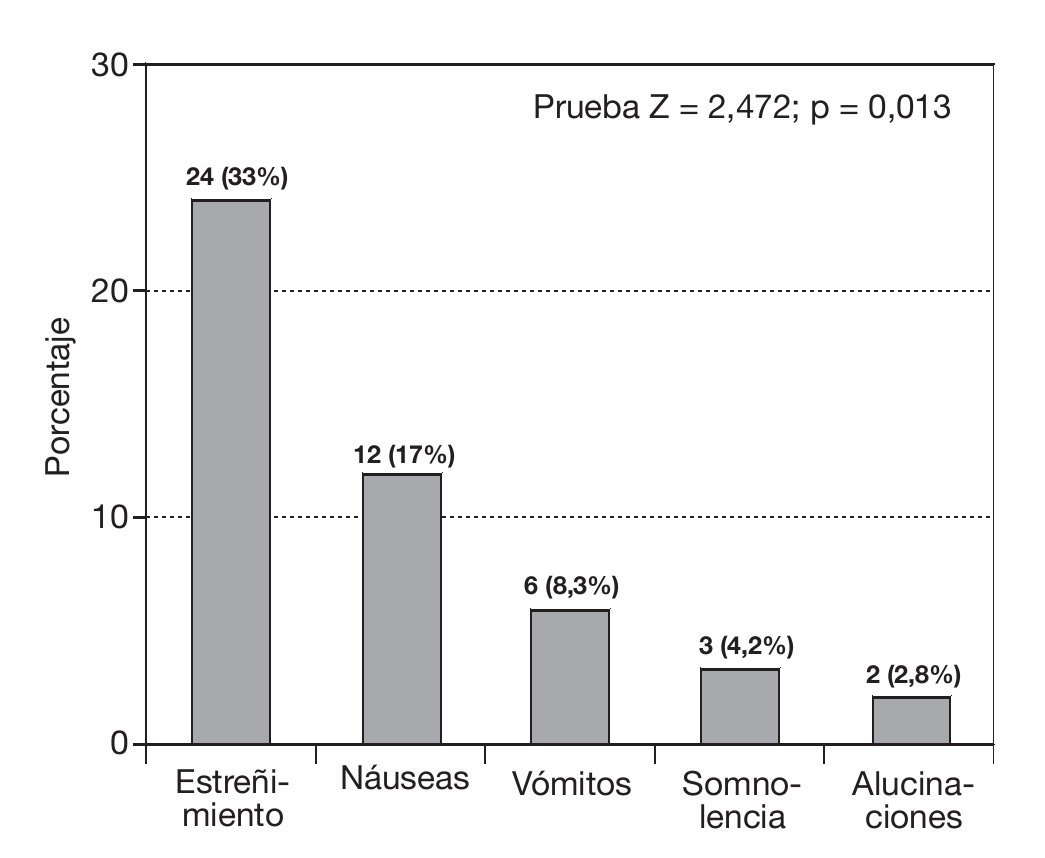
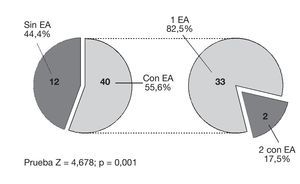
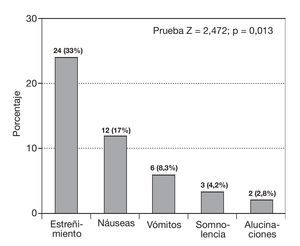
En la figura 3 se observa la incidencia de efectos adversos. En la figura 4 se observan los efectos adversos que se presentaron, con sus respectivos porcentajes. Observamos que el estreñimiento fue el que presentó una significación estadística mayor, con una p < 0,05. El porcentaje de incidencia del estreñimiento fue del 33%, de náuseas del 17%, de vómitos del 8,3%, de somnolencia del 4,2% y de alucinaciones del 2,8%.
Figura 3 Incidencia de efectos adversos (EA).
Figura 4 Incidencia de efectos adversos.
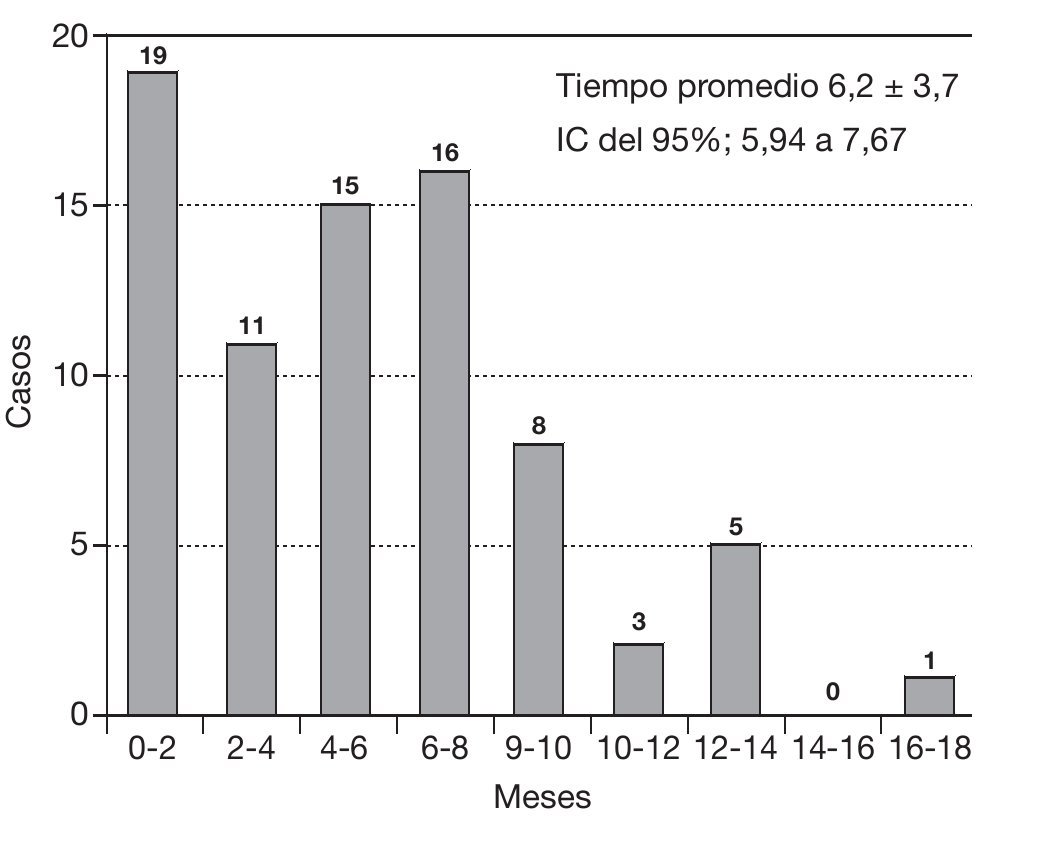
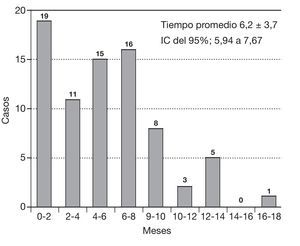
En la figura 5 observamos el tiempo de uso de este fármaco en cada paciente. El tiempo medio de utilización fue de 6,2 ± 3,7 meses.
Figura 5 Tiempo de tratamiento con hidromorfona. IC: intervalo de confianza.
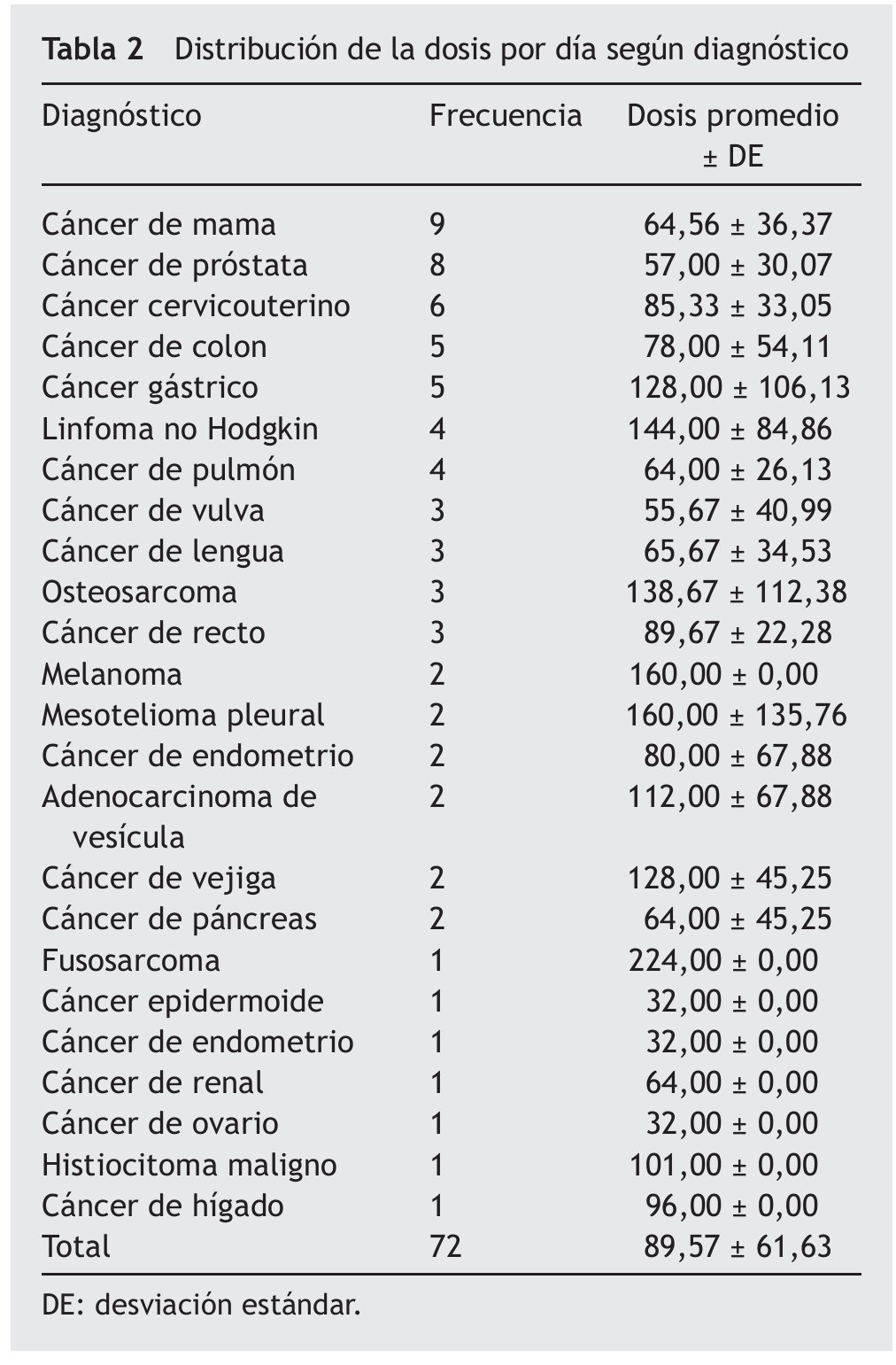
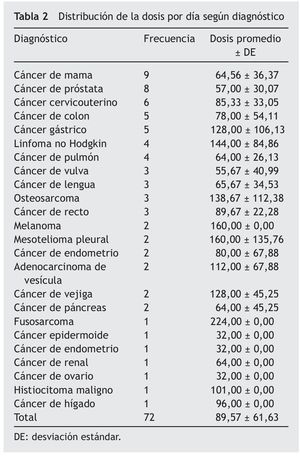
En la tabla 2 se muestran los 23 tipos de cáncer que se presentaron en estos pacientes; los más comunes fueron: el cáncer de mama, el cáncer de próstata, el cáncer cervicouterino, el cáncer de colon y el cáncer gástrico. Se observa también la correlación del tipo de cáncer con las dosis que se utilizó.
Discusión
En este estudio retrospectivo, observamos que de los 72 pacientes solo un paciente abandonó el tratamiento debido a intolerancia al fármaco por efectos adversos. También se muestra que el 55,6% de los pacientes presentaron efectos adversos. Esta cifra es considerable, por lo que sorprende observar la tolerancia que se presentó a ellos. El efecto adverso que más se presentó fue el estreñimiento, con una p < 0,05, lo que indica que fue estadísticamente significativa.
La hidromorfona es una cetona hidrogenada análoga de la morfina, por lo que presenta efectos adversos similares a esta pero, como ya habíamos mencionado anteriormente, con la hidromorfona el prurito, la somnolencia, las náuseas y los vómitos se presentan con menor frecuencia que con la morfina o cualquier otro opiáceo11.
En este estudio también se puede observar que la dosis efectiva promedio para llegar a una EVA < 4 fue de 22 mg/ día, y en 7 pacientes no se logró nunca el control del dolor. La dosis de 22 mg/día se considera todavía una dosis baja. Esto es importante porque cuanto mayor es la dosis de un opiáceo, más aumenta la incidencia de efectos adversos y, por tanto, la tolerancia al fármaco disminuye14.
En cuanto al tiempo de uso del fármaco, observamos que la media fue de 6,2 + 3,7 meses (mínimo de 1 mes y máximo de 18 meses). Con esto podemos observar que es seguro utilizar el fármaco durante períodos prolongados y que, al ir aumentando la dosis paulatinamente, el incremento de los efectos adversos no es estadísticamente significativo. Al igual que el resto de los opiáceos, los pacientes pueden desarrollar tolerancia al fármaco con el uso crónico y necesitarán progresivamente dosis más altas para mantener el control del dolor. También puede aparecer tolerancia cruzada con otros opiáceos. El uso prolongado de este fármaco puede producir dependencia física y la suspensión repentina de la terapia puede dar como resultado un síndrome de abstinencia. Cuando un paciente no requiera continuar el tratamiento con hidromorfona, es aconsejable disminuir la dosis gradualmente para prevenir la aparición de los síntomas de supresión y abstinencia, al igual que debe realizarse con el resto de los opiáceos15,16.
No encontramos una relación ente el tipo de cáncer y la dosis efectiva empleada, lo que nos indica que, independientemente del tipo de cáncer, el comportamiento de cada tumor es diferente4.
Conclusiones
La hidromorfona es un fármaco efectivo, ya que se logró un buen control del dolor en un 88,88% de los casos.
El promedio de dosis efectivas de hidromorfona que se administraron son dosis relativamente bajas, por lo que los efectos adversos son tolerables. El efecto adverso que más se presentó fue el estreñimiento, que es bastante tolerable con fármacos, lo que hace a la hidromorfona efectiva y segura para utilizarse durante períodos prolongados.
Conflicto de intereses
Los autores han declarado no tener ningún conflicto de intereses.
* Autor para correspondencia.
Correo electrónico:bunnyrionda@hotmail.com (E. Rionda).
Recibido el 26 de enero de 2009;
aceptado el 2 de febrero de 2009