La insuficiencia cardiaca (IC) es un síndrome de prevalencia elevada, en España entre el 7 y el 8%, que supone una carga asistencial muy importante, representando uno de los primeros diagnósticos en servicios de medicina interna. Las causas más importantes son la cardiopatía hipertensiva, la miocardiopatía dilatada y la hipertensión arterial, variando su importancia en función de la población estudiada. El diagnóstico clínico no resulta sencillo, por la falta de especificidad de los signos y síntomas. Para su mejor estandarización disponemos de diversos criterios clínico-diagnósticos, entre los cuales, los más utilizados son los de Framingham. Hoy día es imprescindible la práctica de una ecografía a todo enfermo con IC, y la determinación del BNP (o pro-BNP) ha supuesto una importante ayuda para el diagnóstico. Su mortalidad es elevada, entre el 40 y el 50% a los 5 años. La disponibilidad de los inhibidores de la enzima convertidora de angiotensina y los betabloqueantes (que han de emplearse en todos los enfermos sin contraindicación) ha representado un enorme avance en el tratamiento de este síndrome. No debemos olvidar que muchos de estos enfermos serán atendidos en la etapa final de su enfermedad, por lo que requerirán un enfoque más paliativo que curativo.
Heart failure (HF) is a highly prevalent syndrome. In Spain the prevalence is 7-8%, representing a substantial healthcare burden and one of the most frequent diagnoses in internal medicine. The major causes of HF are hypertensive heart disease, dilated cardiomyopathy and high blood pressure. These causes vary in importance depending on the population studied. Because the signs and symptoms of HF are non-specific, clinical diagnosis is not easy. Several clinical diagnostic criteria are available for better standardization, the most widely used being the Framingham criteria. All patients with HF should undergo echocardiography. Determination of B-type natriuretic peptide (BNP) (or pro-BNP) is an important diagnostic aid. Mortality is high, between 40% and 50% at 5 years. The availability of angiotensin converting-enzyme inhibitors and beta blockers (to be used in all patients without contraindications) has represented a huge advance in the treatment of this syndrome. However, many of these patients will be treated in the final stage of their disease and will require a more palliative than curative approach.
La insuficiencia cardiaca (IC) supone uno de los retos asistenciales más importantes para los cardiólogos, internistas y médicos de familia por su elevada prevalencia, la alta tasa de rehospitalización y la elevada necesidad de consultas médicas, representando para el sistema sanitario un proceso de gran coste económico. Con los datos que exponemos a continuación se ilustran muy bien estos aspectos.
En España se registran cerca de 80.000 ingresos hospitalarios anuales por IC, lo que supone el 5% de las hospitalizaciones1, y en los mayores de 65 años acostumbra a ser la primera causa de ingreso. Además, desde los años 1980 hasta final de los años 1990 los ingresos por IC han venido incrementándose, no sólo en nuestro país sino en los países de nuestro entorno2. Otra característica importante de este proceso es la alta tasa de rehospitalizaciones, pudiéndose registrar hasta un 45% de reingresos en los primeros seis meses del alta hospitalaria3.
EpidemiologíaLa prevalencia de la enfermedad, es decir, el número de casos en un período determinado, lo que equivale al número de pacientes que requieren atención, es muy variable y depende de la edad de la población estudiada. Los datos disponibles de nuestro país son escasos, ya que los estudios poblacionales son caros y difíciles de realizar, pero así y todo disponemos de datos de un estudio realizado en Asturias en el que se pone de manifiesto que la prevalencia global es del 5% y que oscila entre el 0,1% en las personas de 40 a 50 años a más del 15% en los mayores de de 80 años4, lo que corrobora la impresión clínica de que la mayoría de pacientes con IC son ancianos. Otro estudio realizado más recientemente en centros de salud ha establecido que la prevalencia en España está en torno al 7-8% en mayores de 45 años5.
Un aspecto interesante a destacar es que la evolución temporal de la prevalencia de la enfermedad ha venido creciendo desde los años 1980 hasta el final del siglo xx, tanto en la población general, en que se ha quintuplicado, pasando del 0,4% a más del 1,4%6, como en la población anciana, mayor de 65 años, en la que ha pasado del 1% en el año 1994 al 12% en 20037.
En lo referente a la incidencia, es decir, a la aparición de casos nuevos en un período especificado entre la población en riesgo, también depende de la edad y oscila entre el 0,1% en los pacientes de 45-54 años a más del 2,5% en los mayores de 80 años8, siendo ésta algo mayor en los varones que en las mujeres, hecho que se acentúa en los mayores de 65 años (1,63 frente a 1,02, respectivamente)9. En cuanto a la evolución temporal, curiosamente la incidencia se ha venido manteniendo desde los años 1950 hasta la actualidad en los varones y ha descendido ligeramente en las mujeres6,10, hechos que también se han comprobado en los ancianos7, todo lo cual supone una paradoja en la que la incidencia (casos nuevos) va manteniéndose o disminuyendo levemente pero la prevalencia (casos totales) va aumentando, hecho que se puede explicar por la mayor supervivencia de los casos nuevos que se van acumulando11.
EtiologíaLa IC es el estadio final de muchas cardiopatías, por lo que sus causas son variables y su frecuencia depende del medio en el que hagan los estudios y de la población evaluada. Podemos analizar grandes series en las cuales las causas más importantes de IC por orden decreciente son la cardiopatía isquémica (40%), la miocardiopatía dilatada (32%), las valvulopatías (12%), la cardiopatía hipertensiva (11%) y otras (5%). Entre éstas se encuentran miocarditis, infección por VIH, conectivopatías, tóxicos (alcohol y drogas) y fármacos, caso de la doxorubicina12.
En nuestro medio las causas más frecuentes de la IC son la cardiopatía isquémica y la hipertensión arterial, variando su importancia según la población estudiada. Entre la población más joven destaca la cardiopatía isquémica, mientras que entre la población anciana lo hace la hipertensión arterial. Otras causas de IC también a considerar son la miocardiopatía dilatada idiopática, las valvulopatías, y etiologías menos frecuentes como la amiloidosis, las cardiopatías tóxicas (por alcohol o fármacos) o la infección por VIH o su tratamiento. En nuestra unidad, que admite pacientes provenientes de cardiología y medicina interna con edades comprendidas entre 24 y 93 años, destaca con mucho la cardiopatía isquémica (55%), seguida de lejos por la cardiopatía hipertensiva (10%) y la miocardiopatía dilatada idiopática (9,5%)13. En el registro BADAPIC de la Sociedad Española de Cardiología se analizan las enfermedades que podrían tener influencia sobre la función cardiaca y estar en el origen de la insuficiencia cardíaca, destacando por su frecuencia también la hipertensión arterial y la cardiopatía isquémica, siendo otros antecedentes destacables la dislipemia, la diabetes mellitus (DM) y las valvulopatías14.
Por otra parte, el peso específico las etiologías ha venido cambiando a lo largo de los años. Desde los años cincuenta hasta la actualidad la cardiopatía isquémica ha ido ganando protagonismo, mientras que la hipertensión y las valvulopatías, a excepción de las valvulopatías degenerativas en los ancianos, han ido perdiendo peso. También ha venido ganado protagonismo la DM, enfermedad de importante y conocido riesgo vascular, como enfermedad asociada a la IC15.
Un aspecto destacable es que hoy día algo más de la mitad de los casos de IC son en forma de fracción de eyección preservada, sobre todo en ancianos y más aún en ancianas16.
Por otra parte, cada vez son más los enfermos, especialmente entre ancianos, que además de la IC padecen otras enfermedades, siendo casi una rareza que un paciente con IC tenga solamente una enfermedad. Entre ellas las más frecuentes son la hipertensión arterial (55%), la DM (31%), la EPOC (26%), la artrosis (16%), enfermedades del tiroides (14%), demencia (9%) o insuficiencia renal (6%)17.
ClínicaLas manifestaciones clínicas clásicas de la IC son la astenia y la fatigabilidad, y los síntomas congestivos como disnea de esfuerzo progresiva hasta el reposo, ortopnea, tos nocturna, disnea paroxística nocturna, distensión abdominal o edemas maleolares por retención hidrosalina, que pueden conllevar ganancia de peso, o dolor abdominal por hígado de estasis o ascitis a tensión. Cuando la enfermedad progresa pueden aparecer anorexia y pérdida de peso, debido a pérdida de masa magra.
En ancianos la presentación clínica puede ser atípica, sobre todo si coexiste demencia y depresión, pudiendo presentarse como síndrome confusional o episodios de ansiedad. En estos pacientes, aunque la expresión clínica puede ser atípica, la exploración física y las exploraciones complementarias son lo suficientemente características para permitir orientar claramente el diagnóstico.
En la exploración física pueden aparecer taquipnea y respiración de Cheyne-Stokes, taquicardia y la posible presencia de un galope por tercer ruido. También es frecuente la presencia de soplos, bien por la propia cardiopatía, bien por la aparición de insuficiencia mitral por dilatación ventricular. Además podemos objetivar signos congestivos, como ingurgitación yugular, reflujo hepatoyugular, crepitantes húmedos diseminados, o sibilantes (asma cardíaco), en algunos casos, derrame pleural (con matidez a la percusión e hipofonesis), hepatomegalia congestiva que puede ser dolorosa, edemas maleolares o edema en región sacra en pacientes encamados y ascitis en casos evolucionados.
DiagnósticoLa IC es una enfermedad de aparente diagnóstico sencillo, pero la práctica nos enseña que establecer con fiabilidad un diagnóstico clínico de este proceso no siempre resulta fácil, pues ni la clínica, ni los signos exploratorios ni algunas de las exploraciones complementarias tienen la suficiente sensibilidad y especificada como para permitirnos afirmar, en muchas ocasiones, con seguridad que nos encontramos ante una IC.
Los signos y síntomas de la IC no son específicos, pues son numerosos los procesos que se pueden presentar con disnea o retención hidrosalina y que nos pueden hacer plantear un diagnóstico diferencial amplio (tabla 1)18. Además, el proceso diagnóstico se puede complicar aún más si tenemos en cuenta que muchos de estos pacientes pueden presentar a la vez dos de estos procesos, por ejemplo una IC y una EPOC19.
Diagnóstico diferencial de los síntomas y signos de la insuficiencia cardiaca.
| Cardiopatía isquémica |
| Enfermedad pulmonar (neumonía, asma, EPOC, tromboembolia pulmonar, hipertensión arterial pulmonar primaria) |
| Trastornos respiratorios asociados a síndrome de apneas del sueño |
| Obesidad |
| Malnutrición |
| Anemia |
| Insuficiencia hepática |
| Insuficiencia renal |
| Hipoalbuminemia |
| Estasis venosa |
| Depresión |
| Síndromes de ansiedad e hiperventilación |
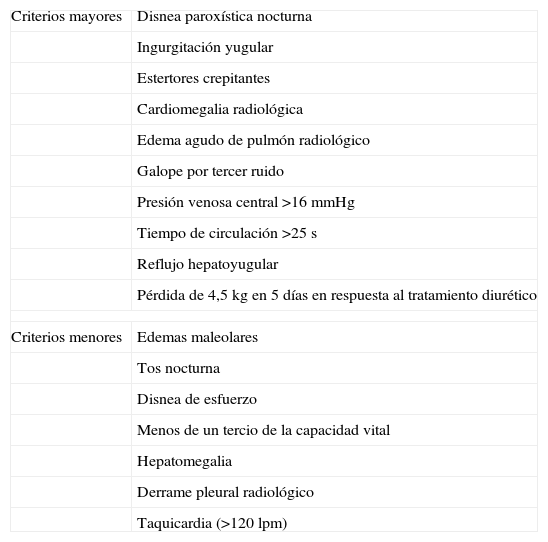
Para poder superar estas dificultades, diversos grupos han establecido criterios diagnósticos, como los de Framingham20,21 o los de Boston22, siendo los más conocidos y empleados los de Framingham, que se exponen en la tabla 2. Más prácticas son las recomendaciones de la Sociedad Europea de Cardiología: síntomas de IC, signos de retención de líquidos, como congestión pulmonar o hinchazón de tobillos, y evidencia objetiva de una alteración cardiaca estructural o funcional en reposo23.
Criterios de Framingham para el diagnóstico de insuficiencia cardiaca.
| Criterios mayores | Disnea paroxística nocturna |
| Ingurgitación yugular | |
| Estertores crepitantes | |
| Cardiomegalia radiológica | |
| Edema agudo de pulmón radiológico | |
| Galope por tercer ruido | |
| Presión venosa central >16 mmHg | |
| Tiempo de circulación >25 s | |
| Reflujo hepatoyugular | |
| Pérdida de 4,5kg en 5 días en respuesta al tratamiento diurético | |
| Criterios menores | Edemas maleolares |
| Tos nocturna | |
| Disnea de esfuerzo | |
| Menos de un tercio de la capacidad vital | |
| Hepatomegalia | |
| Derrame pleural radiológico | |
| Taquicardia (>120 lpm) | |
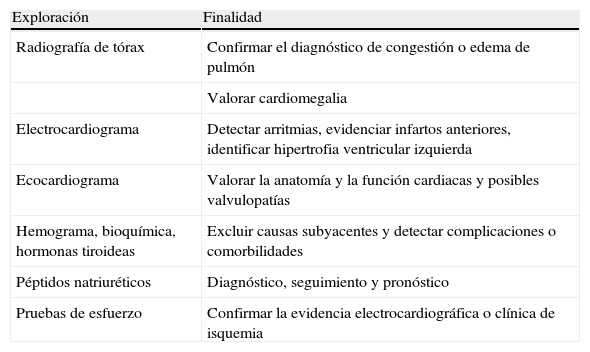
Son varias las exploraciones complementarias que nos pueden ayudar a llegar al diagnóstico de las IC (tabla 3). La práctica de una radiografía de tórax es obligada en el enfermo con IC, ya que puede ayudarnos tanto a valorar su situación clínica como a proporcionarnos datos que serán de gran valor para el diagnóstico. Así, con la radiografía de tórax podremos comprobar si existe cardiomegalia, aumento de los hilios pulmonares, que además suelen estar mal definidos, la aparición en algunos casos de edema alveolar pulmonar, la presencia de redistribución vascular (los vasos que van a los campos superiores son más prominentes que lo normal), líneas de Kerley y derrame pleural.
Pruebas diagnósticas fundamentales y su finalidad en la insuficiencia cardíaca.
| Exploración | Finalidad |
| Radiografía de tórax | Confirmar el diagnóstico de congestión o edema de pulmón |
| Valorar cardiomegalia | |
| Electrocardiograma | Detectar arritmias, evidenciar infartos anteriores, identificar hipertrofia ventricular izquierda |
| Ecocardiograma | Valorar la anatomía y la función cardiacas y posibles valvulopatías |
| Hemograma, bioquímica, hormonas tiroideas | Excluir causas subyacentes y detectar complicaciones o comorbilidades |
| Péptidos natriuréticos | Diagnóstico, seguimiento y pronóstico |
| Pruebas de esfuerzo | Confirmar la evidencia electrocardiográfica o clínica de isquemia |
De igual forma, resulta obligada la práctica de un electrocardiograma (ECG), con el que podremos detectar arritmias o bloqueos, evidenciar infartos anteriores o signos de cardiopatía isquémica o identificar signos de hipertrofia ventricular izquierda, entre otros datos. Resulta difícil pensar que estamos delante de una IC si el ECG del paciente es estrictamente normal, especialmente en los casos con disfunción sistólica24. Asimismo resulta poco adecuado aceptar el diagnóstico y el tratamiento de un paciente con diagnóstico clínico de IC sin la práctica de un ecocardiograma, que nos será de utilidad para ver la estructura y las dimensiones de las cavidades cardíacas, valorar si hay derrame pericárdico, comprobar la función del miocardio, objetivar la fracción de eyección y estudiar las válvulas.
A los enfermos con IC se les debe realizar un hemograma, que valorará la presencia de anemia, una bioquímica con estudio de glucosa, hemoglobina glucosilada, si el enfermo es diabético, colesterol total, sus fracciones y triglicéridos, pruebas hepáticas y función renal con valoración del filtrado glomerular. Es conveniente, además, obtener un estudio funcional tiroideo, porque algunos de estos enfermos reciben compuestos yodados (caso de la amiodarona) y otros son ancianos, en los que la valoración clínica de la función tiroidea es poco fidedigna.
Dentro de las exploraciones analíticas, en la actualidad la determinación de los péptidos natriuréticos auriculares (BNP o su propéptido el pro-BNP) ha ganado un merecido papel en el manejo de los paciente con IC, tanto por la ayuda que suponen en el diagnóstico como porque su determinación seriada puede orientar también el tratamiento25. Una concentración plasmática normal en un paciente sin tratar tiene un alto poder predictivo de exclusión de la enfermedad; por lo tanto, en estos casos la IC es una causa poco probable de los síntomas. Esto podría tener un papel importante en la práctica clínica, especialmente en la atención primaria. Por el contrario, una concentración elevada de péptidos natriuréticos pese a un tratamiento óptimo indica un mal pronóstico23. De todas formas, aparte de la IC, otras entidades que se asocian a una elevación de los valores de péptidos natriuréticos son: hipertrofia ventricular izquierda, taquicardia, sobrecarga del ventrículo derecho, isquemia miocárdica, hipoxemia, disfunción renal, edad avanzada, cirrosis hepática, sepsis e infección. Por otra parte, la obesidad puede reducir los valores de los péptidos natriuréticos.
Se pueden realizar otras pruebas no invasivas, como resonancia magnética (RM) cardiaca, tomografía computarizada (TC) o gammagrafía cardiaca, en pacientes en los que con las exploraciones realizadas no obtengamos información suficiente para el diagnóstico etiológico y en los pacientes con sospecha de enfermedad coronaria.
El test de los 6min [marcha durante 6min (TM6M)] es una prueba sencilla, fácil de realizar, que no requiere instrumentos sofisticados y reproducible, que se utiliza para medir la capacidad funcional y para evaluar la respuesta a una posible intervención. Un pico normal de ejercicio en un paciente sin tratar excluye el diagnóstico de IC sintomática.
El cateterismo cardíaco no es una prueba necesaria para el diagnóstico de la IC, pero sí lo puede ser para confirmar la posible etiología isquémica, valorar las coronarias y, en su caso, plantearnos la cirugía, ya sea coronaria o valvular.
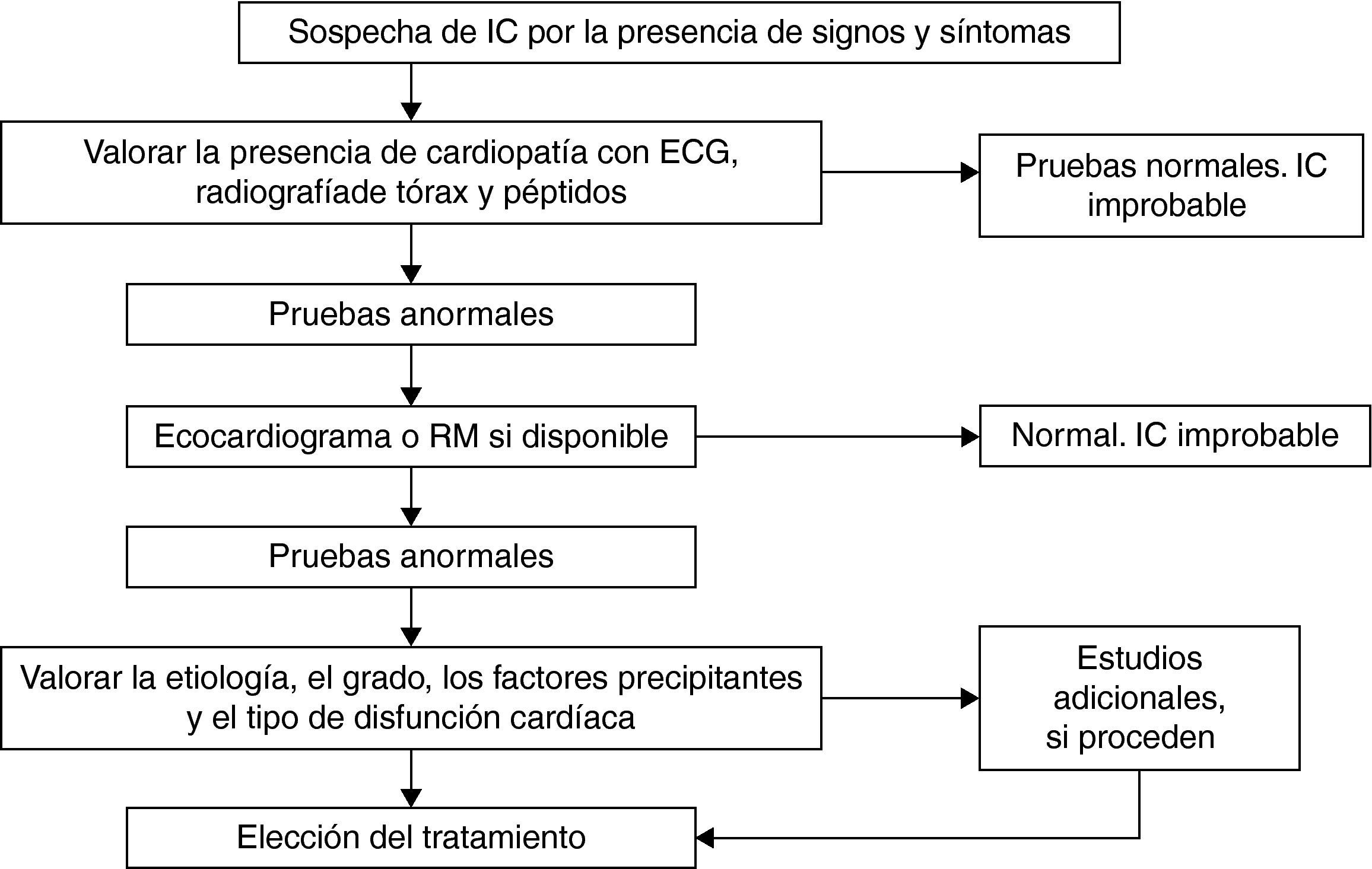
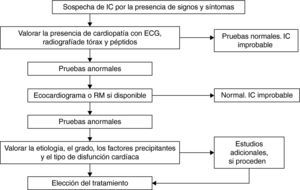
Con estos datos podemos establecer un algoritmo que nos permite aproximarnos con bastante fiabilidad al diagnóstico26 (fig. 1).
Algoritmo diagnóstico de la insuficiencia cardiaca. ECG: electrocardiograma; IC: insuficiencia cardiaca; RM: resonancia magnética. Adaptado de Remme y Swedberg26.
En el momento del diagnóstico es importante establecer la situación funcional del paciente, pues nos será de utilidad para evaluar la gravedad y el pronóstico de la IC, así como su manejo. La más extendida es la clasificación de la New York Heart Association (NYHA)27 (tabla 4).
Clasificación funcional de la insuficiencia cardiaca según la New York Heart Association (NYHA).
| Clase I. Ausencia de síntomas y de limitación funcional |
| Clase II. Síntomas o limitación funcional. |
| Actividades ordinarias producen disnea: Subir cuestas/Subir más de 2 pisos/Correr o caminar de prisa en plano/Llevar peso significativo/Coito |
| Clase III. Síntomas importantes o marcada limitación funcional. |
| Actividades menores de las ordinarias ocasionan disnea: Caminar a paso normal en plano/Subir menos de 2 pisos/Vestirse o desnudarse/Ducharse o secarse |
| Clase IV. Síntomas graves o limitación funcional grave. |
| Síntomas con cualquier tipo de esfuerzo o en reposo: Hablar, levantarse de la cama/Disnea paroxística nocturna/Ortopnea franca |
Un aspecto complementario en el diagnóstico de la IC y fundamental para el manejo de dichos pacientes es el reconocimiento del factor precipitante de su descompensación, entre los que el fundamental es el incumplimiento del tratamiento, ya sea con la dieta o la medicación, en casi la mitad de los enfermos28. Otros factores son: infecciones, cardiopatía isquémica, agravamiento de enfermedades concomitantes, como EPOC, anemia, insuficiencia renal, tromboembolia pulmonar, arritmias, HTA mal controlada o tratamiento previo inadecuado. Aproximadamente en el 15% de los pacientes no se evidencia una causa de la descompensación.
PronósticoLa IC es una enfermedad con mal pronóstico. En términos generales se puede afirmar que a los 24 meses ha muerto el 13% de los enfermos14 y que a los 5 años sobrevive alrededor del 50%, algo menos para los varones y algo más para las mujeres6. Además, otro aspecto pronóstico importante es que a los 2 años sólo el 20% ha podido vivir sin ingresar en el hospital14.
No todos los enfermos tienen las mismas probabilidades de supervivencia, ya que hay diversos factores asociados a peor pronóstico. Así, en la literatura se recogen entre otros la clase funcional (peor pronóstico para los que están en clase III/IV), la historia previa de IC, la coexistencia de otras enfermedades y uno muy significativo, como es la edad, ya que los pacientes que hayan cumplido 75 años tienen claramente un pronóstico mucho peor. En nuestra unidad la mortalidad acumulada oscila entre el 10,6% a los 12 meses hasta el 40% a los 5 años y el 50,8% a los 7 años. La edad mediana en el momento de la muerte era de 75,2 años y el tiempo mediano entre el diagnóstico de la IC y la muerte era de 62 meses [32,3-107,8]13. Entre nuestros enfermos tenían peor supervivencia los más mayores, los varones, los de peor clase funcional, los de peor fracción de eyección, los de causa isquémica, los de mayor duración de la IC, los diabéticos, los afectos de vasculopatía periférica, los más frágiles y los que tenían peor función renal, todos ellos factores asociados a peor pronóstico de forma independiente13.
Afortunadamente, a lo largo de los años la supervivencia ha venido mejorando, tanto para los varones como para las mujeres10 y para la mayoría de los grupos etáreos, a excepción de los mayores de 85 años29.
TratamientoEl tratamiento de la IC es quizá uno de los aspectos que más ha cambiado en la enfermedad, no sólo por las modificaciones derivadas del concepto fisiopatológico neurohormonal y la consecuente introducción del correspondiente bloqueo neurohormonal, sino también porque la gran carga asistencial que conlleva esta enfermedad ha motivado cambios en el acercamiento a estos enfermos con la introducción de las unidades de IC y la participación multidisciplinar en su atención.
Disponemos de elementos farmacológicos y no farmacológicos, pero, como con toda enfermedad crónica, el tratamiento de la IC requiere el planteamiento de un cambio permanente en el estilo de vida, con la idea de comprometerse a seguir un régimen de vida que podríamos denominar genéricamente «sano», que supone sobre todo el abandono de los hábitos de vida nocivos, como el tabaquismo y el abuso de alcohol, en el seguimiento de una dieta adecuada y la consecución de un nivel suficiente de autocuidado.
Entre las medidas no farmacológicas destaca la información y la educación sanitaria, que resultan un elemento esencial, puesto que en las enfermedades crónicas las personas que mejor entienden su enfermedad y son capaces de autocuidarse evolucionan mejor30. La educación engloba diversos aspectos, como el conocimiento de los síntomas esperados y cuándo llamar al médico, el autocontrol del peso y el control periódico de la presión arterial con participación, si es preciso, de la familia o de los cuidadores en el plan de tratamiento. Es importante también educar sobre la medicación centrándonos en la importancia del cumplimento, la correcta dosificación y la frecuencia de administración y el adiestramiento sobre los posibles efectos colaterales. Esta educación es mucho más fácil de lograr en el ámbito de unidades multidisciplinarias con la participación de enfermeras con interés en esta enfermedad, que además pueden ayudar a realizar un seguimiento ambulatorio estrecho31.
Entre las medidas no farmacológicas es conveniente que el paciente con IC siga una dieta asódica de 2-3g, aunque podría ser aceptable hasta 4g/día, en función de los signos congestivos. En muchas ocasiones, para que al enfermo le resulte tolerable esta dieta es conveniente la consulta con un dietista. También resulta conveniente para los pacientes en clase I-III de la NYHA la práctica de ejercicio físico aeróbico regular. Entre los ejercicios recomendables están caminar y la marcha en bicicleta, pero si hay problemas reumáticos pueden realizarse ejercicios en agua y, si hay sedentarismo, ejercicios sedentarios.
Entre las medidas generales recomendables para los pacientes con IC está la vacunación antigripal y antineumocócica, y también es importante que todo enfermo con IC tenga un correcto control de los factores de riesgo cardiovascular como la presión arterial, las concentraciones de lípidos y un buen control de la diabetes.
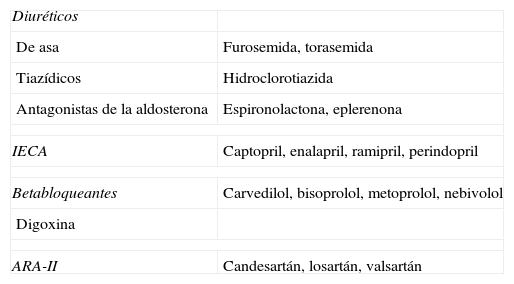
Disponemos de diversos grupos farmacológicos para el tratamiento de la IC (tabla 5). Los más conocidos y los que se instauran en primer lugar en caso de congestión son los diuréticos, fundamentalmente los de asa, que se pueden complementar en los enfermos avanzados con las tiazidas o los antagonistas de la aldosterona. De estos fármacos, sólo los antagonistas de la aldosterona han mostrado mejora en la mortalidad en pacientes con disfunción sistólica32, o tras un IAM33, porque los demás diuréticos no han podido ser sometidos nunca a ensayos clínicos, dada la evidencia patente de la mejoría sintomática que produce su uso.
Grupos farmacológicos fundamentales empleados en la insuficiencia cardíaca.
| Diuréticos | |
| De asa | Furosemida, torasemida |
| Tiazídicos | Hidroclorotiazida |
| Antagonistas de la aldosterona | Espironolactona, eplerenona |
| IECA | Captopril, enalapril, ramipril, perindopril |
| Betabloqueantes | Carvedilol, bisoprolol, metoprolol, nebivolol |
| Digoxina | |
| ARA-II | Candesartán, losartán, valsartán |
En cursiva los que han demostrado mejoría de la supervivencia.
ARA-II: antagonistas de los receptores de angiotensina-II; IECA: inhibidores de la enzima convertidora de angiotensina.
Gran parte de la mejora en el pronóstico de los enfermos con IC se debe a la introducción de fármacos que bloquean la actividad neurohormonal propia de la enfermedad, entre los que han destacado por su efecto los inhibidores de la enzima convertidora de angiotensina (IECA)34 y los betabloqueantes (BB)35,36.
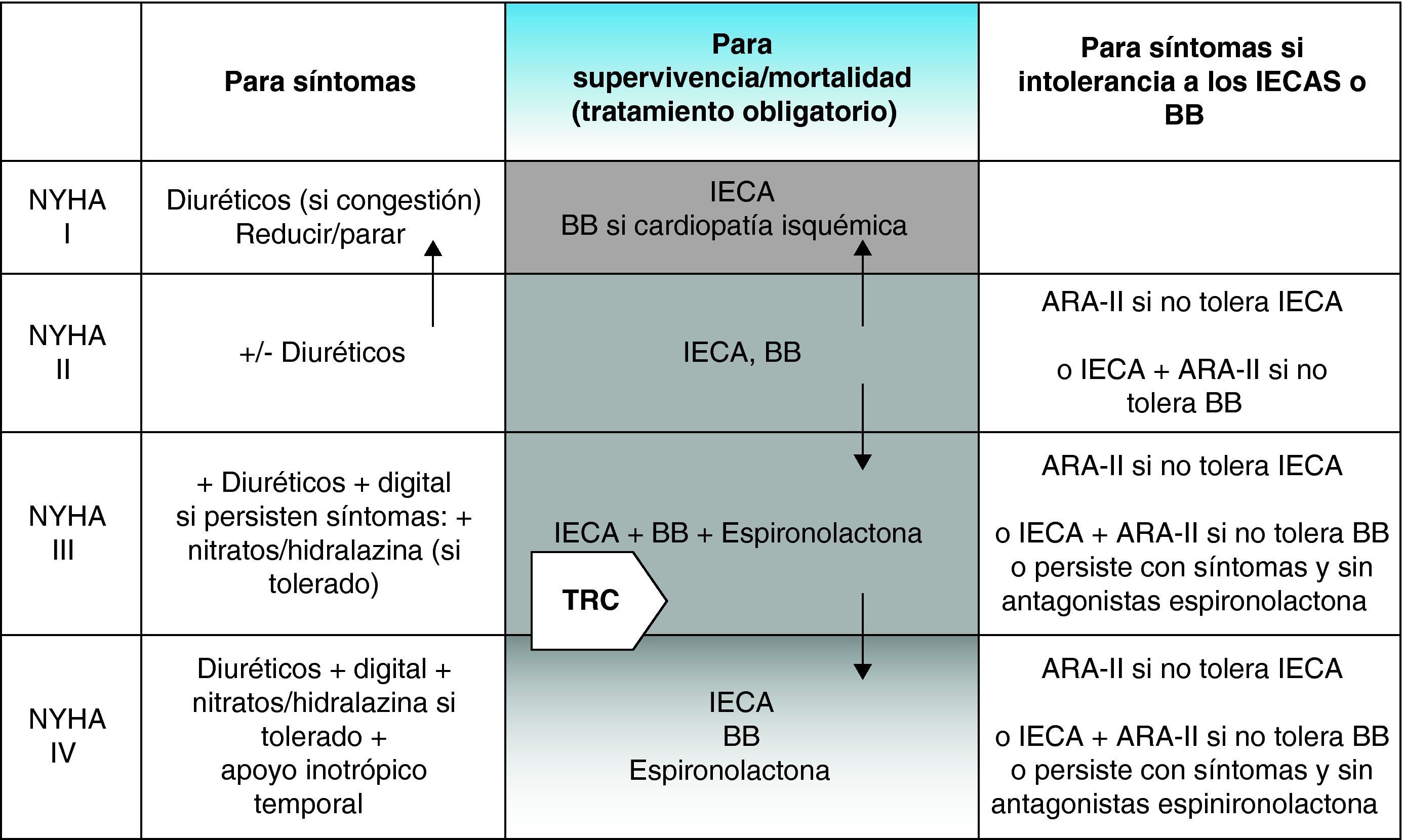
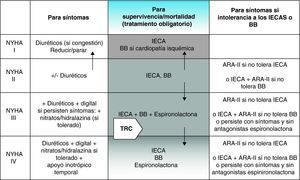
Un protocolo sencillo, utilizando la clase funcional de la NYHA para valorar la situación del paciente, como el que explicamos a continuación (fig. 2), puede servir para aplicar correctamente los fármacos en la IC.
Algoritmo del tratamiento de la insuficiencia cardiaca (IC). En la columna central se exponen los fármacos obligatorios para los pacientes con IC según su clase funcional. También se muestra el lugar que puede ocupar la resincronización. En la columna de la izquierda están expuestos los fármacos a emplear para aliviar síntomas, también según su clase funcional. Finalmente, en la columna de la derecha se exponen fármacos que se pueden emplear para sustituir o complementar los fármacos fundamentales. ARA-II: antagonistas de los receptores de angiotensina-II; BB: betabloqueantes; IECA: inhibidores de la enzima convertidora de angiotensina; TRC: terapia de resincronización cardiaca. Adaptado de Remme y Swedberg26.
En clase I se ha emplear un IECA y se puede utilizar un BB, sobre todo si el paciente es isquémico o ha padecido un IAM. En clase I los diuréticos pueden no ser necesarios. En clase II, podemos necesitar (o no, aunque la mayoría de las veces sí) diuréticos, y siempre se ha de emplear un IECA, un BB y digoxina de forma opcional si la FE <25%, el índice cardiotorácico (ICT) >0,55 o existe fibrilación auricular (FA). En clase III se han de emplear diuréticos, IECA, BB, digoxina y espironolactona [siempre que no haya insuficiencia renal crónica (IRC)] y en clase IV se ha de emplear diuréticos, IECA, BB, digoxina y espironolactona (si no hay IRC).
Además disponemos de diversos fármacos alternativos o complementarios como los ARAII, que se pueden emplear como alternativa a los IECA (cuando haya contraindicación o intolerancia a los mismos, como en caso de tos, pero no en caso de IRC en que también están contraindicados), o también asociadas a los IECA, fundamentalmente en pacientes con disfunción sistólica y que reciban antagonistas de la aldosterona. La ivabradina es una alternativa para los pacientes con taquicardia sinusal en los que no se pueden emplear BB o asociados a los BB en los pacientes, que a pesar del tratamiento con este grupo de fármacos, se mantienen en ritmo sinusal y taquicárdicos37. El ácido acetilsalicílico está indicado en los pacientes isquémicos, y los anticoagulantes orales se han de emplear en caso de embolismo periférico o cerebral, si hay FA, y de forma individualizada, en caso de estar en presencia de grandes cavidades cardiacas o de depresión muy importante de la fracción de eyección. Finalmente, las estatinas se utilizarían si el paciente es dislipémico o tiene indicación por su cardiopatía isquémica, aunque no se ha demostrado beneficio pronóstico en pacientes con IC38,39.
Normas de empleo de los fármacosDiuréticosEntre los diuréticos de asa se suelen emplear 40-80mg/día de furosemida o 10-20mg de torasemida, aunque se pueden utilizar dosis más altas. A igualdad de eficacia y si hay gran fluctuación diaria en la diuresis, es mejor la torasemida. Cuando 40-80mg de furosemida o 10-20mg de torasemida sean insuficientes, se pueden añadir 25-50mg de hidroclorotiazida. En caso de IC derecha y función renal normal, sin hiperpotasemia, se añadirá espironolactona a dosis diuréticas (50-100mg/día). La situación ideal es el autocontrol de los diuréticos con pautas flexibles, situación en la que se puede llegar en contadas ocasiones, siempre en el paciente que ha alcanzado un buen nivel de autocuidado. No suelen ser necesarios los suplementos de potasio.
IECASe han de emplear en todos los pacientes, sea cual sea su clase funcional. Los fármacos más utilizados son el enalapril y el captopril, en caso de disfunción ventricular post-IAM, el ramipril, y en pacientes mayores de 70 años también se puede utilizar el perindopril. Las dosis diana son 50mg/8h (captopril); 10mg/12h (enalapril, excepcionalmente 20/12h); 5mg/12h (ramipril), y 4mg/día (perindopril).
La introducción ha de ser de forma progresiva, por ejemplo, con 6,25mg/8h de captopril, y las dosis se irán doblando hasta alcanzar la dosis tolerada. Con los otros IECA las dosis iniciales son: 2,5-5mg/día de enalapril, 1,25-2,5mg/día de ramipril, y 2mg/día de perindopril. Los incrementos de las dosis se realizarán cada 1-2 semanas, pero se podrán hacer más rápidamente, siempre bajo supervisión estricta. Se debe realizar un control analítico a las 1-2 semanas de cada incremento de dosis.
El aumento moderado de les cifras de creatinina y K es frecuente y aceptable. Si el incremento es menor del 50% de la cifra basal o no supera los 3mg/dl de creatinina o los 5,8 mmol/l de K, se pueden mantener el tratamiento siempre bajo un control analítico estrecho. Si la creatinina supera los 4mg/dl o dobla los valores iniciales o el K supera los 6 mmol/l, se deben suspender hasta que el nefrólogo realice una valoración. En incrementos intermedios se debe considerar la disminución de la dosis de diuréticos o bien suspender posibles fármacos nefrotóxicos concomitantes, antes de pensar en la retirada de los IECA.
BetabloqueantesLos deben recibir todos los pacientes en clase funcional II-III, o IV «estable» (que no reciban inotrópicos o vasodilatadores intravenosos y sin retención hídrica) y los que estén en clase I con disfunción ventricular asintomática si tienen cardiopatía isquémica. El asma bronquial es una contraindicación absoluta para BB, pero no así el EPOC sin hiperreactividad bronquial. También el bloqueo auriculoventricular avanzado es una contraindicación, y los trastornos de conducción nos obligarán a una vigilancia más estrecha. La edad mayor de 75 años no supone una contraindicación, aunque ante estos enfermos hemos de aumentar las precauciones40. Si el paciente tiene una vasculopatía periférica es mejor emplear carvedilol, y en caso de hiperreactividad bronquial el nebivolol es el más cardioselectivo.
En pacientes en clase I-III se suele emplear carvedilol, bisoprolol o metoprolol, y en pacientes en clase IV el carvedilol es el más estudiado. En mayores de 70 años y sobre todo en mayores de 75 años se puede utilizar nebivolol.
Las dosis diana son: 25mg/12h de carvedilol, 10mg/día de bisoprolol y 10mg/día de nebivolol. La introducción ha de ser progresiva, siendo las dosis iniciales de 3,125mg/12h de carvedilol, 1,25mg/día de bisoprolol y 1,25mg/día de nebivolol. La dosis se irá doblando cada 2-3 semanas hasta alcanzar la dosis máxima tolerada o la dosis deseada. Es conveniente iniciarlos durante el ingreso, antes del alta hospitalaria, siempre y cuando el paciente esté sin signos de retención hídrica.
A la hora de introducir esta medicación valoraremos que la presión arterial (PA) sea >85 mmHg y la frecuencia cardíaca (FC) sea >55 lpm. Estas cifras son también el límite inferior que nos permitirá incrementar la medicación, pero se aconseja, en general, no hacerlo si la PA es <90 mmHg o la FC es <60 lpm.
En ocasiones, para que se puedan cumplir estas premisas que permiten introducir los BB podremos reducir la dosis de diuréticos y/o de IECA, ya que puede ser preferible administrar dosis medias de IECA y de BB que dosis altas de sólo uno de los dos41. Si al introducir los BB apareciera retención hídrica (edemas o congestión), podemos introducir o aumentar los diuréticos.
DigoxinaSu utilización sigue siendo controvertida. Se ha de reservar para pacientes en FA, los que estén en clase III-IV y en clase II con FE <25%, dilatación importante del ventrículo izquierdo o cardiomegalia (ICT >0,55), sobre todo en varones y sin cardiopatía isquémica. La dosis recomendada general es de 0,75-1,75mg a la semana, que se puede administrar en 1 comprimido (0,25mg) de 3 a 7 días a la semana, dependiendo de la edad, la función renal y la situación clínica, pudiéndose administrar también medio comprimido (0,125mg) diariamente. La dosis se ha de ajustar para lograr cifras ideales de digoxinemia entre 0,5 y 0,8 ng/ml, si bien, en los pacientes que estén en FA, este valor podrá ser más alto, sin sobrepasar 1,2 ng/ml. Estos niveles se han vigilar periódicamente y en función de cambios en el tratamiento (p. ej., si se añade amiodarona) o empeoramiento de la función renal.
Antagonistas de los receptores de angiotensina-IISon sustitutos de los IECA en los casos en que su contraindicación no sea la insuficiencia renal. Los de elección son el candesartán y el valsartán, por haber demostrado su eficacia en pruebas clínicas42. La dosis diana es de 16mg/12h para el candesartán y de 160mg/12h para el valsartán, y se ha introducir de forma progresiva en los que no reciban IECA (candesartán a 4mg/12h o valsartán a 40mg/12h), doblando la dosis si hay buena tolerancia, con controles analíticos de función renal y de potasio, de forma similar a los IECA. Si el paciente ya recibía IECA a dosis diana, la introducción de los ARA II será directa con la dosis equivalente a la de los IECA. También pueden asociarse a los IECA, sobre todo en los pacientes que no puedan tomar BB, que persistan sintomáticos a pesar de terapia triple y que no reciban antagonistas de la aldosterona.
Otros fármacosLa combinación de hidralazina + nitratos puede emplearse como sustitutiva de los IECA en pacientes con contraindicación por insuficiencia renal o hiperpotasemia.
La dosis diana de la combinación será de 50mg/8h (podrá aumentarse a 50mg/6h) de hidralazina + 40mg/8h de mononitrato de isosorbida (éste podrá ser sustituido por 50 o 60mg/día de una forma retardada). Su introducción será igualmente progresiva, empezando con 12,5mg/8h de hidralazina + 20mg/8h de mononitrato de isosorbida, y se irá doblando la dosis de hidralazina hasta alcanzar los 50mg/8h; posteriormente, si se tercia, se doblará la dosis de nitratos a 40mg/8h o se cambiará a una forma de administración retardada.
Los antagonistas de la aldosterona se han de emplear en enfermos en clase III-IV que no tengan insuficiencia renal significativa (creatinina <2,5mg/dl) y potasio <5 mmol/l antes del tratamiento. En pacientes que reciban IECA o ARA II la dosis diana será de 25mg/día, pero ésta se ajustará en función de las concentraciones de potasio y de la función renal, pudiéndose también administrar 25mg a días alternos o 12,5mg/día.
En pacientes que no reciban IECA o ARA II la dosis podrá ser superior, o sea 50-100mg/día, sobre todo en aquéllos con predominio de la insuficiencia cardíaca derecha.
La eplerenona será el fármaco de elección en los pacientes con disfunción ventricular-insuficiencia cardíaca post-IAM reciente, al haber demostrado efectos beneficiosos en este subgrupo de pacientes. Este fármaco también se puede utilizar como sustitutivo de la espironolactona en caso de ginecomastia significativa, molesta o dolorosa33.
Terapia de resincronización cardiacaSe recomienda la resincronización mediante marcapasos biventricular (TRC-P), en pacientes en clase funcional III-IV de la NYHA que permanecen sintomáticos a pesar de tratamiento médico óptimo y que tienen una fracción de eyección disminuida (FEVI ≤35%) y prolongación del QRS (ancho QRS ≥120ms) para reducir la morbimortalidad. En estos pacientes también se podría implantar un TRC, pero con desfibrilador implantable (TRC-D) si cumplen los criterios de la TRC, además de una expectativa de vida con buen estado funcional >1 año23.
Además, en pacientes con IC e indicación concomitante de marcapasos permanente (primer implante o sustitución de marcapasos convencional), con síntomas de clase funcional II-IV de la NYHA, con una FEVI baja (≤35%) o dilatación ventricular izquierda, se considerará la terapia de resincronización cardiaca mediante la implantación TRC-P, ya que en estos pacientes el uso de marcapasos ventricular derecho puede ser perjudicial y puede causar o aumentar la desincronización43.
Desfibrilador automático implantable (DAI)Se recomienda la implantación de un DAI para la prevención secundaria en pacientes que han sobrevivido a fibrilación ventricular (FV) y en pacientes con taquicardia ventricular (TV) documentada y hemodinámicamente inestable y/o TV con síncope, una FEVI ≤40%, tratamiento médico óptimo y una expectativa de vida con buen estado funcional >1 año25.
También se recomienda la implantación de un DAI para la prevención primaria y la reducción de la mortalidad en pacientes con disfunción ventricular izquierda secundaria a infarto de miocardio previo (transcurridos como mínimo 40 días del infarto), o con miocardiopatía no isquémica con una FEVI ≤35%, en clase funcional II-III de la NYHA, que reciben tratamiento médico óptimo y tienen una expectativa razonable de vida con buen estado funcional >1 año.
Enfermedad terminalFinalmente, en muchos casos habremos de enfocar la asistencia al paciente con IC, sin ánimo curativo sino simplemente con intención paliativa, atendiendo a la situación terminal de la enfermedad, empleando recursos dirigidos al confort del enfermo. Esta situación nos la plantearemos cuando se cumplan determinados criterios, que se exponen en la tabla 644.
Criterios de la National Hospice Organization para definir insuficiencia cardiaca terminal.
| 1. Insuficiencia cardiaca congestiva recurrente con ingresos hospitalarios repetidos |
| 2. Clase funcional IV de la NYHA, persistente |
| 3. Fracción de eyección del ventrículo izquierdo <20% |
| 4. Administración de tratamiento óptimo |
| 5. Contraindicación para trasplante cardíaco |
Tomado de Mast et al44.
La IC es un síndrome de prevalencia elevada, sobre todo en edades avanzadas, que supone una gran carga asistencial. Sus causas más frecuentes son la cardiopatía isquémica, la miocardiopatía dilatada y la hipertensión arterial. La importancia de las enfermedades asociadas es patente sobre todo en el caso de la diabetes.
Las nuevas maneras de enfocar su atención como unidades multidisciplinares y la mejor aplicación de las medidas farmacológicas, junto con otros avances en el tratamiento, han conseguido una mejora en la supervivencia. A partir de ahora será más difícil seguir mejorando la supervivencia, pero hay otros objetivos terapéuticos que no debemos olvidar, como son aumentar la calidad de vida y asistir a los enfermos en la fase terminal de su proceso.
Conflicto de interesesLos autores declaran no tener ningún conflicto de intereses.