INTRODUCCIÓN
La hipertensión arterial pulmonar (HAP) es una enfermedad caracterizada por el aumento progresivo de las resistencias vasculares pulmonares (RVP) que conduce al fallo del ventrículo derecho y a la muerte prematura. Es una complicación grave, aunque poco frecuente, en las enfermedades reumáticas sistémicas. La esclerosis sistémica (ES) es una de las principales causas de mortalidad junto con la enfermedad pulmonar intersticial (EPI). Su pronóstico es sombrío, con una supervivencia a los 2 años del 40-55%1. Sus síntomas clínicos son tardíos e inespecíficos, aunque ya exista afectación hemodinámica, por lo que el diagnóstico se suele retrasar varios años. Últimamente, con la aparición de nuevas terapias como los inhibidores de la fosfodiesterasa-5 y los antagonistas del receptor de endotelina se han incrementado los esfuerzos en diagnosticar la enfermedad en estadios tempranos, para iniciar un tratamiento precoz y poder mejorar su elevada morbimortalidad.
DEFINICIÓN
Actualmente la definición que se utiliza es la hemodinámica medida por cateterismo cardíaco derecho (CCD), que es el patrón oro para el diagnóstico: una presión media en la arteria pulmonar superior a 25 mmHg en reposo o superior a 30 mmHg con el ejercicio2, con una presión de enclavamiento pulmonar (PCP) menor de 15 mmHg y una RVP superior a 3 unidades Wood (mmHg/l/min).
HIPERTENSIÓN ARTERIAL PULMONAR EN REUMATOLOGÍA
La HAP asociada a enfermedades del tejido conjuntivo constituye un apartado específico dentro de la actual clasificación clínica de la HAP, modificada en 2003 en el Tercer Congreso Mundial sobre HAP en Venecia (tabla 1)3. Entre estas enfermedades la mayor prevalencia la encontramos en la ES (12% por cateterismo)4, donde se ha descrito clásicamente en las formas limitadas de larga evolución, pero también en las formas difusas, y en algunos casos asociada a EPI. Asimismo, esta complicación puede aparecer en pacientes con enfermedad mixta del tejido conjuntivo (EMTC) (10-45%)5, lupus eritematoso sistémico (LES) (4-14%)6,7, y con menor prevalencia en la artritis reumatoide (21% por ecocardiografía)8, la dermatomiositis-polimiositis4 y el síndrome de Sjögren (41 casos en la literatura medica inglesa)9.
MANIFESTACIONES CLÍNICAS
La HAP se caracteriza por un aumento progresivo de las RVP, que desembocan en insuficiencia car-díaca congestiva, que será la causa de la muerte10. En las primeras fases la enfermedad es asintomática y sólo se manifiesta durante el ejercicio o al realizar actividades que requieran un esfuerzo superior al habitual. El síntoma inicial más frecuente es la disnea de esfuerzo, que en ocasiones se acompaña de fatiga, mareos y palpitaciones. Otros síntomas inespecíficos que pueden observarse con la evolución de la enfermedad son el dolor torácico (que puede ser indistinguible del de la cardiopatía isquémica), el síncope recurrente y la tos.
Con el paso del tiempo se produce una reducción progresiva del gasto cardíaco y un aumento de las RVP. Así, en las fases tardías de la enfermedad son evidentes los síntomas y signos característicos de insuficiencia cardíaca derecha, tales como edema, ascitis, hepatomegalia, soplo sistólico paraesternal izquierdo y aumento del componente pulmonar del segundo tono a la auscultación cardíaca. A la larga, esto evoluciona hacia la insuficiencia cardíaca y la muerte a causa de ella.
DIAGNÓSTICO
Dado que la clínica es tardía e inespecífica, precisamos del uso de exploraciones complementarias para su diagnóstico precoz. Las pruebas de función respiratoria (PFR) y la ecocardiografía Doppler transtorácica (ETT) son las principales herramientas de cribado, y la sospecha diagnóstica siempre debe confirmarse mediante CCD. Otras exploraciones, como el electrocardiograma (ECG), las pruebas de imagen o el test de la marcha de 6 min, pueden ayudar al diagnóstico y, en ocasiones, a controlar el tratamiento.
Ecocardiografía Doppler
Actualmente es el test de cribado no invasivo de elección en poblaciones de riesgo para desarrollar HAP. La sensibilidad y la especificidad de esta técnica son variables y dependen de diferentes factores, como la precisión del aparato, la pericia del técnico y los valores de normalidad utilizados. Además, es útil para diferenciar otras causas (fallo ventricular izquierdo, valvulopatías y cardiopatías congénitas) y controlar la evolución de la enfermedad y la respuesta al tratamiento.
Permite el cálculo de los valores de presión arterial pulmonar sistólica (PAPS) mediante la medición de la velocidad de regurgitación tricuspídea (VRT) y estimando la presión en la aurícula derecha (PAD) por las características de la vena cava inferior. Se utiliza la siguiente fórmula: PAPS = 4 3 VRT2 + PAD. Con el fin de evitar incorrecciones en la estimación de la PAD, como ocurre en pacientes obesos, se ha propuesto utilizar únicamente la VRT. Aunque todavía no se ha alcanzado un consenso al respecto, se considera que existe una HAP ligera cuando la PAPS es mayor de 35-40 mmHg o la VRT es superior a 2,5 m/s11. Valores de PAPS > 50 mmHg o VRT > 3 m/s corresponderían a una HAP moderada.
Cuando la HAP se ha establecido, los hallazgos característicos son: aumento de tamaño de cavidades derechas, disminución de tamaño de cavidad del ventrículo izquierdo, desplazamiento del tabique en la diástole y una dependencia marcada de la sístole auricular para el llenado ventricular. El derrame pericárdico, la dilatación de la aurícula derecha y el desplazamiento del tabique son predictores de mal pronóstico en pacientes con HAP grave12.
Sin embargo, esta técnica presenta limitaciones. Es dependiente del explorador, precisa regurgitación tricuspídea para estimar la PAPS, y no es detectable en el 15-26% de los pacientes13, es necesaria una buena ventana acústica y la correcta alineación de la señal Doppler, y no es capaz de determinar la presión arterial pulmonar diastólica.
En la mayor parte de los estudios en pacientes con HAP idiopática se ha observado una elevada correlación (0,57-0,93) entre las mediciones de la PAPS realizadas mediante ETT y CCD. Sin embargo, esto no ocurre en la HAP asociada a ES, y la discordancia es aún mayor en pacientes más graves (PAPS > 100 mmHg y clase IV), en las formas asociadas a enfermedad pulmonar avanzada y en valores límites (PAPS < 50 mmHg y/o VRT < 3 m/s)14, por eso es necesaria la confirmación mediante CCD.
La ecocardiografía de esfuerzo es una técnica sensible para identificar a los pacientes que sólo presentan una elevación de las RVP con el ejercicio15, pero aún no se ha concretado el rango de presiones fisiológicas (p. ej., se han encontrado valores más elevados en atletas). Se necesitan, pues, más estudios para precisar su utilidad como cribado preclínico en la HAP asociada a conectivopatías, así como su posible valor pronóstico.
Pruebas de función respiratoria
Los pacientes con HAP tienen normalmente una capacidad de difusión para el monóxido de carbono (DLCO) disminuida, típicamente en el rango del 40-80% del predecible, de forma desproporcionada a la reducción leve o moderada de la capacidad vital forzada (CVF). Por esta razón, si calculamos el cociente CVF%/DLCO% (ambos valores en porcentaje respecto a la población normal), estará generalmente por encima de 1,8. Esto nos va a ayudar en el diagnóstico diferencial de la EPI, en la que ambos valores disminuyen de forma paralela y el cociente CVF%/DLCO% se encontrará por debajo de 1,4. Cuando coexisten ambas patologías tendremos cifras medias en torno a 1,4-1,8. Además, hay que tener en cuenta que una atrofia de la musculatura respiratoria o una afectación cutánea extensa condicionan también un patrón restrictivo en las PFR.
Por otra parte, las PFR tienen valor pronóstico. Se ha demostrado que la disminución de DLCO por debajo del 55% y un cociente CVF%/DLCO% elevado son excelentes predictores del desarrollo de HAP en pacientes con ES16, y se asocian a la gravedad de ésta y a la supervivencia17.
Gasometría arterial
La presión arterial de oxígeno (PaO2) es normal o sólo ligeramente más baja de lo normal, y la presión arterial de dióxido de carbono (PaCO2) está disminuida y existe moderada alcalosis respiratoria como resultado de la hiperventilación alveolar.
Electrocardiograma
Encontramos signos de hipertrofia con sobrecarga del ventrículo derecho y dilatación de la aurícula derecha, pero los hallazgos son tardíos y su sensibilidad es baja para ser útil como técnica de cribado. Un ECG normal no excluye la presencia de HAP grave18. Sin embargo, es útil para descartar trastornos del ritmo asociados y aporta información pronóstica en pacientes con HAP conocida: el aumento de la altura y la amplitud de la onda P en la derivación II y los criterios de hipertrofia de ventrículo derecho de la OMS predicen la supervivencia19.
Radiografía torácica
Los hallazgos en la radiografía de tórax también aparecen de forma tardía y no se correlacionan con la gravedad de la HAP. Se observa aumento de hilios pulmonares con hiperclaridad pulmonar periférica y aumento de cavidades cardíacas derechas. Es útil a la hora de valorar la progresión de la enfermedad y para descartar patología asociada, como la EPI, la enfermedad pulmonar obstructiva crónica o la insuficiencia cardíaca moderada o grave.
Test de la marcha de 6 min
La disnea de esfuerzo es el síntoma principal de la HAP, y es fundamental su valoración y control sistemático. Los pacientes se pueden clasificar según el estadio funcional de la OMS/NYHA (tabla 2). También se puede valorar el grado de disnea de los pacientes con HAP, su evolución y la respuesta al tratamiento, recogiendo la distancia recorrida en el test de la marcha de 6 min y mediante la subsiguiente evaluación de la disnea percibida con la escala de Borg (tabla 3). Se ha demostrado, asimismo, que esta evaluación de la capacidad de esfuerzo tiene valor pronóstico20. Una reducción de la saturación arterial de oxígeno > 10% durante la prueba de la marcha de 6 min se asocia con un incremento del riesgo de mortalidad de 2,9 veces durante un período medio de 26 meses21.
Otras exploraciones complementarias
La pulsioximetría nocturna es útil para el diagnóstico del síndrome de apnea-hipopnea del sueño, aunque también puede existir hipoxemia nocturna en pacientes con HAP. La tomografía computarizada de alta resolución (TCAR) permite obtener imágenes muy detalladas del parénquima pulmonar y facilita el diagnóstico de EPI y de enfisema. Para descartar HAP asociada a tromboembolismo pulmonar (TEP) crónico, la gammagrafía de ventilación-perfusión y la tomografía computarizada con contraste (detecta TEP proximales pero no descarta lesiones distales) son las exploraciones iniciales, y la angiografía es el patrón oro. La ecografía abdominal se solicita en casos de sospecha de cirrosis o hipertensión portal. Se precisa analítica sanguínea con serologías víricas para descartar alteraciones tiroideas, trastornos mieloproliferativos, coagulopatías e infección por el VIH, que puede ser causa de HAP.
La resonancia magnética cardiopulmonar funcional está en desarrollo. Puede calcular fracciones de eyección ventricular, así como velocidades y volúmenes en arterias pulmonares. El fragmento N-terminal del pro-BNP (brain natriuretic peptide) en plasma está relacionado con el grado o la gravedad de la HAP. Los pacientes con ES que presentan valores de N-TproBNP por encima de 395 pg/ml tienen una alta probabilidad de presentar HAP22.
Cateterismo cardíaco derecho
Es el patrón oro en el diagnóstico de HAP, y es necesario para valorar la gravedad del impacto hemodinámico y para medir la vasorreactividad de la circulación pulmonar10. Deberían valorarse siempre los siguientes parámetros: frecuencia cardíaca, PAD, presión arterial pulmonar (PAP) (sistólica, diastólica y media), PCP, gasto cardíaco, presión arterial, RVP, resistencia vascular sistémica, saturación arterial y venosa mixta. La HAP se define como una PAP media > 25 mmHg en reposo o > 30 mmHg durante el ejercicio, con una PCP # 15 mmHg y una RVP > 3 unidades Wood.
En la valoración de la vasorreacitividad, la respuesta aguda positiva se define como una reducción de la PAP media # 10 mmHg, para alcanzar un valor absoluto de PAP media # 40 mmHg con un gasto cardíaco aumentado o sin cambios23. Se utilizan fármacos intravenosos como la adenosina y el epoprostenol, y el óxido nítrico inhalado. Un test positivo predice sólo una respuesta favorable al tratamiento con antagonistas del calcio. Su utilidad es dudosa en la ES, ya que menos del 10% de pacientes presentan respuesta y, de éstos, sólo la mitad la mantienen al cabo de un año.
ALGORITMO DE CRIBADO
Basándonos en las guías de práctica clínica para el diagnóstico precoz de la HAP del American College of Chest Physicians (ACCP)24 y en otros trabajos realizados en población europea10,11,25, exponemos las actuales recomendaciones basadas en la evidencia:
Conocer las enfermedades reumáticas que se pueden asociar a HAP (ES, LES y EMTC, y con menor frecuencia artritis reumatoide, dermatomiositis-polimiositis y síndrome de Sjögren).
Realizar a todo paciente con sospecha de HAP un ECG, una radiografía de tórax, una PFR y una ETT.
Especialmente en los pacientes con ES, las PFR y la ETT se deben realizar cada 6 o 12 meses.
Otras pruebas, como el test de la marcha de 6 min y la determinación de la clase funcional, se deben realizar periódicamente para valorar la progresión de la enfermedad y la respuesta al tratamiento.
Confirmar siempre la sospecha diagnóstica con el CCD, que además permite establecer la etiología y determinar el estadio o la gravedad de la HAP.
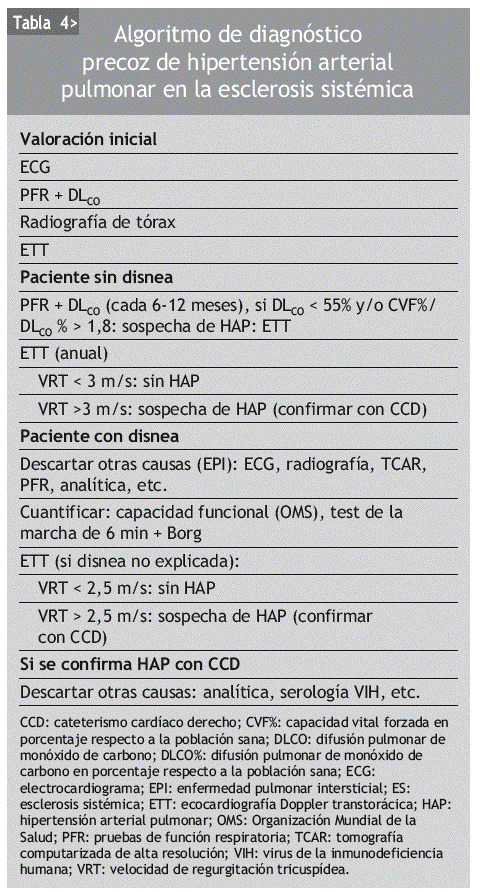
En la tabla 4 proponemos un algoritmo diagnóstico que combina los hallazgos ecocardiográficos y de las PFR con la clínica respiratoria.
CONCLUSIÓN
La falta de síntomas y signos clínicos tempranos es la razón para el uso periódico de herramientas de cribado que descarten la HAP en pacientes con ES y en otros pacientes de riesgo. Como ya hemos visto, ninguna exploración complementaria no invasiva tiene suficiente sensibilidad para el diagnóstico precoz, y aún no se ha establecido un método de cribado definitivo. Por esta razón es interesante utilizar un algoritmo que combine los hallazgos clínicos con las diferentes exploraciones complementarias para acercarnos al diagnóstico de sospecha de la HAP, que siempre debe confirmarse mediante CCD.