Objetivo. Sustitución endoprotésica de la fractura de la cabeza radial no reconstruible para restituir la estabilidad de la articulación del codo y para evitar complicaciones secundarias como la deformidad en valgo del codo y la migración proximal del radio.
Indicaciones. Asistencia primaria de una fractura de cabeza radial no reconstruible sin lesiones asociadas (Mason Tipo III) y con lesiones asociadas (Mason Tipo IV), lesión de Essex-Lopresti, asistencia secundaria después de la resección de la cabeza radial e inestabilidad en la articulación del codo o molestias en la articulación radioulnar distal, intento de conservación fallido después de la reconstrucción de la cabeza radial mediante osteosíntesis, así como resección tumoral del cuello o de la cabeza del radio.
Contraindicaciones. Contraindicaciones médicas generales de cualquier intervención quirúrgica, alergia al cobalto-cromo, así como osteoporosis del radio proximal.
Técnica quirúrgica. Con el paciente en posición de decúbito supino, el acceso a la articulación del codo se realiza lateral o posterolateral. Después de seccionar el ligamento anular, la cabeza radial se reseca justo por encima de la tuberosidad del radio. Con el antebrazo en posición pronadora se efectúa el escariado del canal intramedular con la raspa correspondiente sin dañar el nervio radial y se determina el tamaño de la prótesis, asegurando la estabilidad de cúbito y radio. Se deberá tener en cuenta la estabilidad ulnar y radial. El fabricante recomienda una distancia de 0,5 mm aproximadamente entre la cabeza de la prótesis y el cóndilo humeral. La prótesis se introducirá mediante la técnica de cementación y usando un tapón intramedular. Se deberá tener en cuenta que el cuello del vástago se encuentre sobre la superficie de resección del radio y que la concavidad del cuello de la prótesis esté ajustada en sentido radial hacia el antebrazo en posición de pronación. Después de suturar el ligamento anular, se verificará la estabilidad de la articulación; en caso necesario, se reconstruirá el ligamento colateral medial y se cerrará la herida.
Tratamiento postoperatorio. Tratamiento funcional postoperatorio precoz ilimitado a partir del primer día postoperatorio. Si se presentan lesiones asociadas se puede aplicar una férula de yeso durante tres o cuatro semanas. Para prevenir osificaciones hetereotópicas se suministrarán antiinflamatorios no esteroideos dos veces al día previa protección suficiente de la mucosa gástrica durante dos a cuatro semanas.
Resultados. En total, se pudo hacer el seguimiento de trece pacientes con quince prótesis en un periodo medio de 29,5 ± 20,8 meses. El codo afectado se había estabilizado en todos los pacientes. A modo subjetivo, con una excepción, los pacientes valoraron los resultados entre buenos y muy buenos. En comparación con el estado anterior al accidente, la valoración subjetiva del codo fue del 78 ± 12%. La función del codo se valoró con seis resultados buenos y nueve excelentes según la escala de evaluación de Radin y Riseborough. Según la escala de Broberg y Morrey, se obtuvo un resultado excelente, ocho resultados buenos y seis regulares. El valor medio de la escala DASH fue de 9,9 ± 9,7 puntos. Las complicaciones postoperatorias que aparecieron fueron dos casos de lesiones nerviosas temporales de carácter regresivo. En cinco casos se diagnosticaron heterotopias de grado I, en dos casos osificaciones de grado II según la escala Brooker.
Introducción
La fractura de la cabeza del radio supone el 30% de las fracturas y es la más frecuente en la articulación de codo16.
Además de los traumatismos directos, el mecanismo de fractura más frecuente es la caída sobre la articulación de la mano en posición dorsal con el antebrazo extendido en pronación2. La cabeza del radio golpea contra el cóndilo humeral y se fractura. Amis y Miller2 detectaron en un estudio realizado con cadáveres que la cabeza del radio absorbe la fuerza en la articulación del codo hasta una flexión de 80º y que luego se rompe por sobreesfuerzo.
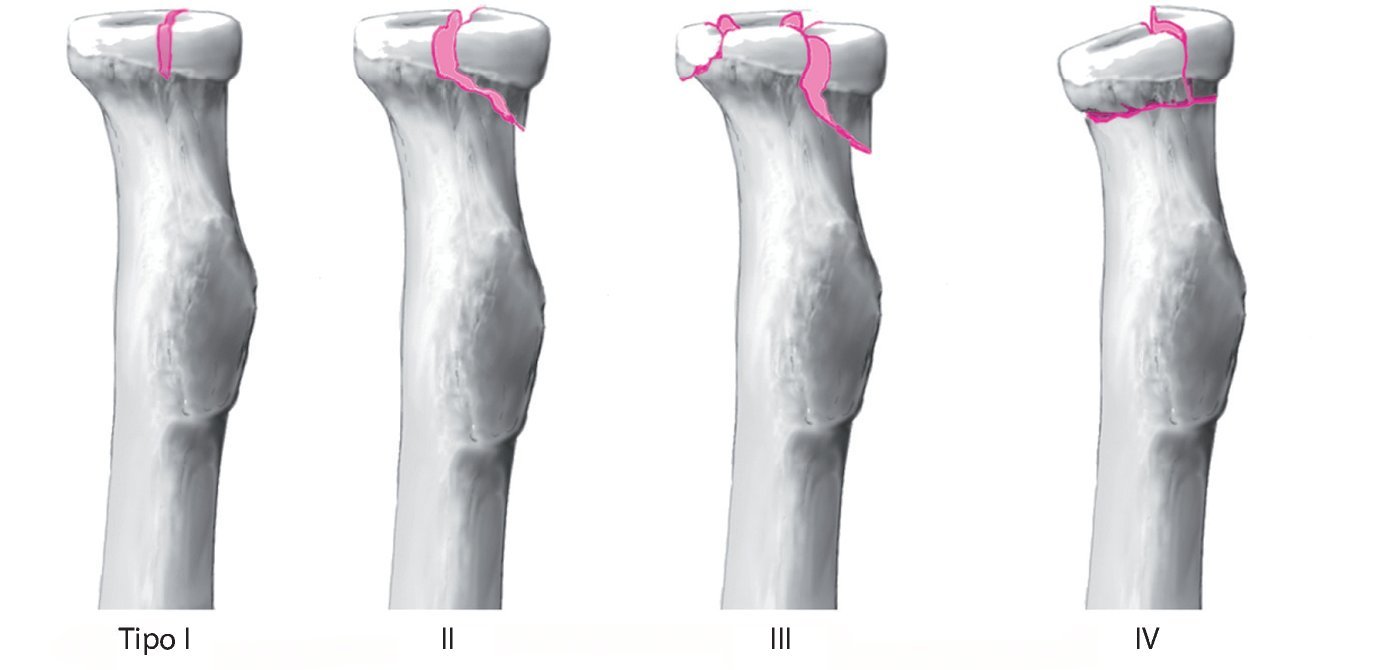
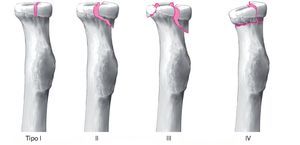
La clasificación de las formas de fractura según el grado y la dislocación descrita por Mason en el año 195416 y ampliada por Johnston11 en 1962 tiene amplia aceptación en la literatura especializada (fig. 1):
Fig. 1 El sistema de clasificación de las fracturas de cabeza radial según Mason16, modificado por Johnston11. Johnston describió la fractura de tipo IV como fractura de cabeza radial con luxación de la articulación del codo.
—Tipo I: fractura no desplazada.
—Tipo II: fractura marginal de la cabeza radial con desplazamiento de articulación radiológicamente visible de más de 2 mm y con afectación de más de una cuarta parte de la superficie de la articulación.
—Tipo III: fractura conminuta de la cabeza radial sin lesiones asociadas.
—Tipo IV: fractura conminuta de la cabeza radial con lesiones asociadas.
El objetivo del tratamiento es una terapia por estadios de la fractura de la cabeza radial garantizando la libre movilidad de la articulación radioulnar y humeroradial proximal. El tratamiento de la fractura del tipo I forma parte de la terapia conservadora, ya que esta puede curarse con buenos resultados funcionales16,18,22. Las fracturas del tipo II según la clasificación de Mason se pueden estabilizar internamente después de una reposición abierta y una reconstrucción anatómica de la superficie articular21,23. Con frecuencia, en las fracturas del tipo III y IV no es posible conseguir una reconstrucción anatómica, de modo que en la literatura se opta por una resección precoz1,10,16. Böhler4, por su parte, ya recomendaba la resección de la cabeza radial durante las primeras horas después de originarse la fractura, pero nunca entre el tercer y el vigésimo día después de la misma.
No son raros los casos en los que aparecen efectos negativos a largo plazo en la articulación del codo y de la mano después de una resección única de la cabeza radial5,10,14. Se describe una deformación progresiva en valgo con sensación de inestabilidad en el codo, la migración del radio proximal con molestias en la articulación radioulnar distal y un desgaste precoz de la articulación humeroulnar7,19.
Ello es debido a que la cabeza radial es, junto con el ligamento colateral ulnar, el estabilizador secundario de la articulación del codo contra el estrés en valgo19.
Aproximadamente el 40% de la transferencia de la fuerza que tiene lugar desde el antebrazo hacia el brazo se realiza a través de la cabeza radial19. La no existencia de la cabeza radial puede producir una insuficiencia de la columna radial y, como consecuencia, la inestabilidad de la articulación del codo3.
Por este motivo, se recomienda realizar el reemplazo protésico y la sutura de los ligamentos colaterales afectados inmediatamente después de producirse la herida de cabeza radial o en segundo lugar después de la resección3,13,17,24. Mediante un reemplazo endoprotético de la cabeza radial no reconstruible se garantiza la reconstrucción de la columna radial y con ello la restitución de la integridad de la articulación del codo.
De este modo, se puede evitar la inestabilidad en valgo y prevenir la desviación radial de la mano causada por una posible migración proximal del radio. Ello permite un tratamiento funcional precoz, especialmente en caso de existencia de lesiones asociadas.
La sustitución endoprotética de la cabeza radial no reconstruible es una práctica todavía no muy extendida. Los modelos de prótesis de la primera generación, las prótesis de silicona de Swanson y las de vitalio no cumplían los requisitos biomecánicos ni de técnica ni de material. Durante el periodo en que fueron utilizados se registraron sinovitis debida al desgaste del silástico, dislocaciones de prótesis o desgastes precoces del tejido cartilaginoso en el cóndilo humeral provocadas por una congruencia insuficiente entre metal y cartílago en las prótesis de tipo monoblock de metal25,26.
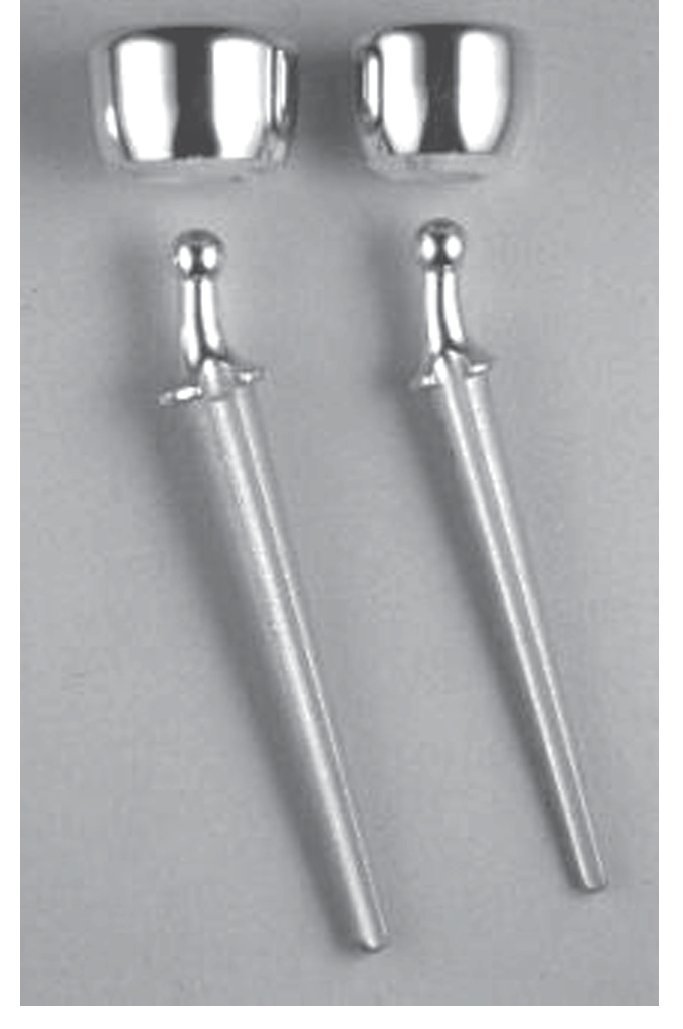
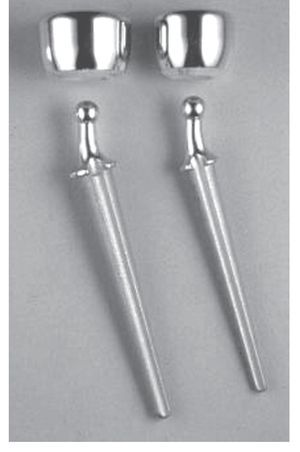
La articulación en bola entre el vástago y la cabeza de la prótesis de las prótesis bipolares CRF-II desarrolladas por Judet et al12 (fabricante Tornier, Burscheid, Alemania; fig. 2) permiten un ángulo de movimiento de 35º en todos los niveles y, por tanto, un ajuste óptimo entre la cabeza de la prótesis, el cóndilo humeral correspondiente y la incisura radial. Su diseño anatómico y su sistema modular permiten diferentes tamaños de cabeza y de vástago, de modo que se pueden adaptar perfectamente a la anatomía de cada paciente.
Fig. 2 Prótesis de cabeza radial bipolar (CRF II según Judet, fabricante Tornier, Burscheid, Alemania) formada por una cabeza de polietileno (con revestimiento de cromo-cobalto) y un vástago de cromo-cobalto.
Nuestro equipo de trabajo pudo demostrar que con la prótesis CRF-II, especialmente en presencia de lesiones asociadas, se obtiene una buena estabilidad y se evitan complicaciones típicas como las que aparecen después de una resección única de cabeza radial20. Los pacientes no mostraron ninguna sensación permanente de inestabilidad y no se dio tampoco ningún caso de cubitus valgus, de desmineralización, artritis en el cóndilo humeral o molestias en la articulación de la muñeca. Mientras que el uso de la prótesis en lesiones asociadas como la inestabilidad del ligamento colateral cubital y/o fracturas (Mason IV) es ya un hecho reconocido8,9, creemos -como Judet et al12- a causa de los excelentes y buenos resultados subjetivos, así como a las bajas tasas de complicaciones intra y postoperatorias, que sería indicada también para ser implantada en lesiones únicas de la cabeza radial (Mason III).
Principios quirúrgicos y objetivos
Reconstrucción de la columna radial de la articulación del codo como prevención de una inestabilidad en valgo y una proximalización del radio con la consecuencia de una desviación radial de la mano y las molestias resultantes en la articulación radioulnar distal. Protección mecánica de lesiones asociadas eliminadas mediante intervención quirúrgica como la sutura del ligamento colateral ulnar o la osteosíntesis de fracturas de codo proximales.
Ventajas
—Restitución de la estabilidad de la articulación del codo.
—Evitar deformaciones en la articulación radioulnar distal.
—Movilización funcional precoz de la articulación del codo.
—Protección mecánica de lesiones asociadas.
—Gran aceptación entre los pacientes.
—Adaptación de la cabeza invertida al cóndilo humeral y a la incisura radial.
—Diseño de prótesis modular para la adaptación a diferentes estructuras anatómicas.
Desventajas
—Osificaciones periarticulares.
—Falta de resultados a largo plazo.
—Coste de las prótesis.
—Técnica quirúrgica de gran complejidad técnica.
Indicaciones
—Asistencia primaria de una fractura de cabeza radial no reconstruible sin (Mason III) y con (Mason IV) lesiones asociadas.
—Lesión de Essex-Lopresti.
—Asistencia secundaria postraumática después de la resección de la cabeza radial e inestabilidad en la articulación del codo o molestias en la articulación radioulnar distal.
—Intento de conservación fallido después de la reconstrucción de la cabeza radial mediante osteosíntesis.
—Resección del cuello o cabeza radial debida a un tumor.
Contraindicaciones
—Contraindicaciones médicas generales de una intervención quirúrgica.
—Alergia al cromo-cobalto.
—Osteoporosis del radio proximal.
Información para el paciente
—Riesgos quirúrgicos generales.
—Posibilidad de una resección de cabeza radial única sin sustitución endoprotética.
—Debilidad temporal del nervio ulnar y del nervio radial.
—Osificaciones periarticulares.
—Posible falta de flexión y/o extensión.
—Posibilidad de que la prótesis se afloje con posible retirada de material.
—Importancia de un tratamiento postoperatorio de rehabilitación.
—Falta de resultados a largo plazo.
Preparación de la intervención
—Examen físico con inspección de las partes blandas para excluir heridas de abrasión así como verificar el flujo sanguíneo, la motricidad y la sensibilidad del brazo herido.
—Información al paciente sobre las posibles contraindicaciones.
—Radiografía del codo y de la articulación de la mano en dos niveles.
Instrumental
—Prótesis bipolar (CRF II según Judet, fabricante Tornier, Burscheid, Alemania: fig. 1) compuesta por una cabeza de polietileno (con revestimiento de cobalto-cromo) y un vástago de cobalto-cromo; a elegir entre dos tamaños diferentes y totalmente combinables.
¿Cabeza de la prótesis: diámetro de 19 o 22 mm para una altura unitaria de 14,7 mm.
¿Vástago de la prótesis: diámetro de 8 mm (por debajo de la base) y 60 mm de longitud, así como diámetro de 6,5 mm (por debajo de la base) y 55 mm de longitud. Ángulo cuello-vástago de 15º para la reconstrucción de la morfología disminuida del radio. Articulación reversa de la cabeza de la prótesis con la bola del cuello de la prótesis con un ángulo de movimiento de 35º en todas las direcciones.
—Ganchos pequeños Hohmann para la exposición del radio proximal.
—Sierra oscilante para la resección de la cabeza fracturada.
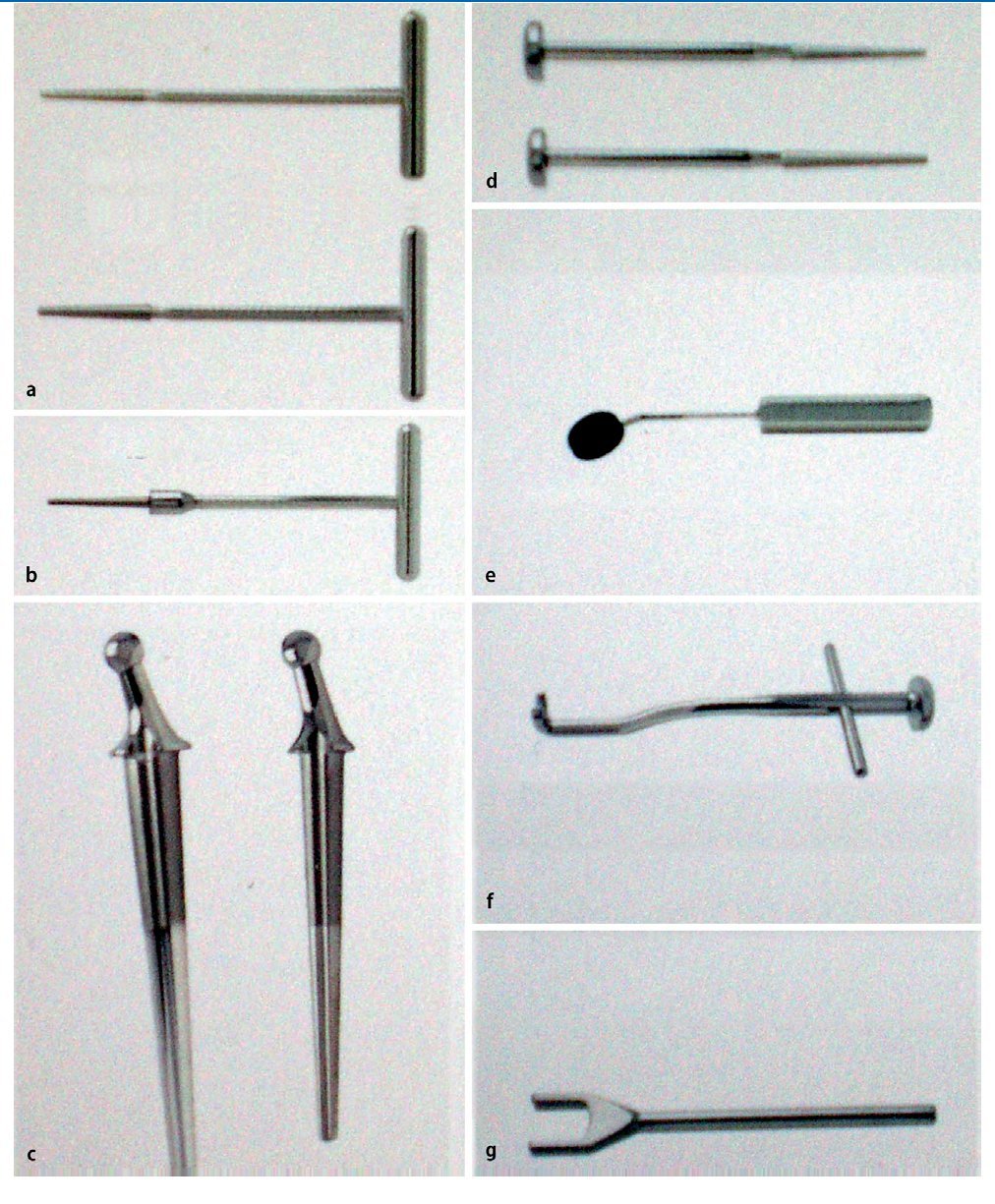
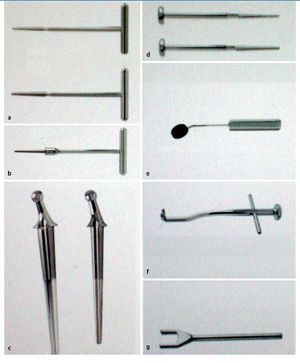
—Instrumental especial (fabricante Tornier, Burscheid, Alemania; fig. 3).
Fig. 3 Instrumental especial (fabricante Tornier, Burscheid, Alemania). Escariador de 6,5 y 8 mm de diámetro para preparar el canal intermedular (a); fresa piloto para la regulación de la superficie de osteotomía
(b); vástago de prueba de 6,4 y 8 mm de diámetro para la elección del tamaño de la prótesis (c); raspa de 6,5 y 8 mm de diámetro para rellenar el canal intermedular con fragmentos óseos de la cabeza radial reseccionada a modo de tapón restrictor de cemento (d); cabeza de prueba para determinar el tamaño de la cabeza (e); impactador para la introducción del vástago de la prótesis (f); plantilla para la determinación de la altura de resección (g).
Anestesia y posición del paciente
—Operación con anestesia total o regional.
—Posición decúbito supino, vaciado venoso del brazo proximal.
—Soporte para el brazo (aprox. 25 ´ 25 cm), que no se montará a la altura del hombro, sino a la altura del tórax del paciente, de modo que el codo está apoyado y el cirujano tiene un buen acceso al codo por rotación en el hombro.
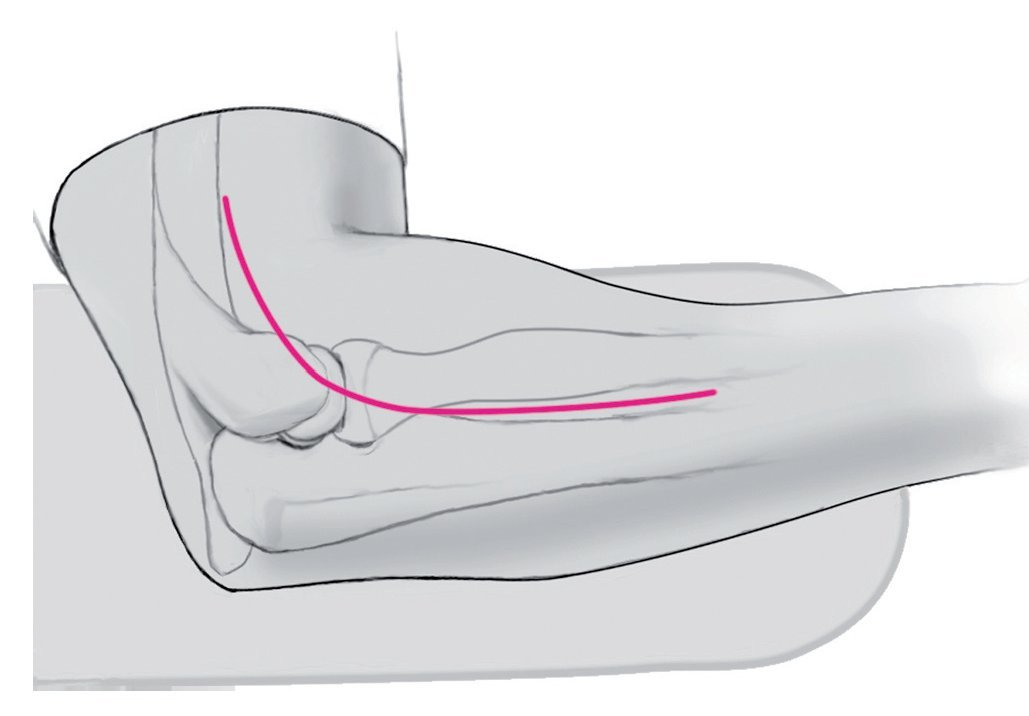
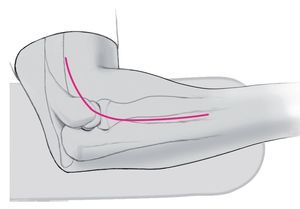
—Marcar la incisión sobre la piel (fig. 4).
Técnicas quirúrgicas
(Figs. 4-15)
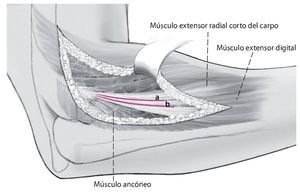
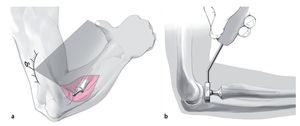
Fig. 4 Colocar el antebrazo en pronación para desplazar el nervio radial a posición medial. Realizar una incisión lateral de aproximadamente 8 cm en ángulo sobre la piel del codo doblado. La incisión se realizará desde proximal 2 cm a lo largo del eje del brazo y 6 cm en dirección diáfisis.
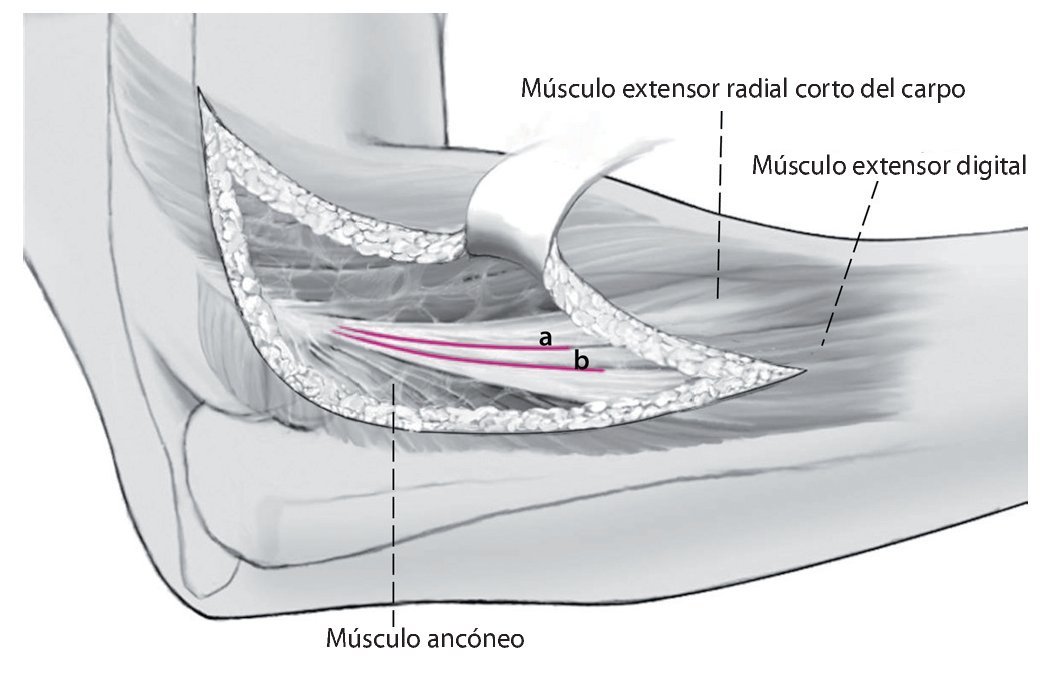
Fig. 5 Abordaje lateral (a) entre el músculo extensor radial corto del carpo y el músculo digital común. Como alternativa se puede elegir el abordaje posterolateral (b) entre el músculo extensor digital común y el músculo ancóneo. Este ofrece un abordaje algo más distal con respecto al radio.
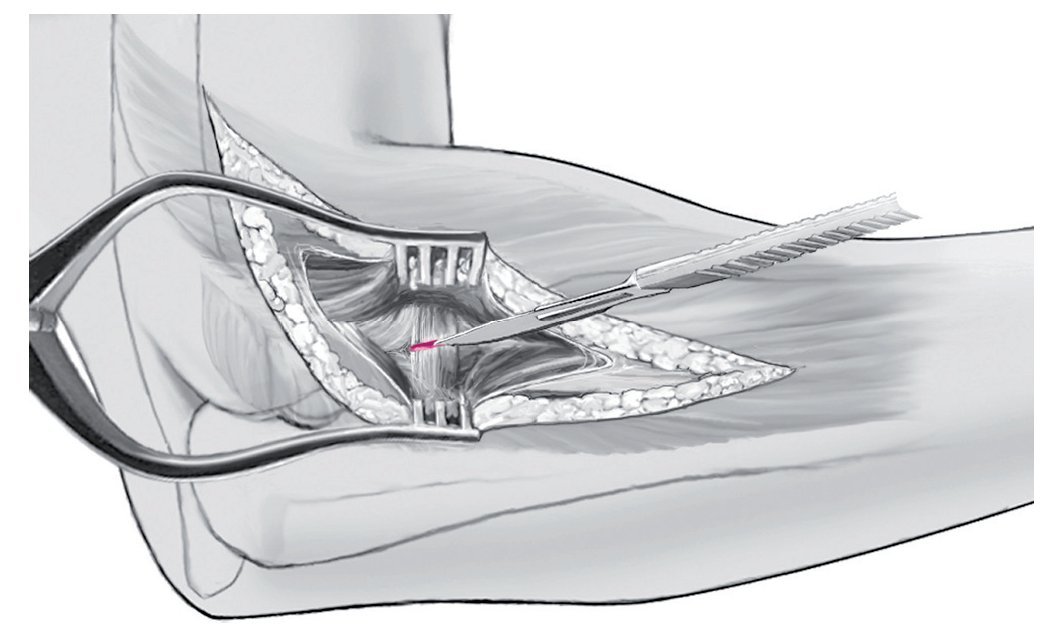
Fig. 6 El abordaje a la cabeza radial se realiza a través de la abertura del ligamento anular.
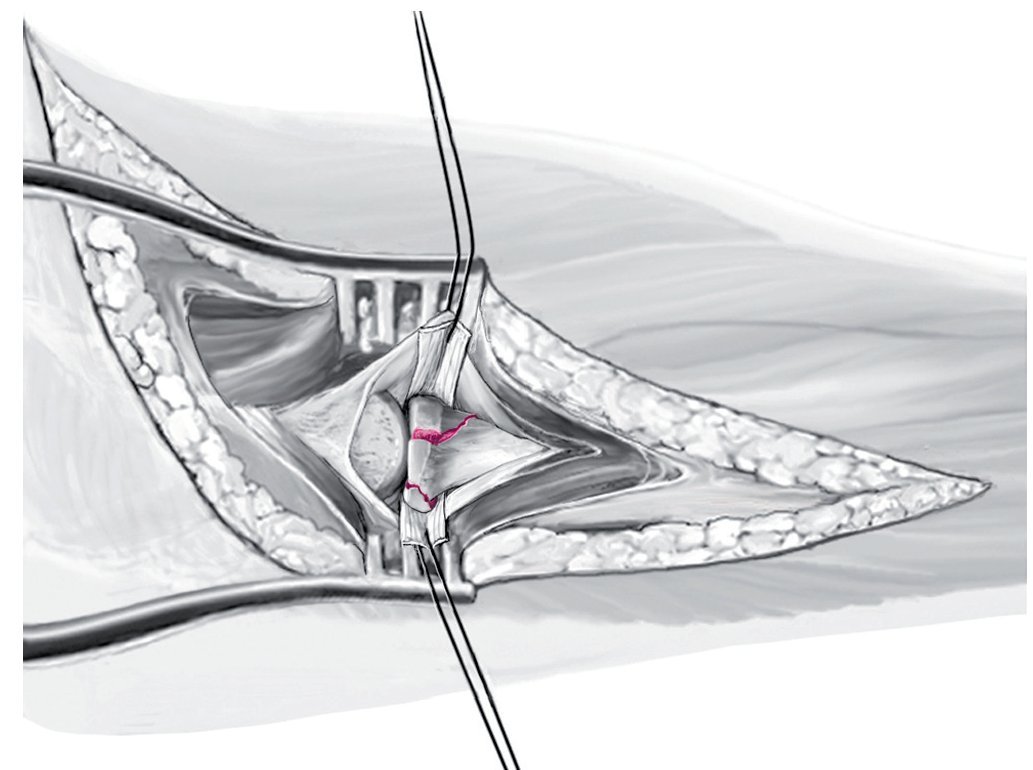
Fig. 7 Después de separar el ligamento anular se sujetan los dos extremos con hilos.
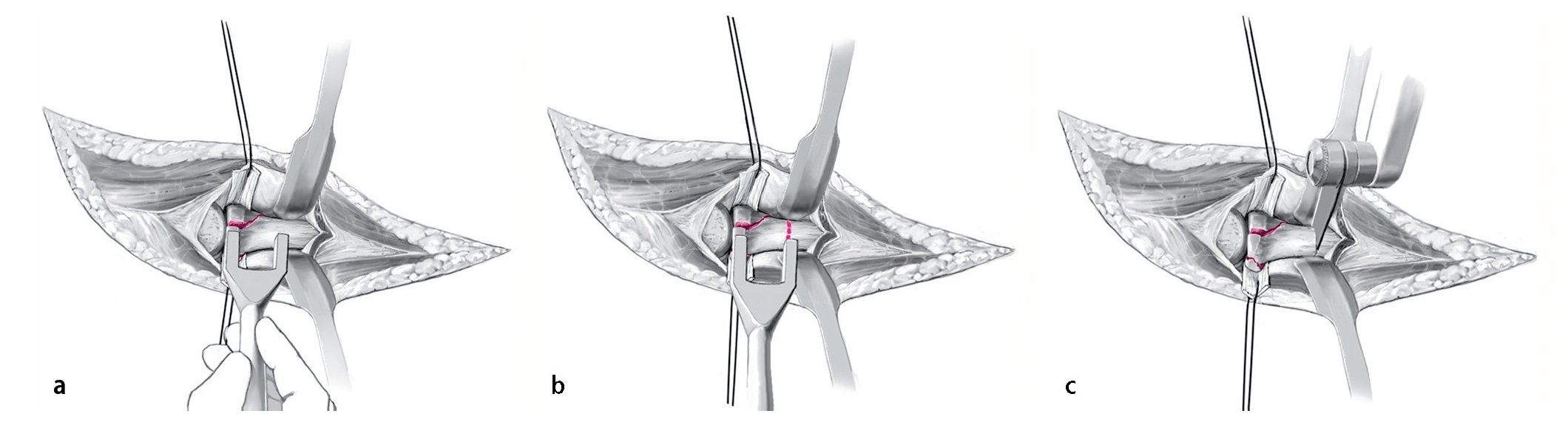
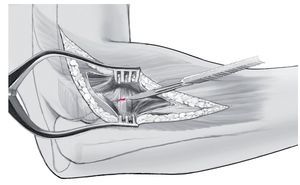
Fig. 8 Para la exploración de la cabeza radial fracturada se colocan dos ganchos Hohmann angulados en el cuello del radio. La altura de resección en el cuello del radio se determina con una plantilla (a, b). La resección se realiza mediante una sierra oscilante a una distancia de 23 mm por debajo del cóndilo humeral (c).
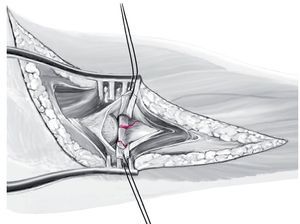
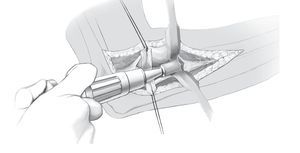
Fig. 9 La superficie para la osteotomía se regula con una fresa piloto, de manera que se crea una congruencia entre el cuello de la prótesis y la superficie de resección (a). El lecho diafásico del implante se prepara con escariadores de medida secuencial (b). Así también es posible determinar el diámetro de vástago definitivo.
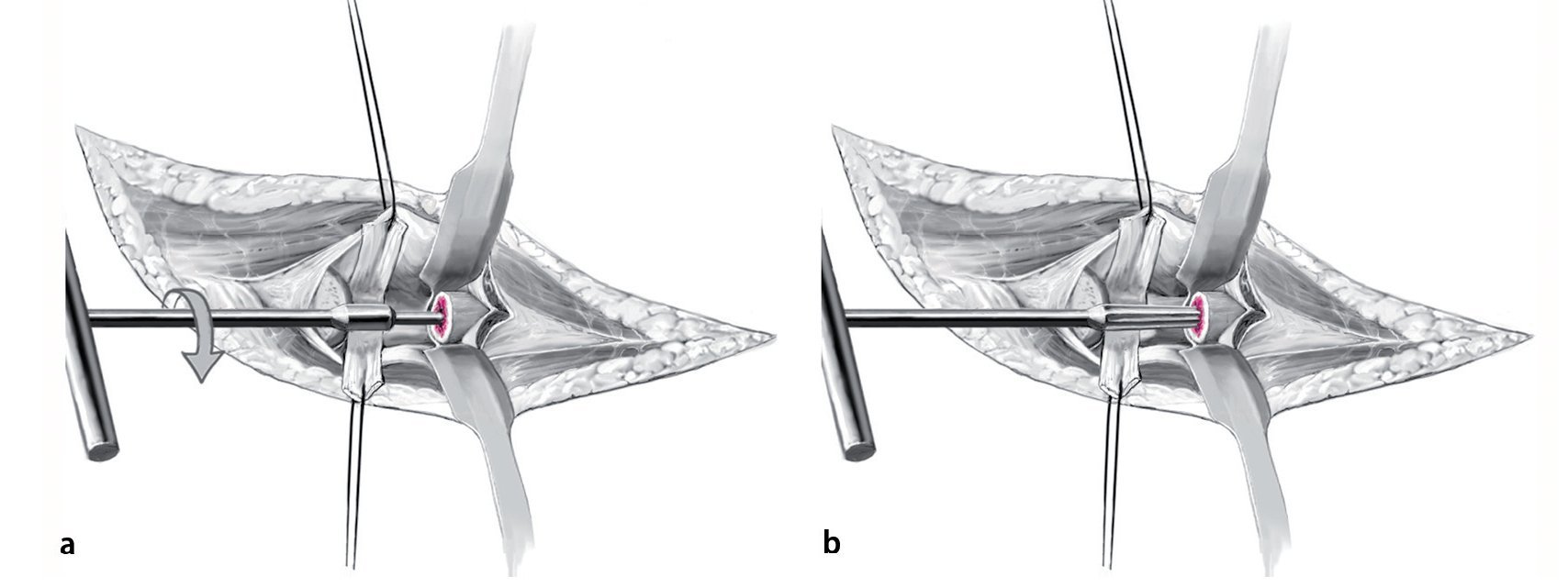
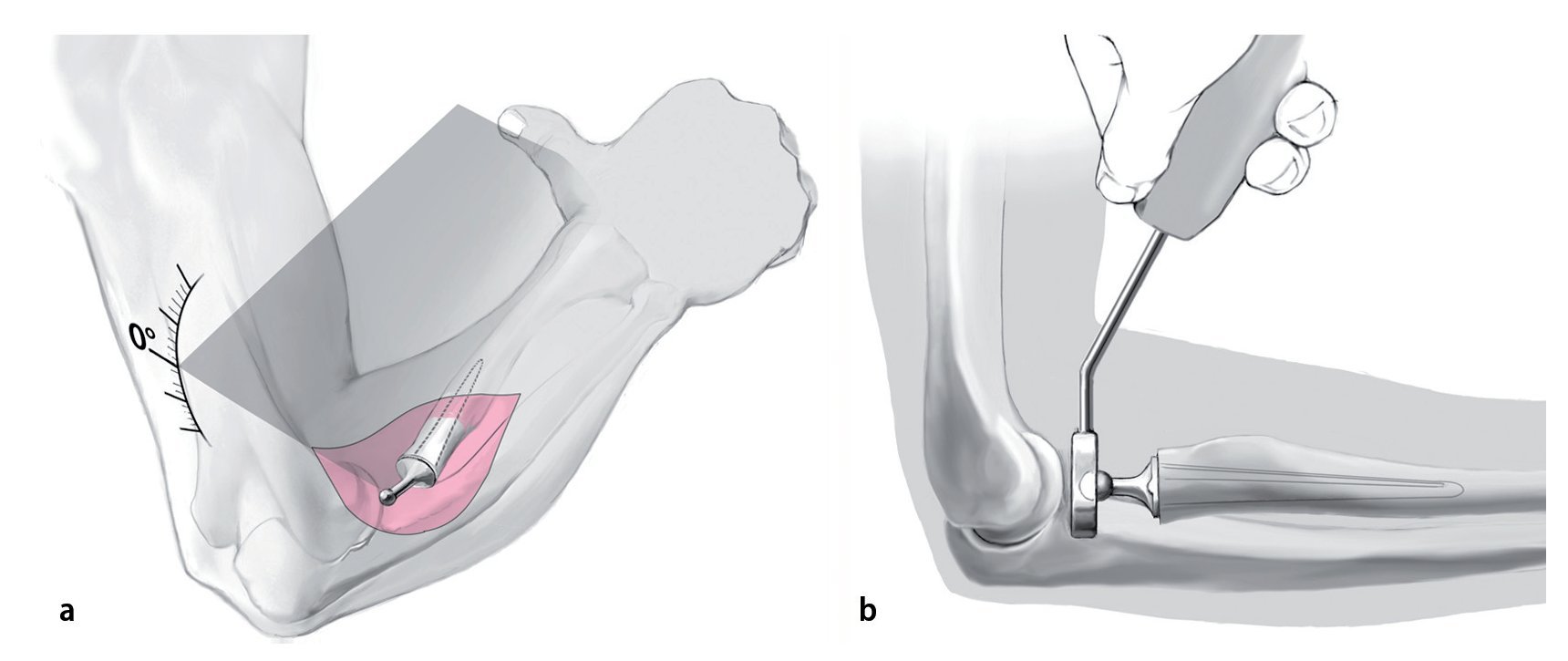
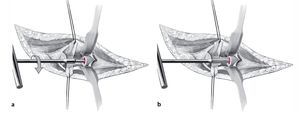
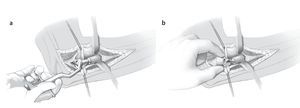
Fig. 10 En el momento de introducir la cabeza de prueba se debería tener en cuenta que el cuello de la prótesis esté situado sobre la superficie de osteotomía y que esté alineado según el ángulo anatómico, es decir, hacia cubital y hacia radial (a). De este modo se reconstruye la morfología normal curva del radio. La cabeza de prueba se orienta a la cabeza radial del paciente. El fabricante recomienda mantener una distancia de 0,5 mm aproximadamente entre la cabeza de prueba y el cóndilo humeral (b).
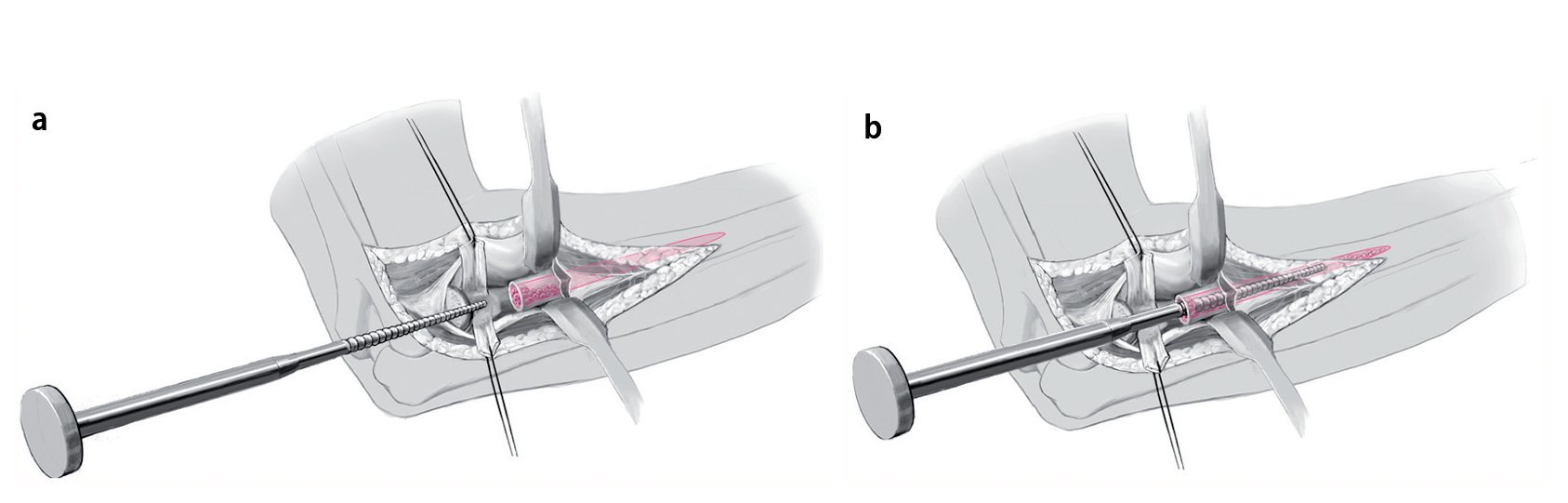
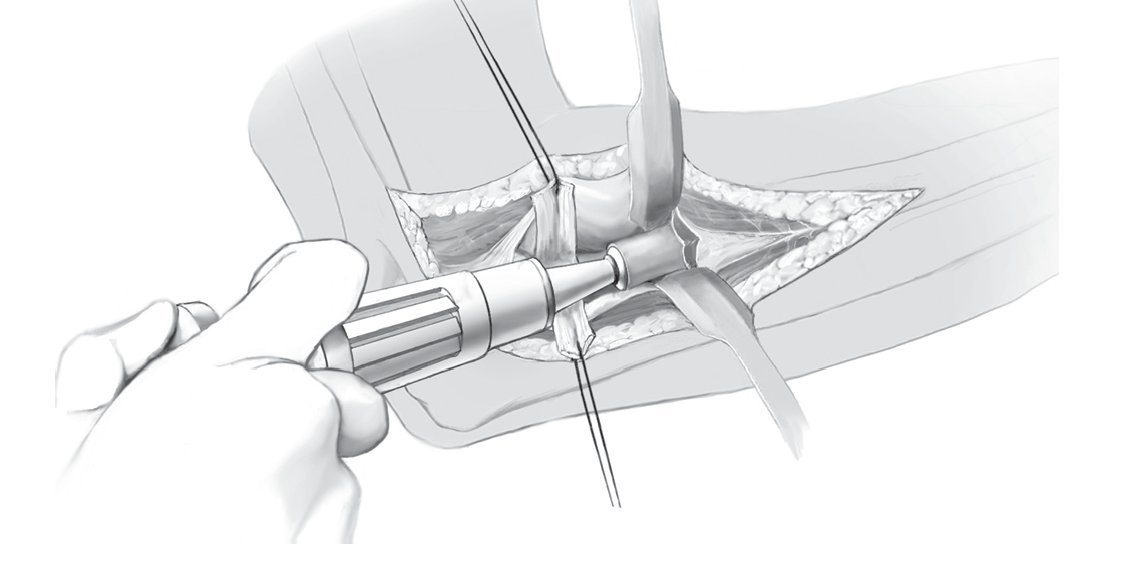
Fig. 11 Como tapón intramedular se utilizan fragmentos óseos obtenidos de la resección de la cabeza radial (a) y con ayuda del escariador, que se corresponde al tamaño de la prótesis, se introducen en el vástago de la prótesis (b). A continuación se lava la cavidad intramedular.
Fig. 12 Usando la técnica de cementación de tercera generación se inyecta mediante jeringa cemento óseo de baja viscosidad en la cavidad intramedular.
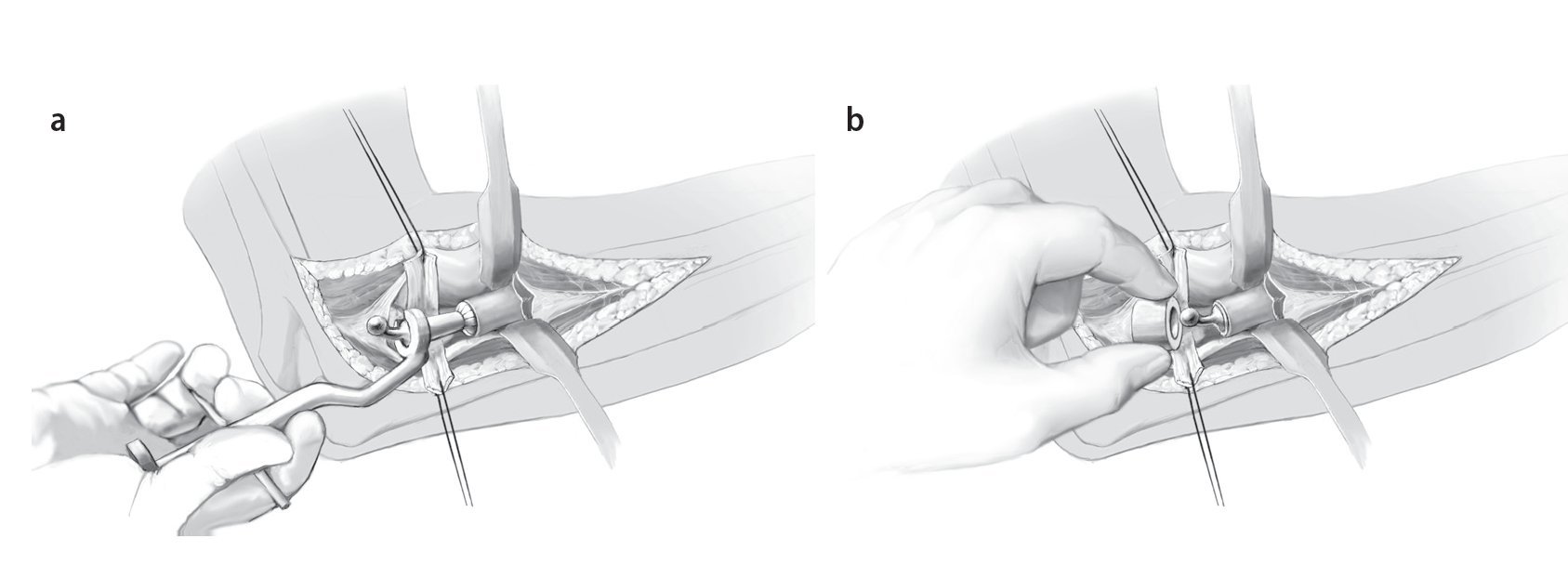
Fig. 13 Mediante un impactador se inserta el vástago de la prótesis dentro de la cavidad intramedular llena de cemento óseo y se posiciona en alineación anatómica (a). Se tendrá en cuenta que el collar de la prótesis esté situado sobre el borde de resección ósea. De este modo, la prótesis queda sujeta hasta el completo endurecimiento del cemento. La cabeza radial elegida se coloca sobre el collar de la prótesis y tiene que encajar de forma audible (b).
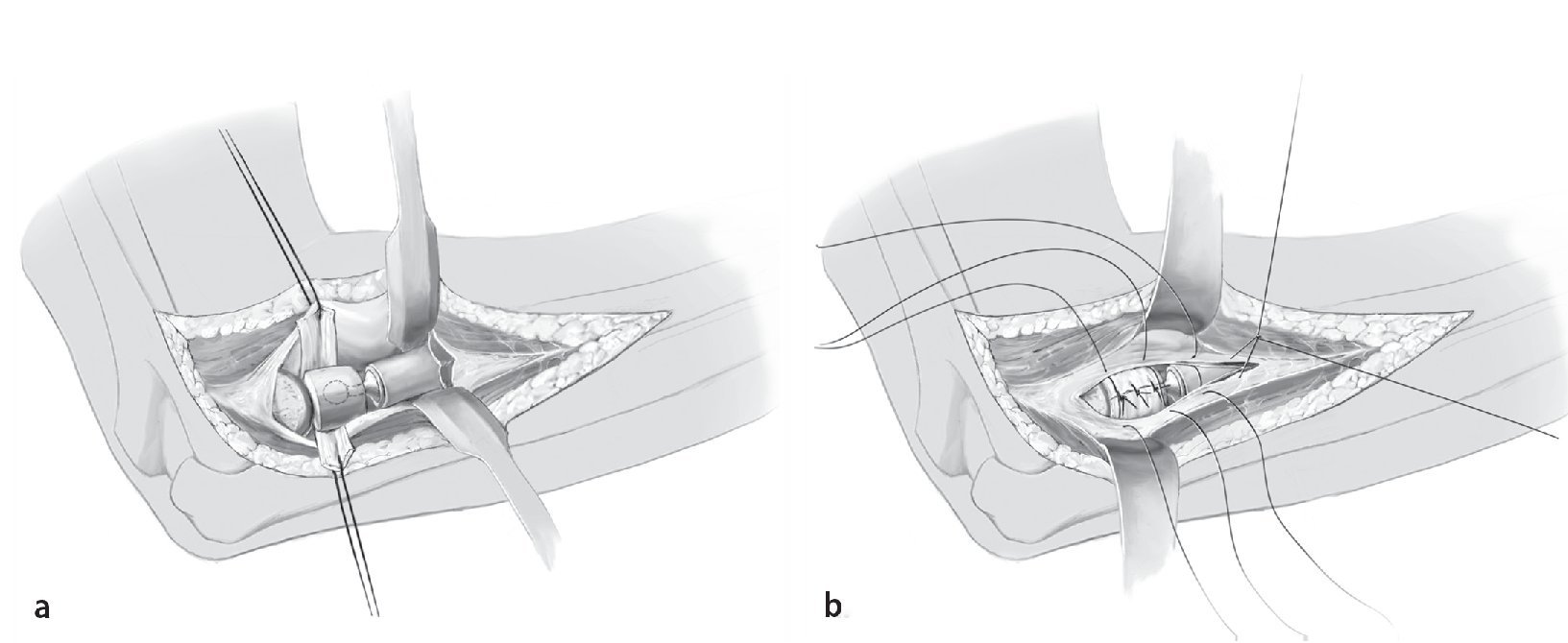
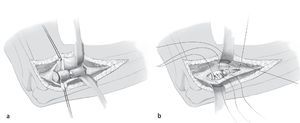
Fig. 14 Después de la reposición se verificarán la movilidad y la estabilidad de la articulación del codo en posición de extensión, flexión, pronación y supinación antes (a) y después de la sutura del ligamento anular (b). Si a pesar de implantar la prótesis persiste una inestabilidad en valgo, se deberán seguir las indicaciones para la reconstrucción del ligamento medial colateral. Finalmente, el asiento de la prótesis se controla mediante monitorización y se documenta. La sutura de la herida se realiza por capas mediante la técnica de sutura de punto simple después de efectuar un drenaje de Redón del n.º 10 subcutáneo (monocryl 3/0, reabsorbible). El cierre se realiza con sutura intracutánea continua de la piel (monocryl 4/0, reabsorbible) y sutura adhesiva Steri Strip.
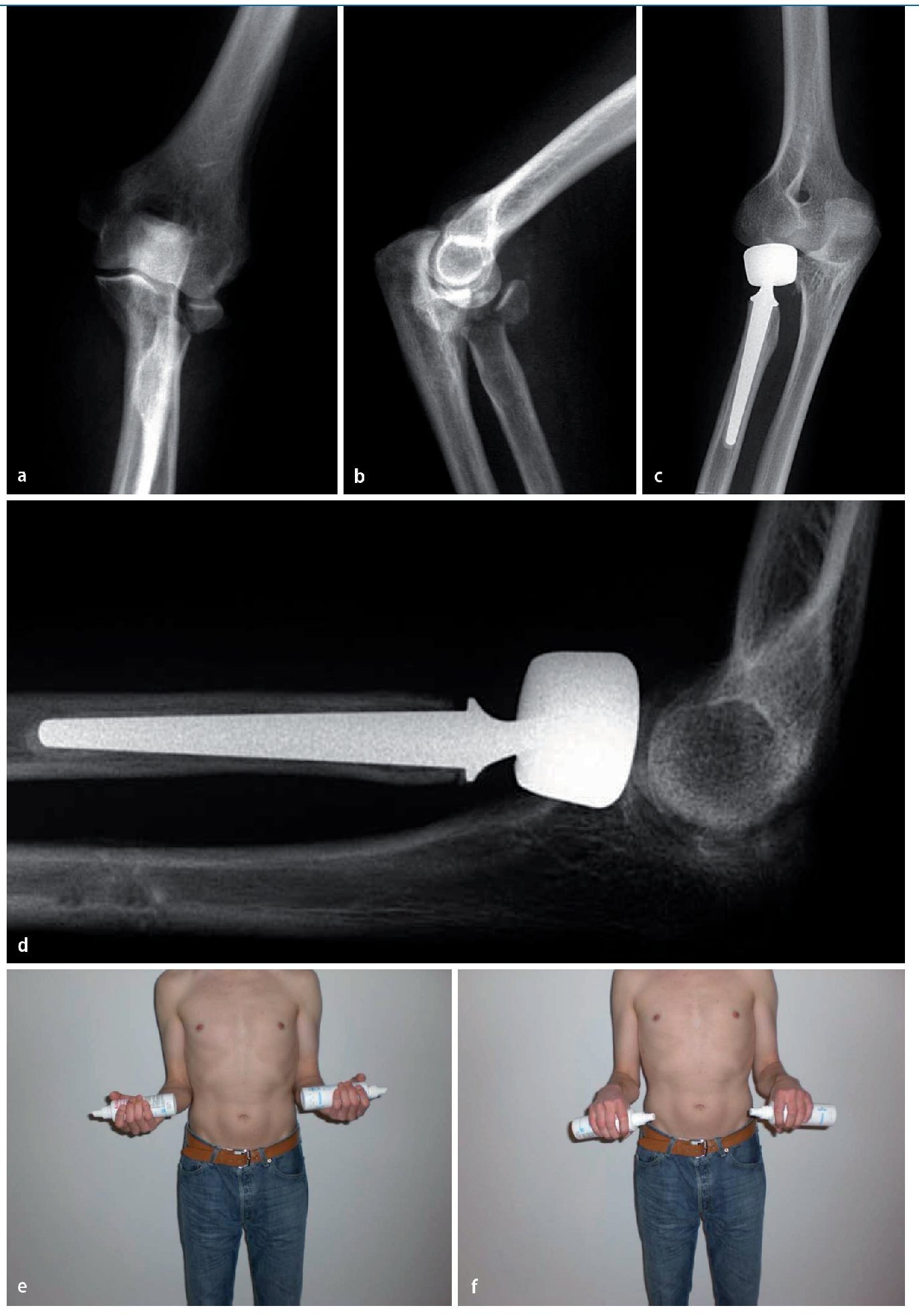
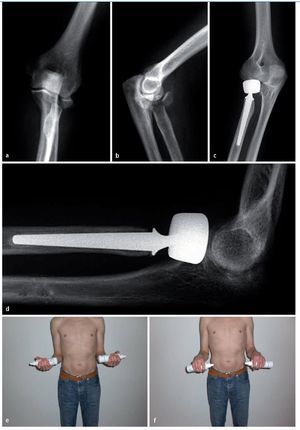
Fig. 15 Ejemplo de transcurso del caso de un paciente de 33 años, montador de cubiertas, que sufrió un accidente de motocicleta. La radiografía preoperatoria anteroposterior (a) muestra una fractura de cabeza radial Mason Tipo III en proyección anterior-posterior (a) y lateral (b). Las radiografías antero-posterior (c) y lateral (d) realizadas el tercer día postoperatorio muestran el resultado después del implante de la prótesis de cabeza radial bipolar de Judet en posición lateral. En el reconocimiento clínico posterior realizado 36 meses después del implante el paciente mostró un movimiento de rotación reducido del antebrazo (e, f).
Tratamiento postoperatorio
—No existe inmovilización postoperatoria después de sustitución única de la cabeza radial.
—Tratamiento precoz funcional a partir del primer día postoperatorio con movilidad activa ilimitada.
—En caso de existir lesiones asociadas (por ejemplo, sutura de ligamento colateral ulnar), se puede aplicar en el antebrazo una férula de yeso durante tres-cuatro semanas, con la que diariamente se realizarán ejercicios con la articulación del codo.
—Retirar los puntos a partir del undécimo día postoperatorio. En caso dado, utilización de hilos reabsorbentes.
—Control radiológico postoperatorio del codo en dos niveles.
—Durante cuatro semanas tomar dos veces al día antiinflamatorios no esteroides (por ejemplo, Indometacin 75 mg per os) previa protección suficiente de la mucosa gástrica como prevención de osificaciones heterotópicas.
Errores, riesgos y complicaciones
—Se deberá tener en cuenta la altura de resección de 23 mm, dado que puede producirse inestabilidad (demasiada altura de resección) o un «impingement» (insuficiente altura de resección).
—Se tendrá en cuenta la posición de rotación de la prótesis anatómica, para que la cavidad del collar de la prótesis restablezca la morfología normal curvada del radio.
—El tamaño de la cabeza de la prótesis tiene que corresponderse con el de la cabeza radial reseccionada.
—Se protegerá el nervio radial (fig. 10) mediante pronación total del antebrazo durante la intervención.
—El ligamento anular se tiene que volver a fijar (fig. 11) para evitar subluxaciones de la prótesis.
—Se prestará atención a la prevención de osificaciones, especialmente en los pacientes con lesiones asociadas en el codo, así como con lesiones cerebrales, ya que suelen tener tendencia a sufrir grandes calcificaciones.
—Las osificaciones a partir del Grado II según Brooker6 deben eliminarse de tres a seis meses después de la operación, a fin de no poner en peligro la rehabilitación.
Resultados
En el periodo de noviembre de 2001 hasta agosto de 2008 implantamos 16 prótesis de cabeza radial bipolares según Judet a 14 pacientes (8 hombres, 6 mujeres) con un promedio de edad de 51 años (27-74 años) después de una fractura de cabeza radial no reconstruible (Mason III y IV). Dos pacientes sufrieron una rotura de radio bilateral, que fue tratada en ambos casos con la implantación de una prótesis. Los pacientes fueron operados en una media de 14,6 (1-65) días después del accidente. En un análisis retrospectivo pudimos examinar en el periodo postoperatorio 13 pacientes (93%) en una media de 29,5 ± 20,8 meses. Se evaluaron los resultados de 15 articulaciones de codo de acuerdo con los parámetros siguientes: examen físico, radiografías del codo en 2 niveles (toma lateral con proyección clara sobre la prótesis), autovaloración del paciente en cuanto a su grado de satisfacción subjetivo (1 = muy bueno, 2 = bueno, 3 = medio, 4 = malo), así como valoración del codo en comparación con el estado anterior al accidente (en %). La función del brazo en su uso diario fue valorada en base a 30 preguntas de la escala de DASH («disability of the arm, shoulder, and hand questionnaire», 0-100 puntos, 0 como valor óptimo15), la utilización del codo según los esquemas de valoración de Radin y Riseborough21, así como de Broberg y Morrey5.
En el momento de la revisión postoperatoria, las articulaciones operadas de codo y también de muñeca ipsilateral de todos los pacientes eran estables. La autovaloración de los 13 pacientes examinados postoperatoriamente en cuanto a su grado de satisfacción dio muy buenos resultados; la valoración subjetiva del codo fue del 78 ± 12% en comparación con el estado anterior al accidente.
Los resultados funcionales de la articulación del codo dieron como promedio 6 resultados buenos y 9 satisfactorios según la escala de Radin y Risborough, 1 resultado excelente, 8 buenos y 6 resultados satisfactorios según la escala de Broberg y Morrey. La función del brazo en el uso diario, evaluada en base a la escala DASH, obtuvo 9,9 ± 9,7 puntos.
Una paciente de 74 años a la que después de una luxación de codo y una resección de cabeza radial con sutura de ligamento colateral ulnar y radial se tuvo que practicar una nueva luxación y a la que después implantamos la prótesis el día 62 después del accidente, obtuvo un resultado subjetivo y funcional satisfactorio.
El análisis de las radiografías no mostró ningún cubitus valgus, ninguna deformación o aflojamiento de la prótesis ni tampoco artrosis del cóndilo humeral. En 5 casos se detectaron osificaciones heterotópicas de grado I, en 2 casos de grado II según Brooker. La dimensión de la calcificación no estaba relacionada con las lesiones asociadas, ni tampoco reflejaba la dimensión de las molestias ni las limitaciones de movilidad.
Dos pacientes presentaron en el periodo postoperatorio debilidades del nervio cubital y del nervio radial, los cuales mostraron una evolución totalmente regresiva al cabo de 48 y/o 30 meses.
Una paciente desarrolló osificaciones heterotópicas de grado II, que fueron reseccionadas en una operación posterior y a continuación tratadas con radioterapia. En el momento de la revisión médica posterior, la paciente declaró no experimentar mejora alguna en la movilidad en comparación con el periodo anterior a la revisión. A pesar de la radioterapia y de la administración de Indometacin, se habían desarrollado nuevas osificaciones de grado I. Desde el punto de vista clínico, la paciente declaró estar ahora subjetivamente satisfecha por el resultado funcional satisfactorio y se le siguió aplicando rehabilitación.
Conflicto de intereses. El autor manifiesta que no existe ningún conflicto de intereses.
Correspondencia
Dr. M.C. Müller
Klinik und Poliklinik für Orthopädie und Unfallchirurgie, Universitätsklinikum Bonn Sigmund-Freud-Str. 25
53105 Bonn (Alemania)
marcus.mueller@ukb.uni-bonn.de