El síndrome de liberación de citocinas (SLC) es una complicación grave de los pacientes COVID-19. La base del tratamiento es tocilizumab. El uso de glucocorticoides (GC) es controvertido. En otros SLC muy parecidos, como son el síndrome de activación macrofágica (SAM) y el síndrome hemofagocítico (SHF) el tratamiento con los corticoides es fundamental. Nuestro objetivo es evaluar la eficacia de los GC en el SLC por COVID-19.
PacientesIncluimos 92 pacientes con SLC por COVID-19 que recibieron GC, GC y tocilizumab y solo tocilizumab. Determinamos marcadores de SLC. Evaluamos mortalidad, intubación y una variable combinada.
ResultadosEn todos los casos los porcentajes de eventos fueron menores en el grupo de pacientes en los que se administraron GC. Las razones de riesgo de las variables finales de los grupos con GC frente al grupo en el que se administró solo tocilizumab fue menor conforme se consideraron los GC, con significación estadística para la supervivencia.
DiscusiónEl uso precoz de pulsos de GC puede controlar el SLC, con un menor requerimiento de uso de tocilizumab y una disminución de eventos como la intubación y la muerte.
Cytokine storm syndrome (CSS) is a serious complication of COVID-19 patients. Treatment is tocilizumab. The use of glucocorticoids (GC) is controversial. In other very similar CSS, such as macrophage activation syndrome (MAS) and hemophagocytic syndrome (HFS), the main treatment are corticosteroids. Our objective is to evaluate the efficacy of GC in the CSS by COVID-19.
PatientsWe included 92 patients with CSS associated to COVID-19 who received GC, GC, and tocilizumab and only tocilizumab. We determine CSS markers. We evaluated mortality, intubation, and a combined variable.
ResultsIn all cases the percentages of events were lower in the group of patients with GC was administered. The hazard ratio of the final variables with GC versus the group in which only tocilizumab was administered was lower as CGs were considered, with statistical significance for survival.
DiscussionThe early use of GC pulses could control SLC, with a lower requirement to use tocilizumab and a decrease in events such as intubation and death.
El síndrome de liberación de citocinas (SLC) es una complicación grave de la enfermedad por SARS-CoV-2 (COVID-19)1,2. La base de su tratamiento es fundamentalmente tocilizumab, un anti-IL-63. El empleo de glucocorticoides (GC) es controvertido4–6. Sin embargo, en la fase de hiperinflamación podrían ser muy beneficiosos, como sucede en otras enfermedades en las que existe una tormenta de citocinas muy parecida a la que acontece en COVID-19, como son el síndrome de activación macrofágica (SAM) y el síndrome hemofagocítico (SHF)7,8.
El objetivo de este estudio es evaluar la eficacia de la administración de pulsos de GC en pacientes que presentan un SLC por COVID-19.
Pacientes y métodoEstudio retrospectivo observacional en los servicios de medicina interna e intensivos. Se incluyeron pacientes ingresados con infección por SARS-CoV-2 confirmada por PCR y que cumplían criterios de SLC definidos por: elevación de IL-6>40pg/ml y/o 2 de los siguientes: ferritina >300μg/l, dímeros-D>1mg/l y/o triglicéridos >300mg/dl. Clasificamos a los pacientes en 3 grupos: 1) los que recibieron solo pulsos de GC; 2) pulsos de GC y tocilizumab, simultáneamente, y 3) exclusivamente tocilizumab. Se clasificaron los pulsos en 2mg/kg/día durante 3 días, 250mg/día durante 3 días y 500mg/día durante 3 días. Determinamos los niveles séricos de ferritina, PCR y dímeros-D antes de su administración y durante el seguimiento, con intervalos de 24-72h siguiendo la práctica habitual. Se determinaron como variables resultado finales la supervivencia, la necesidad de intubación y una variable combinada de estas 2 últimas. Todos los pacientes dieron su consentimiento para el tratamiento.
Se describieron las variables fundamentales del estudio atendiendo a la distribución de frecuencias y a las medidas básicas de resumen numérico, media, desviación típica y rango. El análisis del tiempo hasta que ocurría cada una de las variables de respuesta se hizo mediante la estimación de las curvas de supervivencia por el método de Kaplan-Meier y las estimaciones de las razones de riesgos se hizo mediante el modelo de riesgos proporcionales de Cox. Las comparaciones entre tratamientos y dentro de tratamientos entre instantes, se analizaron mediante un modelo lineal mixto con comparaciones por parejas cuando resultó significativo. Se empleó Stata v.14.1.
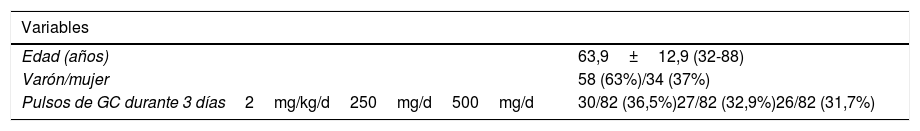
ResultadosSe incluyeron un total de 92 pacientes. Las características basales se muestran en la tabla 1.
De los 92 pacientes, 60 (65,2%) recibieron solo pulsos de GC, 23 (25%) pulsos asociados a tocilizumab y 9 (9,8%) solo tocilizumab. Se produjeron 7 (7,6%) fallecimientos y 5 (5,6%) intubaciones, falleciendo uno de los pacientes que requirió intubación. La variable combinada intubación/fallecimiento ocurrió en 11 (12,4%) casos. La mediana de seguimiento de los pacientes fue de 11 días.
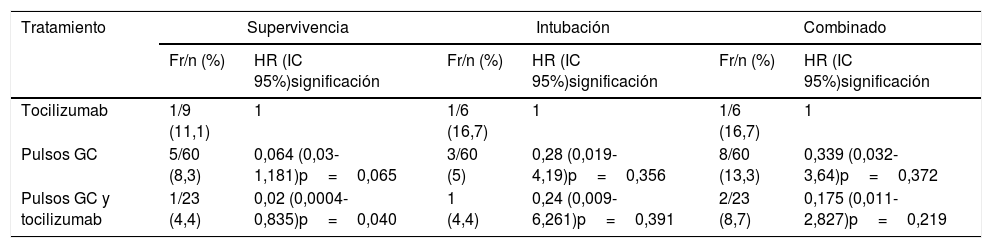
En la tabla 2 figuran los porcentajes por tratamientos, de presentación de cada una de las variables finales consideradas, así como la razón de riesgos de los tratamientos frente al tratamiento en el que no se incluyen GC. En todos los casos los porcentajes de eventos fueron menores en el grupo de pacientes en que se administraron GC, siendo el grupo de tratamiento combinado en el que se consiguió un menor porcentaje de eventos.
Frecuencias de las 3 medidas de desenlace por tratamientos y HR para los modelos de regresión de Cox de tiempo hasta el evento
| Tratamiento | Supervivencia | Intubación | Combinado | |||
|---|---|---|---|---|---|---|
| Fr/n (%) | HR (IC 95%)significación | Fr/n (%) | HR (IC 95%)significación | Fr/n (%) | HR (IC 95%)significación | |
| Tocilizumab | 1/9 (11,1) | 1 | 1/6 (16,7) | 1 | 1/6 (16,7) | 1 |
| Pulsos GC | 5/60 (8,3) | 0,064 (0,03-1,181)p=0,065 | 3/60 (5) | 0,28 (0,019-4,19)p=0,356 | 8/60 (13,3) | 0,339 (0,032-3,64)p=0,372 |
| Pulsos GC y tocilizumab | 1/23 (4,4) | 0,02 (0,0004-0,835)p=0,040 | 1 (4,4) | 0,24 (0,009-6,261)p=0,391 | 2/23 (8,7) | 0,175 (0,011-2,827)p=0,219 |
Fr/n: frecuencias por desenlace; GC: glucocorticoides; HR: hazard ratio (razón de riesgos) estimada mediante modelo de riesgos proporcionales de Cox; IC: intervalo de confianza.
Con respecto a las razones de riesgo de las diferentes variables de desenlace de los grupos con GC frente al grupo en el que se administró solo tocilizumab, se observó que el riesgo de cada uno de los eventos fue menor conforme se consideró el tratamiento con GC, alcanzándose significación estadística en el caso de la supervivencia y una tendencia, aunque sin alcanzar significación, tanto para la intubación como para la variable combinada.
En las curvas de supervivencia de Kaplan-Meier existió una tendencia a una menor necesidad de intubación, fallecimiento y de la variable combinada. Se observó claramente que no hubo un aumento de fallecimientos en el grupo de pacientes que recibieron GC.
La evolución de los marcadores bioquímicos fue muy variable. Los niveles medios de ferritina iniciales fueron de 1.238μg/l en el grupo de GC y tocilizumab, 832μg/l en el de GC y 1.024μg/l en el de tocilizumab, sin observar un descenso significativo en ninguno de los grupos al final del seguimiento. Se observó un descenso significativo en la PCR ya en la primera determinación tras el tratamiento, que se mantuvo hasta el final del seguimiento en los 3 grupos. Los dímeros-D permanecieron elevados sin descensos significativos.
DiscusiónLos resultados de este estudio muestran que, en los pacientes con SLC inducido por COVID-19, la asociación de pulsos de GC parece asociarse a un mejor pronóstico de la enfermedad, con una clara tendencia a una menor mortalidad y necesidad de intubación.
El papel de los GC en los pacientes con COVID-19 no está bien establecido. En la revisión realizada por Rusell et al.4 sobre la lesión pulmonar inducida por diferentes virus incluidos SARS y MERS y en el estudio de Wang et al.5 no se observó ningún efecto beneficioso, incluso se relacionaron con un probable aumento de mortalidad. Por ello, el uso de GC no se ha recomendado. Recientemente Wu et al.6, demostraron una disminución del riesgo de mortalidad en pacientes con distrés respiratorio que recibieron metilprednisolona.
El objetivo de nuestro trabajo ha sido evaluar la eficacia de los GC en otra complicación muy grave del SARS-CoV-2 como es SLC. La elevación de la PCR y de la ferritina son 2 datos característicos y claves para su diagnóstico. A diferencia del SHF que tiene unos criterios diagnósticos7 y un sistema de puntuación para estimar la probabilidad de padecerlo llamado HScore9, no existen unos criterios bien establecidos para la definición del SLC. Nosotros consideramos que un paciente lo presenta ante la presencia de una IL-6 elevada y/o la combinación de 2 o más alteraciones analíticas, con elevación fundamentalmente de los niveles de ferritina. Todos los pacientes incluidos cumplieron los criterios, con unas ferritinas muy elevadas. El tratamiento del SHF, muchas veces asociado con procesos infecciosos7, y otras con diferentes enfermedades autoinmunes sistémicas, denominándose en este caso un SAM8, se fundamenta en 2 pilares: por un lado, el tratamiento etiológico, si lo hubiere, y por otro, el tratamiento de la tormenta de citocinas10. En todos los casos, los GC en dosis altas y principalmente en pulsos constituyen la base del tratamiento. En el caso de SLC por SARS-CoV-2 el tratamiento recomendado ha sido tocilizumab2,3, un fármaco caro y de difícil acceso para todos los pacientes. El hecho de que los GC se hayan mostrado eficaces en un elevado número de pacientes puede permitir administrarlo como segunda opción para los que no respondan.
En nuestro estudio decidimos valorar la respuesta al tratamiento mediante 2 variables clínicas de gran impacto como son la necesidad de intubación y la mortalidad; por ello, solo incluimos los pacientes fallecidos que habían recibido algunos de los brazos de tratamiento, y excluimos a aquéllos que ingresaron directamente para intubación. Observamos que en los pacientes que recibieron pulsos de GC, bien de forma aislada o bien asociados a tocilizumab, hubo una tendencia a la disminución de los eventos muerte, intubación y la combinación de ambas, siendo mayor en los casos de combinación de ambos fármacos. No encontramos diferencias entre las distintas dosis utilizadas, por lo que probablemente, la dosis menor de 2mg/kg/día durante 3 días sea la dosis más recomendable.
El interés de nuestro estudio se basa en la aplicación de pulsos de GC, un tratamiento eficaz contrastado en otras enfermedades similares al SLC por SARS-CoV-2, más económico y accesible a otros tratamientos experimentales empleados en esta enfermedad como es tocilizumab, y que por diferentes motivos se ha desaconsejado, demostrando su beneficio clínico objetivo. Las limitaciones del estudio son el carácter retrospectivo, el tamaño muestral, el número reducido de eventos clínicos y el corto período de seguimiento, por lo que los resultados deben confirmarse con un ensayo clínico con una mayor n y un mayor tiempo de seguimiento.
Concluimos que en pacientes con COVID-19 es fundamental la identificación precoz del SLC y que, en caso de aparición, el uso precoz de pulsos de GC puede controlarlo, probablemente con un menor requerimiento de uso de tocilizumab y con una disminución de eventos como la intubación y la muerte.
Conflicto de interesesLos autores declaran no tener ningún conflicto de intereses.