La infusión continua de levodopa intraduodenal (Duodopa®) constituye una alternativa a la infusión subcutánea de apomorfina y a la cirugía en pacientes con enfermedad de Parkinson (EP) avanzada. Describimos nuestra experiencia con Duodopa® en pacientes con EP avanzada.
MétodosRealizamos un estudio epidemiológico, observacional, no intervencionista, poblacional, descriptivo, y retrospectivo, en el que se incluyen todos aquellos pacientes con EP avanzada tratados con Duodopa® por parte de la Sección de Neurología del Hospital A. Marcide de Ferrol hasta abril de 2010.
ResultadosOnce de un total de 12 pacientes seleccionados fueron tratados con Duodopa® [63,6% varones; edad media 62,7±10,6 (44-74) años]. En el momento de ser seleccionados para recibir Duodopa® presentaban: tiempo medio de evolución de enfermedad de 14,5±8,9 (3-34) años, dosis media de levodopa oral de 918,2±277,7 (450-1300) mg/día, y un estadio de Hoehn y Yahr de 3,7±0,5 (3-4). Nueve pacientes mantienen el tratamiento con Duodopa®. Hubo mejoría en las fluctuaciones motoras (72,7% gran mejoría) y discinesias (55,5% gran mejoría) con reducción del tiempo off/día (90,9%) y tiempo con discinesias/día (66,6%) después de un tiempo total de seguimiento con Duodopa® de 170,5 (3-31) meses. La mejoría en las escalas PDQ-39 y Schwab&England fue de 38,5±19,8 y 24±12,5 puntos respectivamente (p<0,05). La dosis media equivalente oral de levodopa (abril 2010) fue de 1683,4±295,8 (1234-2216) mg/día.
ConclusionesDuodopa® pudiera ser un tratamiento efectivo, seguro, y bien tolerado alternativo a la cirugía y apomorfina subcutánea en pacientes con EP avanzada adecuadamente seleccionados.
Continuous levodopa delivery by enteral infusion (Duodopa®) is an alternative to deep brain stimulation and subcutaneous apomorphine to control motor fluctuations and dyskinesias in advanced Parkinson's disease (PD). We report our experience with Duodopa® therapy in 11 patients with advanced PD.
MethodsWe retrospectively assessed clinical and quality of life changes in all patients with PD with severe motor fluctuations and dyskinesias who started continuous daily levodopa duodenal infusion through percutaneous endoscopic gastrostomy from September 2006 (Duodopa® was approved for advanced PD treatment in Spain at that date) until April 2010 at the A. Marcide Hospital of Spain.
ResultsNine patients received Duodopa® [62.7±10.6 (44-74) years, 63.6% male)]. Pre-Duodopa® clinical characteristics of patients were: disease duration 14.5±8.9 (3-34) years, oral levodopa dose 918.2±277.7 (450-1300) mg/day, and Hoehn and Yahr staging 3.7±0.5 (3-4). Nine patients are still receiving Duodopa®. Patients improved motor fluctuations (72.7% significant improvement), dyskinesia (55.5% significant improvement), daily off-time (90.9%) and daily duration dyskinesia (66.6%) after total infusion time of 170.5 months (3-31). The improvement in Parkinson's Disease Quality of Life Questionnaire-39 (PDQ-39) and Schwab&England Capacity for Daily Living Scale were 38.5±19.8 and 24±12.5 respectively (P<0.05). Equivalent daily dose of levodopa (April 2010) was 1683.4±295.8 (1234-2216) mg/day.
ConclusionsIntraduodenal infusion of levodopa offers an important alternative in treating patients with advanced Parkinson disease.
La progresión de la enfermedad de Parkinson (EP) y el uso de fármacos dopaminérgicos se relaciona con la aparición a largo plazo de complicaciones motoras (fluctuaciones motoras y discinesias) que en ocasiones resultan de difícil control1. En estos pacientes, alternativas al tratamiento sintomático convencional son la cirugía –fundamentalmente la estimulación cerebral profunda del núcleo subtalámico (ECP-NST)−, y los tratamientos de infusión continua mediante bomba (apomorfina subcutánea e infusión enteral de levodopa)2-4. Los primeros resultados sobre pacientes con EP tratados con Duodopa® (suspensión de levodopa/carbidopa con base acuosa formulada para su infusión intraduodenal a través de una sonda insertada mediante PEG) datan de 19935. En 2004, SOLVAY PHARMA obtuvo la indicación para el uso de Duodopa® en pacientes con EP en varios países europeos6. En España fue aprobada para pacientes con EP avanzada con fluctuaciones motoras graves no controladas con medicación oral en enero de 20067.
En el presente trabajo describimos nuestra experiencia en el manejo de pacientes con EP avanzada tratados con Duodopa® y discutimos sobre el mismo como alternativa terapéutica en estos pacientes.
Material y métodosRealizamos un estudio epidemiológico, observacional, no intervencionista, poblacional, descriptivo, y retrospectivo, en el que incluimos a todos aquellos pacientes con EP pertenecientes al área sanitaria de Ferrol, que hayan sido tratados o estén siendo tratados con Duodopa® en seguimiento por la Sección de Neurología del Hospital A. Marcide.
El objetivo es describir la efectividad, tolerancia, y seguridad de Duodopa® en nuestros pacientes con EP avanzada.
La selección de los pacientes con EP candidatos a recibir tratamiento con Duodopa® fue llevada a cabo por el neurólogo experto en EP responsable de la consulta de Trastornos del Movimiento (consulta monográfica realizada una vez por semana con un volumen de 14 pacientes/consulta). Dicha opción de tratamiento es siempre evaluada y aprobada en caso de así considerarse por la Dirección Médica del hospital.
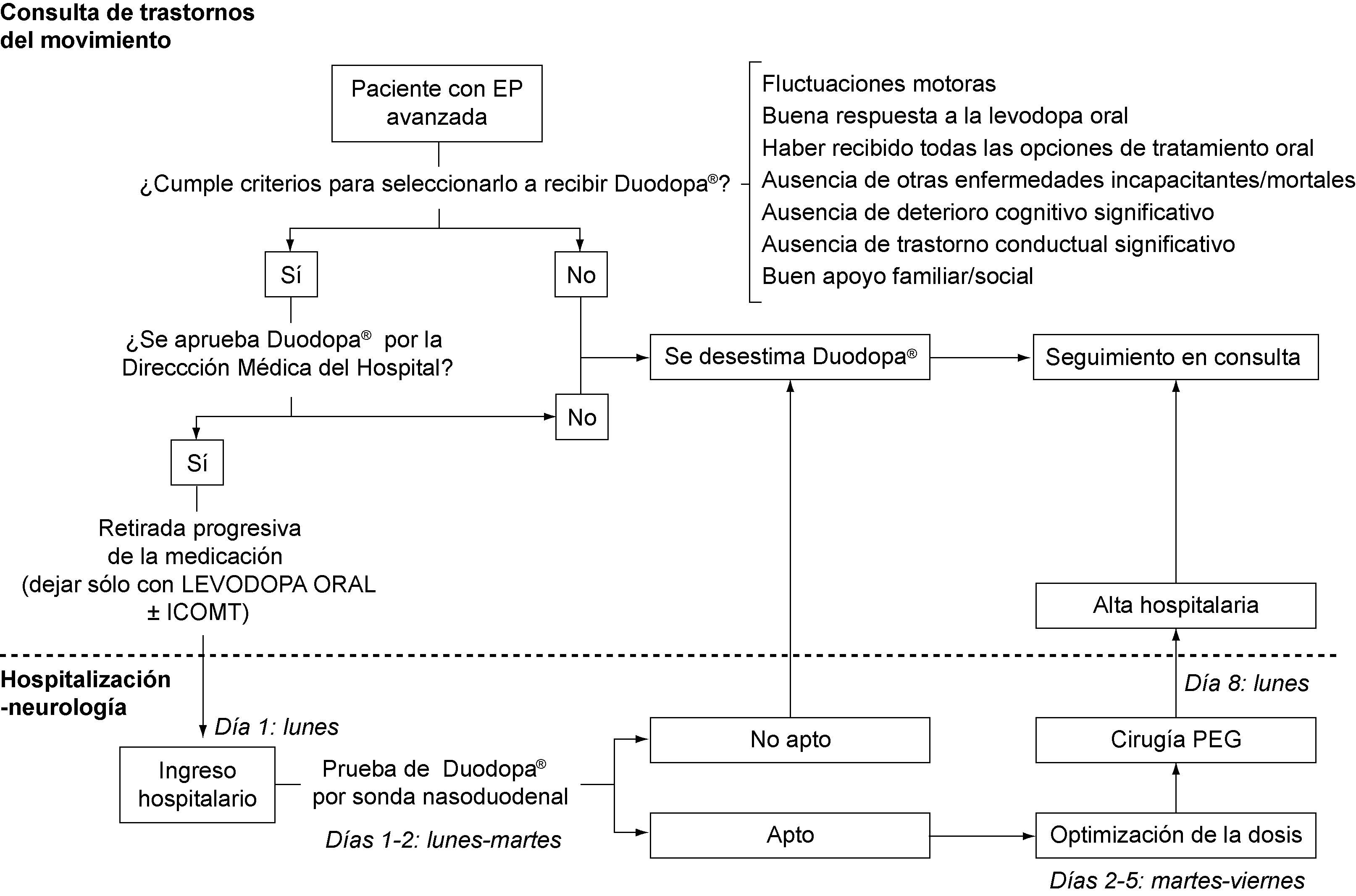
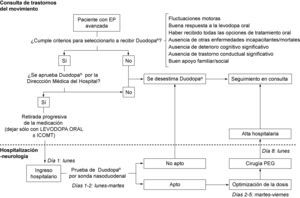
La programación del ingreso hospitalario del paciente para realizar la prueba previa de Duodopa® por sonda nasoduodenal, ajuste de dosis, cirugía PEG, control y evaluación por sonda intraduodenal y posibles complicaciones peri/postoperatorias, se realizó de acuerdo con la disponibilidad del personal de enfermería experto en el manejo de Duodopa® de ABBOTT HEALTHCARE, la Sección de Digestivo de nuestro hospital y el propio paciente. De forma protocolizada, en las semanas previas al ingreso se ajusta el tratamiento del paciente ambulatoriamente, retirándose agonistas dopaminérgicos, inhibidores de la monoaminooxidasa B, amantadina y/o anticolinérgicos, para que en el momento del ingreso esté recibiendo únicamente levodopa oral (± inhibidores de la catecol-o-metil transferasa). El paciente ingresa un domingo, se realiza el ajuste de dosis de Duodopa® por sonda nasoduodenal en las 72-120 horas posteriores al ingreso, cirugía PEG el lunes de la semana siguiente a la del ingreso (es la disponibilidad para realizar la cirugía PEG por parte de la Sección de Digestivo de nuestro hospital), y es dado de alta hospitalaria en las 24-72 horas posteriores a la cirugía en caso de no existir complicaciones. En todos los casos se realiza un preoperatorio (análisis, ECG y radiografía de tórax), consulta de anestesia, radiografía abdominal para comprobar la colocación de la sonda nasoduodenal, y radiografía abdominal para comprobar la colocación de la sonda intraduodenal por gastrostomía. El ajuste de dosis de Duodopa® es realizado según los protocolos establecidos y de acuerdo con la valoración del neurólogo y la enfermera de ABBOTT HEALTHCARE. El paciente es seguido posteriormente en Consultas Externas de Neurología, con una visita a la semana del alta, 15 días, al mes, 3 meses, y posteriormente cada 3-4 meses aproximadamente. En caso de complicaciones posibles, el paciente acude a la consulta de Neurología. La figura 1 muestra el protocolo de actuación que seguimos ante un candidato posible a recibir tratamiento con Duodopa®.
Los datos de cada paciente fueron obtenidos a partir de la información disponible en su historial clínico. Cuantificamos la mejoría experimentada como: 1-Gran mejoría; 2-Mejoría moderada; 3-Mejoría leve; 4-Sin efecto; 5-Empeoramiento. Cuantificamos el tiempo diario off y tiempo con discinesias como: 0%, 0-10%, 10-25%, 25-50%, 50-75%, y 75-100% del tiempo total del día (en vigilia). Fueron utilizadas diferentes escalas de valoración de la EP: Clasificación por estadios de Hoehn y Yahr8, Escala de Actividades de la Vida Diaria de Schwab&England9, y Cuestionario de calidad de vida en la Enfermedad de Parkinson (PDQ-39)10. Utilizamos la Escala de Impresión Clínica Global (CGI, Clinical Global Impression)11 para evaluar el grado de mejoría subjetiva por parte del paciente. Los efectos secundarios y/o acontecimientos adversos recogidos se clasificaron en cuatro grupos: (1) Relacionados con el tratamiento; (2) Relacionados con la gastrostomía; (3) Relacionados con el dispositivo-aspectos técnicos; (4) Otros.
Análisis estadísticoLos datos fueron analizados con el programa estadístico SPSS 16.0. Las variables cuantitativas se expresan como media (desviación estándar) y las cualitativas como un porcentaje. Para realizar el análisis comparativo se utilizó el test de la t Student o el ANOVA de un factor para las variables cuantitativas, y el test de la chi cuadrado para las cualitativas. Fueron considerados como significativos aquellos valores para una p<0,05.
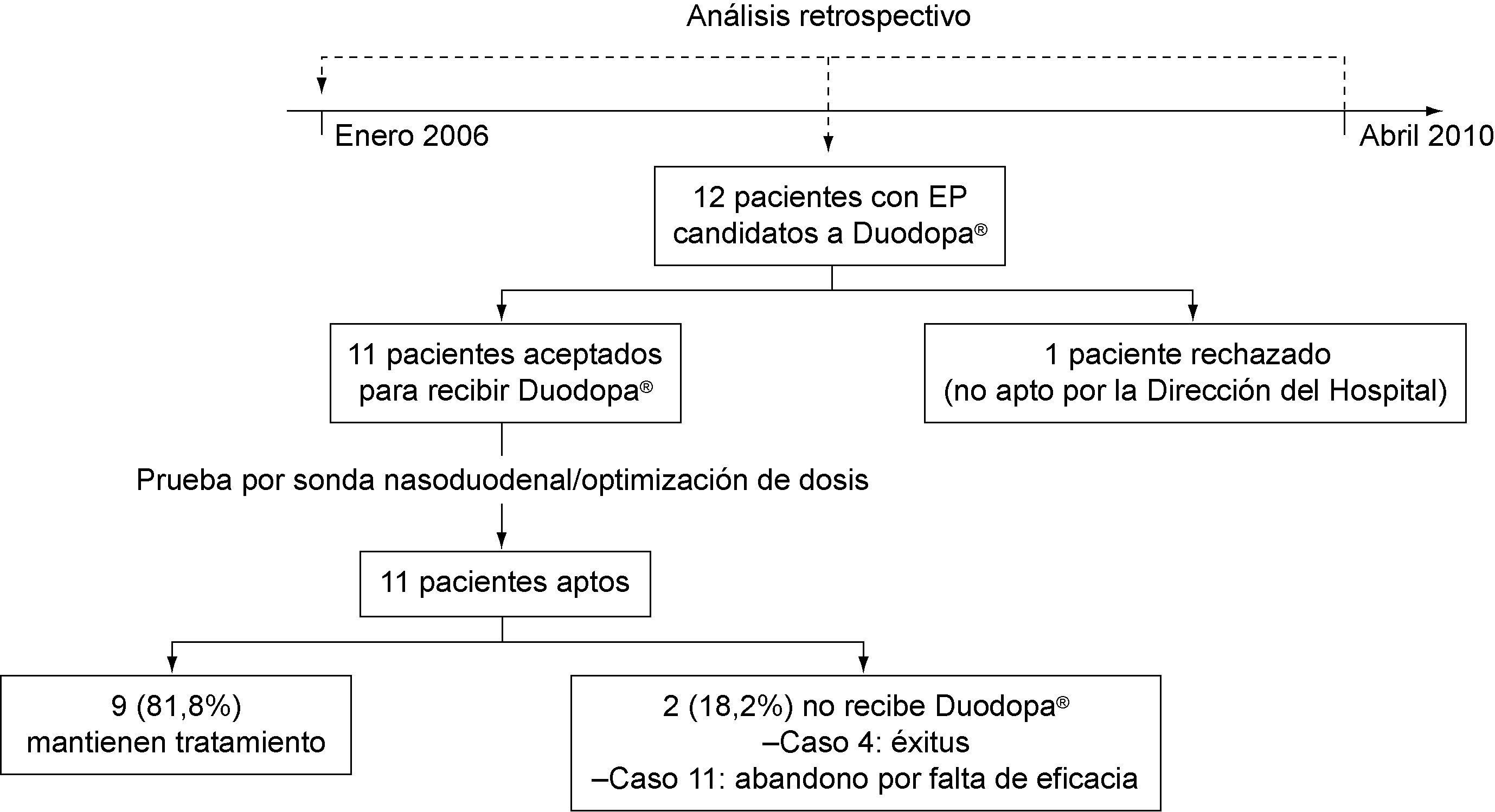
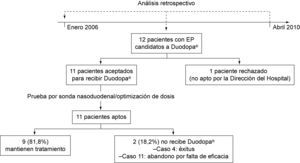
ResultadosEl número de pacientes incluidos fue 11 [63,6% varones, edad media 62,7±10,6 (44-74) años]. Un paciente fue rechazado por la Dirección Médica del hospital para recibir Duodopa®(fig. 2).
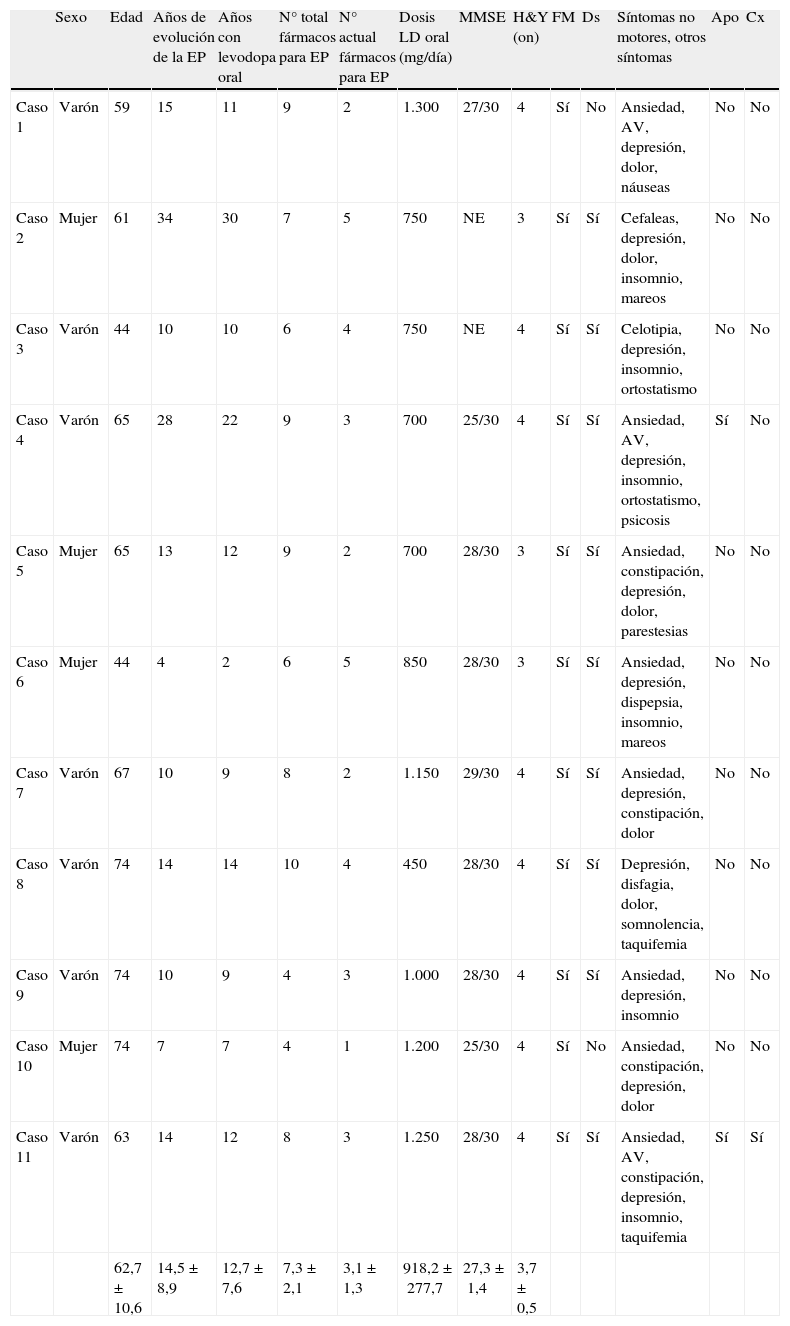
En la tabla 1 figuran las características basales de los pacientes en relación con su EP. El tiempo medio de evolución de la EP fue de 14,5±8,9 (4-34) años, y el tiempo con levodopa 12,7±7,6 (2-30). El estadio Hoehn y Yahr fue 3,7±0,5 (3-4). Con respecto a las complicaciones motoras, todos los pacientes presentaban fluctuaciones motoras (100% deterioro fin de dosis, 36,4% fenómeno on-off), y un 81,8% discinesias. En relación con los síntomas no motores (SNM), los más frecuentes fueron depresión (100%), ansiedad (72,7%), dolor (54,5%) e insomnio (54,5%). Ninguno de los pacientes presentaba deterioro cognitivo (MMSE 27,3±1,4). La dosis media diaria de levodopa oral fue 918,2±277,7 (450-1.300) mg/día. Dos pacientes habían sido tratados previamente con infusión continua de apomorfina subcutánea por bomba, y uno había sido sometido a ECP-NST.
Características basales de los pacientes (pre-tratamiento) con EP que fueron seleccionados para recibir tratamiento con Duodopa®
| Sexo | Edad | Años de evolución de la EP | Años con levodopa oral | N° total fármacos para EP | N° actual fármacos para EP | Dosis LD oral (mg/día) | MMSE | H&Y (on) | FM | Ds | Síntomas no motores, otros síntomas | Apo | Cx | |
| Caso 1 | Varón | 59 | 15 | 11 | 9 | 2 | 1.300 | 27/30 | 4 | Sí | No | Ansiedad, AV, depresión, dolor, náuseas | No | No |
| Caso 2 | Mujer | 61 | 34 | 30 | 7 | 5 | 750 | NE | 3 | Sí | Sí | Cefaleas, depresión, dolor, insomnio, mareos | No | No |
| Caso 3 | Varón | 44 | 10 | 10 | 6 | 4 | 750 | NE | 4 | Sí | Sí | Celotipia, depresión, insomnio, ortostatismo | No | No |
| Caso 4 | Varón | 65 | 28 | 22 | 9 | 3 | 700 | 25/30 | 4 | Sí | Sí | Ansiedad, AV, depresión, insomnio, ortostatismo, psicosis | Sí | No |
| Caso 5 | Mujer | 65 | 13 | 12 | 9 | 2 | 700 | 28/30 | 3 | Sí | Sí | Ansiedad, constipación, depresión, dolor, parestesias | No | No |
| Caso 6 | Mujer | 44 | 4 | 2 | 6 | 5 | 850 | 28/30 | 3 | Sí | Sí | Ansiedad, depresión, dispepsia, insomnio, mareos | No | No |
| Caso 7 | Varón | 67 | 10 | 9 | 8 | 2 | 1.150 | 29/30 | 4 | Sí | Sí | Ansiedad, depresión, constipación, dolor | No | No |
| Caso 8 | Varón | 74 | 14 | 14 | 10 | 4 | 450 | 28/30 | 4 | Sí | Sí | Depresión, disfagia, dolor, somnolencia, taquifemia | No | No |
| Caso 9 | Varón | 74 | 10 | 9 | 4 | 3 | 1.000 | 28/30 | 4 | Sí | Sí | Ansiedad, depresión, insomnio | No | No |
| Caso 10 | Mujer | 74 | 7 | 7 | 4 | 1 | 1.200 | 25/30 | 4 | Sí | No | Ansiedad, constipación, depresión, dolor | No | No |
| Caso 11 | Varón | 63 | 14 | 12 | 8 | 3 | 1.250 | 28/30 | 4 | Sí | Sí | Ansiedad, AV, constipación, depresión, insomnio, taquifemia | Sí | Sí |
| 62,7±10,6 | 14,5±8,9 | 12,7±7,6 | 7,3±2,1 | 3,1±1,3 | 918,2±277,7 | 27,3±1,4 | 3,7±0,5 |
APO: apomorfina subcutánea en infusión continua; AV: alucinaciones visuales; Cx: cirugía (estimulación cerebral profunda); MMSE: Minimental State Examination; NE: no evaluado (casos 2 y 3, evidente ausencia de deterioro cognitivo).
La estancia media del ingreso hospitalario fue de 11,8±4,6 (7-22) días. El tiempo medio para comprobar una respuesta adecuada a Duodopa® y ajuste de dosis correspondiente fue de 3,4±0,7 (3-5) días. No hubo complicaciones durante el ingreso excepto problemas con la migración de la sonda en el caso 7 en relación con estreñimiento y deficiencia de motilidad intestinal, y migración de la sonda en el caso 11 que hubo que recolocar. La dosis equivalente de levodopa oral al alta fue de 1796,7±487,1 (1.160-2.670) mg/día.
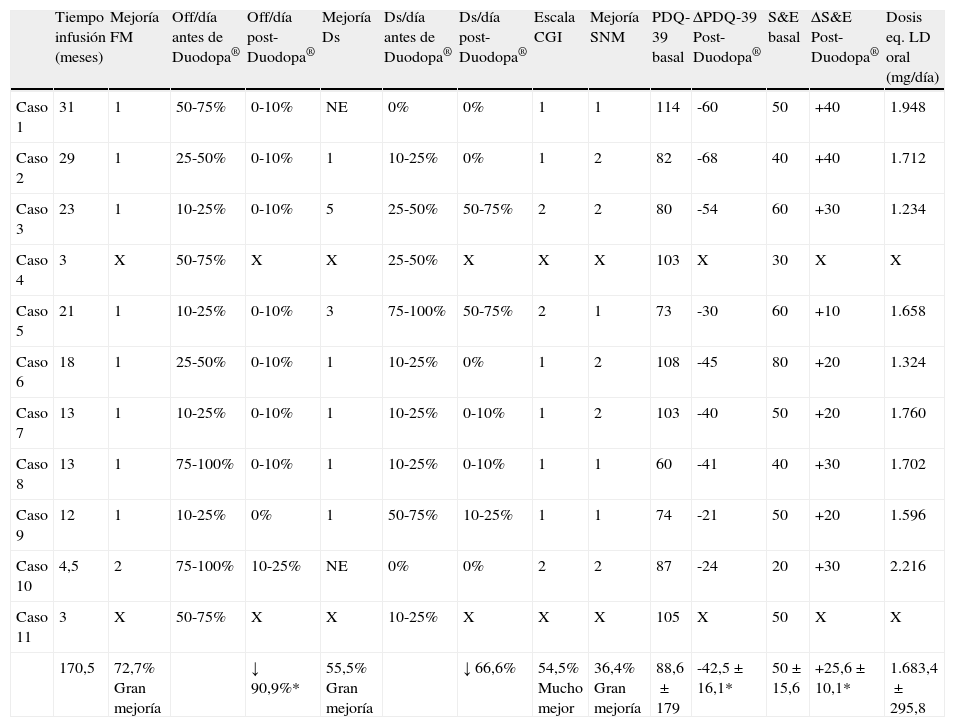
La tabla 2 muestra la evolución de los pacientes tratados con Duodopa®. El tiempo total acumulado de seguimiento con Duodopa® fue de 170,5 meses (3-31). Nueve pacientes mantienen el tratamiento en el momento actual. El caso 4 resultó éxitus a los 3 meses de seguimiento por autolisis. El caso 9 interrumpió el tratamiento a los 3 meses por ausencia de la mejoría esperada. Una paciente (caso 2) recibía infusión continua durante 24 horas. El 72,7% y 55,5% presentaron gran mejoría en cuanto a las fluctuaciones motoras y discinesias respectivamente (reducción del tiempo off en el 90,9% y del tiempo con discinesias en el 66,6%). En cuanto a los SNM, el 81,8% presentaron algún grado de mejoría (36,6% gran mejoría, 45,5% mejoría moderada). Hubo igualmente una mejoría significativa en la calidad de vida y autonomía (reducción de 42,5±16,1 puntos en la PDQ-39 e incremento de 25,6±10,1 en la escala de Schwab/England; p<0,05). La dosis media equivalente oral de levodopa a fecha de 15 de abril de 2010 fue de 1683,4±295,8 (1234-2216) mg/día.
Datos relacionados con el seguimiento de los pacientes con Duodopa®
| Tiempo infusión (meses) | Mejoría FM | Off/día antes de Duodopa® | Off/día post- Duodopa® | Mejoría Ds | Ds/día antes de Duodopa® | Ds/día post-Duodopa® | Escala CGI | Mejoría SNM | PDQ-39 basal | ΔPDQ-39 Post-Duodopa® | S&E basal | ΔS&E Post-Duodopa® | Dosis eq. LD oral (mg/día) | |
| Caso 1 | 31 | 1 | 50-75% | 0-10% | NE | 0% | 0% | 1 | 1 | 114 | -60 | 50 | +40 | 1.948 |
| Caso 2 | 29 | 1 | 25-50% | 0-10% | 1 | 10-25% | 0% | 1 | 2 | 82 | -68 | 40 | +40 | 1.712 |
| Caso 3 | 23 | 1 | 10-25% | 0-10% | 5 | 25-50% | 50-75% | 2 | 2 | 80 | -54 | 60 | +30 | 1.234 |
| Caso 4 | 3 | X | 50-75% | X | X | 25-50% | X | X | X | 103 | X | 30 | X | X |
| Caso 5 | 21 | 1 | 10-25% | 0-10% | 3 | 75-100% | 50-75% | 2 | 1 | 73 | -30 | 60 | +10 | 1.658 |
| Caso 6 | 18 | 1 | 25-50% | 0-10% | 1 | 10-25% | 0% | 1 | 2 | 108 | -45 | 80 | +20 | 1.324 |
| Caso 7 | 13 | 1 | 10-25% | 0-10% | 1 | 10-25% | 0-10% | 1 | 2 | 103 | -40 | 50 | +20 | 1.760 |
| Caso 8 | 13 | 1 | 75-100% | 0-10% | 1 | 10-25% | 0-10% | 1 | 1 | 60 | -41 | 40 | +30 | 1.702 |
| Caso 9 | 12 | 1 | 10-25% | 0% | 1 | 50-75% | 10-25% | 1 | 1 | 74 | -21 | 50 | +20 | 1.596 |
| Caso 10 | 4,5 | 2 | 75-100% | 10-25% | NE | 0% | 0% | 2 | 2 | 87 | -24 | 20 | +30 | 2.216 |
| Caso 11 | 3 | X | 50-75% | X | X | 10-25% | X | X | X | 105 | X | 50 | X | X |
| 170,5 | 72,7% Gran mejoría | ↓ 90,9%* | 55,5% Gran mejoría | ↓ 66,6% | 54,5% Mucho mejor | 36,4% Gran mejoría | 88,6±179 | -42,5±16,1* | 50±15,6 | +25,6±10,1* | 1.683,4±295,8 |
Ds: discinesias; NE: no evaluado (casos 1 y 10 por ausencia de discinesias previas); FM: fluctuaciones motoras; SNM: síntomas no motores.
Mejoría en las FM, discinesias, y SNM: 1-Gran mejoría; 2-Mejoría moderada; 3-Mejoría leve; 4-Sin efecto; 5-Empeoramiento.
Escala de Impresión Clínica Global (CGI, Clinical Global Impression): 1-Mucho mejor; 2-Moderadamente mejor; 3-Levemente mejor; 4-Sin cambios; 5-Levemente peor; 6-Moderadamente peor; 7-Mucho peor.
X: sin datos por falta de seguimiento.
*p<0,05.
Las complicaciones a lo largo del seguimiento fueron: (1) relacionadas con el tratamiento: discinesias (casos 3 y 11), y mareo (caso 9); (2) relacionadas con la gastrostomía: 6 pacientes presentaron granuloma, y 2 infección local el estoma; (3) relacionadas con el dispositivo-aspectos técnicos: 3 pacientes migración de la sonda a estómago, 2 anudamientos, 1 acodamiento de la sonda, y 1 rotura de la sonda externa; (4) otros: autolisis (caso 3), colecistitis (caso 5), y polineuropatía axonal leve asociada a déficit de B12 y pérdida de peso (caso 9). El número total de pruebas radiológicas realizadas fue: 46 rx abdomen, 15 endoscopias digestivas, 4 TCs abdominales, y 3 ecografías de abdomen (incluyendo la endoscopia digestiva para la PEG y las 2 rx de abdomen de control que se hacen por protocolo).
DiscusiónEl presente trabajo constituye un análisis retrospectivo sobre el manejo de Duodopa® en una serie de 11 pacientes con EP avanzada. Dicho análisis demuestra que Duodopa® resultó ser un tratamiento efectivo, bien tolerado, y seguro. Sin embargo, esto debe ser interpretado en el contexto de las limitaciones metodológicas correspondientes.
Con respecto a las características epidemiológicas de nuestra muestra, varios datos resultan interesantes. La edad media es relativamente baja (62,7 años), si tenemos en cuenta que la edad recomendable para cirugía es aquella no superior a 70 años12. En cualquier caso, en otras series ésta no es demasiado elevada y varía entre los 59 (45-83)13, 60 (39-79)6, 66 (57-78)14, 68 (57-74)15 o 72,7 (36-87)16 años. El tiempo de evolución y de tratamiento con levodopa es similar al de otras series13-17. Todos nuestros pacientes presentaban complicaciones motoras que no se habían podido controlar con diversos fármacos orales recibidos a lo largo del curso de su enfermedad. Otro aspecto importante es la presencia de diversos SNM. Especialmente relevante es que todos los pacientes presentaban sintomatología depresiva asociada a su EP, y más de la mitad ansiedad. El hecho de que son pacientes en estadio avanzado y limitados de forma muy importante por su enfermedad probablemente explique estos datos, que están por encima de lo habitual (un metanálisis reciente mostró una prevalencia de depresión del 50% [17% depresión mayor, 22% depresión menor, y 13% distimia] en pacientes con EP18).
En relación con la respuesta al tratamiento, hubo mejoría significativa en relación con las fluctuaciones motoras y discinesias, con reducción del tiempo off y tiempo total diario con discinesias. Igualmente, los pacientes experimentaron mejoría en relación con su calidad de vida y su capacidad para desempeñar actividades de la vida diaria. Esto se acompañó también de una mejoría subjetiva en todos los casos evaluada mediante la escala CGI. Estos datos están en consonancia con publicaciones previas, que han demostrado reducción del tiempo off6,13-17,19-21, reducción del tiempo y severidad de las discinesias12,14, y mejoría en la calidad de vida y autonomía en pacientes con EP avanzada tratados con Duodopa®14,16,22,23. Con respecto a los SNM, todos los pacientes que se mantienen con tratamiento han presentado algún grado de mejoría (fundamentalmente depresión, ansiedad, dolor, e insomnio). Estudios recientes han demostrado mejoría de diversos SNM en pacientes con EP tratados con Duodopa®23.
Observamos también un incremento en la dosis equivalente de levodopa oral diaria con respecto a la previa a Duodopa®. Los resultados en otras serias varían entre aquellas en las cuales se incrementa y otras sin variaciones. Sin embargo, lo más importante es que no existe fenómeno de tolerancia y que las discinesias no empeoran con dosis más elevadas6, lo cual se explicaría por una concentración plasmática de levodopa más constante24. En comparación con otras opciones de EDC (cirugía y apomorfina subcutánea), con Duodopa® se suele conseguir la monoterapia, y evitamos la administración pulsátil de otros fármacos adicionales25. Una paciente recibe infusión las 24 horas. Estudios previos han evidenciado que la infusión continua con Duodopa® durante 24 horas parece ser bien tolerada y produce una mejoría en el sueño23,26.
Nueve pacientes (81,8%) mantienen el tratamiento con Duodopa® en el momento actual. La tasa de mantenimiento es mayor que en otras series (57,1%13, 73%16, 76,9%15, ó 77,8%14), aunque hay que tener en cuenta el tiempo de seguimiento (170,5 frente a 9214, 104513, o más de 125016 meses de otras series) y el número de casos tratados (11 frente a 914, 1515, 2813 o 9116 en otras series). El caso 4 resultó éxitus debido a un suicidio consumado 3 meses después de haber iniciado dicho tratamiento.27 La presencia de complicaciones relacionadas con la gastrostomía y el dispositivo fueron frecuentes. El número de pruebas radiológicas realizadas resultó igualmente elevado.
El tratamiento con Duodopa® ofrece ventajas frente a la cirugía y la apomorfina: no existe mortalidad asociada (1% con la ECP-NST), carece de efectos secundarios irreversibles (hemorragia cerebral con la ECP-NST), reversibilidad, monoterapia la mayoría de las veces, tolerabilidad similar a la levodopa oral, eficacia demostrada, menores criterios de exclusión que para la ECP-NST (edad), mecanismo terapéutico “más limpio” similar al fisiológico, y regulación individual del ritmo de infusión con posibilidad de administración de dosis adicionales7. Además, los pacientes pueden ser controlados en Unidades o Servicios de hospitales pequeños, como es nuestro caso, frente a las mayores necesidades en el caso de la cirugía. Por el contrario, los principales inconvenientes son la necesidad de PEG y cuidados diarios del estoma, necesidad de soporte familiar o cuidador, posible estigmatización por la necesidad de llevar bomba externa para la infusión, efectos adversos relacionados con el sistema de infusión, aumento del número de exploraciones radiológicas, y un coste económico elevado. No existen unos criterios claramente definidos para seleccionar un paciente con EP avanzada como candidato a una terapia u otra (dependerá de muchos factores, como las características del paciente, soporte familiar, preferencias del paciente y/o familia, disponibilidad del centro, experiencia del centro, etc.), pero sí está claro que una buena selección resulta fundamental para una respuesta óptima28. El candidato ideal para Duodopa® es un paciente joven con óptima respuesta a la levodopa oral y buena situación cognitivo-conductual-emocional28. Sin embargo, pacientes descartados para cirugía o apomorfina pueden en ocasiones ser tratados con Duodopa® satisfactoriamente.29 En nuestra serie, Duodopa® fue considerada como primera opción de tratamiento en 7 de los 11 casos (63,6%). Los casos 3 y 6 rechazaron la posibilidad de cirugía, el caso 4 fue tratado con apomorfina (buena respuesta pero tuvo que abandonarla por efectos adversos) y desestimado para ECP-NST, y el caso 11 fue tratado con apomorfina y ECP-NST previamente sin éxito. En dichos casos (4 y 11), se consideró Duodopa® como la última opción de tratamiento, y son precisamente los dos casos con respuesta/evolución no óptima. Los datos en otras series varían. Recientemente, Duodopa® fue utilizada como última opción por detrás de la cirugía y apomorfina hasta en el 98% de los casos en Francia (French DUODOPA Study Group)16. En España, desde enero de 2006 a enero de 2010, 246 pacientes con EP avanzada fueron considerados para recibir Duodopa®. Un 12% no recibieron el tratamiento por ser considerados no aptos después del test de sonda naso-duodenal. De los 217 pacientes tratados, un 82% se mantenían en tratamiento a fecha de enero de 2010 (información proporcionada por ABBOTT HEALTHCARE).
El presente trabajo tiene muchas y muy importantes limitaciones. Se trata de un análisis retrospectivo, y no un estudio prospectivo diseñado específicamente para valorar la eficacia y seguridad de Duodopa®. No está recogida la UPDRS debido a que no disponemos de esa información en todos los casos. El tiempo diario off y tiempo diario con discinesias está reflejado en porcentajes de tiempo diario y no en horas. Finalmente, los datos correspondientes a dolor, depresión o ansiedad se basan en los datos recogidos de la historia clínica, sintomatología referida por el paciente, o tratamiento recibido para los mismos, sin que dispongamos de escalas para su identificación y cuantificación.
En conclusión, y en relación con nuestra experiencia, consideramos que Duodopa® pudiera ser un tratamiento efectivo, seguro, y bien tolerado alternativo a la cirugía y apomorfina subcutánea en pacientes con EP avanzada adecuadamente seleccionados. En cualquier caso, un mayor tiempo de seguimiento y un mayor número de pacientes se antojan necesarios para poder sacar conclusiones más definitivas. En este sentido, pensamos que un análisis sobre todos los pacientes tratados con Duodopa® en España similar al del grupo francés recientemente publicado resultaría muy interesante.
Conflicto de interesesLos autores declaran no tener ningún conflicto de intereses.
Este trabajo (parcialmente) ha sido presentado como comunicación oral en la pasada reunión de la Sociedad Española de Neurología, que aconteció en Barcelona entre los días 17 y 21 de noviembre de 2009.