El pronóstico en la epilepsia implica la probabilidad de alcanzar la remisión de las crisis epilépticas (CE) de forma espontánea o bajo tratamiento con fármacos antiepilépticos (FAE), o no conseguirla a pesar de un tratamiento oportuno.
El tratamiento con FAE es recomendable después de una segunda CE no provocada. Tras una primera CE la decisión de iniciar o no el tratamiento con FAE depende de los riesgos de recurrencia y las ventajas o inconvenientes del tratamiento con FAE. El objetivo del tratamiento es alcanzar la ausencia de CE sin efectos adversos (EA). La selección de los FAE se realiza según tipo de epilepsia y las características demográficas y clínicas del paciente.
DesarrolloBúsqueda de artículos en Pubmed y recomendaciones de las Guías de Práctica Clínica (GPC) y Sociedades Científicas más relevantes referentes a pronóstico de la epilepsia y su tratamiento. Se clasifican las evidencias y recomendaciones según los criterios pronósticos del Oxford Center for Evidence-Based Medicine (2001) y de la European Federation of Neurological Societies (2004) para las actuaciones terapéuticas.
ConclusionesLa mayoría de pacientes que inician una epilepsia consigue el control de sus CE. La mayoría de los FAE disponibles son útiles para el control de cualquier tipo de CE, su elección depende de las características del paciente. Se debe iniciar el tratamiento en monoterapia y a la menor dosis eficaz del FAE elegido, que suele controlar las CE en la mitad de los pacientes y con buena tolerancia. Ante la falta de eficacia del primer FAE, debe intentarse otra terapia alternativa, a ser posible en monoterapia, antes de instaurar una politerapia. Las posibilidades de control de las CE disminuyen con sucesivos fracasos terapéuticos.
Prognosis in epilepsy refers to the probability of either achieving seizure remission (SR), whether spontaneously or using antiepileptic drugs (AED), or failing to achieve control of epileptic seizures (ES) despite appropriate treatment.
Use of AED is recommended after a second unprovoked ES. For a first episode, the decision of whether or not to start drug treatment depends on the risk of recurrence and the advantages or disadvantages of the antiepileptic drug. The main goal of treatment is achieving absence of ES without adverse effects (AE). AED is selected according to epilepsy type and the demographic and clinical characteristics of the patient.
DevelopmentA PubMed search located articles and recommendations by the most relevant scientific societies and clinical practice guidelines concerning epilepsy prognosis and treatment. Evidence and recommendations are classified according to the prognostic criteria of the Oxford Centre for Evidence-Based Medicine (2001) and the European Federation of Neurological Societies (2004) for therapeutic actions.
ConclusionsMost newly diagnosed epileptic patients achieve good control over their ES. The majority of the AEDs available at present provide effective control over all types of ES, and choice therefore depends on the patient's individual characteristics. Treatment should be initiated as monotherapy at the lowest effective dose, which in half of all patients provides ES control and is well tolerated. In cases in which the first AED is not effective, alternative therapy should be started, and monotherapy should be employed before combination therapy where possible. The probability of achieving good control over ES decreases with each successive treatment failure.
El pronóstico en la epilepsia implica varias probabilidades: alcanzar la remisión de las crisis epilépticas (CE) de forma espontánea o bajo tratamiento con fármacos antiepilépticos (FAE); mantener esta remisión de manera prolongada, incluso tras la retirada de los mismos; o no alcanzar el control de las CE a pesar del tratamiento oportuno.
En este artículo incluimos la revisión de la historia natural de la epilepsia y la eficacia de los FAE sobre el riesgo de recurrencia de una primera CE y el tratamiento crónico farmacológico de la epilepsia.
Historia natural de la epilepsiaLa historia natural de la epilepsia sin tratamiento puede deducirse de los estudios poblacionales («puerta-puerta»), con menor seguridad diagnóstica, basados en datos semiológicos exclusivamente y realizados en países pobres y con reducido acceso al tratamiento farmacológico. La posibilidad de remisión prolongada sin tratamiento en alguno de estos países alcanza cifras del 41-46%1,2. Un estudio finlandés de cohortes con pocos casos de pacientes sin tratamiento, pero de largo seguimiento, detectó tasas de remisión del 42% a los 10 años y del 52% a los 20 años del inicio de la epilepsia. Las tasas de remisión espontánea en los estudios poblacionales alcanzan cifras alrededor del 30-50% entre los pacientes que no recibían tratamiento1–3 NE I.
Los estudios epidemiológicos en países desarrollados observacionales, tanto prospectivos como retrospectivos en pacientes de todas las edades, y en la mayoría de ellos con tratamiento antiepiléptico detectaron remisiones prolongadas entre un 60-76%2,4–6 NE I. La mitad de pacientes que no eran tratados con FAE tras una primera crisis generalizada tónico-clónica (CGTC) nunca experimentan otra6 NE I.
En las epilepsias de inicio en la infancia, los estudios hospitalarios también demuestran remisiones prolongadas. Entre el 68-93%, según duración del tiempo de remisión evaluado7,8 NE I.
Eficacia de los fármacos antiepilépticos en el riesgo de recurrencia de una primera crisis epiléptica y la epilepsiaEl tratamiento con FAE, tanto en niños como en adultos, es recomendable después de una segunda CE no provocada, a partir de la cual la Liga Internacional contra la Epilepsia9 considera que el paciente padece una epilepsia. Tras una primera CE, la decisión de iniciar o no el tratamiento con FAE es más complejo y contempla los riesgos de una recurrencia, los factores pronósticos que la facilitan y las ventajas o inconvenientes del tratamiento crónico con FAE. En esta situación, la decisión que se debe tomar ha de consensuarse con el paciente, sus familiares o cuidadores.
Un metaanálisis (MA) de estudios observacionales detectó que el riesgo de recurrencia a los 2 años de una primera CE, en los estudios prospectivos, fue del 36%, y del 47% en los estudios retrospectivos10 NE I y II.
El estudio europeo prospectivo y randomizado, Multicentre trial for Early Epilepsy and Single Seizure (MESS) tras una primera CE, de cualquier tipo, detectó un riesgo de recurrencia en población adulta y pediátrica no tratada de un 39% a los 2 años y de un 51% a los 5 años11 NE I.
Otro estudio multicéntrico italiano, el First seizure trial Group, prospectivo y randomizado, detectó un riesgo de recurrencia tras una primera crisis generalizada tónico-clónica (CGTC), no provocada, mayor entre los pacientes no tratados (51%) respecto a los que recibieron tratamiento (25%) durante los 2 primeros años de seguimiento6 NE I.
El riesgo de recurrencia inmediato tras una primera CE es mayor en los primeros años entre los pacientes no tratados. El conjunto de los estudios observacionales estima el riesgo de recurrencia a los 2 años del 40% entre los pacientes no tratados. Y entre el 80-90% de los que presentan una recurrencia lo hacen en los 2 años siguientes de la primera CE. Sin embargo el pronóstico para el desarrollo de una epilepsia no lo altera el tratamiento inmediato de una primera CE6,11,12 NE I.
El riesgo global tras más de una CE aumenta según el número de las mismas, alcanzando en los estudios observacionales entre los pacientes no tratados el 70%13 NE I.
Los factores asociados con un alto riesgo de recurrencia incluyen: el tipo y número de CE, etiología sintomática, alteraciones en la exploración neurológica, crisis parciales (CP), presencia de anomalías epileptiformes en el electroencefalograma (EEG) y estructurales en la neuroimagen11,12 NE II. En la tabla 1 se recoge la gradación del índice pronóstico de recurrencia del estudio MESS.
Gradación del índice pronóstico de recurrencia según el estudio MESS
| Índice pronóstico | |
|---|---|
| Puntuación de inicio | |
| Una CE antes de la primera consulta | 0 |
| Dos o 3 CE antes de la primera consulta | 1 |
| ≥4 CE antes de la primera consulta | 2 |
| Sumar si está presente | |
| Trastorno o déficit neurológico, trastorno del aprendizaje o retraso en el desarrollo | 1 |
| EEG anormal (alteraciones epileptiformes u ondas lentas) | 1 |
| Clasificación por grupos del riesgo de recurrencia de las CE | Puntuación final |
|---|---|
| Bajo riesgo | 0 |
| Riesgo medio | 1 |
| Riesgo alto | 2-4 |
El tratamiento tras la primera CE debe tener en cuenta varios riesgos14:
- -
No evita en el futuro el desarrollo de una epilepsia.
- -
La afectación psicológica y social y las limitaciones legales del paciente.
- -
Los posibles efectos adversos (EA) de los FAE: neurotóxicos, idiosincrásicos, teratógenos o crónicos.
Qué deben superponerse a los beneficios del tratamiento:
- -
Disminución del riesgo de recurrencia.
- -
Capacidad legal de conducción de vehículos y determinados trabajos.
- -
Beneficios psicosociales.
La Academia Americana de Neurología (AAN) refiere que el tratamiento con FAE no está indicado para la prevención del desarrollo de una epilepsia y que el tratamiento con FAE tras una primera CE debe sopesar los beneficios de la reducción del riesgo de una segunda CE con los riesgos farmacológicos y psicosociales del tratamiento10 NE IV.
La mayoría de autores y Guías de Práctica Clínica (GPC) recomiendan el inicio del tratamiento en las siguientes situaciones clínicas9,12,15–17 NE III-IV:
- -
Después de 2 o más CE y con sintomatología clínica importante y que se hayan presentado en un periodo inferior a 6-12 meses.
- -
Después de una primera CE, si el paciente se encuentra en un grupo de riesgo de recurrencia medio o alto y desea iniciar el tratamiento.
- -
Después de 2 o más CE con sintomatología menor separada por un periodo de tiempo prolongado, si el paciente se encuentra en un grupo de riesgo de recurrencia medio o alto y desea iniciar el tratamiento.
- -
Después de un estado epiléptico (EE), de una primera CGTC durante el embarazo, en una CE no provocada en pacientes ancianos o con discapacidad y en pacientes VIH+.
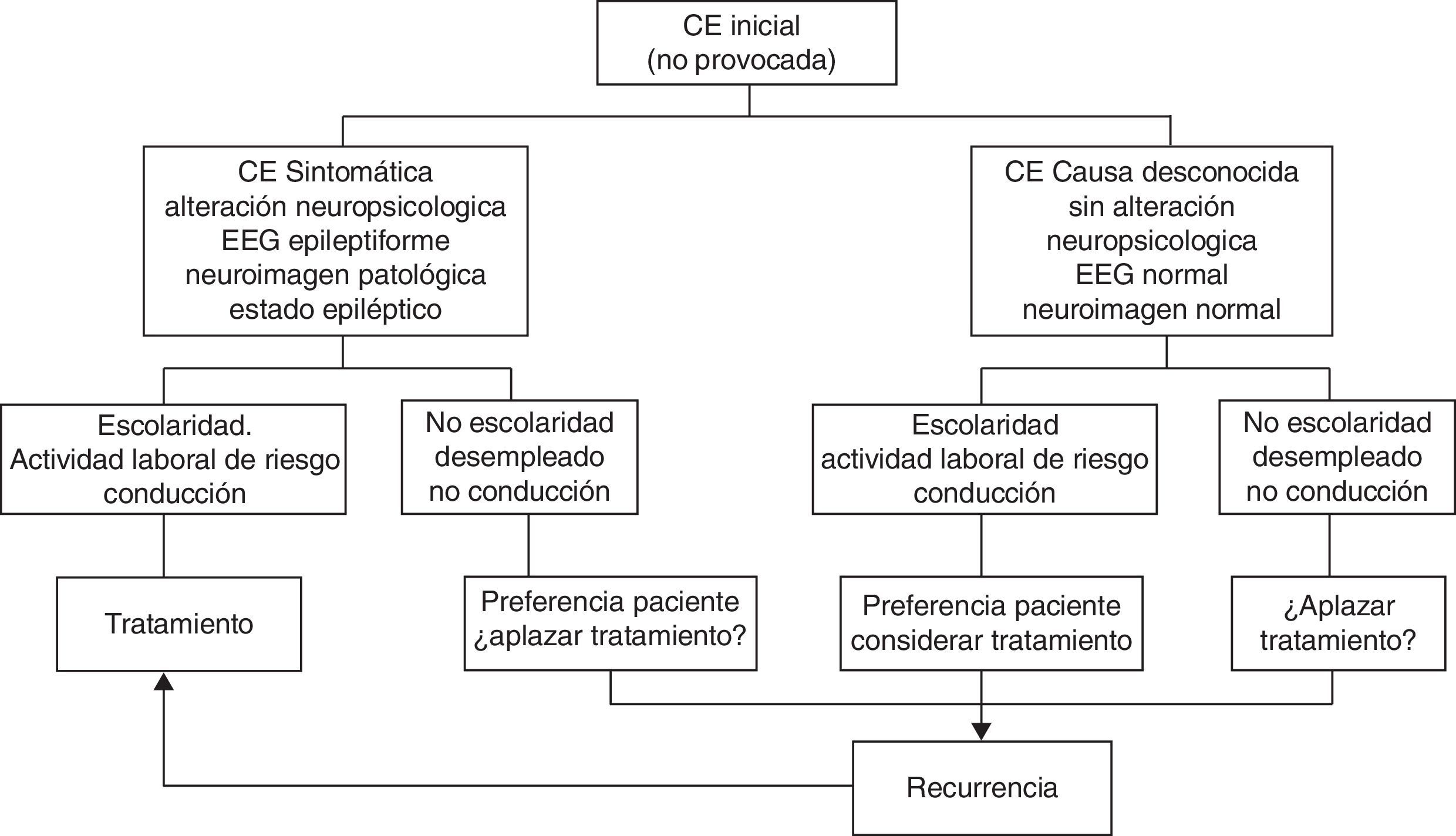
En la figura 1 se indica la pauta de actuación terapéutica de consenso entre los autores de la Guía tras una primera CE.
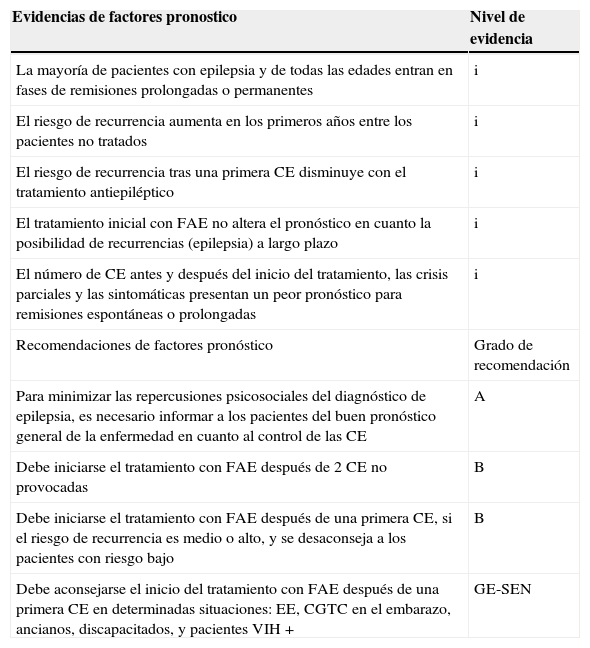
Cuadro general de las evidencias y recomendaciones de los factores pronostico en epilepsia
| Evidencias de factores pronostico | Nivel de evidencia |
|---|---|
| La mayoría de pacientes con epilepsia y de todas las edades entran en fases de remisiones prolongadas o permanentes | i |
| El riesgo de recurrencia aumenta en los primeros años entre los pacientes no tratados | i |
| El riesgo de recurrencia tras una primera CE disminuye con el tratamiento antiepiléptico | i |
| El tratamiento inicial con FAE no altera el pronóstico en cuanto la posibilidad de recurrencias (epilepsia) a largo plazo | i |
| El número de CE antes y después del inicio del tratamiento, las crisis parciales y las sintomáticas presentan un peor pronóstico para remisiones espontáneas o prolongadas | i |
| Recomendaciones de factores pronóstico | Grado de recomendación |
| Para minimizar las repercusiones psicosociales del diagnóstico de epilepsia, es necesario informar a los pacientes del buen pronóstico general de la enfermedad en cuanto al control de las CE | A |
| Debe iniciarse el tratamiento con FAE después de 2 CE no provocadas | B |
| Debe iniciarse el tratamiento con FAE después de una primera CE, si el riesgo de recurrencia es medio o alto, y se desaconseja a los pacientes con riesgo bajo | B |
| Debe aconsejarse el inicio del tratamiento con FAE después de una primera CE en determinadas situaciones: EE, CGTC en el embarazo, ancianos, discapacitados, y pacientes VIH+ | GE-SEN |
El objetivo del tratamiento con FAE es alcanzar la ausencia de CE sin EA. Debemos seleccionar el FAE más adecuado según el tipo de epilepsia y las características del paciente (edad, sexo, peso, comorbilidad…). Aunque existen muy pocos estudios comparativos entre monoterapia y politerapia, la experiencia clínica muestra que el tratamiento con un solo FAE es efectivo para controlar las CE en la mayoría de los pacientes, facilita el cumplimiento y disminuye la posibilidad de EA18–25.
Evidencias sobre el tratamiento de las crisis epilépticas en adultosRevisamos las clasificaciones por NE de las siguientes sociedades científicas y/o demostradas por ensayos controlados aleatorios (ECA) o revisiones sistemáticas.
En la tabla 2 se incluyen las abreviaturas de los FAE:
- -
Veterans Affairs Epilepsy Cooperative Study. 1985-1992 (PHT, CBZ, VPA, PB,PRM)18,19.
- -
ILAE. 2006. Revisión sistemática monoterapia inicial para crisis y síndromes epilépticos (CBZ, PHT, PB, PRM, VPA, VGB, CZP, GBP, LTG, OXC, TPM)20.
- -
Academia Americana de Neurología (AAN) y Sociedad Americana de Epilepsia. 2004. Revisión sistemática monoterapia inicial (GBP, LTG, TPM, OXC) y del tratamiento de la epilepsia refractaria (GBP, LTG, TPM, TGB, OXC, LEV, ZNS)21,22.
- -
SANAD: Standard and New Antiepileptic Drugs. 2007. ECA no ciego (CBZ, VPA,GBP, LTG, OXC, TPM)23,24.
- -
National Institute for Health and Clinical Excellence 2012. GPC en epilepsia para niños y adultos16.
- -
Sociedad Andaluza de Epilepsia. Guía Andaluza de Epilepsia 200917.
- -
ILAE 2013. Updated25. Revisión sistemática monoterapia inicial para crisis y síndromes epilépticos. Añaden (LEV y ZNS).
Abreviaturas de los fármacos antiepilépticos
| BZD benzodiazepina |
| CBZ carbamazepina |
| CLB clobazam |
| CZP clonazepam |
| DZP diazepam |
| ESL eslicarbacepina |
| ESM etosuximida |
| FAE fármaco antiepiléptico |
| FBM felbamato |
| GBP gabapentina |
| LCM lacosamida |
| LEV levetiracetam |
| LTG lamotrigina |
| LZP lorazepam |
| MDZ midazolam |
| OXC oxcarbazepina |
| PB fenobarbital |
| PER perampanel |
| PGB pregabalina |
| PHT fenitoína |
| PRM primidona |
| RFM rufinamida |
| RTG retigabina |
| TGB tiagabina |
| TPM topiramato |
| VGB vigabatrina |
| VPA ácido valproico |
| ZNS zonisamida |
Los FAE se autorizan fundamentalmente para un determinado tipo de CE sobre las que han demostrado eficacia en ECA y en escasas ocasiones, sobre síndromes epilépticos basados en estudios de poca calidad metodológica.
Todos los FAE clásicos han demostrado su eficacia en CP con generalización secundaria y en CGTC primarias18,19 NE I. CBZ, PHT, VPA son mejor tolerados que los barbitúricos (Pb, PRM)18,19 NE I.
La totalidad de los nuevos FAE han demostrado su eficacia frente a CP con o sin generalización secundaria en terapia añadida en los ECA, y algunos de ellos también en monoterapia (GBP, LEV, LTG, OXC, TPM, ZNS)16,17,22,25 NE I.
Algunos de los nuevos FAE (TPM, OXC, LTG) son también eficaces en CGTC primarias20,24 NE III. Y LTG en ausencias20 NE III.
Se observa en la práctica clínica que CBZ, GBP, OXC, PGB, TGB, VGB, PHT, y LTG pueden provocar o empeorar las crisis generalizadas del tipo, ausencias y/o mioclónicas16,17 NE IV.
Recientemente se ha suspendido el inicio de nuevas terapias con RTG por sus EA idiosincráticos dermatológicos y oculares, severos.
Este año se ha aprobado el nuevo FAE, Perampanel (PER) en terapia añadida en CP refractarias26.
Las variables determinantes de la elección del FAE en pacientes con una epilepsia de reciente diagnóstico deben contemplar las características del FAE en cuanto a, especificidad sobre a las crisis; su espectro de eficacia; tolerabilidad; farmacocinética; interacciones; formas de presentación; velocidad de la titulación y número de tomas/día. Y del paciente en cuanto a su base genética; género; edad; comorbilidad y otros posibles tratamientos.
El FAE de primera elección es el que tiene más probabilidad de ser eficaz y menos de causar EA y su dosis correcta es la más pequeña que alcanza el control de las CE sin EA.
En la tabla 3 se establecen las dosis de inicio, pautas de escalada temporal, y dosis habituales de mantenimiento de los FAE.
Pauta de dosificación oral de FAE en adultos
| FAE | Dosis de inicio | Ritmo de escalada | Dosis mantenimiento | Dosis diaria definida (OMS)* | N.° tomas día |
|---|---|---|---|---|---|
| CBZ | 100-200mg/día | 200mg/día/ semana | 600-1.200mg/día | 1.000 | 2-3 |
| CLB | 10-15mg/día | 10mg/día/semana | 20-40mg/día | - | 1-2 |
| CZP | 1mg/día | 0,5-1mg/ día/semana | 1 -4mg/día | 8 | 1-3 |
| ESM | 500mg/día | 250mg/día/semana | 500-2.000mg/día | 1.250 | 2-3 |
| ESL | 400mg/día | 400mg/día/ semana | 800-1.200mg/día | - | 1 |
| GBP | 300-900mg/día | 300mg/día/1-3 días | 1.200-3.600mg/día | 1.800 | 3 |
| LCM | 100mg/día | 100mg/día/semana | 200-400mg/día | - | 2 |
| LEV | 500mg/día | 500-1.000/día/semana | 1.000-3.000mg/día | 1.500 | 2 |
| LTG | a) monoterapia:25mg/díab) asociada a VPA:12,5mg/díac) asociada a inductores:50mg/día | a) monoterapia/y con inductores:50mg/ día/ cada 1- 2 semanasb) asociado VPA 25mg/ día/cada 1-2 semanas | a) monoterapia o asociado a VPA: 100-200mg/díab) asociado a inductores:100-500mg/día | 300 | 2-3 |
| OXC | 600mg/día | 600mg/día/semana | 900-2.400mg /día | 1.000 | 2 |
| PB | 50mg/día | 30-50mg/día/semana | 50-200mg/ día | 100 | 1-2 |
| PER | 2mg/día | 2mg/semana | 4-12mg/día | - | 1 |
| PGB | 150mg/día | 150mg/ día /semana | 300-600mg/día | 300 | 2 |
| PHT | 100-300mg/ día | 50-100mg/ día/semana | 200-500mg/día | 300 | 1-3 |
| PRM | 125mg/día | 125mg/día /semana | 500-1.500mg/día | 1.250 | 2-3 |
| RFM | 400-800mg/día | 400-800mg/día/2 días | 1.800-3.200mg/día(límite dosis inferior asociado a VPA) | 1.400 | 2 |
| RTG | 300mg/día | 150mg/día/ semana | 900-1.200mg/día | - | 3 |
| TGB | 5-10mg/día | 5-10mg/día/ semana | a) no asociada a inductores: 15-30mg/díab) asociada a inductores: 30-50mg/día | 30 | 3 |
| TPM | 25-50mg/día | 25-50mg/día/semana | 200-500mg/día | 300 | 2 |
| VGB | 1.000mg/día | 500mg / día / semana | 1.000-3.000mg/día | 2.000 | 2 |
| VPA | 500mg/ día | 250-500mg/día/semana | 1.000-3.000mg/día | 1.500 | 2-31-2 (crono) |
| ZNS | 50-100mg/día | 100mg/día/ semana | 300-500mg/ día | 200 | 1-2 |
Los pacientes deben tratarse al comienzo con un único FAE (monoterapia inicial), y a la menor dosis eficaz, para reducir al mínimo los EA y facilitar el cumplimiento terapéutico. En un estudio prospectivo observacional, casi la mitad de los pacientes recién diagnosticados de cualquier edad, tipo de CE y etiología, permanecieron sin CE con el primer FAE que recibieron y más del 90% de ellos lo hicieron a dosis bajas. Entre los pacientes que no respondieron al primer FAE sin presentar EA, las posibilidades de control de sus CE disminuyen en los sucesivos ensayos terapéuticos27 NE II.
Otro estudio prospectivo de una cohorte de pacientes de nuevo diagnóstico y observacional de sus pautas de respuesta terapéutica detectó que el 68% de los pacientes en su última visita ambulatoria, estaban libres de crisis durante más de un año y el 62% recibían tratamiento con un solo FAE. Las respuestas terapéuticas fueron categorizadas en 4 grupos: control de las crisis de forma rápida y mantenida (37%); control retardado pero mantenido de las crisis (22%); fluctuante entre periodos de control y recidivas (16%), y sin control de las crisis en ningún momento (25%)28 NE II.
El FAE inicial seleccionado debe retirarse si se producen EA inaceptables, si continúan las CE o aparecen nuevas CE debidas al tratamiento. En cualquiera de estos casos debe cambiarse a otro FAE con expectativas terapéuticas de éxito.
Aunque un ECA multicéntrico en pacientes con epilepsia parcial criptogénica o sintomática, randomizados en monoterapia con un FAE alternativo o en biterapia con un segundo FAE, no encontró diferencias entre ambos grupos tanto en el control de las CE como en los EA durante un año de seguimiento29. La mayoría de autores y de GPC recomiendan tras el fracaso de la primera monoterapia por falta de eficacia, continuar con algún intento más en monoterapia alternativa antes de iniciar una biterapia.
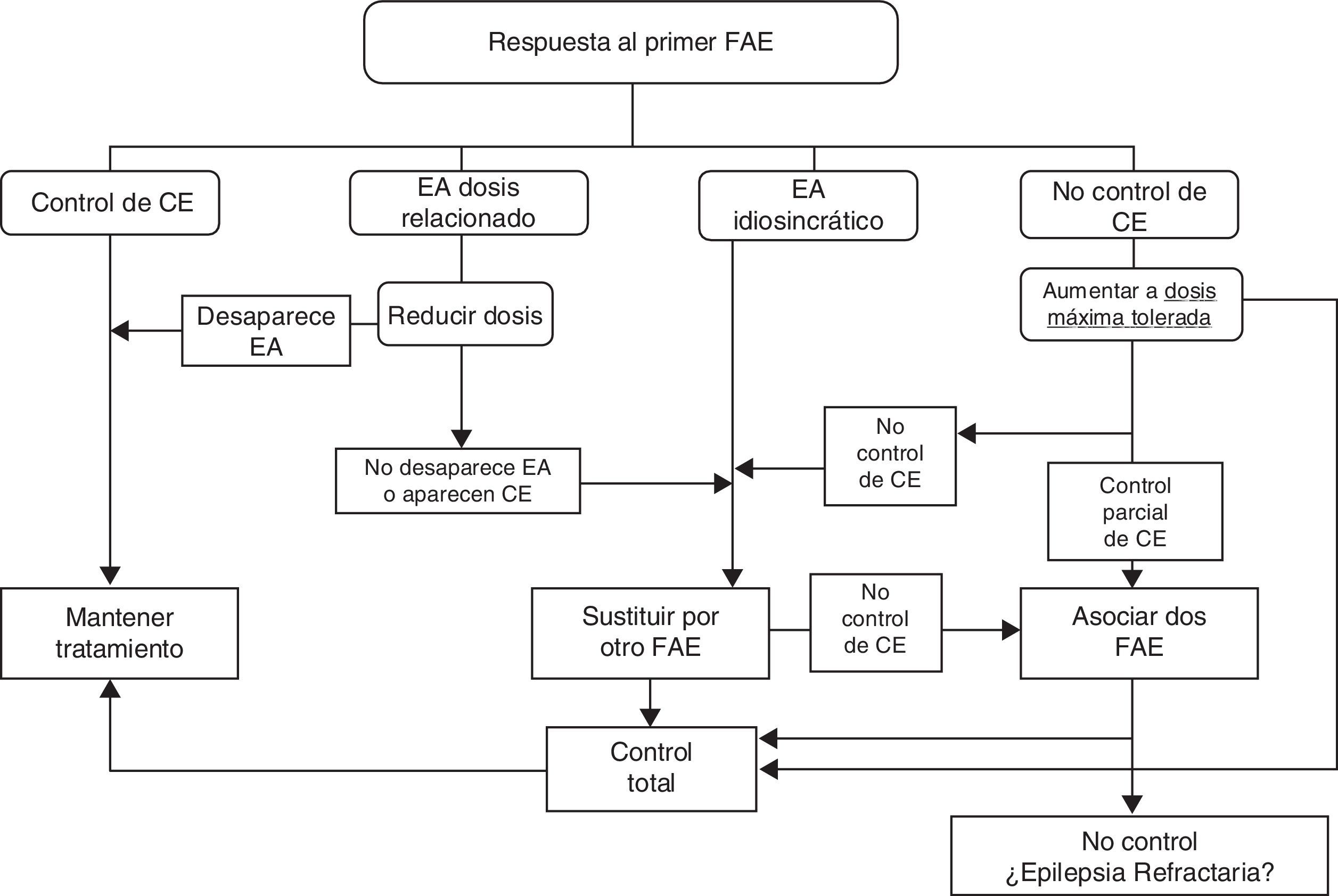
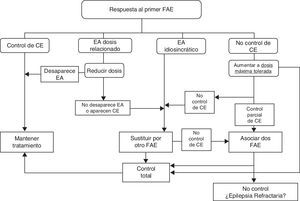
Si después de un par de ensayos en monoterapia no se controlan las CE es aconsejable el empleo de asociaciones de FAE con eficacia probada sobre el tipo de CE y sin sinergia en EA. En la figura 2 se establecen las actuaciones terapéuticas ante las posibles respuestas al tratamiento inicial farmacológico según consenso de los autores de la Guía.
Ajustar el tratamiento a los pacientes individuales ya sea dentro o fuera de la recomendación de una guía, sigue siendo una prerrogativa que los médicos no debemos sacrificar30.
Cuadro general de evidencias y recomendaciones sobre el tratamiento farmacológico cónico de la epilepsia en adultos:
| Nivel | |
|---|---|
| Evidencias en crisis parciales | |
| CBZ, GBP, LEV, LTG, OXC, PB, PHT, TPM, VPA y ZNS son eficaces para el tratamiento inicial en monoterapia | i |
| CBZ y PHT tienen la misma eficacia que PB pero son mejor toleradas | i |
| No hay diferencias en eficacia o tolerabilidad entre PHT y CBZ o VPA | i |
| CBZ es algo más eficaz que VPA y similar en tolerabilidad | i |
| OXC es igual de eficaz pero mejor tolerada que CBZ y PHT | i |
| LTG es igual de eficaz pero mejor tolerada que CBZ | i |
| LTG Y OXC son más efectivas que CBZ, GBP y TPM | iii |
| LEV y ZNS son igual de eficaces que CBZ de liberación retardada | i |
| CLB, GBP, LTG, TGB, TPM, OXC, LEV, ZNS, PGB, LCM, ESL y PER son eficaces en CP refractarias en terapia añadida. | i |
| Evidencias en crisis generalizadas | |
| CBZ, LTG, OXC, PB, PHT, TPM y VPA son eficaces para el tratamiento de las CGTC | i-ii |
| ESM, LTG y VPA, son eficaces para el tratamiento de las ausencias | iii |
| Se desconoce cuál de ellos es más eficaz | |
| ESM no es eficaz contra las CGTC | iv |
| Pueden ser eficaces para el tratamiento de las CE mioclónicas | iv |
| CZP, LEV, LTG, TPM, VPA y ZNS | |
| Para el tratamiento de la epilepsias generalizadas con varios tipos de CE, VPA es más eficaz que LTG y mejor tolerado que TPM | iii |
| CBZ, GBP, OXC, PGB, TGB, VGB, PHT y LTG pueden empeorar las CE de ausencias y/o mioclónicas | iv |
| Recomendaciones sobre FAE de inicio | |
| En CE de comienzo focal con o sin generalización secundaria | GE-SEN |
| LTG, OXC, LEV y ZNS | |
| En CGTC primarias: VPA, LTG | GE-SEN |
| En ausencias: VPA, ESM, LTG | GE-SEN |
| En mioclónicas: VPA, LEV | GE-SEN |
| Epilepsia mioclónica juvenil: VPA | C |
| Alternativa en la mujer en la edad fértil: LTG | GE-SEN |
Los autores declaran no tener ningún conflicto de intereses.