El objetivo del proyecto EPICON es desarrollar una serie de recomendaciones sobre la forma adecuada de realizar el cambio de carbamazepina (CBZ) y oxcarbazepina (OXC) a acetato de eslicarbazepina (ESL) en determinados pacientes con epilepsia.
MétodosUn comité coordinador preparó un cuestionario con 56 preguntas en relación con el cambio de CBZ u OXC a ESL en la práctica clínica (metodología y situaciones del cambio). Posteriormente, se consultó a 54 expertos en epilepsia con el empleo de metodología Delphi (2 rondas de consulta). Se definió un consenso en acuerdo o desacuerdo si las respuestas para el ítem estudiado alcanzaban una mediana ≥ 7 o ≤ 3, respectivamente, y un rango intercuartílico relativo ≤ 0,40. Se analizaron los resultados y se formularon las conclusiones.
ResultadosLas recomendaciones fundamentales fueron: el cambio de CBZ a ESL debe ser realizado en 1-3 semanas, con una equivalencia de dosis CBZ:ESL de 1:1.3, siendo recomendado en pacientes con olvidos de medicación, trabajos por turnos, polimedicados, problemas cognitivos, osteoporosis-osteopenia severa, dislipidemia o enfermedad hepática (ausencia de fallo hepático grave), así como en varones con disfunción eréctil causada por CBZ. El cambio de OXC a ESL puede realizarse de un día para otro con una equivalencia de dosis 1:1 y es recomendado en pacientes con olvidos de medicación, trabajos por turnos, polimedicados o problemas cognitivos. Se desaconsejó el cambio en caso de rash con CBZ u OXC.
ConclusiónEl proyecto EPICON proporciona algunas recomendaciones sobre el manejo clínico del cambio de CBZ u OXC a ESL, mediante el empleo de la metodología Delphi.
The objective of the EPICON Project is to develop a set of recommendations on how to adequately switch from carbamazepine (CBZ) and oxcarbazepine (OXC) to eslicarbazepine acetate (ESL) in some patients with epilepsy.
MethodsA steering committee drafted a questionnaire of 56 questions regarding the transition from CBZ or OXC to ESL in clinical practice (methodology and change situation). The questionnaire was then distributed to 54 epilepsy experts in 2 rounds using the Delphi method. An agreement/disagreement consensus was defined when a median ≥ 7 points or ≤ 3 was achieved, respectively, and a relative interquartile range ≤ 0.40. We analysed the results obtained to reach our conclusions.
ResultsOur main recommendations were the following: switching from CBZ to ESL must be carried out over a period of 1 to 3 weeks with a CBZ:ESL dose ratio of 1:1.3 and is recommended for patients who frequently forget to take their medication, those who work rotating shifts, polymedicated patients, subjects with cognitive problems, severe osteoporosis–osteopaenia, dyslipidaemia, or liver disease other than acute liver failure, as well as for men with erectile dysfunction caused by CBZ. The transition from OXC to ESL can take place overnight with an OXC:ESL dose ratio of 1:1 and it is recommended for patients who frequently forget to take their medication, those who work rotating shifts, polymedicated patients, or those with cognitive problems. The transition was not recommended for patients with prior rash due to CBZ or OXC use.
ConclusionThe EPICON Project offers a set of recommendations about the clinical management of switching from CBZ or OXC to ESL, using the Delphi method.
El objetivo fundamental del tratamiento en epilepsia es conseguir el control de las crisis sin producir efectos adversos1. A su vez, las características de los pacientes y las comorbilidades que puedan tener asociadas son factores importantes a considerar para decidir el tratamiento antiepiléptico más adecuado. Sin embargo, en relación con estos aspectos existe una falta de estudios con un nivel de evidencia de clase i en favor de ningún fármaco antiepiléptico (FAE), lo que hace esta tarea más complicada2. Otros aspectos importantes a considerar para elegir un tratamiento antiepiléptico son las interacciones farmacocinéticas3 y el número de tomas diarias, que puede condicionar la adherencia al tratamiento e incrementar los costes en el caso de mal cumplimiento4,5.
El hecho de que algunos de los aspectos previamente planteados en relación con el tratamiento antiepiléptico sigan sin ser resueltos explica la aparición de nuevos fármacos en los últimos años e incluso el desarrollo de fármacos diferentes dentro de una misma familia. Esto permite a los clínicos disponer de más opciones para elegir el fármaco más adecuado para cada situación. Como previamente ha sido mencionado, existe una falta de estudios con un nivel de evidencia elevado que soporten la elección terapéutica, por consiguiente, la opinión de los clínicos a través de diferentes modelos (consensos o recomendaciones de expertos) constituye una estrategia frecuente en la práctica habitual. Este tipo de estudios presentan un nivel de evidencia bajo pero son útiles para abordar la elección terapéutica en la práctica clínica y pueden servir de guía en algunas situaciones para aquellos especialistas con menos experiencia6-8.
El acetato de eslicarbazepina (ESL) es un FAE de tercera generación aprobado por la European Medicines Agency en 2009 y por la Food and Drug Administration en 2013 y comercializado en España desde febrero del 2011. El fármaco tiene actualmente indicación como terapia añadida para adultos con crisis parciales con o sin generalización secundaria, sobre la base de los resultados de 4 ensayos clínicos fase iii aleatorizados, doble ciego y controlados con placebo9-13. Estos ensayos han mostrado un perfil óptimo en cuanto a eficacia y tolerabilidad con una dosis de ESL entre 800-1.200mg con una toma única diaria.
ESL, junto con carbamazepina (CBZ) y oxcarbazepina (OXC), pertenecen a la familia de las dibenzazepinas. Entre estos fármacos existen diferencias desde el punto de vista estructural, en la posición 10,11 del núcleo de las dibenzazepinas, así como desde el punto de vista de la vía metabólica: CBZ es metabolizada a CBZ 10-11 epóxido, a diferencia de OXC, que es metabolizada al metabolito activo S (+) licarbazepina (78,1%), y ESL, que es metabolizado al mismo metabolito en una proporción mayor (93,9%)14,15. El número de tomas diarias también es diferente: Una toma para ESL y OXC de liberación prolongada (no disponible en España), 2 para OXC de liberación inmediata y CBZ de liberación prolongada (no disponible es España) y 2 a 3 para CBZ de liberación inmediata. Además, con respecto al mecanismo de acción, ESL presenta algunas particularidades con respecto a los otros fármacos de la familia, sintetizadas recientemente en un estudio de Soares Da Silva et al.: 1) interacción selectiva con el estado inactivo de los canales de sodio voltaje dependientes (CSVD); 2) efecto en los CSVD a través de la inactivación lenta de los mismos, en lugar de la inactivación rápida asociada a CBZ y OXC, y 3) inhibición de las corrientes hCaV3.2 con mayor afinidad que CBZ16. En consecuencia, estas diferencias en el perfil de los diferentes FAE de la familia de las dibenzazepinas pueden asociarse a cambios relacionados con la efectividad, la tolerabilidad y la adherencia17. Todo esto hace que en la práctica clínica se plantee el cambio de uno a otro de los fármacos de esta familia, para adaptarse lo mejor posible al perfil del paciente. Sin embargo, el número de estudios realizados para evaluar recomendaciones y situaciones específicas que pudieran tenerse en cuenta para llevar a cabo un cambio adecuado en determinados pacientes es limitado18-21.
El Proyecto EPICON, mediante el empleo de la metodología Delphi entre un grupo de expertos en epilepsia, sometió a evaluación determinadas situaciones y metodología de cambio de CBZ y OXC a ESL. El objetivo del estudio fue tratar de establecer un consenso de recomendaciones que pudieran considerarse para llevar a cabo un cambio adecuado de CBZ u OXC a ESL en determinados pacientes. Estas recomendaciones pueden servir de ayuda fundamentalmente a especialistas con menos experiencia en epilepsia para tomar decisiones en la práctica clínica con un grado de seguridad mayor.
Material y métodosMetodología DelphiLa metodología Delphi se establece sobre la base de una serie de técnicas de investigación dirigidas a determinar las decisiones de grupos, basadas en información cualitativa representada por un número de opiniones de expertos, sobre la base de su experiencia, conocimiento y datos acumulados. Constituye una fuente de información alternativa o complementaria, e incluso en algunos casos única, con el fin de reducir el nivel de incertidumbre y ayudar en el proceso de decisión que pueden plantear algunos temas22.
Así pues, la metodología Delphi es empleada para encontrar consenso entre grupos de expertos y es definida por los siguientes aspectos: 1) es un proceso interactivo en el cual un grupo de expertos es preguntado al menos 2 veces acerca de cuestiones, con una cierta probabilidad de alcanzar un consenso en la segunda ronda de preguntas, en la cual los participantes ya conocen la opinión definida por el grupo en relación con una cuestión específica, de manera que ellos pueden modificar o mantenerse en su primera respuesta; 2) está basado en la opinión anónima de los expertos que participan; 3) el flujo de información es controlado por un comité coordinador del estudio, y 4) se trata de un método cualitativo y aunque algunos conceptos, como errores de muestreo y nivel de significación estadística, no son relevantes, la clave es contar con un grupo de expertos, en número no muy elevado pero con conocimiento y experiencia sobre el tema planteado. En cualquier caso, todas las preguntas son planteadas de modo que las opiniones pueden ser tratadas de un modo cuantitativo, con el fin de obtener indicadores y medidas diferentes que faciliten el intercambio de información y la toma de decisiones en relación con el nivel de consenso alcanzado en las diferentes cuestiones propuestas.
Diseño del estudioEn primer lugar, se creó un comité coordinador para la elaboración del proyecto EPICON, formado por 8 especialistas en epilepsia (HB, JO, JP, RR, JRU, PS, VV, CV). Se encargaron del diseño del estudio, la coordinación del proyecto y el análisis de los resultados. Posteriormente, se constituyó un panel con 54 especialistas en el manejo clínico de la epilepsia distribuidos geográficamente en España. Los panelistas expertos fueron escogidos por los coordinadores del proyecto sobre la base de su experiencia en el campo de la epilepsia, considerándose neurólogos con especial interés en epilepsia, consultas monográficas en epilepsia o desarrollo del trabajo en unidades de epilepsia con una distribución geográfica lo más representativa. Todos ellos accedieron a participar en el proyecto.
Posteriormente, se realizó una consulta a los 54 miembros del panel mediante el empleo de la metodología Delphi. Los coordinadores del estudio diseñaron un cuestionario con 56 preguntas (tablas 1A–D), distribuidas en 4 secciones y referidas a diferentes situaciones que afectan al cambio desde CBZ u OXC a ESL: Sección «Carbamazepina. Metodología del cambio» (preguntas 1-11), tabla 1A; Sección «Carbamazepina. Situaciones de cambio» (preguntas 12-29), tabla 1B; Sección «Oxcarbazepina. Metodología del cambio» (preguntas 30-40), tabla 1C, y Sección «Oxcarbazepina. Situaciones de cambio» (preguntas 41-56), tabla 1D. El cuestionario fue preparado por el comité coordinador, tras evaluar las ideas y sugerencias previamente formuladas por el mismo, en relación con los aspectos a incluir en el estudio. La bibliografía empleada para la redacción de las preguntas se incluyó al final del cuestionario.
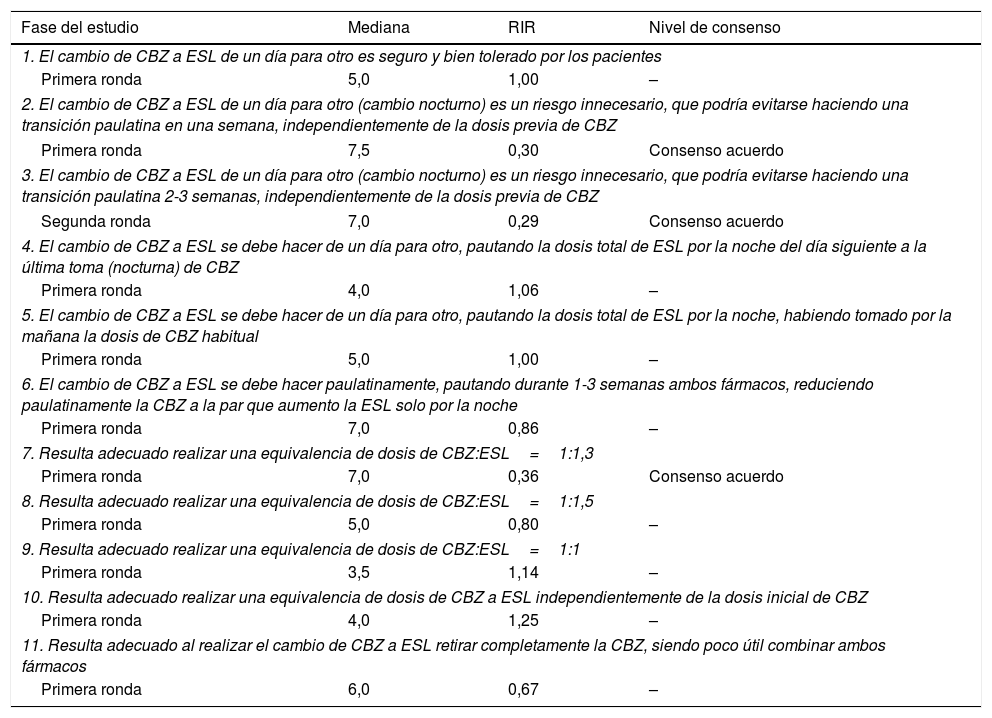
Cuestiones y resultados de la Sección «Carbamazepina. Metodología del cambio»
| Fase del estudio | Mediana | RIR | Nivel de consenso |
|---|---|---|---|
| 1. El cambio de CBZ a ESL de un día para otro es seguro y bien tolerado por los pacientes | |||
| Primera ronda | 5,0 | 1,00 | – |
| 2. El cambio de CBZ a ESL de un día para otro (cambio nocturno) es un riesgo innecesario, que podría evitarse haciendo una transición paulatina en una semana, independientemente de la dosis previa de CBZ | |||
| Primera ronda | 7,5 | 0,30 | Consenso acuerdo |
| 3. El cambio de CBZ a ESL de un día para otro (cambio nocturno) es un riesgo innecesario, que podría evitarse haciendo una transición paulatina 2-3 semanas, independientemente de la dosis previa de CBZ | |||
| Segunda ronda | 7,0 | 0,29 | Consenso acuerdo |
| 4. El cambio de CBZ a ESL se debe hacer de un día para otro, pautando la dosis total de ESL por la noche del día siguiente a la última toma (nocturna) de CBZ | |||
| Primera ronda | 4,0 | 1,06 | – |
| 5. El cambio de CBZ a ESL se debe hacer de un día para otro, pautando la dosis total de ESL por la noche, habiendo tomado por la mañana la dosis de CBZ habitual | |||
| Primera ronda | 5,0 | 1,00 | – |
| 6. El cambio de CBZ a ESL se debe hacer paulatinamente, pautando durante 1-3 semanas ambos fármacos, reduciendo paulatinamente la CBZ a la par que aumento la ESL solo por la noche | |||
| Primera ronda | 7,0 | 0,86 | – |
| 7. Resulta adecuado realizar una equivalencia de dosis de CBZ:ESL=1:1,3 | |||
| Primera ronda | 7,0 | 0,36 | Consenso acuerdo |
| 8. Resulta adecuado realizar una equivalencia de dosis de CBZ:ESL=1:1,5 | |||
| Primera ronda | 5,0 | 0,80 | – |
| 9. Resulta adecuado realizar una equivalencia de dosis de CBZ:ESL=1:1 | |||
| Primera ronda | 3,5 | 1,14 | – |
| 10. Resulta adecuado realizar una equivalencia de dosis de CBZ a ESL independientemente de la dosis inicial de CBZ | |||
| Primera ronda | 4,0 | 1,25 | – |
| 11. Resulta adecuado al realizar el cambio de CBZ a ESL retirar completamente la CBZ, siendo poco útil combinar ambos fármacos | |||
| Primera ronda | 6,0 | 0,67 | – |
RIR: rango intercuartílico relativo.
Cuestiones y resultados de la Sección «Carbamazepina. Situaciones de cambio»
| Fase del estudio | Mediana | RIR | Nivel de consenso |
|---|---|---|---|
| 12. Resulta adecuado el cambio de CBZ a ESL en paciente en el que se presumen olvidos de medicación frecuentes | |||
| Primera ronda | 9,0 | 0,22 | Consenso acuerdo |
| 13. Resulta adecuado el cambio de CBZ a ESL en paciente que trabaja por turnos (variabilidad de horarios) | |||
| Segunda ronda | 8,0 | 0,16 | Consenso acuerdo |
| 14. Resulta adecuado el cambio de CBZ a ESL en paciente polimedicado por pluripatología (con diversas tomas de medicación al día por los diversos tratamientos) | |||
| Primera ronda | 8,0 | 0,25 | Consenso acuerdo |
| 15. Resulta adecuado el cambio de CBZ a ESL en paciente con problemas cognitivos (tales como dificultad de concentración y somnolencia diurna) | |||
| Primera ronda | 8,0 | 0,37 | Consenso acuerdo |
| 16. Con el objetivo de intentar mejorar las crisis resulta adecuado el cambio por ESL ante un paciente sin control de crisis en biterapia con CBZ y un fármaco bloqueante de canales de sodio | |||
| Segunda ronda | 2,5 | 0,5 | Consenso desacuerdo |
| 17. Con el objetivo de intentar mejorar las crisis resulta adecuado el cambio por ESL ante un paciente sin control de crisis en biterapia con CBZ y un fármaco no bloqueante de canales de sodio | |||
| Segunda ronda | 8 | 0,25 | Consenso acuerdo |
| 18. Con el objetivo de intentar mejorar las crisis resulta adecuado el cambio por ESL ante un paciente sin control de crisis en biterapia con CBZ y un fármaco antiepiléptico inductor enzimático | |||
| Segunda ronda | 7,0 | 0,14 | Consenso acuerdo |
| 19. Con el objetivo de intentar mejorar las crisis resulta adecuado el cambio por ESL ante un paciente sin control de crisis en biterapia con CBZ y un fármaco antiepiléptico no inductor enzimático | |||
| Segunda ronda | 7,0 | 0,14 | Consenso acuerdo |
| 20. Resulta adecuado el cambio de CBZ a ESL en paciente mujer en edad fértil | |||
| Primera ronda | 5,0 | 1,20 | – |
| 21. Resulta adecuado el cambio de CBZ a ESL en paciente mujer en edad fértil que toma anticonceptivos | |||
| Primera ronda | 6,0 | 0,58 | – |
| 22. Resulta adecuado el cambio de CBZ a ESL en pacientes diagnosticado de dislipidemia | |||
| Primera ronda | 8,0 | 0,25 | Consenso acuerdo |
| 23. Resulta adecuado el cambio de CBZ a ESL en paciente que ha presentado hiponatremia atribuible a CBZ | |||
| Segunda ronda | 7,0 | 0,43 | – |
| 24. Resulta adecuado el cambio de CBZ a ESL en paciente con hepatopatía, excepto insuficiencia hepática grave (incluyendo aquellos pacientes con incremento aislado de GOT y GPT) | |||
| Segunda ronda | 7,0 | 0,14 | Consenso acuerdo |
| 25. Resulta adecuado el cambio de CBZ a ESL en paciente que ha presentado un «rash» previamente atribuible a CBZ | |||
| Segunda ronda | 2,0 | 1,00 | Consenso desacuerdo |
| 26. Resulta adecuado el cambio de CBZ a ESL en paciente que presenta un cuadro depresivo asociado | |||
| Primera ronda | 5,5 | 0,73 | – |
| 27. Considero adecuado el cambio de CBZ a ESL en un paciente que presenta disfunción eréctil con CBZ | |||
| Segunda ronda | 7,5 | 0,13 | Consenso acuerdo |
| 28. En un paciente controlado con CBZ y osteopenia-osteoporosis severa, ¿considera adecuado el cambio a ESL? | |||
| Primera ronda | 7,0 | 0,32 | Consenso acuerdo |
| 29. En un paciente controlado con CBZ y antecedentes de riesgo cardiovascular independientemente de la dislipidemia, ¿considera adecuado el cambio a ESL? | |||
| Primera ronda | 6,0 | 0,30 | – |
RIR: rango intercuartílico relativo.
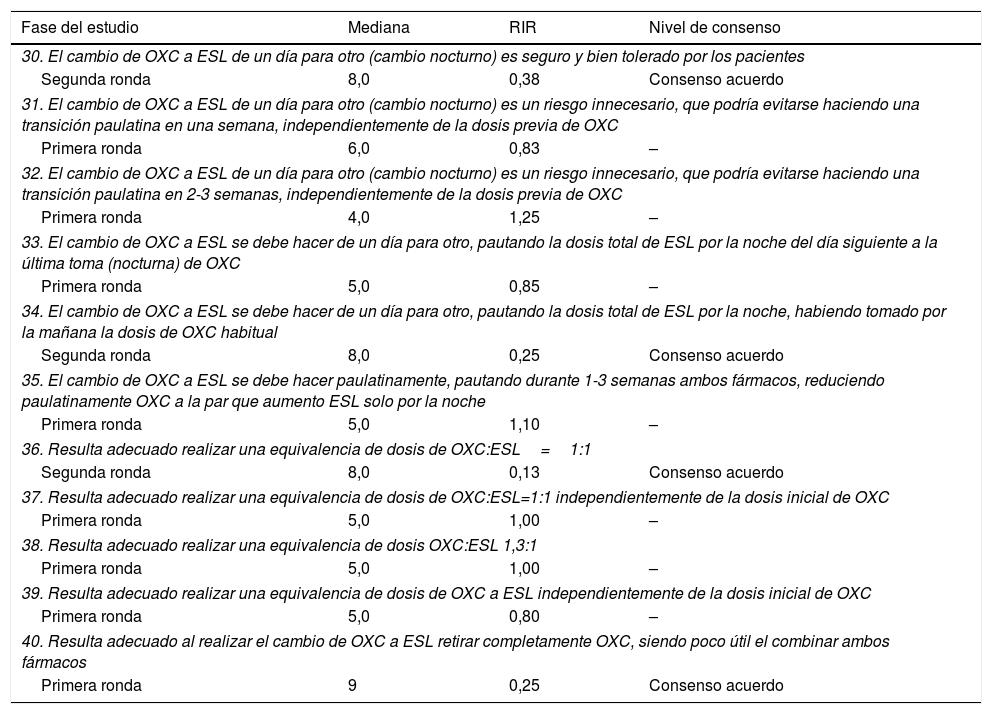
Cuestiones y resultados de la Sección «Oxcarbazepina. Metodología del cambio»
| Fase del estudio | Mediana | RIR | Nivel de consenso |
|---|---|---|---|
| 30. El cambio de OXC a ESL de un día para otro (cambio nocturno) es seguro y bien tolerado por los pacientes | |||
| Segunda ronda | 8,0 | 0,38 | Consenso acuerdo |
| 31. El cambio de OXC a ESL de un día para otro (cambio nocturno) es un riesgo innecesario, que podría evitarse haciendo una transición paulatina en una semana, independientemente de la dosis previa de OXC | |||
| Primera ronda | 6,0 | 0,83 | – |
| 32. El cambio de OXC a ESL de un día para otro (cambio nocturno) es un riesgo innecesario, que podría evitarse haciendo una transición paulatina en 2-3 semanas, independientemente de la dosis previa de OXC | |||
| Primera ronda | 4,0 | 1,25 | – |
| 33. El cambio de OXC a ESL se debe hacer de un día para otro, pautando la dosis total de ESL por la noche del día siguiente a la última toma (nocturna) de OXC | |||
| Primera ronda | 5,0 | 0,85 | – |
| 34. El cambio de OXC a ESL se debe hacer de un día para otro, pautando la dosis total de ESL por la noche, habiendo tomado por la mañana la dosis de OXC habitual | |||
| Segunda ronda | 8,0 | 0,25 | Consenso acuerdo |
| 35. El cambio de OXC a ESL se debe hacer paulatinamente, pautando durante 1-3 semanas ambos fármacos, reduciendo paulatinamente OXC a la par que aumento ESL solo por la noche | |||
| Primera ronda | 5,0 | 1,10 | – |
| 36. Resulta adecuado realizar una equivalencia de dosis de OXC:ESL=1:1 | |||
| Segunda ronda | 8,0 | 0,13 | Consenso acuerdo |
| 37. Resulta adecuado realizar una equivalencia de dosis de OXC:ESL=1:1 independientemente de la dosis inicial de OXC | |||
| Primera ronda | 5,0 | 1,00 | – |
| 38. Resulta adecuado realizar una equivalencia de dosis OXC:ESL 1,3:1 | |||
| Primera ronda | 5,0 | 1,00 | – |
| 39. Resulta adecuado realizar una equivalencia de dosis de OXC a ESL independientemente de la dosis inicial de OXC | |||
| Primera ronda | 5,0 | 0,80 | – |
| 40. Resulta adecuado al realizar el cambio de OXC a ESL retirar completamente OXC, siendo poco útil el combinar ambos fármacos | |||
| Primera ronda | 9 | 0,25 | Consenso acuerdo |
RIR: rango intercuartílico relativo.
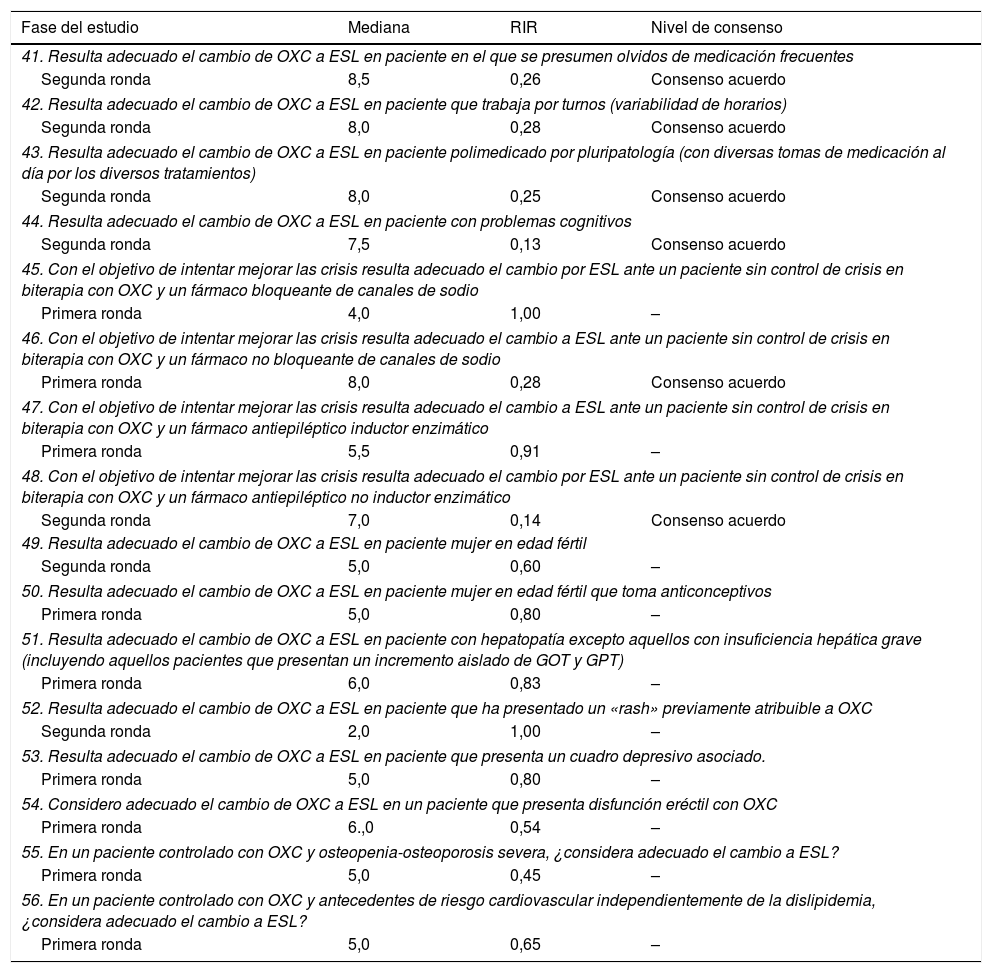
Cuestiones y resultados de la Sección «Oxcarbazepina. Situaciones de cambio»
| Fase del estudio | Mediana | RIR | Nivel de consenso |
|---|---|---|---|
| 41. Resulta adecuado el cambio de OXC a ESL en paciente en el que se presumen olvidos de medicación frecuentes | |||
| Segunda ronda | 8,5 | 0,26 | Consenso acuerdo |
| 42. Resulta adecuado el cambio de OXC a ESL en paciente que trabaja por turnos (variabilidad de horarios) | |||
| Segunda ronda | 8,0 | 0,28 | Consenso acuerdo |
| 43. Resulta adecuado el cambio de OXC a ESL en paciente polimedicado por pluripatología (con diversas tomas de medicación al día por los diversos tratamientos) | |||
| Segunda ronda | 8,0 | 0,25 | Consenso acuerdo |
| 44. Resulta adecuado el cambio de OXC a ESL en paciente con problemas cognitivos | |||
| Segunda ronda | 7,5 | 0,13 | Consenso acuerdo |
| 45. Con el objetivo de intentar mejorar las crisis resulta adecuado el cambio por ESL ante un paciente sin control de crisis en biterapia con OXC y un fármaco bloqueante de canales de sodio | |||
| Primera ronda | 4,0 | 1,00 | – |
| 46. Con el objetivo de intentar mejorar las crisis resulta adecuado el cambio a ESL ante un paciente sin control de crisis en biterapia con OXC y un fármaco no bloqueante de canales de sodio | |||
| Primera ronda | 8,0 | 0,28 | Consenso acuerdo |
| 47. Con el objetivo de intentar mejorar las crisis resulta adecuado el cambio a ESL ante un paciente sin control de crisis en biterapia con OXC y un fármaco antiepiléptico inductor enzimático | |||
| Primera ronda | 5,5 | 0,91 | – |
| 48. Con el objetivo de intentar mejorar las crisis resulta adecuado el cambio por ESL ante un paciente sin control de crisis en biterapia con OXC y un fármaco antiepiléptico no inductor enzimático | |||
| Segunda ronda | 7,0 | 0,14 | Consenso acuerdo |
| 49. Resulta adecuado el cambio de OXC a ESL en paciente mujer en edad fértil | |||
| Segunda ronda | 5,0 | 0,60 | – |
| 50. Resulta adecuado el cambio de OXC a ESL en paciente mujer en edad fértil que toma anticonceptivos | |||
| Primera ronda | 5,0 | 0,80 | – |
| 51. Resulta adecuado el cambio de OXC a ESL en paciente con hepatopatía excepto aquellos con insuficiencia hepática grave (incluyendo aquellos pacientes que presentan un incremento aislado de GOT y GPT) | |||
| Primera ronda | 6,0 | 0,83 | – |
| 52. Resulta adecuado el cambio de OXC a ESL en paciente que ha presentado un «rash» previamente atribuible a OXC | |||
| Segunda ronda | 2,0 | 1,00 | – |
| 53. Resulta adecuado el cambio de OXC a ESL en paciente que presenta un cuadro depresivo asociado. | |||
| Primera ronda | 5,0 | 0,80 | – |
| 54. Considero adecuado el cambio de OXC a ESL en un paciente que presenta disfunción eréctil con OXC | |||
| Primera ronda | 6.,0 | 0,54 | – |
| 55. En un paciente controlado con OXC y osteopenia-osteoporosis severa, ¿considera adecuado el cambio a ESL? | |||
| Primera ronda | 5,0 | 0,45 | – |
| 56. En un paciente controlado con OXC y antecedentes de riesgo cardiovascular independientemente de la dislipidemia, ¿considera adecuado el cambio a ESL? | |||
| Primera ronda | 5,0 | 0,65 | – |
RIR: rango intercuartílico relativo.
En relación con los fármacos evaluados en el consenso Delphi las presentaciones disponibles en España son: CBZ de liberación inmediata, comprimidos de 200 y 400mg, OXC de liberación inmediata, comprimidos de 300 y 600mg, además de suspensión oral (60mg/ml) y ESL, comprimidos de 800mg23-25.
Trabajo de campo y análisis de resultadosMetodológicamente, el estudio se desarrolló en 2 fases. En primer lugar, entre el 21 de enero y el 10 de febrero del 2015, los 54 miembros del panel de especialistas respondieron anónimamente a través de una plataforma digital al cuestionario planteado. Para responder a las preguntas se empleó una escala ordinal (el rango de la respuesta podía variar desde 0 a 10 puntos, «0» significaba «desacuerdo total» y 10 «acuerdo total»). Se definió que se alcanzaría un consenso de acuerdo si las respuestas para el ítem estudiado alcanzaban una mediana de 7 o más puntos y un rango intercuartílico relativo (RIR) menor o igual a 0,40. Por su parte, se estableció que se alcanzaría un consenso en desacuerdo si la mediana de respuestas era de 3 o menos puntos y el RIR menor o igual a 0,40.
Posteriormente, el comité coordinador del estudio realizó un primer análisis de los resultados. Se acordó que las preguntas que alcanzaran un nivel suficiente de acuerdo (mediana ≥ 7) o desacuerdo (mediana ≤ 3), pero con un grado de dispersión en las respuestas alto (RIR ¿ 0,40) serían incluidas en la segunda vuelta del cuestionario. Por el contrario, aquellos ítems con opiniones muy polarizados y, por consiguiente, con un alto grado de dispersión en las respuestas y con medianas lejanas a los valores del consenso de acuerdo (≥ 7) o desacuerdo (≤ 3) serían descartadas para incluirlas en una segunda fase.
Entre el 17 marzo y el 7 abril del 2015, las preguntas seleccionadas (con los criterios previamente indicados) se enviaron para ser reconsideradas por el panel de especialistas en la segunda vuelta. El proceso se repitió nuevamente a través de la plataforma digital con la colaboración anónima de 40 de los 54 especialistas del panel (74%), no obteniéndose respuestas de 14 especialistas del panel original en el periodo planeado. Cabe mencionar que en los estudios Delphi con un número relativamente alto de expertos participantes, como en este trabajo, la reducción en el número de participantes entre la primera y la segunda fase es frecuente, considerándose los resultados como admisibles. El objetivo de esta segunda fase fue reducir la dispersión en las respuestas, cumpliendo los criterios establecidos en la metodología (RIR ≤ 0,40) y por consiguiente alcanzar un consenso en el mayor número de preguntas posible.
Finalmente, y a través de una teleconferencia (mayo del 2015), se realizó un segundo análisis de los resultados por el comité coordinador. Se establecieron las preguntas que alcanzaron un consenso en acuerdo/desacuerdo, se formularon las conclusiones y se cerró el estudio.
ResultadosLos resultados del estudio en las diferentes cuestiones planteadas se muestran en la tablas 1A–D. Las situaciones en los que se alcanzó un consenso se sintetizan a continuación.
Carbamazepina. Metodología de cambioLa mayoría de los expertos (62%) consideraron que el cambio de CBZ a ESL de un día para otro es un riesgo innecesario que debiera ser evitado con un cambio progresivo en un periodo de 1 a 3 semanas independientemente de la dosis previa de CBZ. Los miembros del panel también coincidieron en que el cambio de CBZ a ESL debiera llevarse a cabo considerando una equivalencia de dosis CBZ:ESL de 1:1.3 (tabla 1A).
Carbamazepina. Situaciones de cambioLos miembros del panel alcanzaron un consenso de acuerdo en el cambio de CBZ a ESL en pacientes en los que se presumen olvidos frecuentes de medicación, en aquellos que trabajan por turnos (variabilidad de horarios), pacientes polimedicados por pluripatología (con diversas tomas de medicación al día por diversos tratamientos), aquellos con problemas cognitivos, en los controlados con CBZ y osteopenia-osteoporosis severa, aquellos diagnosticados de dislipidemia, con hepatopatía, excepto aquellos con insuficiencia hepática severa (incluyendo aquellos con incremento aislado de GOT y GPT), así como aquellos pacientes con disfunción eréctil con CBZ. A su vez, se alcanzó un consenso en desacuerdo sobre el cambio de CBZ a ESL en pacientes que habían presentado un rash atribuible a CBZ.
Los expertos también alcanzaron un consenso sobre el cambio de tratamiento de CBZ a ESL en pacientes sin control de crisis tratados en biterapia con: CBZ y un fármaco no bloqueante de canales de sodio (NBS), CBZ y un FAE inductor enzimático (IE) y aquellos con CBZ y un FAE no IE (NIE). Por su parte, se alcanzó un consenso en desacuerdo sobre el cambio de CBZ a ESL en pacientes en biterapia con CBZ y un fármaco bloqueante de canales de sodio (BCS) (tabla 1B).
Oxcarbazepina. Metodología de cambioLos panelistas alcanzaron un consenso de acuerdo en relación con el cambio nocturno de OXC a ESL de un día para otro, pautando la dosis total de ESL por la noche, habiendo tomado por la mañana la dosis de OXC habitual. Se acordó realizar el cambio con una equivalencia de dosis de OXC: ESL 1:1, recomendándose retirar completamente la OXC al realizar el cambio a ESL, por considerarse poco útil la combinación de ambos fármacos (OXC+ESL) (tabla 1C).
Oxcarbazepina. Situaciones de cambioLos expertos alcanzaron un consenso de acuerdo en relación con la idoneidad del cambio de OXC a ESL en pacientes en los que se presumen olvidos de medicación frecuentes, en pacientes que trabajan por turnos (variabilidad de horarios), en pacientes medicados por pluripatología (con diversas tomas de medicación al día por diversos tratamientos) y en pacientes con problemas cognitivos. Por su parte, los expertos alcanzaron un consenso en desacuerdo sobre el cambio de OXC a ESL en pacientes que habían presentado previamente un rash atribuible a OXC.
Finalmente, los expertos llegaron a un consenso de acuerdo en el cambio de tratamiento en pacientes sin control de crisis en biterapia con OXC y un fármaco NIE o un NBS (tabla 1D).
DiscusiónCarbamazepina. Metodología de cambioEl consenso alcanzado por los panelistas de este trabajo en relación con la equivalencia de dosis en el cambio de CBZ a ESL (1:1.3) coincidió con las recomendaciones de Peltola et al.19 y Massot et al.26. Al igual que Peltola et al19, se alcanzó un acuerdo en emplear un periodo mínimo de 1-3 semanas en el cambio. La excepción para realizar el cambio de un día para otro, no planteada en el consenso Delphi, podría ser aplicada en el caso de pacientes hospitalizados26. Por otra parte, no se alcanzó un consenso en acuerdo ni en desacuerdo sobre la retirada completa de CBZ al iniciar ESL. En este contexto, se han de considerar ambas opciones, teniendo en cuenta que aunque la administración concomitante de CBZ y ESL se ha asociado a un incremento significativo en el porcentaje de efectos adversos27, en los ensayos clínicos fase iii más del 55% de los pacientes recibieron CBZ y ESL simultáneamente9-13.
Carbamazepina. Situaciones de cambioLos panelistas alcanzaron un consenso de acuerdo sobre el cambio de CBZ a ESL en pacientes con problemas de cumplimentación: olvidos de medicación o pacientes que trabajan por turnos. Debe ser considerado que ESL tiene una vida media de 20-24 h28 con una dosis única diaria, a diferencia de CBZ de liberación inmediata (12-17 h tras administración continuada), formulación disponible en España, que requiere 2 o 3 dosis por día24. La idoneidad del cambio de CBZ a ESL fue también considerada en el paciente polimedicado por pluripatología, que requiere diferentes tomas al día de los diferentes tratamientos, con el fin de simplificar el tratamiento antiepiléptico con una sola toma al día29. Finalmente, se llegó a un consenso de acuerdo en el cambio de CBZ a ESL en pacientes con problemas cognitivos; en este sentido, diferentes estudios han probado que la CBZ produce un deterioro en diversos parámetros cognitivos30, especialmente el procesamiento de la información y la capacidad de concentración31; sin embargo los efectos adversos cognitivos observados con ESL son en general bajos en la práctica clínica (3,3%-9,8%)17,26,32.
Se consideró adecuada la sustitución por ESL en pacientes con un control de crisis inadecuado, que recibían biterapia con CBZ y un fármaco IE o un fármaco NIE, y en pacientes que reciben una biterapia con un fármaco NBS, no considerándose adecuado si el fármaco era BCS. Un estudio de práctica clínica mostró que el porcentaje de respondedores se incrementó cuando ESL fue combinado con un fármaco NBS (66,7% vs. 44,7%)17. El hecho de presentar un mecanismo de acción diferente en los canales de sodio (inactivación lenta) a CBZ, al igual que sus diferencias en otras vías (corrientes en canales hCaV3.2), puede explicar la decisión de recomendar la combinación de ESL con otros fármacos sobre la base del mecanismo de acción16. Además, el menor efecto IE de ESL comparado con CBZ puede explicar la decisión de combinar con otros fármacos sobre la base de su efecto IE23,24.
En relación con la mujer en edad fértil, los miembros del panel no alcanzaron un consenso en acuerdo ni en desacuerdo en relación con la idoneidad del cambio de CBZ por ESL. Así, aunque se observa que los fármacos IE, tales como CBZ, pueden provocar un incremento en la globulina fijadora de hormonas sexuales (GFHS), provocando un descenso en los niveles de estradiol que puede conllevar problemas a nivel sexual o de fertilidad33, la falta de información en los registros de embarazo con ESL, a diferencia de CBZ, podría explicar la falta de consenso. Tampoco se alcanzó un consenso (en acuerdo o en desacuerdo) en relación con el cambio de tratamiento en mujeres en edad fértil que toman anticonceptivos. Así, CBZ ha mostrado un incremento en el metabolismo del etinilestradiol y progestágenos, y contraindica el uso de implantes de levonorgestrel34, pero el tratamiento con ESL también está asociado a un descenso en la exposición a etinilestradiol y levonorgestrel35. Respecto a los varones, CBZ puede reducir los niveles de testosterona33 e incrementar la GFHS, provocando en consecuencia una disminución de la actividad de los andrógenos libres y la dehidroepiandrosterona36,37. Estos efectos, descritos en general con fármacos IE como CBZ, pueden asociarse a disfunción sexual en el varón38. En este sentido, los expertos llegaron a un consenso de acuerdo en el cambio de CBZ a ESL en pacientes con disfunción eréctil en tratamiento con CBZ, probablemente en relación con un menor efecto inductor de ESL a nivel hormonal14,39.
En relación con las alteraciones en los parámetros analíticos de los pacientes y las posibilidades de cambio de CBZ a ESL, se pueden destacar 3 aspectos. 1) Los expertos llegaron a un consenso en el cambio de CBZ a ESL en pacientes con dislipidemia. El tratamiento con CBZ se ha asociado a un incremento significativo en los niveles de colesterol total y las lipoproteínas de baja densidad (LDL)40. Con respecto a ESL, Gil-Nagel et al.13 mostraron en los ensayos clínicos que su efecto en los niveles de triglicéridos (TG) y colesterol fue similar a placebo y algunas evidencias recientes en práctica clínica sugieren un descenso en los niveles de LDL y TG cuando se cambia el tratamiento de CBZ a ESL41. 2) Los miembros del panel no alcanzaron ningún acuerdo en el cambio a ESL en pacientes con hiponatremia producida por CBZ. De acuerdo con el estudio de Dong et al.42, el 13,5% de los pacientes en tratamiento con CBZ presentaron hiponatremia, siendo esta cifra superior al porcentaje descrito en los ensayos clínicos con ESL (1,5-8,8%)9-13, aunque se ha de considerar que las poblaciones son diferentes. Un estudio retrospectivo reciente reportó una mejoría en relación con las cifras de hiponatremia cuando se cambió de CBZ u OXC a ESL; sin embargo, el número de pacientes evaluados en este estudio fue limitado433) Los expertos llegaron a un consenso en el cambio de tratamiento de CBZ a ESL en pacientes con enfermedad hepática, incluyendo a aquellos con incremento aislado de GOT y GPT, excepto aquellos con insuficiencia hepática grave. En este sentido, el estudio de Hussein et al. mostró una correlación negativa estadísticamente significativa entre la duración de la administración de CBZ y los niveles de GOT y GPT44, mientras que las tasas de alteración de los parámetros hepáticos en los ensayos clínicos con ESL fue inferior al 1%13.
Finalmente, en relación con el rash, la ausencia de estudios comparativos entre CBZ y ESL y la experiencia personal de los panelistas pueden justificar que no se considerase adecuado el cambio de CBZ a ESL en un paciente con rash previo por CBZ. Por el contrario, en cuanto al metabolismo óseo, el cambio de CBZ a ESL en pacientes con osteopenia-osteoporosis severa alcanzó un consenso de acuerdo. Así, el potente efecto IE de CBZ se correlaciona con una disminución significativa de la densidad mineral ósea y un incremento en el riesgo de fracturas45. Específicamente, en el estudio de Vestergaard, la odds ratio (OR) de una posible fractura causada por el uso de CBZ fue 1,1846. Una menor capacidad inductora de ESL podría prevenir este efecto, aunque hay una falta de estudios a largo plazo para probar este hecho.
Oxcarbazepina. Metodología de cambioLos miembros del panel de expertos consideraron que el cambio de OXC a ESL podría ser realizado de un día para otro. Otros autores también han apoyado esta forma de realizar el cambio de tratamiento18,26, incluyendo las recientes recomendaciones de Peltola et al.19. La similitud en la vía metabólica entre ambos fármacos (OXC y ESL) puede explicar esta modalidad de cambio. Tal y como es recomendado por otros autores, los panelistas coincidieron en prescribir la dosis total de ESL por la noche tras tomar la dosis de la mañana de OXC y usar una equivalencia de dosis OXC: ESL 1:118,19,26,29. Se alcanzó igualmente un consenso de acuerdo en la retirada completa de OXC al asociar ESL debido a la pobre respuesta obtenida con la administración de ambos.
Oxcarbazepina. Situaciones de cambioEl tratamiento con OXC de liberación inmediata (presentación existente en España) consiste en 2 o en algunas ocasiones 3 tomas por día para minimizar los efectos adversos asociados a pacientes que reciben una dosis elevada47. Por esta razón, y sobre la base de mejorar adherencia al tratamiento descrita con un menor número de tomas48, los panelistas consideraron adecuado el cambio de OXC a ESL en pacientes que frecuentemente olvidan tomar su medicación o que trabajan por turnos (variabilidad de horarios), o en aquellos polimedicados por pluripatología que requieren varias tomas al día de diferentes fármacos. Además, los miembros del panel llegaron a un consenso en la idoneidad del cambio de OXC a ESL en pacientes con problemas cognitivos, en relación con la baja frecuencia de efectos adversos cognitivos asociados a ESL29. Así, tras analizar los resultados de los ensayos clínicos aleatorizados con ambos fármacos, se ha observado una reducción en los efectos adversos neurológicos con ESL comparado con OXC49. Por otra parte, un trabajo en voluntarios sanos mostró un pico precoz de fármaco en el líquido cefalorraquídeo y el plasma tras la administración de OXC comparándola con ESL, lo cual puede asociarse a una peor tolerabilidad de OXC15. Finalmente, un estudio de práctica clínica mostró una mejoría en el perfil de tolerabilidad en más de la mitad de los pacientes que cambiaron de OXC a ESL por efectos adversos17.
Los expertos también consideraron adecuado el cambio de OXC por ESL en pacientes que presentaban un mal control de crisis con una biterapia de OXC y un fármaco NIE, y una biterapia de OXC con un fármaco NBS. El mecanismo de acción diferente en los canales de sodio (inactivación lenta) de ESL respecto a OXC puede explicar la decisión para su combinación con otros fármacos sobre la base del mecanismo de acción50. Existe una falta de evidencia que aconseje o desaconseje la combinación con otros FAE sobre la base de las propiedades de inducción enzimática de ESL respecto a OXC.
Finalmente, en relación con el rash, la ausencia de estudios comparativos entre OXC y ESL, la experiencia personal, así como la similitud en la vía metabólica de ambos fármacos, pueden justificar que los especialistas no considerasen adecuado el cambio de OXC a ESL en un paciente con rash previo por OXC. En cuanto al metabolismo óseo, con la administración de OXC se ha reportado una OR de fractura ósea de 1,1446. Sin embargo, los expertos no llegaron a un consenso en el cambio de OXC a ESL en pacientes con osteopenia-osteoporosis severa probablemente por la falta de resultados a largo plazo con ESL.
El estudio tiene diversas limitaciones y fortalezas. Las mayores limitaciones del mismo son, en primer lugar, la falta de un nivel elevado de evidencia en los resultados (se trata de una opinión de expertos basada en metodología Delphi); en segundo lugar, la arbitrariedad y la subjetividad de las preguntas propuestas, que cubren algunos aspectos del tratamiento pero no todos, y en tercer lugar, que no todos los panelistas participaron en la segunda fase del estudio. La mayor fortaleza de este estudio es la recogida de opiniones de un amplio panel de expertos en epilepsia, con el empleo de una metodología novedosa (Delphi) en la evaluación de este tema y, por último, la comunicación de nuevos datos en un campo con escasa información útil en la práctica clínica.
ConclusionesEste artículo proporciona una revisión sistemática, usando la metodología Delphi, en algunas situaciones clínicas en las que un grupo de expertos españoles en epilepsia considerarían adecuado el cambio de CBZ u OXC a ESL. Aunque algunas controversias en determinadas situaciones no se han resuelto con este trabajo, el análisis del mismo proporciona algunas recomendaciones sobre el manejo clínico del cambio de CBZ u OXC a ESL, que podría servir de ayuda en la práctica diaria, particularmente a especialistas con menor experiencia.
Conflicto de interesesEl trabajo ha contado con la colaboración de los laboratorios BIAL y ESAI para las labores de edición y difusión. Estas compañías no intervinieron en la elección de las preguntas, el análisis de los resultados ni redacción del artículo.
A los 54 miembros del panel de expertos que participaron en el proyecto EPICON.
Dra. Ainhoa Marinas (Hospital Universitario Cruces, Bilbao), Dr. Albert Molins (Hospital Universitario Josep Trueta, Girona), Dr. Alberto García (Hospital Universitario Central de Asturias), Dr. Alberto Moral (Hospital Universitario Central de Asturias), Dr. Álex García (Hospital Imed Levante, Benidorm), Dra. Ana Piera (Hospital Clínico Universitario, Valencia), Dr. Antonio Moreno (Hospital Son Espases, Palma de Mallorca), Dr. Antonio Oliveros (Hospital Reina Sofía de Tudela), Dra. Arantxa Alfaro (Hospital La Vega Baja, Orihuela), Dra. Ascensión Castillo (Hospital General Universitario, Valencia), Dr. Asier Gómez (Hospital Universitario La Fe, Valencia), Dra. Carmen Arenas (Hospital Virgen del Rocío, Sevilla), Dra. Clara Cabeza (Complejo Hospitalario Universitario de Toledo), Dr. David Sopelana (Hospital General Universitario Albacete), Dr. Diego Tortosa (Hospital Universitario Arrixaca, Murcia), Dra. Dulce Campos (Hospital Clínico Universitario, Valladolid), Dr. Emilio Martínez (Hospital Comarcal de Vinaroz), Dr. Francisco Javier López (Complejo Hospitalario Universitario, Santiago), Dr. Francisco Villalobos (consulta privada, Sevilla), Dra. Guillermina García (Hospital Clínico de Málaga), Dr. Guillermo Rubio (consulta privada, Jerez de la Frontera), Dr. Íñigo Garamendi (Hospital Universitario Cruces, Bilbao), Dr. Javier Montoya (Hospital Lluis Alcanyis, Xàtiva).
Dr. Jerónimo Sancho (Hospital General Universitario, Valencia), Dr. José Ángel Mauri (Hospital Clínico Universitario Lozano Blesa), Dr. José Carlos Giner (Hospital General Universitario, Elche), Dr. José María Serratosa (Fundación Jiménez Díaz, Madrid), Dr. Juan Carlos Sánchez (Hospital Clínico Universitario San Cecilio, Granada), Dr. Juan José Poza (Hospital Universitario Donosti), Dr. Juan Luis Becerra (Hospital Universitario Germans Trias i Pujols, Badalona), Dr. Juan Mercadé (Hospital Universitario Carlos Haya, Málaga), Dr. Juan Palau (Hospital de Manises, Valencia), Dra. M. Eugenia García (Hospital Clínico San Carlos, Madrid), Dra. Macarena Bonet (Hospital Universitario Arnau Vilanova, Valencia), Dr. Manuel Domínguez (Clínica la Milagrosa, Madrid), Dr. Manuel Toledo (Hospital Universitario Vall d¿Hebron, Barcelona), Dra. Mar Carreño (Hospital Clínic Universitario, Barcelona), Dra. M. José Aguilar-Amat (Hospital Universitario La Paz, Madrid).
Dra. Marta Agúndez (Hospital Universitario Cruces, Bilbao), Dra. Mercè Falip (Hospital Universitario Bellvitge, L’Hospitalet de Llobregat), Dra. Mercedes Garcés (Hospital Universitario La Fe, Valencia), Dra. Nuria García (Hospital Ramón y Cajal, Madrid), Dr. Óscar Vega (Hospital Cruz Roja, Córdoba), Dr. Pablo Quiroga (Hospital Universitario Torrecárdenas, Almería), Dr. Pedro Bermejo (Hospital Universitario Puerta de Hierro), Dr. Pedro Quesada (Complejo Hospitalario de Navarra).
Dr. Rafael Toledano (Hospital Universitario Ramón y Cajal, Madrid), Dr. Raúl Amela (Hospiten Roca, Gran Canaria), Dra. Rosa Querol (Hospital Universitario Infanta Cristina, Badajoz), Dr. Vicente Bertol (Hospital Miguel Servet, Zaragoza), Dr. Xavier Salas (Hospital Universitario Vall d¿Hebron, Barcelona), Dra. Xiana Rodríguez (Complejo Hospitalario Universitario, Santiago).
A la Agencia Entheos, por su asistencia en la planificación, trabajo de campo y análisis de resultados.