Recientes estudios con datos en vida real sobre el uso de anticoagulantes de acción directa (ACOD) en pacientes con fibrilación auricular no valvular, aportan datos del empleo de los diferentes ACOD según las características de los pacientes. El objetivo de este trabajo fue elaborar un documento sobre las sugerencias de uso de los ACOD en función de la evidencia existente en la literatura y de la experiencia clínica.
Materiales y métodosUn panel multidisciplinar de 8 expertos consensuó y desarrolló el contenido. El documento elaborado fue completado en 10 reuniones regionales con expertos de distintas especialidades. El panel valoró las aportaciones de los expertos regionales y elaboró las sugerencias definitivas.
ResultadosEl documento final recoge las aportaciones generadas a lo largo de todo el proceso en 3 apartados. Se detallan las conclusiones/sugerencias generales sobre el empleo de los ACOD. Se proponen sugerencias concretas de empleo de cada ACOD en función de características clínicas específicas de los pacientes. Por último, se definen las limitaciones al empleo de los ACOD y se proponen acciones para mejorar el manejo de la anticoagulación.
ConclusionesEs necesario superar las barreras clínicas y administrativas que dificultan el óptimo empleo de los ACOD con el fin de mejorar el tratamiento de los pacientes con fibrilación auricular no valvular que precisan anticoagulación.
Recent real-world data studies on the use of direct oral anticoagulants (DOAC) in patients with non-valvular atrial fibrillation, provide data on the use of different DOAC according to patient characteristics. The objective of this work was to elaborate on the suggestions on the use of DOAC based on evidence and clinical experience.
Materials and methodsA multidisciplinary panel of 8 experts developed the agreed content. The document was completed in 10 regional meetings with experts from different specialties. According to these contributions, the panel prepared the final suggestions.
ResultsThe final document includes the contributions generated throughout the entire process in 3 sections. The general conclusions / suggestions on the use of DOAC are detailed. Specific tips on the use of each DOAC are proposed, based on the specific clinical profiles of the patients. Finally, the limitations on the use of DOAC are defined, and a group of actions are proposed to improve the management of anticoagulation.
ConclusionsIt is necessary to overcome the clinical and administrative barriers that hinder the optimal use of DOAC, in order to improve the treatment of patients with non-valvular atrial fibrillation who require anticoagulation.
La fibrilación auricular en España muestra una prevalencia del 4,4% y del 8,5% en la población de edad superior a 40 y 60 años, respectivamente1,2, que aumenta exponencialmente con la edad, alcanzado cifras del 15-20% por encima de los 75-80 años3.
La fibrilación auricular incrementa el riesgo de ictus de 4 a 5 veces4. La tasa media anual de ictus isquémico en pacientes con fibrilación auricular no valvular (FANV) es del 5% y supera el 23% en mayores de 80 años4.
Los antagonistas de la vitamina K (AVK) han demostrado reducir la incidencia de ictus en aproximadamente un 64%5, aunque presentan limitaciones bien conocidas6,7. Estas limitaciones son más evidentes en los pacientes de mayor edad, con mayor riesgo hemorrágico y habitualmente polimedicados. Además, distintos estudios observacionales realizados en España8–11 han mostrado que aproximadamente entre un 40% y un 50% de los pacientes tratados con AVK tiene un tiempo del índice normalizado del tiempo de protrombina (INR) en rango terapéutico inferior al 65%.
Los nuevos anticoagulantes orales de acción directa (ACOD) (dabigatrán, rivaroxabán, apixabán y edoxabán) presentan un efecto anticoagulante fijo y predecible que hace innecesaria la realización de controles rutinarios, siendo seguros y cómodos para los pacientes. Tienen algunas interacciones medicamentosas, pero son más predecibles y manejables que las de los AVK. Están recomendados sobre los AVK por sociedades médicas internacionales en pacientes con FANV que precisan anticoagulación oral12,13; empieza a disponerse de datos en la vida real que complementan los resultados de los estudios pivotales14–19 y, conforme la literatura internacional, se muestran como fármacos eficientes e incluso dominantes en determinados perfiles de pacientes.
El documento sobre el empleo de los ACOD en el Sistema Nacional de salud (SNS) para la prevención de eventos tromboembólicos en pacientes con FANV, elaborado en 2012 por el Consejo Interterritorial del SNS, tuvo como objetivo asegurar un acceso adecuado y equitativo a estos fármacos en el sistema de financiación pública. Sin embargo, ni el documento inicial ni las sucesivas actualizaciones del mismo han conseguido el objetivo de eliminar las diferencias entre las comunidades autónomas en los usos considerados aceptados ni en la identificación de pacientes con un control inadecuado del INR20,21.
Por todo ello, se consideró pertinente la elaboración de un documento con el doble objetivo de proporcionar unas sugerencias de uso de los ACOD en función de la evidencia existente en la literatura y de la experiencia clínica, y de proponer unas acciones encaminadas a facilitar el conocimiento y empleo de estos fármacos. En el presente artículo se exponen las conclusiones finales de dicho documento.
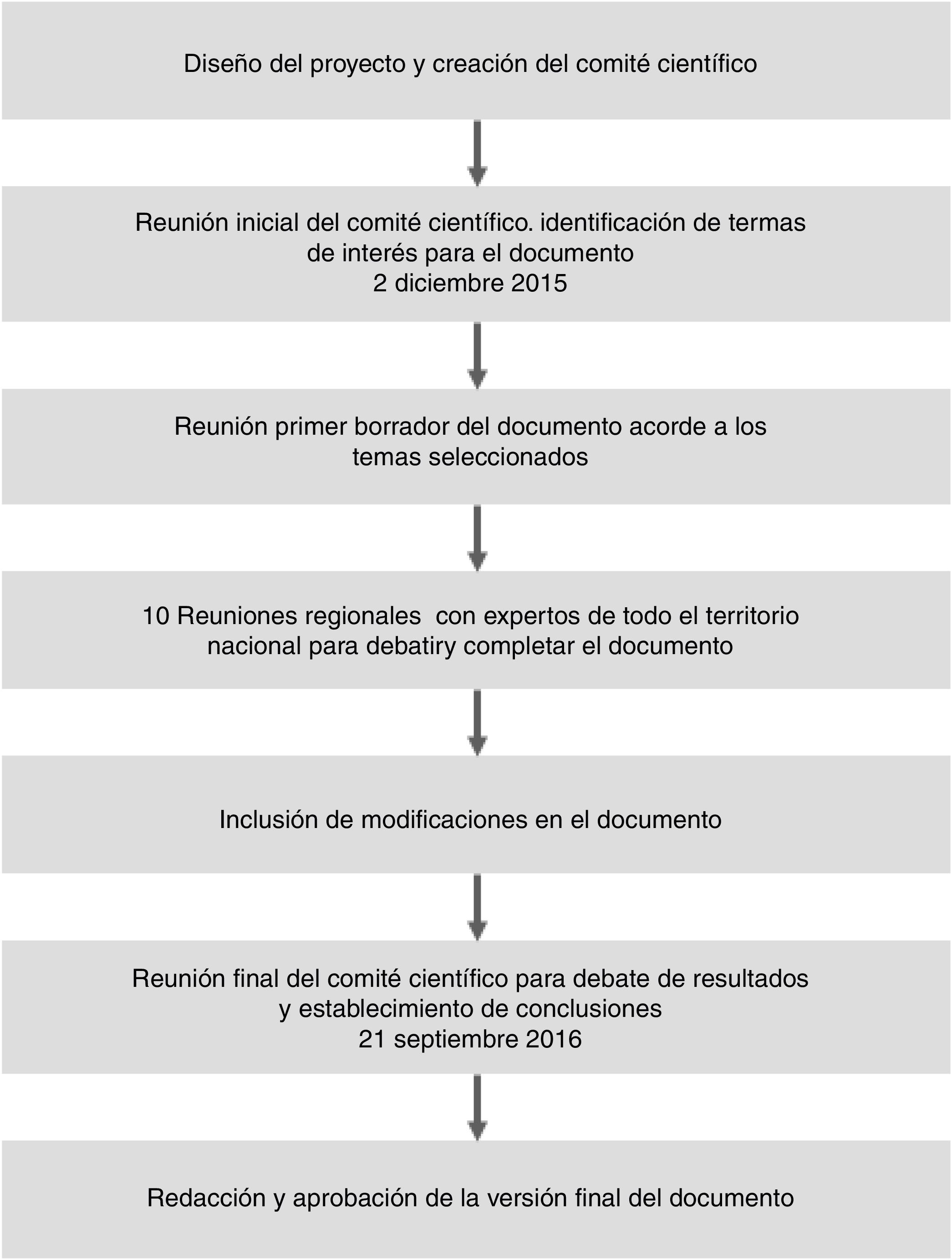
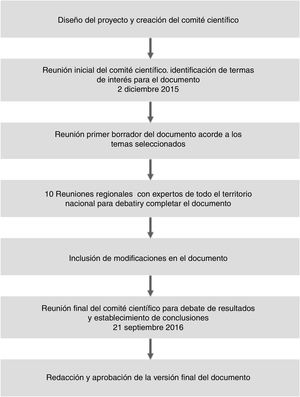
Material y métodosSe creó un comité científico multidisciplinar compuesto por expertos de diferentes especialidades: cardiología, hematología, neurología, medicina interna, farmacología clínica, atención primaria y farmacoeconomía. La metodología seguida para la elaboración del documento se observa en la figura 1. En una primera reunión presencial los expertos consensuaron un índice de temas y el contenido de cada uno de ellos. De forma general, los bloques temáticos identificados fueron: situación actual de la anticoagulación en la FANV en España, prevención de los eventos tromboembólicos con ACOD en pacientes con FANV en la práctica clínica real y evaluación económica de los ACOD. Posteriormente, los propios expertos desarrollaron dichos temas basándose en la literatura existente, lo que cristalizó en un primer borrador de documento.
A continuación, entre marzo y junio de 2016, se realizaron 10 reuniones regionales en las que participaron expertos de distintas áreas y especialidades implicadas en el manejo de los ACO. Las reuniones fueron moderadas por un consultor externo de GOC Networking utilizando la técnica de brainstorming estructurado22 (Metaplan®). En ellas, los participantes aportaron sus ideas y experiencia clínica en aspectos relacionados con los ACOD, los perfiles de los pacientes tributarios de anticoagulación y las barreras existentes al empleo de estos fármacos y sus posibles soluciones.
En la segunda reunión del comité se valoraron las aportaciones de los expertos regionales y se establecieron las bases para la elaboración del documento final.
ResultadosEl documento final consta de 3 apartados: conclusiones/sugerencias generales sobre los ACOD, sugerencias concretas de empleo de cada ACOD y propuestas de acciones a llevar a cabo para mejorar el manejo de la anticoagulación.
Conclusiones/sugerencias generales- 1.
Existen tasas elevadas de mal control de la anticoagulación con AVK en España, por lo que los ACOD son una alternativa de la que estos pacientes se podrían beneficiar. Es necesario mejorar el acceso a los ACOD para este grupo de pacientes.
- 2.
Todos los ACOD han demostrado un beneficio-riesgo favorable en la prevención del ictus y la embolia sistémica en pacientes con FANV.
- 3.
Los ACOD son fármacos con mejor perfil de seguridad que los AVK, sobre todo en relación con el riesgo de hemorragia intracraneal. Son también los indicados en casos de insuficiencia renal leve o moderada y en pacientes frágiles o con elevado riesgo de sangrado.
- 4.
Aunque no hay datos comparativos entre los diferentes ACOD, existen algunas situaciones o perfiles de pacientes que se pueden beneficiar según el ACOD que se utilice. Se sugiere la selección del ACOD más adecuado según el perfil del paciente, considerando el riesgo trombótico y el hemorrágico.
- 5.
Los datos obtenidos en estudios de vida real complementan y son consistentes con los observados en los ensayos clínicos aleatorizados.
- 6.
Los ACOD no necesitan terapia puente con heparinas de bajo peso molecular en procedimientos invasivos o quirúrgicos, en la mayoría de los casos.
- 7.
Además del resultado sobre los pacientes los ACOD también suponen potenciales mejoras del bienestar de su entorno familiar. Es necesario considerar la perspectiva social en la evaluación económica de los ACOD, dado el impacto de los eventos en el tiempo y la calidad de vida de la familia/cuidadores.
- 8.
Los ACOD son fármacos que presentan una buena relación coste-resultado en salud frente a los AVK, en aquellos pacientes con los perfiles adecuados.
- 9.
Los ACOD son la primera elección tanto en prevención primaria como secundaria, tal como recomiendan las guías de práctica clínica. Las eventuales restricciones que se establezcan por razones de impacto presupuestario deben justificarse y comunicarse adecuadamente en unos criterios revisados de uso de ACOD en el SNS.
- 10.
Es necesario usar la dosis correcta para cada ACOD.
- 11.
Los ACOD son los fármacos más adecuados en casos de pacientes sometidos a cardioversión eléctrica23.
- 12.
Es importante realizar un seguimiento periódico a los pacientes en tratamiento con ACOD, por ejemplo, de la adherencia terapéutica o la función renal.
- 13.
Existe la posibilidad de elegir el ACOD en función de la frecuencia de toma diaria (1v/día vs. 2v/día). Sin embargo, esta conclusión parece poco relevante.
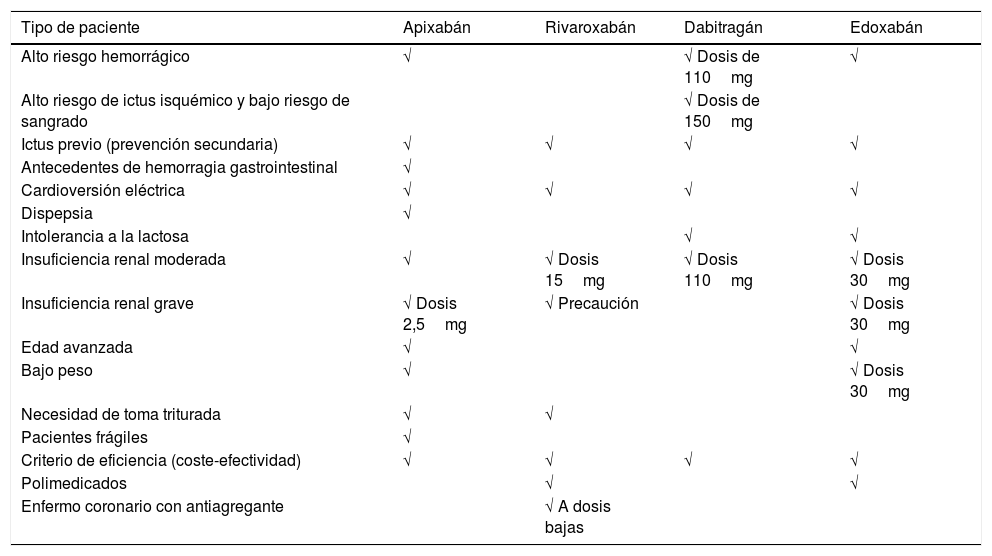
Durante las reuniones se definieron unos perfiles de pacientes para los que se establecieron unas sugerencias de empleo del ACOD más adecuado, tal y como se describe a continuación y se resume en la tabla 1.
Sugerencias de empleo preferencial de los diferentes ACOD en función del perfil del paciente, según el grupo de expertos
| Tipo de paciente | Apixabán | Rivaroxabán | Dabitragán | Edoxabán |
|---|---|---|---|---|
| Alto riesgo hemorrágico | √ | √ Dosis de 110mg | √ | |
| Alto riesgo de ictus isquémico y bajo riesgo de sangrado | √ Dosis de 150mg | |||
| Ictus previo (prevención secundaria) | √ | √ | √ | √ |
| Antecedentes de hemorragia gastrointestinal | √ | |||
| Cardioversión eléctrica | √ | √ | √ | √ |
| Dispepsia | √ | |||
| Intolerancia a la lactosa | √ | √ | ||
| Insuficiencia renal moderada | √ | √ Dosis 15mg | √ Dosis 110mg | √ Dosis 30mg |
| Insuficiencia renal grave | √ Dosis 2,5mg | √ Precaución | √ Dosis 30mg | |
| Edad avanzada | √ | √ | ||
| Bajo peso | √ | √ Dosis 30mg | ||
| Necesidad de toma triturada | √ | √ | ||
| Pacientes frágiles | √ | |||
| Criterio de eficiencia (coste-efectividad) | √ | √ | √ | √ |
| Polimedicados | √ | √ | ||
| Enfermo coronario con antiagregante | √ A dosis bajas |
ACOD: anticoagulantes orales de acción directa.
- 1.
Pacientes con insuficiencia renal moderada (tasa de aclaramiento renal 30-49ml/min), apixabán 5mg; si además la edad es>80 años, el peso<60kg o la creatinina>1,5mg/dl la dosis de apixabán será de 2,5mg.
- 2.
Pacientes con insuficiencia renal grave (tasa de aclaramiento renal 15-29ml/min): apixabán 2,5mg.
- 3.
Pacientes con antecedentes de hemorragia gastrointestinal independientemente de la etiología de la misma. Los resultados de vida real concuerdan con los obtenidos en los ensayos clínicos pivotales.
- 4.
Pacientes con alto riesgo hemorrágico. Los resultados de vida real complementan los obtenidos en los ensayos clínicos pivotales.
- 5.
Pacientes de edad avanzada (>85-90 años), aunque resulta complicado establecer un límite de edad. Son pacientes considerados frágiles y por esa razón presentan más riesgo de sangrado (la complicación más peligrosa de la anticoagulación). Apixabán destaca por su seguridad en este perfil.
- 6.
Pacientes con bajo peso.
- 7.
Pacientes con ictus previo (prevención secundaria).
- 8.
Pacientes con dispepsia.
- 9.
Pacientes sometidos a cardioversión eléctrica.
- 10.
Pacientes que necesiten tomar apixabán de forma triturada.
- 11.
Pacientes frágiles.
- 12.
En aquellos pacientes con los perfiles adecuados su uso es eficiente (buena relación coste-resultado en salud) frente a los AVK.
- 1.
Pacientes polimedicados. La toma única de este fármaco facilita la adherencia terapéutica. Sin embargo, los AVK pueden presentar ventajas en esta situación debido al estrecho seguimiento que se realiza.
- 2.
Pacientes con insuficiencia renal moderada (tasa de aclaramiento renal 30-49ml/min), rivaroxabán 15mg.
- 3.
Pacientes con insuficiencia renal grave (tasa de aclaramiento renal 15-29ml/min), rivaroxabán se debe usar con precaución en estos pacientes.
- 4.
Pacientes con ictus previo (prevención secundaria).
- 5.
Pacientes sometidos a cardioversión eléctrica.
- 6.
Pacientes que necesiten tomar rivaroxabán de forma triturada.
- 7.
En el caso del enfermo coronario con antiagregante es más adecuada la utilización de rivaroxabán a dosis bajas.
- 8.
En aquellos pacientes con los perfiles adecuados su uso es eficiente (buena relación coste-resultado en salud) frente a los AVK.
- 1.
Pacientes con un alto riesgo trombótico, como prevención secundaria de ictus en su dosis de 150mg. En la práctica clínica se suele administrar la dosis de 150mg a pacientes menores de 80 años y la de 110mg a los mayores de 80 años.
- 2.
Pacientes con alto riesgo hemorrágico: dabigatrán 110mg.
- 3.
Pacientes con insuficiencia renal moderada (tasa de aclaramiento renal 30-49ml/min): dabigatrán 110mg.
- 4.
En pacientes con insuficiencia renal grave (tasa de aclaramiento renal<30ml/min) está contraindicado.
- 5.
Pacientes con ictus previo (prevención secundaria).
- 6.
Pacientes sometidos a cardioversión eléctrica.
- 7.
Pacientes con intolerancia a la lactosa.
- 8.
En aquellos pacientes con los perfiles adecuados su uso es eficiente (buena relación coste-resultado en salud) frente a los AVK.
- 1.
Pacientes polimedicados, con igual reflexión que en el caso de rivaroxabán.
- 2.
Pacientes con insuficiencia renal moderada o grave (aclaramiento de la creatinina 15-50ml/min): edoxabán 30mg.
- 3.
Pacientes de bajo peso (≤60kg), edoxabán 30mg.
- 4.
Paciente con alto riesgo hemorrágico.
- 5.
Pacientes con ictus previo (prevención secundaria).
- 6.
Pacientes sometidos a cardioversión eléctrica. Este perfil no está incluido en la ficha técnica, aunque tiene algún estudio realizado que lo avala.
- 7.
Pacientes de edad avanzada.
- 8.
Pacientes con intolerancia a la lactosa.
- 9.
En aquellos pacientes con los perfiles adecuados su uso es eficiente (buena relación coste-resultado en salud) frente a los AVK.
Se destacaron 2 tipos de barreras a la indicación de los ACOD: clínicas y administrativas. Entre las primeras están la falta de conocimiento general sobre la eficacia y seguridad de los ACOD, los problemas asociados al control del INR (ya sea su control deficiente o el desconocimiento de los valores) y al tiempo en rango terapéutico, la falta de agente reversor para los ACOD anti-Xa y la presencia de insuficiencia renal grave, de insuficiencia hepática y de barreras asociadas al estatus del paciente (edad, historia de enolismo, discapacidad, etc.).
En el caso de las barreras administrativas se destacaron las relacionadas con el Informe de posicionamiento terapéutico y la visión cortoplacista del impacto presupuestario frente a los AVK, un exceso de burocracia, la no disponibilidad de prescripción de ACOD como primera opción y la no existencia de protocolos multidisciplinares para el manejo de los pacientes tratados con estos fármacos.
Para salvar o paliar el efecto de las anteriores barreras, y conseguir un mejor manejo de las situaciones que requieran anticoagulación, se hacen necesarias una serie de acciones:
- •
Campañas de difusión en la prensa general y especializada que involucren a las distintas sociedades científicas. Se debe hacer hincapié en los mensajes sobre la inequidad y el riesgo innecesario que corren los pacientes mal anticoagulados con AVK, y que es posible reducir con la anticoagulación adecuada.
- •
Difusión de los mensajes a los responsables decisores (ministerio y comunidades autónomas). Es importante conocer cuáles son los criterios políticos y económicos que se emplean para la toma de decisiones. Existen otros fármacos de elevado coste y peores resultados en términos de ganancia en salud que no tienen tantas barreras. Estos criterios deberían asignar el uso de recursos en función de los resultados obtenidos en salud24.
- •
Implicar a las asociaciones de pacientes anticoagulados, al estilo de como se realiza con otras asociaciones (por ejemplo diabéticos), para que realicen también acciones sobre las entidades decisorias.
- •
Formación al profesional sobre el uso y manejo de los ACOD, aprovechando, por ejemplo, las sesiones clínicas realizadas en los centros de atención primaria.
Los resultados de los estudios pivotales han hecho que tanto la guía de la European Society of Cardiology de manejo de la fibrilación auricular como la de la American College of Cardiology/American Heart Association recomienden los ACOD sobre los AVK para reducir el riesgo de ictus y fenómenos tromboembólicos25,26. A los resultados de los estudios pivotales se le suman las recientes publicaciones con datos de vida real que van perfilando y adecuando la utilización de los diferentes ACOD según las situaciones y características de los pacientes, y las valoraciones económicas que muestran que los ACOD son eficientes, e incluso pueden ser dominantes (mayor efectividad y menor coste) en grupos de pacientes de alto y moderado riesgo de ictus frente al resto de anticoagulantes orales.
Es un hecho que el control de la anticoagulación con AVK existente en España es deficiente. Como reiteradamente muestran los datos de los registros, el 40% de la población anticoagulada está mal controlada8–11. Por otro lado, estudios en vida real apuntan que existe un porcentaje significativo de pacientes que no siguen las pautas posológicas de las fichas técnicas27,28: en un análisis del registro ORBIT AF II el 13% de los pacientes estaba infra o supradosificado, lo que se asoció a un incremento del riesgo de efectos adversos28. Por último, en nuestro medio, sigue siendo elevado el porcentaje de pacientes que, teniendo la indicación, no recibe tratamiento anticoagulante29. Todo ello hace fundamental el correcto conocimiento de estos fármacos. Aunque todas las sugerencias/conclusiones realizadas están basadas en la experiencia clínica y la evidencia publicada, el panel de expertos quiso hacer hincapié en algunos aspectos concretos. Así pues señalaron que, en general, rivaroxabán presenta idoneidad en pacientes con menor riesgo hemorrágico, mientras que el resto de ACOD presenta idoneidad en pacientes con elevado riesgo hemorrágico. Asimismo, afirmaron que no existe ningún ACOD que permita asociarse a pacientes con doble antiagregación, a la espera de ver cómo afectarán los resultados del reciente estudio PIONEER-AF-PCI30 a la ficha técnica de rivaroxabán. La sugerencia sobre el empleo de apixabán en insuficiencia renal moderada se basa en la guía del National Institute for Health and Clinical Excellence (NICE)31 sobre la enfermedad renal crónica, que recomienda considerar apixabán en preferencia a la warfarina en personas con una tasa de filtrado glomerular confirmada de 30-50ml/min/1,73m2 y FANV, que tengan uno o más factores de riesgo específicos de ictus. El empleo de dabigatrán en pacientes con un alto riesgo trombótico, como prevención secundaria de ictus en su dosis de 150mg, está avalado por el estudio RE-LY32 y en el metaanálisis de Ruf et al.33. En el RE-LY se utilizaron las dosis de 150mg y 110mg de forma aleatorizada, y no se demostró una disminución en los eventos trombóticos en prevención secundaria, sino en prevención global.
El documento de 2012 sobre el empleo de los ACOD en el SNS para la prevención de eventos tromboembólicos en pacientes con FANV, elaborado bajo la coordinación de la Agencia Española de Medicamentos y Productos Sanitarios en consenso con representantes de las comunidades autónomas y expertos clínicos, estableció unas indicaciones de uso en el SNS que, entre otros factores, tenía en cuenta: «el impacto presupuestario de la sustitución de los AVK por los nuevos anticoagulantes, que aconseja disponer de un análisis que identifique los grupos de pacientes prioritarios para estos nuevos tratamientos y permita así establecer una estrategia racional para su uso en el Sistema Nacional de Salud en las indicaciones autorizadas».
Aunque este documento se ha considerado un «informe de posicionamiento terapéutico» de nuevos medicamentos, no nació como tal, ya que fue elaborado tras la decisión de financiación y tras tomas de posición de algunas comunidades autónomas. Quizás por ello ni el documento inicial ni las sucesivas actualizaciones del mismo han conseguido el objetivo de eliminar las diferencias entre las comunidades autónomas en los usos considerados aceptados, ni en la identificación de pacientes con un control inadecuado del INR20.
Adicionalmente, el visado añade nuevas inseguridades. Es frecuente hacer una interpretación totalmente rígida y administrativa de los criterios, olvidando que la decisión de instaurar el tratamiento debe individualizarse en función del paciente y debería ser posible, por tanto, justificar siempre los casos individuales.
Por otro lado, los datos disponibles de empleo de anticoagulantes en España dentro del SNS34 muestran, a finales del año 2015, un porcentaje de uso de ACOD de un 22,0% frente a un 76,2% de AVK, sensiblemente inferior al que la misma fuente refiere en los países de nuestro entorno, como Francia, Italia, Portugal o Alemania (38,7%, 35,1%, 50% y 53,0% respectivamente) y similar al del Reino Unido (22,1%).
El impacto presupuestario que supondría acercarnos a los porcentajes de estos países se vería compensado en parte por la reducción de los costes, derivados de una reducción de los eventos. En este sentido cabe destacar que tanto los datos españoles como las evaluaciones presentadas por el NICE muestran una buena relación entre el coste y el resultado en salud para los perfiles adecuados de pacientes, en comparación con los anticoagulantes tradicionales35–37.
Las distintas sociedades científicas reclamaron, en 2015, que el nuevo documento de los criterios para el uso de los ACOD en el SNS fuera una actualización real y acorde con las nuevas evidencias38. Sin embargo, la nueva versión, publicada el 21 de noviembre de 201639, no presenta cambios sustanciales.
En resumen, es acorde con nuestro ordenamiento que, por motivos económicos y de impacto presupuestario, se establezcan prioridades y restricciones en el uso de los ACOD en el SNS. Pero dichas decisiones deben responder a un proceso de análisis riguroso y participativo, que incluya de forma explícita las consideraciones económicas que forman parte de la decisión, deben comunicarse adecuadamente a los ciudadanos y profesionales y deben, finalmente, ser respetadas por las instituciones que han participado en su elaboración y las han adoptado.
ConclusionesLos estudios pivotales, de vida real y las evaluaciones económicas ponen de manifiesto las ventajas de los ACOD en comparación con los AVK.
La elección del perfil de paciente que más se beneficie de los ACOD en general, y de cada uno de ellos en particular, puede ayudar a obtener los mejores resultados, no solo de efectividad y seguridad, sino también en términos de eficiencia.
Los criterios de uso de los ACOD deberían tener en cuenta las nuevas evidencias de eficacia y seguridad disponibles, la experiencia acumulada de la implementación práctica de los vigentes criterios de uso de los ACOD en España y el respeto a los principios de equidad y eficiencia en el uso de los recursos en nuestro SNS; sin embargo, los actuales criterios de uso de los ACOD en España no parecen ser sensibles a los mencionados elementos.
Es necesario poner en marcha diversas acciones para conseguir superar las barreras clínicas y administrativas que dificultan el óptimo empleo de los ACOD y, con ello, conseguir una mejoría en la situación vital de los pacientes que precisan anticoagulación.
FinanciaciónEl presente trabajo ha sido financiado por laboratorios Bristol-Myers Squibb y Pfizer.
Conflicto de interesesManuel Anguita: declara no tener conflicto de intereses.
Antonio Dávalos: declara haber sido ponente en reuniones patrocinadas por Bayer, Daiichi-Sankyo, Boehringer Ingelheim, asesor de Boehringer Ingelheim y Bayer, así como miembro del Steering Committee NAVIGATE ESUS (Bayer).
Esteban López de Sá: declara no tener conflicto de intereses.
José Mateo: declara haber recibido ayudas para la asistencia a congresos, el pago de ponencias y disfrutar de ayudas a la investigación por parte de BMS-Pfizer, Boehringer-Ingelheim, Daiichi-Sankyo y Bayer.
Manuel Monreal: declara haber recibido ayudas para la investigación clínica de Sanofi y de Bayer, así como haber participado como asesor en reuniones con Sanofi, Bayer, Bristol, Leo y Boehringer Ingelheim.
Juan Oliva: declara haber recibido ayudas para participar en paneles de discusión por parte de BMS-Pfizer y ayudas a la investigación por parte de AstraZeneca y Lilly.
José Polo: declara haber participado como asesor y ponente en reuniones patrocinadas por Bayer, Bristol, Pfizer y Boehringer Ingelheim.
Los autores quieren agradecer a los asistentes a las sesiones regionales por sus aportaciones (anexo A), a los laboratorios Bristol-Myers Squibb y Pfizer por el apoyo económico para la realización de este trabajo, y a GOC Networking, por su apoyo en la conducción metodológica a lo largo de todo el proceso.