La agenesia completa del páncreas dorsal (ADP por sus siglas en inglés) es una infrecuente anomalía congénita del páncreas, compatible con la vida. La mayoría son asintomáticos y suelen ser diagnosticadas de manera incidental. En casos sintomáticos las manifestaciones clínicas varían desde dolor abdominal, pancreatitis y diabetes mellitus a insuficiencia exocrina con esteatorrea. Presentamos el caso clínico de una mujer de 28 años con ADP que, cursando cuadro de SARS-CoV2, evoluciona con hiperglicemias. El estudio con resonancia magnética (RM) confirma la ausencia de cuello, cuerpo y cola pancreática. Es de gran utilidad el conocimiento de la embriogénesis pancreática, de la sintomatología que pueden producir sus malformaciones y sus principales características radiológicas para el correcto diagnóstico por imagen de estas anomalías
Complete agenesis of the dorsal pancreas (ADP) is an exceedingly rare congenital anomaly, compatible with life. It is frequently asymptomatic and usually incidentally diagnosed. In symptomatic cases, the clinical manifestations vary from abdominal pain, pancreatitis and diabetes mellitus to exocrine insufficiency with steatorrhea. We present a case report of a 28-year-old female with ADP, diagnosed incidentally during radiological evaluation for hyperglycemias during a SARS-CoV2 concomitant infection. Magnetic resonance cholangiopancreatography confirmed the absence of neck, body and tail of the pancreas.
Familiarization with pancreatic embryogenesis, as well as the clinical presentation and main radiological characteristics of its anomalies is important for the proper diagnosis of these malformations.
La agenesia del páncreas dorsal es una anomalía congénita extremadamente rara. El primer caso se informó en 1911 durante una autopsia y hasta la fecha se han reportado menos de 100 casos en la literatura mundial1.
En este trabajo presentamos el caso de una paciente que concurre al servicio con un cuadro de encefalopatía secundaria a SARS-CoV2 y presenta como hallazgo incidental una malformación pancreática compatible con ADP. Consideramos de interés la publicación del caso dado su baja frecuencia.
Caso ClínicoMujer de 28 años con antecedente de asma bronquial en tratamiento con salbutamol SOS, normopesa, quien consulta por un cuadro de 7 días de evolución caracterizado por cefalea, mialgias, calofríos y tos. Se realiza examen de PCR para SARS-CoV2 con resultado positivo. A los dos días, se asocia compromiso cualitativo de conciencia, inatención, desorientación temporo-espacial y pérdida de control de esfínteres, por lo que es derivada desde atención primaria al Hospital Carlos van Buren (HCVB). En la evaluación inicial destaca paciente en regulares condiciones generales, hemodinámica estable, saturando 98% ambiental, hidratada,con un hemoglucotest (HGT) >400mg/dl y glicemia venosa de 399mg/dl. Adicionalmente, al laboratorio destaca estado ácido-base normal, electrolitos en rango normal, cetonemia negativa, osmolalidad plasmática estimada de 296 mOsm/L y pO2 de 96mmHg.
La paciente es evaluada por neurología con tomografía computada (TC) y resonancia magnética (RM) de cerebro, sin lesiones agudas y con un estudio de líquido cefalorraquídeo que concluye líquido no inflamatorio con estudio microbiológico ampliado negativo. Finalmente, posterior a una extensa evaluación en donde se descartaron síndrome hiperglicémico hiperosmolar, encefalopatía hipoxica y deshidratación, se plantea encefalopatía secundaria a infección por SARS-CoV2 y manejo expectante con adecuada respuesta, recuperando vigilia y atención.
Posteriormente, evoluciona con poliuria de hasta 6 litros/día, cursando con deshidratación moderada, hipokalemia, hipocalcemia, hipomagnesemia e hiperfosfemia, sin deterioro de función renal. Prueba diagnóstica con desmopresina negativa, por sospecha de diabetes insípida, persistiendo con poliuria y agregandose hiponatremia leve (hasta 130 mEq/L), la cual es manejada con aporte de volumen hasta normalización de volemia. El estudio de orina arroja sodio urinario bajo y glucosuria, por lo que es manejada con hipoglicemiantes, con adecuada respuesta, impresionando poliuria secundaria a cuadros de hiperglicemia.
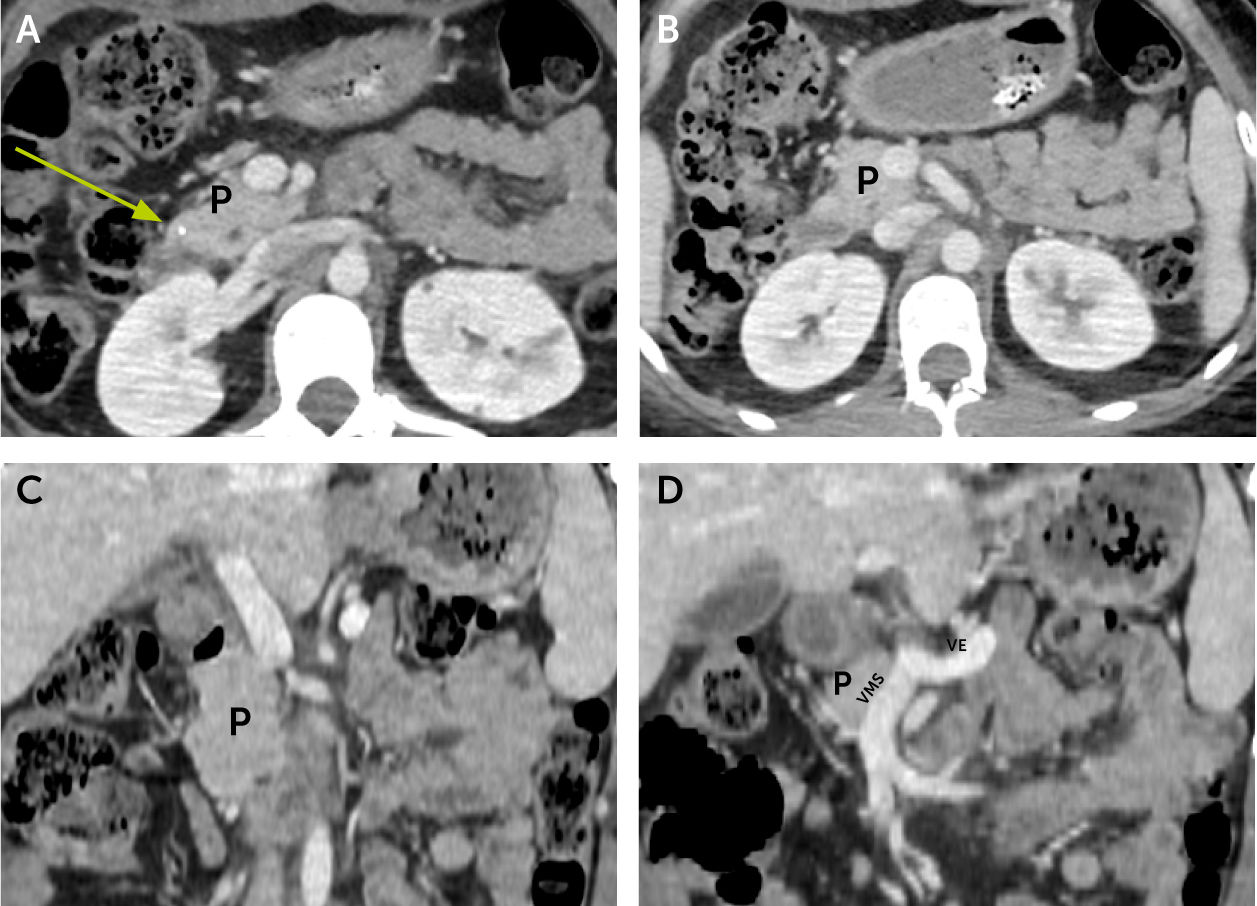
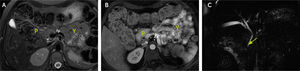
Paciente se maneja con bomba de infusión de insulina logrando adecuado control glicémico; en estudio metabólico destaca hemoglobina glicosilada (HbA1c) de 9,8% y pruebas tiroideas normales. En contexto de debut de diabetes en paciente joven y sin sobrepeso ni signos de insulirresistencia se plantea estudio con pruebas inmunológicas de diabetes mellitus tipo 1 (anticuerpos anti-células beta (ICA), anti-insulina (IAA), anti-ácido glutámico descarboxilasa (GAD), anti-tirosina fosfatasa (IA2) y anti-transportador 8 de Zinc (ZnT8)), todas negativas. Se solicita TC de abdomen con contraste para estudio de causas estructurales de diabetes mellitus, en donde destaca la no visualización de cuerpo y cola pancreática, sólo evidenciándose cabeza y proceso uncinado de tamaño normal, con calcificación de 5mm (Fig. 1). Se complementa estudio de anatomía pancreática con RM de abdomen con contraste y colangio-RM, concluyendo agenesia completa del páncreas dorsal (Fig. 2). Se diagnostica diabetes pancreatogénica exacerbada en contexto de infección por SARS-CoV2.
TC con contraste en fase porta. Cortes axiales (A y B). Cortes coronales (C y D). Se identifica calcificación intrapancreática (flecha). Porción cefálica del páncreas (P) con densidad habitual y realce homogéneo. Segmentos corporal y caudal ausentes. VMS: vena mesentérica superior; VE: vena esplénica.
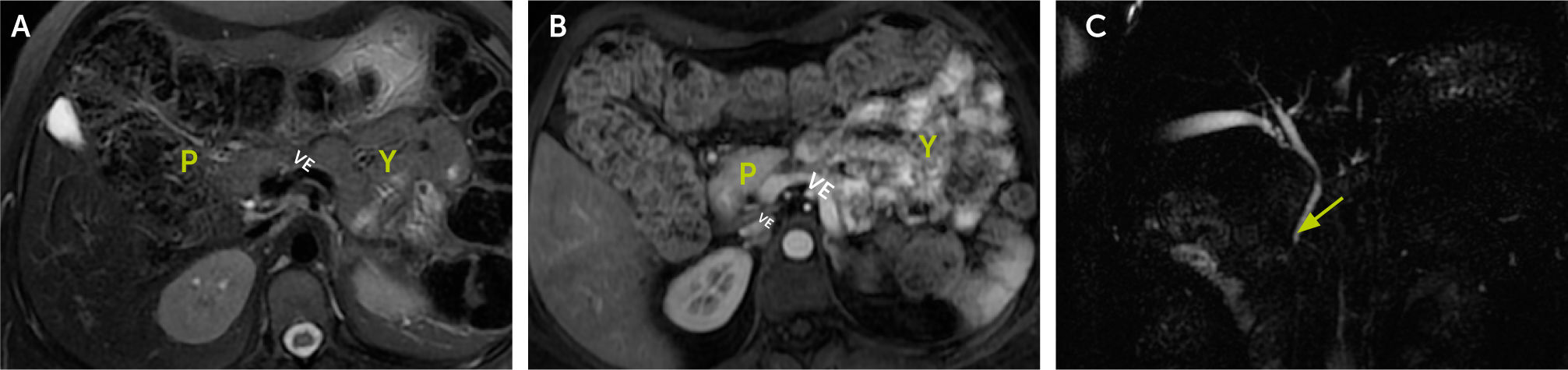
Cortes axiales RM. A. Imagen potenciada T2 FATSAT. B. Fase dinámica con contraste precoz. Se reconoce cabeza y proceso uncinado del páncreas (P) y ausencia de cuello, cuerpo y cola. Anterior a vena esplénica (VE), asas de yeyuno (Y). C. Colangio-RM, se constata solo ducto pancreático ventral (flecha).
Tras completar el estudio y normalización de glicemia y estado de conciencia se decide egreso hospitalario con insulina basal, que se controla de forma ambulatoria reduciendo de forma progresiva, hasta los actuales requerimientos mínimos.
Manifestaciones clínicasLa mayoría de los pacientes con esta anomalía son asintomáticos y se detectan de manera incidental. En casos sintomáticos las manifestaciones incluyen dolor abdominal, hiperglicemia, diabetes mellitus y pancreatitis aguda o crónica2. El síntoma más frecuente es el dolor abdominal, localizado en el epigastrio que empeora postprandial. Este fenómeno estaría supeditado a pancreatitis transitorias por obstrucción duodenal, disfunción del esfínter de Oddi o neuropatía autonómica1.
La asociación con la diabetes mellitus es común ya que las células beta productoras de insulina se encuentran en el cuerpo y cola del páncreas2. Esta manifestación se observa en aproximadamente el 43 a 50% de los casos3.
También se relaciona con pancreatitis. Los mecanismos propuestos para explicar la pancreatitis incluyen disfunción del esfínter de Oddi, hipertrofia compensadora e hipersecreción enzimática del páncreas ventral con elevación de la presión intraductal3. Además, se han reportado en algunos pacientes esteatorrea y signos de insuficiencia pancreática exocrina1.
Embriología del páncreasConocer el desarrollo embriológico del páncreas es fundamental para comprender las anomalías congénitas.
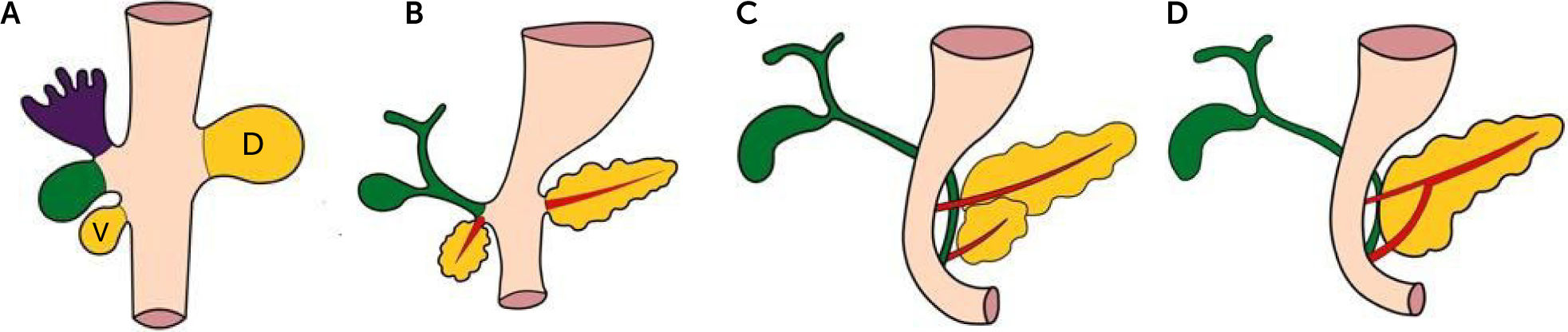
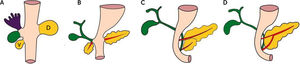
El páncreas se origina entre las sexta y octava semana de vida embrionaria, deriva del endodermo, al igual que otros órganos gastrointestinales. Se desarrolla a partir de dos evaginaciones o brotes del duodeno primitivo: dorsal y ventral. El brote ventral del duodeno primitivo surge de un divertículo hepático, que tiene conexión directa con el conducto biliar común. El conducto que se origina a partir del brote ventral se conoce como ducto de Wirsung. Durante la séptima semana de gestación, el duodeno primitivo gira de derecha a izquierda, y el brote ventral sigue este movimiento de rotación, pasando por detrás del duodeno y fusionándose con el brote dorsal. Esto permite la fusión del conducto ventral (ducto de Wirsung) con el conducto dorsal (ducto de Santorini) en la cabeza del páncreas. El brote ventral origina la parte posterior de la cabeza del páncreas y el proceso uncinado, mientras que la evaginación dorsal origina la parte anterior de la cabeza, el cuerpo y la cola del páncreas4,5. (Fig. 3).
A. El páncreas se desarrolla a partir de dos brotes endodérmicos del duodeno primitivo: dorsal (D) y ventral (V). En la séptima semana de gestación, el duodeno primitivo gira de derecha a izquierda y el brote ventral sigue este movimiento de rotación, pasando por detrás del duodeno y fusionándose con el brote dorsal (B, C y D).
El complejo proceso de la morfogénesis del páncreas explica la existencia de varias malformaciones congénitas pancreáticas en relación con el momento del desarrollo embrionario en el que se produce la alteración. Se pueden clasificar en:
- •
Alteraciones de la proliferación: hipoplasia/agenesia
- •
Alteraciones de la migración (páncreas anular, páncreas ectópico)
- •
Anomalías de la fusión. El páncreas divisum es la más común de todas las malformaciones congénitas pancreáticas. Se trata de un páncreas con dos conductos y orificios de drenaje independientes4.
- •
Variaciones de contornos y forma5.
La agenesia del páncreas ventral y la agenesia total del páncreas son incompatibles con la vida. La agenesia dorsal ocurre cuando hay un desarrollo anormal del brote pancreático dorsal, pero hay un desarrollo normal del brote ventral. La agenesia del páncreas dorsal puede ser completa o parcial6.
En la agenesia dorsal completa, la parte anterior de la cabeza, el cuello, el cuerpo y cola del páncreas, la papila menor y el conducto pancreático accesorio de Santorini están ausentes y el lecho pancreático anterior a la vena esplénica es ocupado por el estómago y asas intestinales. En la agenesia dorsal parcial, una cantidad variable de tejido pancreático está ausente, pero la papila menor está presente junto con un remanente del conducto pancreático accesorio6. En el caso de nuestra paciente, no se demostró conducto accesorio, por lo que se trata de una agenesia dorsal completa.
La ADP parcial ocurre aproximadamente 1-2 cada 10.000 pacientes y se asocia con otras malformaciones congénitas como poliesplenia, bazo ectópico, malrotación intestinal, riñón en herradura, coartación de la aorta, tetralogía de Fallot y defectos del septo ventricular2.
Hay muchos factores que pueden alterar la regulación de la glicemia, determinada por un desequilibrio entre las hormonas hipo e hiperglicemiantes. Múltiples virus pueden ser gatillantes de diabetes tipo 1, sin embargo, el SARS-CoV2, no ha demostrado ser diabetogénico per se. Recientemente, se postula que el SARS-CoV2 puede unirse a un receptor de células beta, produciendo disfunción celular con hiperglicemia aguda. Por lo que, en nuestra paciente, postulamos que el SARS-CoV2 actuó como agente estresante que agotó la exigua dotación de células beta presentes dada la ADP7.
Se ha reportado una posible asociación entre ADP y neoplasias pancreáticas, como tumores quísticos, adenocarcinoma, neoplasia mucinosa papilar intraductal (IPMN) y tumor neuroendocrino8, lo que estaría explicado por una respuesta reparativa anómala del páncreas residual frente a cuadros inflamatorios a repetición. Por ende, se sugiere que todo paciente con diagnóstico de ADP debe ser controlado con imágenes para la detección precoz de tumores malignos9.
El diagnóstico de una malformación pancreática se logra con estudios de imágenes. La mayoría de los pacientes con ADP se descubren incidentalmente en cuadros de dolor abdominal agudo, siendo el ultrasonido el estudio de imagen inicial en la mayoría de los casos. En la ADP, el lecho pancreático distal está ocupado por el estómago o el intestino, que se encuentran en estrecha relación con la vena esplénica. El estómago y las asas intestinales llenos de aire puede interferir con la visualización adecuada de estos segmentos o malinterpretarse como cuerpo y cola del páncreas normal. La adecuada distensión del estómago con líquido puede proporcionar una buena ventana para la mejor visualización del cuerpo y cola pancreáticos. De todas formas, es frecuente que la ecotomografía no aporte información fidedigna sobre el páncreas distal3. La TC y la RM permiten una mejor valoración del páncreas. La TC es útil en el diagnóstico diferencial de malformaciones pancreáticas, pero tiene limitaciones para el estudio detallado de los conductos pancreáticos. Otros hallazgos en la TC, incluyen la cabeza pancreática de mayor tamaño y/o presencia de calcificaciones3–10, tal como en nuestro caso. En la RM las secuencias ponderadas en T2 con saturación de la grasa son mejores que las imágenes ponderadas en T1 para visualizar la presencia de asas intestinales en el lecho pancreático. Las asas colapsadas del intestino delgado en el lecho pancreático distal son isointensas con la cabeza pancreática y pueden malinterpretarse como cuerpo y cola pancreáticos normales en ausencia de un espacio intermedio entre ellas3. La colangio-RM es el estudio de elección para la confirmación de ADP, ya que es una técnica no invasiva que visualiza los conductos pancreáticos sin la inyección de contraste. Su precisión diagnóstica se puede mejorar con la reconstrucción 3D o dinámicamente con inyección de secretina2. La colangiopancreatografía endoscópica retrógrada (ERCP) se considera el gold standard para la evaluación detallada del árbol biliar y pancreático. Sin embargo, es un procedimiento invasivo que conlleva exposición a la radiación y riesgo de morbilidad por pancreatitis por cateterización de las papilas duodenales. La ultrasonografía endoscópica es una técnica de imagen mínimamente invasiva, que proporciona una visualización directa del parénquima pancreático total y del sistema ductal2.
El diagnóstico diferencial de la ADP incluye tumores de la cabeza del páncreas, páncreas divisum, pseudolipo-distrofia pancreática, y lipomatosis pancreática distal2. Es necesario diferenciar la agenesia del páncreas dorsal de la pseudoagenesia del páncreas. Esta última resulta de la atrofia del cuerpo y la cola del páncreas por autodigestión secundaria a pancreatitis crónica o fibrosis quística y puede simular una ADP10. Estas causas de atrofia pancreática fueron descartadas en nuestra paciente, reafirmando lo que orientaban las imágenes, la ausencia congénita del segmento dorsal del páncreas.
ConclusiónLa ADP es una entidad poco frecuente, su conocimiento y correcto diagnóstico es importante, ya que puede ser causa de sintomatología y manifestaciones clínicas variadas. El reconocimiento por el radiólogo permite optimizar el manejo del paciente, evitando otras técnicas y procedimientos diagnósticos. El seguimiento de pacientes con ADP con imágenes, podría aconsejarse para detectar el eventual desarrollo de neoplasias pancreáticas.
Declaración de conflicto de interésLos autores declaran no tener conflictos de intereses.