La reparación valvular mitral es la técnica quirúrgica de elección en el tratamiento de la insuficiencia mitral degenerativa. El objetivo del presente estudio es evaluar los resultados a muy largo plazo de la reparación valvular mitral por prolapso de velo posterior en nuestro centro.
MétodosEstudio retrospectivo de todos los pacientes consecutivos con insuficiencia mitral severa degenerativa por prolapso de velo posterior operados en nuestro centro (2001-2021). Se recogieron las técnicas y los resultados quirúrgicos y el seguimiento clínico y ecocardiográfico.
ResultadosSe intervinieron 260 pacientes (edad media 65,3±12,4años, hombres 67,7%). Se utilizaron exclusivamente técnicas resectivas en 185 pacientes (71,2%), neocuerdas en 53 (20,4%) y otras técnicas en 15 (5,8%). La tasa de reparabilidad fue del 97,3%. En 45 pacientes (17,3%) se realizó una anuloplastia tricuspídea. La mortalidad hospitalaria fue del 1,5%. El seguimiento medio fue de 6,6±5años (0-20). La tasa libre de mortalidad fue del 51,3% a los 20años, con una edad media de los pacientes en el momento de la muerte de 82,1±7,2años. Las tasas libres de recidiva de insuficiencia mitral grado ≥II y reintervención de la insuficiencia mitral fueron, respectivamente, del 59,2% y del 97,7% a los 20años. Se observaron menores tasas libres de recidiva de insuficiencia mitral ≥II y reintervención de la insuficiencia mitral en la reparación con neocuerdas respecto a las técnicas resectivas (p=0,001 y p=0,002, respectivamente).
ConclusionesLos resultados a largo plazo de la reparación mitral del prolapso de velo posterior en nuestro centro han sido excelentes. Las técnicas resectivas parecen relacionarse con una mayor durabilidad a largo plazo.
Mitral valve repair is the gold standard treatment of degenerative mitral regurgitation. The objective of this study is to evaluate the very long-term results of mitral valve repair for posterior leaflet prolapse in our center.
MethodsRetrospective study of all consecutive patients with severe degenerative mitral regurgitation due to posterior leaflet prolapse operated in our center (2001-2021). Surgical techniques and results, and clinical and echocardiographic follow-up were recorded.
ResultsA total of 260 patients were operated (mean age 65.3±12.4 years, men 67.7%). Isolated resection techniques were used in 185 patients (71.2%), neochords in 53 (20.4%) and other techniques in 15 (5.8%). Successful repair rate was 97.3%. Tricuspid annuloplasty was performed in 45 patients (17.3%). Hospital mortality was 1.5%. The mean follow-up was 6.6±5years (0-20). Actuarial survival was 51.3% at 20years, with a mean age of the patients at the time of death of 82.1±7.2years. The freedom of recurrent grade ≥II mitral regurgitation and reoperation at 20years were 59.2% and 97.7% respectively. Worse freedom of recurrent mitral regurgitation and reoperation were observed in the neochord repair compared to resection techniques (P=.001 and P=.002, respectively).
ConclusionsLong-term results of mitral valve repair of posterior leaflet prolapse in our center have been excellent. Resective techniques seem to be related with greater long-term durability than neochord implantation.
En la insuficiencia mitral (IM) degenerativa se producen cambios morfológicos en el tejido conectivo de la válvula mitral que afectan en diversos grados a la estructura anatómica de los velos y causan elongación o rotura de cuerdas tendinosas, provocando prolapso valvular, regurgitación mitral y grados variables de dilatación del anillo mitral1.
El prolapso de velo posterior (PVP) es la causa más frecuente de IM degenerativa, siendo la reparación valvular mitral (RVM) la técnica quirúrgica de elección2,3. En comparación con la sustitución protésica, la RVM presenta menor tasa de mortalidad quirúrgica y mejores tasas de supervivencia y función ventricular izquierda en el seguimiento4-6. Las técnicas de reparación publicadas por Carpentier han demostrado una gran efectividad, reproducibilidad y durabilidad7,8.
El objetivo del presente estudio es evaluar los resultados a muy largo plazo de la RVM por PVP en nuestro centro.
MétodosObjetivos del estudioEl objetivo primario del estudio fue la evaluación de la mortalidad tardía. Los objetivos secundarios fueron la evaluación de la tasa libre de reintervención de la IM y de la tasa libre de recidiva de la IM, considerada como la ausencia de IM grado ≥II después de la cirugía.
Diseño del estudioSe realizó un estudio retrospectivo de todos los pacientes intervenidos de manera consecutiva en nuestro centro por IM degenerativa entre enero de 2001 y julio de 2021.
De los 426 pacientes con IM degenerativa intervenidos durante este periodo, 307 presentaban PVP aislado. Se excluyeron los enfermos con severa calcificación del anillo mitral que afectaba de forma determinante a la técnica quirúrgica y aquellos con cirugía asociada diferente de anuloplastia tricuspídea, obteniendo una muestra final de 260 pacientes.
SeguimientoLos datos se obtuvieron de la base de datos propia del servicio de cirugía cardíaca, así como de la historia clínica digitalizada del Sistema Catalán de Salud. En algunos casos, se completó el seguimiento mediante contacto telefónico.
Técnica quirúrgicaEl abordaje quirúrgico fue por esternotomía media hasta el año 2016. El tipo de protección miocárdica ha ido evolucionando a lo largo de los años, desde la cardioplejía sanguínea intermitente hasta soluciones cristaloides de dosis única, junto con hipotermia moderada al principio, hasta la normotermia actualmente. La exposición valvular se realizó por atriotomía izquierda o transeptal, dependiendo de la anatomía cardíaca y de la actuación sobre la válvula tricúspide. En el año 2016 se inició el programa de cirugía mínimamente invasiva con abordaje por minitoracotomía derecha por 4.° espacio intercostal y con canulación femoral. En estos casos se utilizó cardioplejía de tipo Custodiol, hipotermia ligera y atriotomía izquierda para la exposición valvular. Desde 2021 se utilizó videotoracoscopia 3D para la RVM.
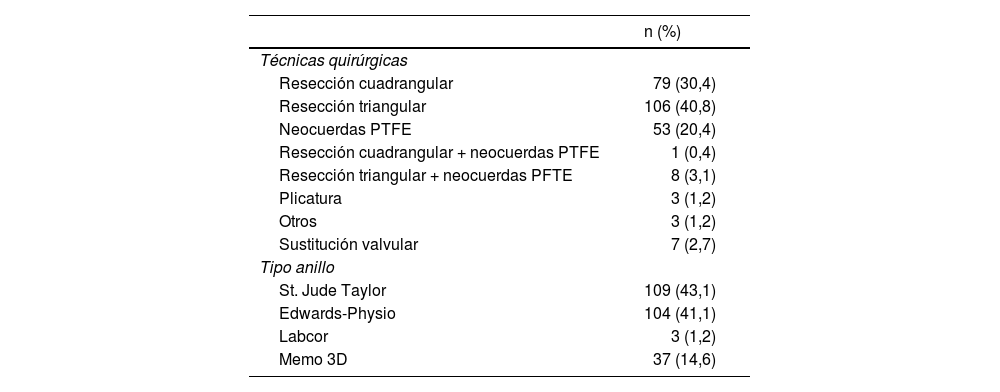
Una vez expuesta la válvula mitral, se procedió al análisis valvular, a la detección de áreas con prolapso valvular y a la reparación de estas con diferentes técnicas (tabla 1) ya descritas en la literatura8-11. En los primeros años se utilizaron fundamentalmente las técnicas clásicas de Carpentier y posteriormente se fueron introduciendo técnicas que disminuían la resección del tejido y evitaban la plicatura del anillo para no deformar la base del ventrículo, mantener su geometría y no distorsionar la arteria circunfleja en su recorrido. Por ello se fue reduciendo de forma progresiva la amplitud de la resección, y en ocasiones complementando la reparación con neocuerdas de politetrafluoroetileno (PTFE) CV-4 (WL Gore & Associates Inc, Flagstaff, Arizona EE.UU.), para finalmente utilizar, en determinados pacientes, neocuerdas asociadas a anuloplastia mitral como única técnica de reparación.
Técnicas quirúrgicas
| n (%) | |
|---|---|
| Técnicas quirúrgicas | |
| Resección cuadrangular | 79 (30,4) |
| Resección triangular | 106 (40,8) |
| Neocuerdas PTFE | 53 (20,4) |
| Resección cuadrangular + neocuerdas PTFE | 1 (0,4) |
| Resección triangular + neocuerdas PFTE | 8 (3,1) |
| Plicatura | 3 (1,2) |
| Otros | 3 (1,2) |
| Sustitución valvular | 7 (2,7) |
| Tipo anillo | |
| St. Jude Taylor | 109 (43,1) |
| Edwards-Physio | 104 (41,1) |
| Labcor | 3 (1,2) |
| Memo 3D | 37 (14,6) |
En todos los pacientes se utilizó una anuloplastia con anillo flexible abierto o semirrígido cerrado dependiendo, inicialmente, de la disponibilidad del dispositivo y, posteriormente, de las preferencias de los cirujanos.
En todas las cirugías se evaluó la RVM mediante ecocardiografía transesofágica (ETE) tras finalizar la circulación extracorpórea. La severidad de la IM fue definida según las guías de valoración ecocardiográfica de la insuficiencia valvular vigentes12-14. Se consideró como buen resultado de la cirugía la ausencia de IM o la IM residual gradoI.
Características de los pacientesLos datos preoperatorios incluyeron sexo, edad, EuroScoreII, clase funcional de la NYHA, hábito tabáquico, obesidad, hipertensión, dislipemia, diabetes, fibrilación auricular, ictus, arteriopatía periférica, insuficiencia renal y EPOC (tabla 2). Las ecocardiografías preoperatorias fueron realizadas por la Unidad de Imagen Cardíaca del hospital.
Características clínicas preoperatorias
| Edad | 65,3 ± 12,4 años |
| Género, hombres | 176 (67,7) |
| Tabaquismo | 23 (8,9) |
| Hipertensión arterial | 116 (44,6) |
| Dislipemia | 95 (36,6) |
| Diabetes mellitus | 25 (9,6) |
| Arteriopatía periférica | 4 (1,5) |
| Ictus | 12 (4,6) |
| Obesidad | 16 (6,2) |
| Insuficiencia renal | 13 (5,0) |
| Fibrilación auricular | 73 (28,1) |
| EPOC | 19 (7,3) |
| EuroScore II | 2,2 (rango 0,5-18) |
| Clase funcional de la NYHAIIIIIIIV | 25 (9,6)107 (41,2)106 (40,8)22 (8,5) |
Datos presentados como n (%) o media ± desviación estándar.
Las variables cuantitativas se describieron mediante la media y la desviación estándar o la mediana y el rango en función de la distribución de la variable. Se analizó el índice de curtosis para determinar la distribución normal de las variables continuas, considerando que a partir de un índice de curtosis >2 o <−2 la distribución no era normal. Las variables cualitativas se describieron mediante frecuencia y porcentaje. Se analizó la mortalidad global desglosada en mortalidad perioperatoria (mortalidad hospitalaria) y postoperatoria a largo plazo (mortalidad tardía), la tasa libre de reintervención y la tasa libre de recidiva de la IM ≥II. La prueba de t de Student para muestras apareadas se utilizó para comparar los resultados ecocardiográficos precirugía y al final del seguimiento. El análisis de la supervivencia y de las tasas libres de reintervención y recidiva de la IM se realizaron mediante el método de Kaplan-Meier. Las curvas de Kaplan-Meier de los subgrupos de técnicas resectivas y neocuerdas se compararon mediante la prueba de log rank. Los datos fueron analizados con el programa SPSSS 25.0 Statistical Package (SPSS Inc, Chicago, IL, EE.UU.).
Consideraciones éticasTras consultar con el Comité de Ética de Investigación del centro, este consideró que, al tratarse de un trabajo asistencial de carácter retrospectivo, no era precisa su autorización. Todos los pacientes fueron informados sobre los riesgos y las posibles complicaciones de la cirugía y firmaron el consentimiento informado.
ResultadosDurante el periodo estudiado se intervinieron 260 pacientes con PVP mediante técnicas de RVM. El 67,7% de los pacientes eran hombres y la edad media fue de 65,3±12,4años. Las características clínicas preoperatorias se resumen en la tabla 2.
Resultados intrahospitalariosTécnica quirúrgicaDoscientos dieciocho pacientes (83,8%) fueron intervenidos mediante esternotomía media completa y 42 (16,2%) mediante minitoracotomía derecha. En 45 pacientes (17,3%) se asoció anuloplastia tricuspídea.
Las técnicas quirúrgicas empleadas para la RVM se resumen en la tabla 1. La técnica más utilizada fue la resección triangular en 106 pacientes (40,8%), seguida de la resección cuadrangular en 79 pacientes (30,4%) y la implantación aislada de neocuerdas en 53 pacientes (20,4%). En 9 pacientes (3,5%) se combinaron técnicas resectivas con implantación de neocuerdas. Solo 7 pacientes (2,7%) requirieron una sustitución valvular mitral, lo que conllevó una tasa de reparabilidad del 97,3%.
En 109 pacientes (43,1%) se implantó un anillo SJM Tailor (St. Jude Medical, Inc. Minnesota, EE.UU.), en 104 pacientes (41,1%), un anillo Edwards Physio (Edwards Lifesciences LLC, Irvine, CA, EE.UU.) y en 37 pacientes (14,6%) se utilizó un anillo Sorin Memo 3D (Sorin Biomedica Cardio S.R.L., Saluggia, Italia). El tamaño medio de los anillos empleados fue de 31,2±2,8mm (rango 36-40).
En pacientes intervenidos mediante esternotomía media completa, el tiempo de circulación extracorpórea (CEC) fue de 105±33 minutos y el de isquemia, de 82±25 minutos. En pacientes intervenidos mediante minitoracotomía el tiempo de CEC fue de 152±29 minutos y el de isquemia, de 106±23 minutos.
Resultados ecocardiográficosEn la valoración ecocardiográfica intraoperatoria, 5 pacientes (1,9%) presentaron una IM residual en el ETE intraoperatorio de gradoII. No obstante, en estos enfermos se consideró que el resultado era adecuado por tratarse de una IM de tipo central, sin áreas de prolapso residual y con una superficie de coaptación amplia.
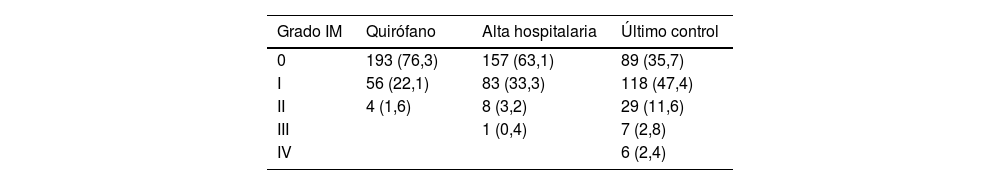
En la valoración ecocardiográfica prealta, 240 pacientes (96,4%) presentaban IM grado 0-I, 8 pacientes (3,2%), IMII, y 1paciente, IMIII (0,4%) (tabla 3).
Mortalidad intrahospitalariaLa mortalidad durante el ingreso hospitalario fue del 1,5% (4 pacientes). Las causas de muerte fueron: mediastinitis (en un paciente con obesidad mórbida), neumonía (en dos pacientes con comorbilidad respiratoria severa) e insuficiencia cardíaca biventricular (en un paciente con disfunción ventricular izquierda severa preoperatoria).
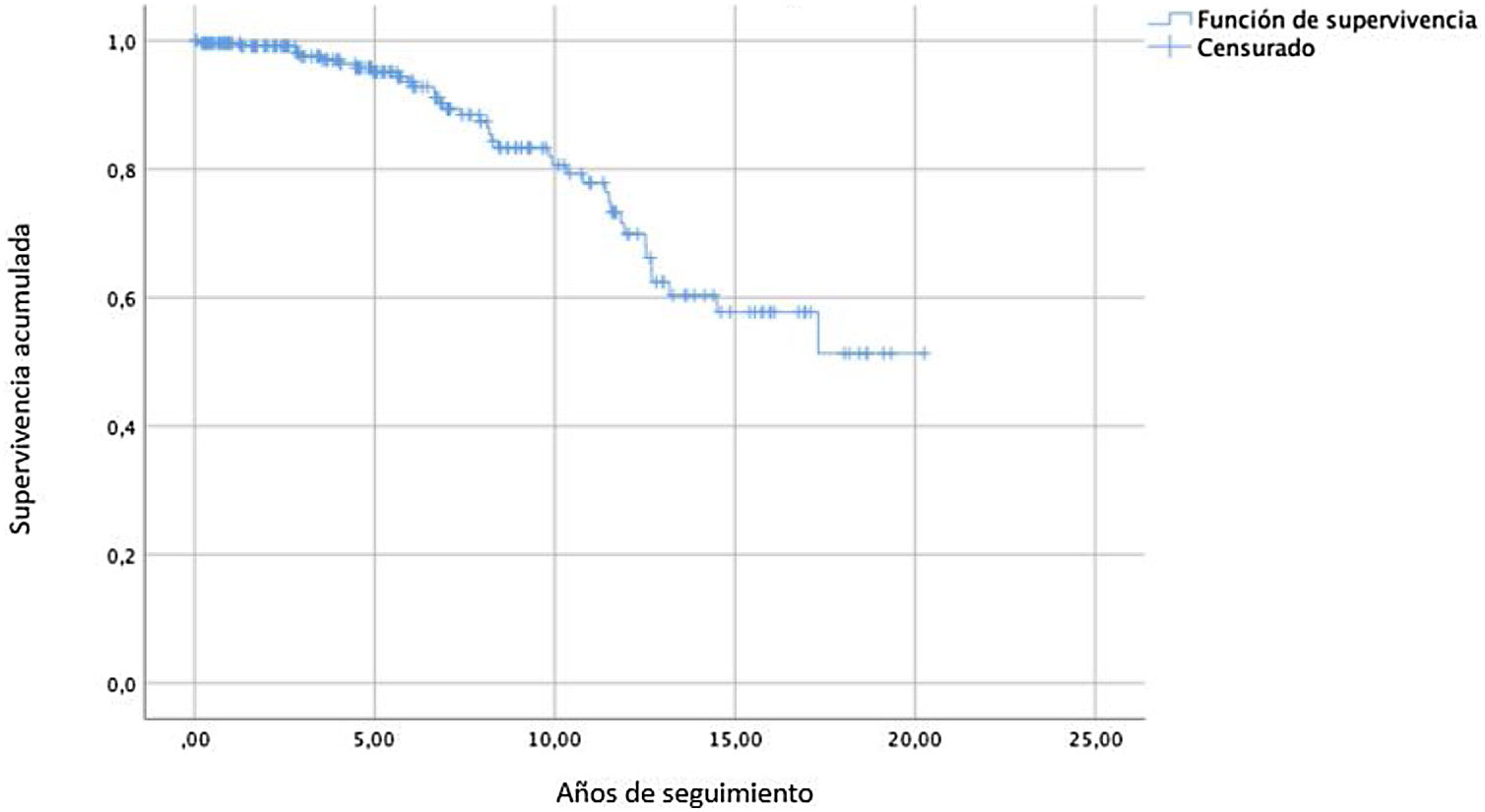
Resultados a largo plazoMortalidad tardíaEl seguimiento medio fue de 6,6±5años (rango 0-20). La pérdida de seguimiento fue de 6 pacientes. Las tasas libres de mortalidad observadas a los 10 y 20años fueron del 80,7% (IC95%: 79,5-81,9) y del 51,3% (IC95%: 50,1-52,5), respectivamente (fig. 1). La mortalidad tardía fue de 38 pacientes: 9 (23,7%) de origen cardiovascular, 25 (65,8%) de otras causas y 4 (10,5%) de motivo desconocido. Las causas de muerte cardiovascular fueron insuficiencia cardíaca en 4 enfermos (3 por disfunción ventricular izquierda y 1 por recidiva de la IM), 2 hemorragias relacionadas con la anticoagulación, 1 ictus y 2 muertes súbitas. La edad media de estos pacientes en el momento de la muerte fue de 82,1±7,2años. Solamente uno de ellos presentaba recidiva de la IM: se trataba de un paciente al que se le había practicado una resección cuadrangular y que desarrolló IMIV a los 13años de seguimiento.
Tasas libres de recidiva y reintervención de la insuficiencia mitralEl tiempo medio de seguimiento hasta el último control ecocardiográfico fue de 5,3±4,5años.
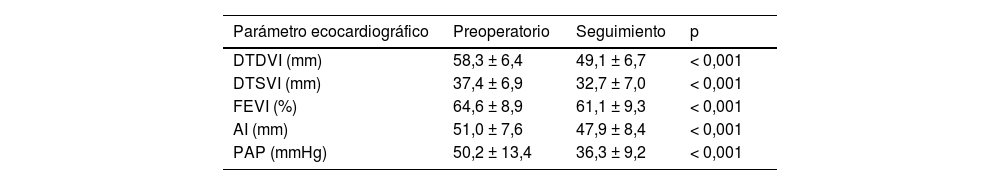
La tabla 4 muestra la comparación de los parámetros ecocardiográficos prequirúrgicos y al final del seguimiento. Se observó una disminución significativa de los diámetros y de la fracción de eyección del ventrículo izquierdo, del diámetro de la aurícula izquierda, así como de la hipertensión pulmonar (p<0,001).
Comparación evolutiva de los parámetros ecocardiográficos prequirúrgicos y al final del seguimiento
| Parámetro ecocardiográfico | Preoperatorio | Seguimiento | p |
|---|---|---|---|
| DTDVI (mm) | 58,3 ± 6,4 | 49,1 ± 6,7 | < 0,001 |
| DTSVI (mm) | 37,4 ± 6,9 | 32,7 ± 7,0 | < 0,001 |
| FEVI (%) | 64,6 ± 8,9 | 61,1 ± 9,3 | < 0,001 |
| AI (mm) | 51,0 ± 7,6 | 47,9 ± 8,4 | < 0,001 |
| PAP (mmHg) | 50,2 ± 13,4 | 36,3 ± 9,2 | < 0,001 |
DTDVI: diámetro telediastólico ventrículo izquierdo; DTSVI: diámetro telesistólico ventrículo izquierdo; FEVI: fracción de eyección del ventrículo izquierdo; PAP: presión arterial pulmonar sistólica; AI: diámetro de la aurícula izquierda.
Los datos se expresan en media ± desviación estándar.
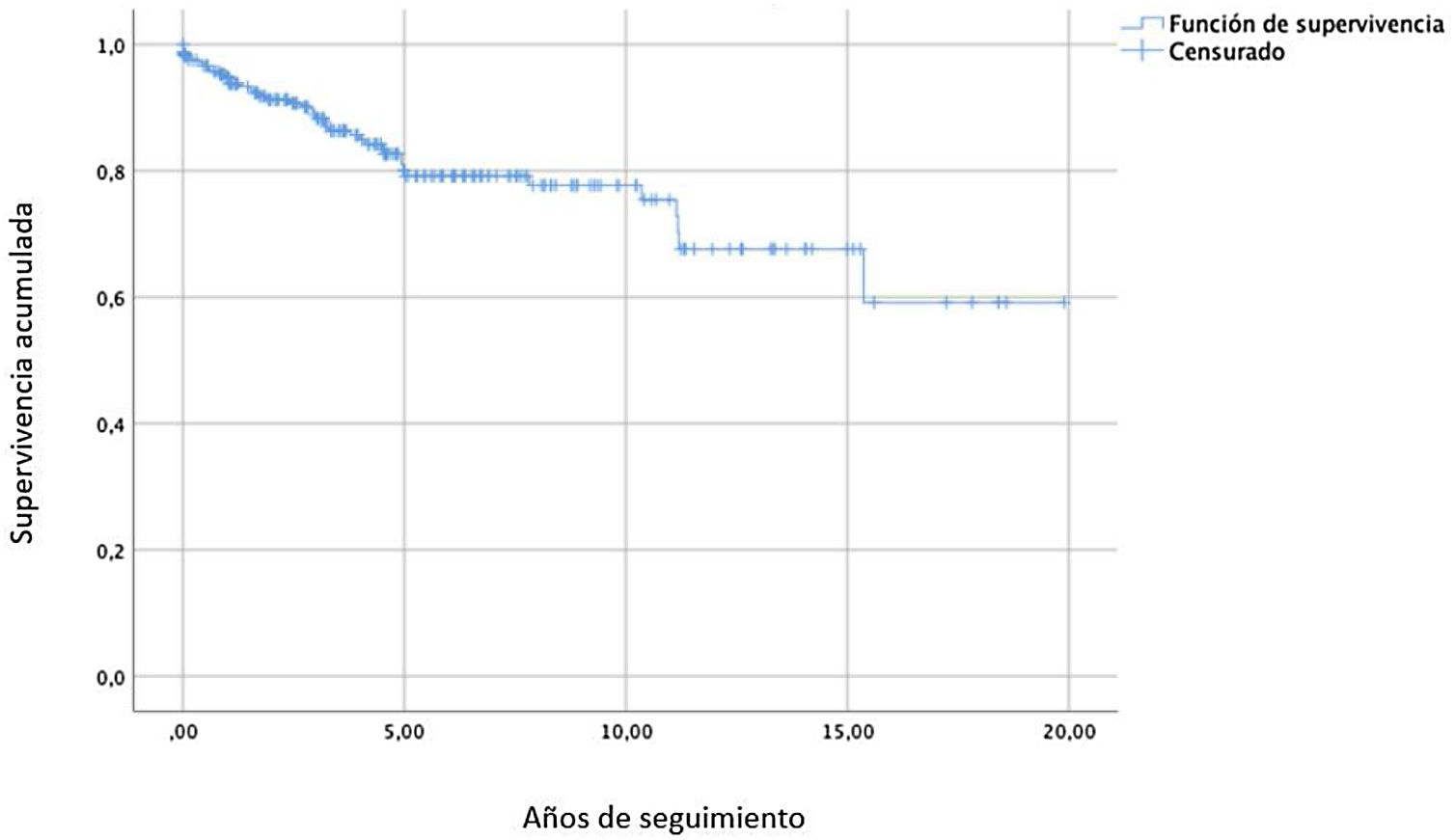
La evolución de la IM tras la RVM se recoge en la tabla 3. Los pacientes con IM0-I en el momento del alta hospitalaria eran 240 (96,4%), mientras que al final del seguimiento solo eran 207 (83,1%). La presencia de IM ≥II también se incrementó de 9 pacientes (3,6%) en el momento del alta, a 42 pacientes (16,6%) al final del seguimiento. El análisis de supervivencia libre de recidiva se muestra en la figura 2. La tasa libre de recidiva de la IM fue del 77,7% (IC95%: 76,3-79,1) y del 59,2% (IC95%: 57,8-60,6) a los 10 y a los 20años de seguimiento, respectivamente.
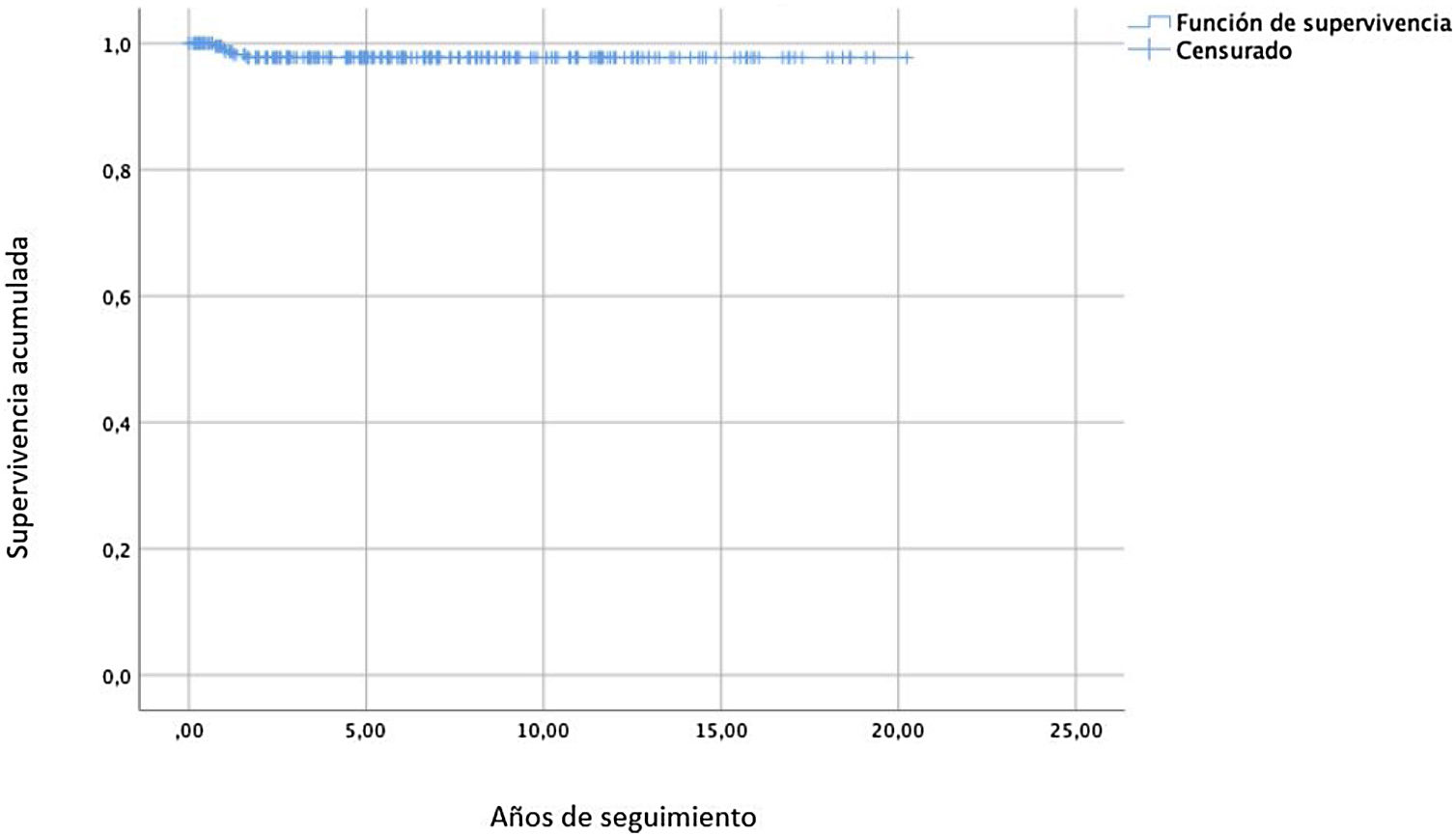
Cinco pacientes requirieron reintervención por fallo de plastia, representando una tasa de reintervención del 2,0%. La mediana del tiempo entre la cirugía y el momento de la reintervención fue de 1,3meses (rango 0-19). La figura 3 muestra el análisis de supervivencia libre de reintervención, que fue del 97,7% (IC95%: 97,3-98,1) a los 10 y a los 20años de seguimiento.
En los análisis de supervivencia libre de recidiva y necesidad de reintervención se observó una diferente evolución según la técnica empleada.
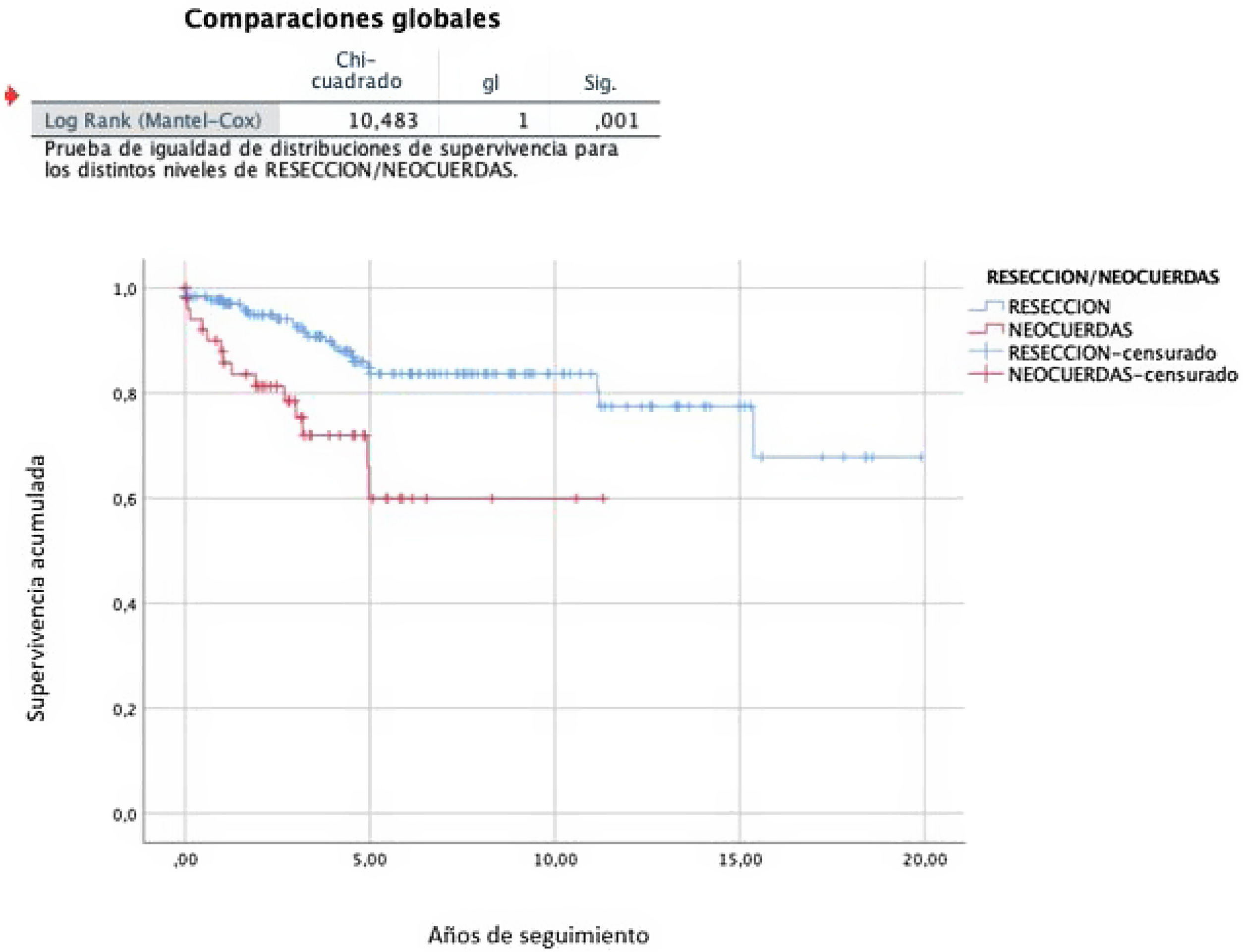
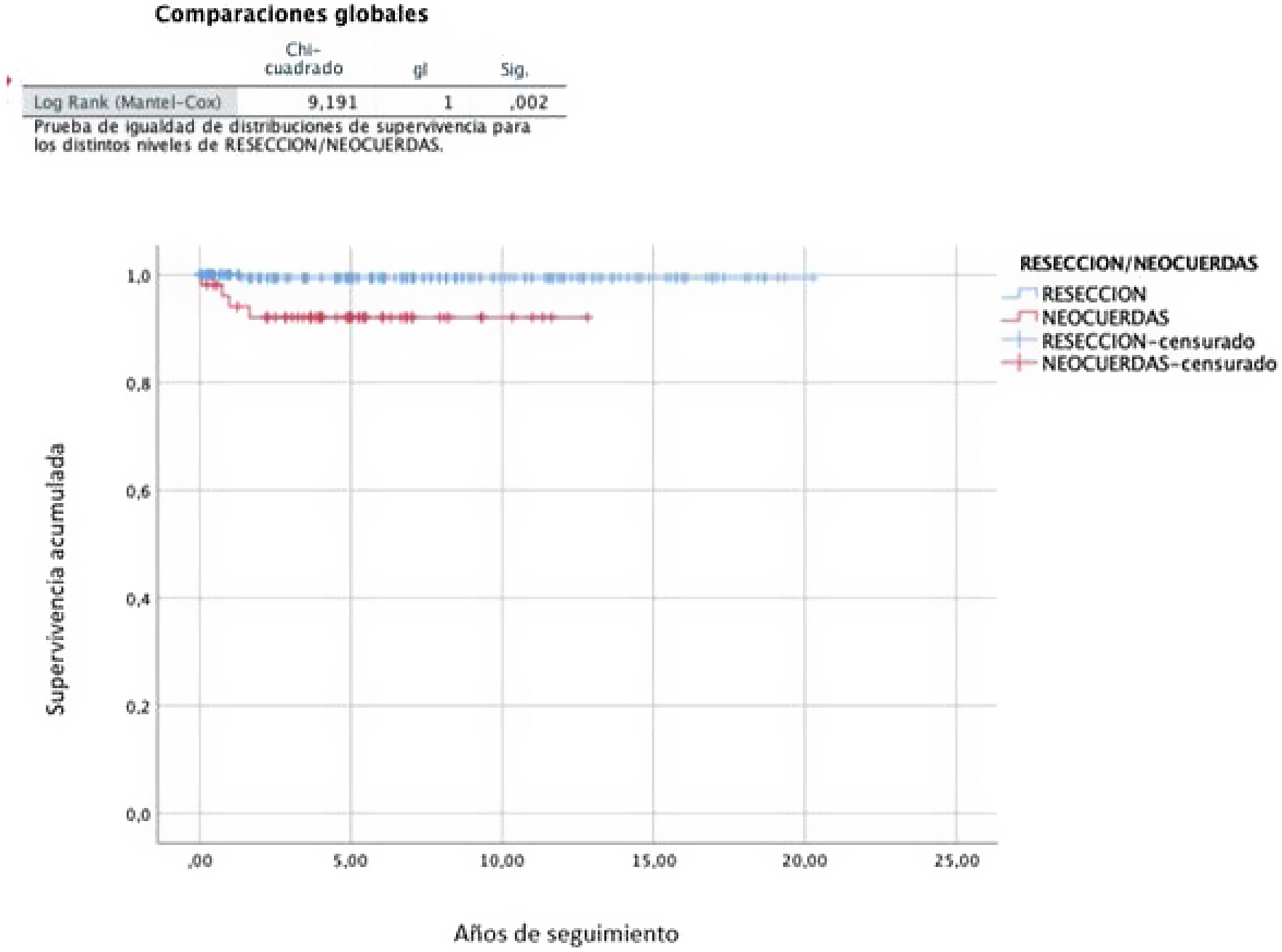
En las RVM realizadas con técnicas resectivas, la tasa libre de recidiva a los 10 y a los 20 años fue del 83,7% (IC95%: 82,2-85,2) y del 67,8% (IC95%: 66,3-69,3), respectivamente, mientras que en el caso del uso de neocuerdas fue del 59,9% (IC95%: 58,4-61,4) a los 10años (p=0,001) (fig. 4). La tasa libre de reintervención a los 10años fue del 99,4% (IC95%: 99,2-99,6) en las RVM realizadas con técnicas resectivas y del 92,1% (91,2-93,0) en las reparaciones con neocuerdas (p=0,002) (fig. 5).
Los resultados de nuestro estudio muestran que la RVM es una técnica segura en pacientes con IM degenerativa con PVP, obteniendo una mortalidad hospitalaria del 1,5%, inferior a la esperada según EuroScoreII.
Respecto a las técnicas quirúrgicas, el uso de neocuerdas de PTFE ha sido menor que el de las técnicas resectivas, dado que se introdujeron en nuestro servicio en el año 2008, tras la experiencia publicada por Perier et al.10. Siguiendo la tendencia general del resto de grupos, en los últimos años hemos priorizado cada vez más la preservación del tejido de los velos frente a la resección con el fin de lograr una reparación más fisiológica10. De esta forma, se ha abandonado progresivamente la resección cuadrangular, reduciendo la extensión de las resecciones triangulares y complementándolas con neocuerdas o directamente usándolas como técnica de reparación aislada.
En cuanto al tipo de anillo implantado, se ha evolucionado desde el uso de anillos abiertos hasta la implantación actual únicamente de anillos cerrados. Aunque en la enfermedad degenerativa se dilata fundamentalmente el anillo posterior15, el control de la distancia anteroposterior contribuye a mantener una correcta superficie de coaptación de los velos, pudiendo favorecer la durabilidad de la reparación a largo plazo16.
Comparando los parámetros ecocardiográficos prequirúrgicos y al final del seguimiento, se observa una disminución significativa de los diámetros del ventrículo izquierdo y de la aurícula izquierda, así como de la hipertensión pulmonar. También se objetiva una disminución significativa de la fracción de eyección del ventrículo izquierdo después de la cirugía que es atribuible a diferentes causas17,18. Los cambios volumétricos intracardíacos tras la RVM, como son la disminución del volumen telediastólico y el consiguiente aumento de la poscarga ventricular, conllevan un empeoramiento del acoplamiento ventrículo-arterial19. Por otro lado, la afectación directa de la contractilidad miocárdica por la fibrosis intersticial generada por la propia IM puede estar enmascarada por las condiciones de carga prequirúrgicas20,21. Por último, el daño miocárdico por isquemia-reperfusión provocado por el pinzamiento aórtico y la circulación extracorpórea también puede contribuir a la disminución de la fracción de eyección del ventrículo izquierdo después de la cirugía22.
En concordancia con los resultados publicados8,23-26, nuestro estudio demuestra que la RVM ofrece una excelente supervivencia a muy largo plazo, en nuestro caso del 51,3% a los 20años. La edad media de los pacientes en el momento del fallecimiento fue de 82,1±7,2años, similar a la esperanza de vida media en la población española27. Además, de los pacientes fallecidos por causa cardiovascular, solo uno presentaba un grado de IM ≥II en el último control ecocardiográfico, y falleció a los 90años, superando la esperanza de vida media de la población de nuestro país.
En relación con la durabilidad de la RVM, las tasas libres de recidiva de la IM fueron del 77,7% a los 10años y del 59,2% a los 20años. Estos resultados se aproximan a los descritos por autores de referencia en la RVM procedentes de hospitales con gran casuística. David et al.28 y Javadikasgari et al.29 obtienen una tasa libre de recidiva de la IM del 80% a los 12años y del 85,9% a los 10años, respectivamente. Salvador et al.30 presentan incluso mejores resultados, mostrando una tasa libre de recidiva de la IM del 85% a los 15años. Hay que puntualizar que definen la recidiva de la IM como IM significativa (gradosIII yIV) y que asociaron neocuerdas en todos los pacientes. Además, en sus resultados incluyen la RVM de velo anterior, pero en el análisis de regresión de Cox, esta no se observa como un factor independiente para la recidiva de IM30.
Nuestros resultados denotan un lento pero progresivo deterioro de la válvula, condicionado por la persistencia de la enfermedad degenerativa31,32. A pesar de este progresivo deterioro valvular, la tasa libre de reintervención a los 20años fue del 97,7%. Únicamente se reintervinieron a 5 pacientes de entre los 13 que estaban con IMIII-IV en el último seguimiento ecocardiográfico, dado que el resto estaban asintomáticos y no tenían repercusión sobre el ventrículo izquierdo, o por considerarse pacientes no tributarios de cirugía por edad muy avanzada y fragilidad.
Muchos autores reportan tasas libres de reintervención de la IM ligeramente inferiores, posiblemente por incluir pacientes con prolapso de velo anterior, el cual ha demostrado presentar peores resultados tras la reparación24-26,32,33. De entre los autores que analizan la RVM de velo posterior aislado, David et al.28 y Javadikasgari et al.29 presentan una tasa libre de reintervención de la IM del 96% a los 12años y del 93,7% a los 18años, respectivamente. Brescia et al.34 describen una tasa linealizada de reintervención del 0,48% por paciente-año para RVM del velo posterior.
Se observa una mayor tasa de recidiva de la IM y mayor tasa de reintervención en la reparación con neocuerdas respecto a las técnicas resectivas. A pesar de que la implantación de neocuerdas está ampliamente difundida y su eficacia y durabilidad demostrada11,35-37, el gran número de técnicas descritas para la medición de la longitud de las mismas sugiere que es una técnica menos reproducible y que requiere una curva de aprendizaje más larga. Suri et al.25 describen la ausencia de técnicas resectivas como un factor de riesgo para la recidiva de IM, juntamente con la edad, la IM residual intraoperatoria, el prolapso de velo anterior o de ambos velos, el tiempo de isquemia superior a 90minutos y la ausencia de anuloplastia. También mencionan que algunos pacientes reintervenidos tras una RVM con neocuerdas fallida presentan desgarro del velo mitral por la propia cuerda, especialmente cuando la calidad del tejido es pobre, sugiriendo este mecanismo como posible causa de recidiva de IM en la reparación por neocuerdas.
Limitaciones del estudioA pesar de que se trata de un estudio realizado en un único centro, recoge la experiencia quirúrgica de cirujanos diferentes, en distintos momentos de su curva de aprendizaje y mediante abordajes diferentes, lo que podría influir de forma significativa en los resultados. Aun así, seguramente refleja la variabilidad habitual en la práctica de la cirugía cardíaca en nuestro país. Por otra parte, las ecocardiografías preoperatorias, intraoperatorias y al alta fueron realizadas únicamente por cardiólogos expertos en imagen cardíaca de nuestro hospital, referente en valvulopatías, pero las ecocardiografías en el seguimiento se realizaron en los hospitales de referencia de cada paciente, siendo evaluadas por cardiólogos generalistas, a veces sin formación específica en valvulopatías. Finalmente, este estudio presenta las limitaciones de los estudios con diseño retrospectivo, como el sesgo de selección y, especialmente en este caso, la potencial falta de calidad de los datos recogidos de los registros de pacientes.
ConclusionesLos resultados de nuestro estudio muestran que la reparación valvular de velo posterior mitral es una técnica segura y que ofrece una excelente supervivencia a muy largo plazo. A pesar de que la insuficiencia mitral después de la reparación presenta una lenta progresión, la tasa libre de reintervención a largo plazo es muy elevada. Las técnicas resectivas parecen relacionarse con una mayor durabilidad a largo plazo.
FinanciaciónLos autores no recibieron ningún tipo de financiación para la realización de este artículo.
Conflicto de interesesLos autores declaran no tener ningún conflicto de intereses.