Las angiodisplasias constituyen la malformación vascular más común del tracto digestivo, distribuyéndose de forma difusa en la mucosa y submucosa intestinal. Causan anemia crónica o sangrado digestivo en el 10% de los pacientes. Esta enfermedad afecta, sobre todo, en edad avanzada, con una probabilidad de recidiva tras el primer episodio de sangrado de hasta el 50%. A menudo el gran número y la localización de las lesiones dificulta su acceso y erradicación1, considerando el tratamiento endoscópico con gas argón plasma de elección. El abordaje mediante arteriografía y/o cirugía se reserva en casos de hemorragias graves2.
Cuando fracasa o en combinación con el tratamiento endoscópico se han probado distintas alternativas farmacológicas, desde la asociación de estrógenos y progestágenos, pasando por el uso de la talidomida y los análogos de la somatostatina3. El tratamiento hormonal no ha demostrado beneficio a largo plazo4. En cuanto a los análogos de la somatostatina, el octreótido es el principio activo más utilizado en la práctica clínica2,5,6. Otro de los análogos utilizados, ha sido el lanreótido.
En el primer estudio sobre el uso de octreótido se concluyó la seguridad y el éxito en el control de la hemorragia gastrointestinal recurrente debido a angiodisplasia en pacientes de edad avanzada no subsidiaria de tratamiento endoscópico o quirúrgico. Sin embargo, la recurrencia de sangrado en los pacientes tratados con octreótido alcanza hasta el 20%, apareciendo hasta en un 53% de los casos algún efecto adverso.
El lanreótido es una hormona sintética análoga de la somatostatina, que entre otras acciones inhibe los aumentos de flujo de la arteria mesentérica superior y el flujo sanguíneo venoso portal inducidos por la ingestión de alimentos. El lanreótido autogel es una preparación del análogo en una base acuosa que permite su administración subcutánea. Su perfil de seguridad es muy parecido al del octreótido subcutáneo. Las reacciones adversas descritas son básicamente de naturaleza gastrointestinal y aparecen con una frecuencia aproximada del 30%, siendo leves y transitorias.
En nuestro centro están siendo tratados con lanreótido autogel 4 pacientes diagnosticados de angiodisplasias gastrointestinales.
A continuación presentamos los 2 casos con mayor tiempo de seguimiento tras inicio de la terapia con lanreótido:
Caso 1Mujer de 94 años de edad con hemorragia por angiodisplasias gástricas y yeyunales, en la que se inició tratamiento con octreótido LAR y fulguración con argón de las lesiones gástricas. Posteriormente presentó 2 ingresos hospitalarios por hemorragia digestiva grave (hemoglobina de 5g/dl). Entre los ingresos y el seguimiento ambulatorio, precisó ferroterapia intravenosa en una ocasión, y la transfusión de 12 concentrados de hematíes. Dado que el tratamiento no fue efectivo, se cambió el tipo de análogo por lanreótido autogel y en los 10 meses posteriores no ha presentado episodios de melenas, ni ha requerido transfusión sanguínea ni fulguraciones endoscópicas, siendo actualmente los valores de hemoglobina normales.
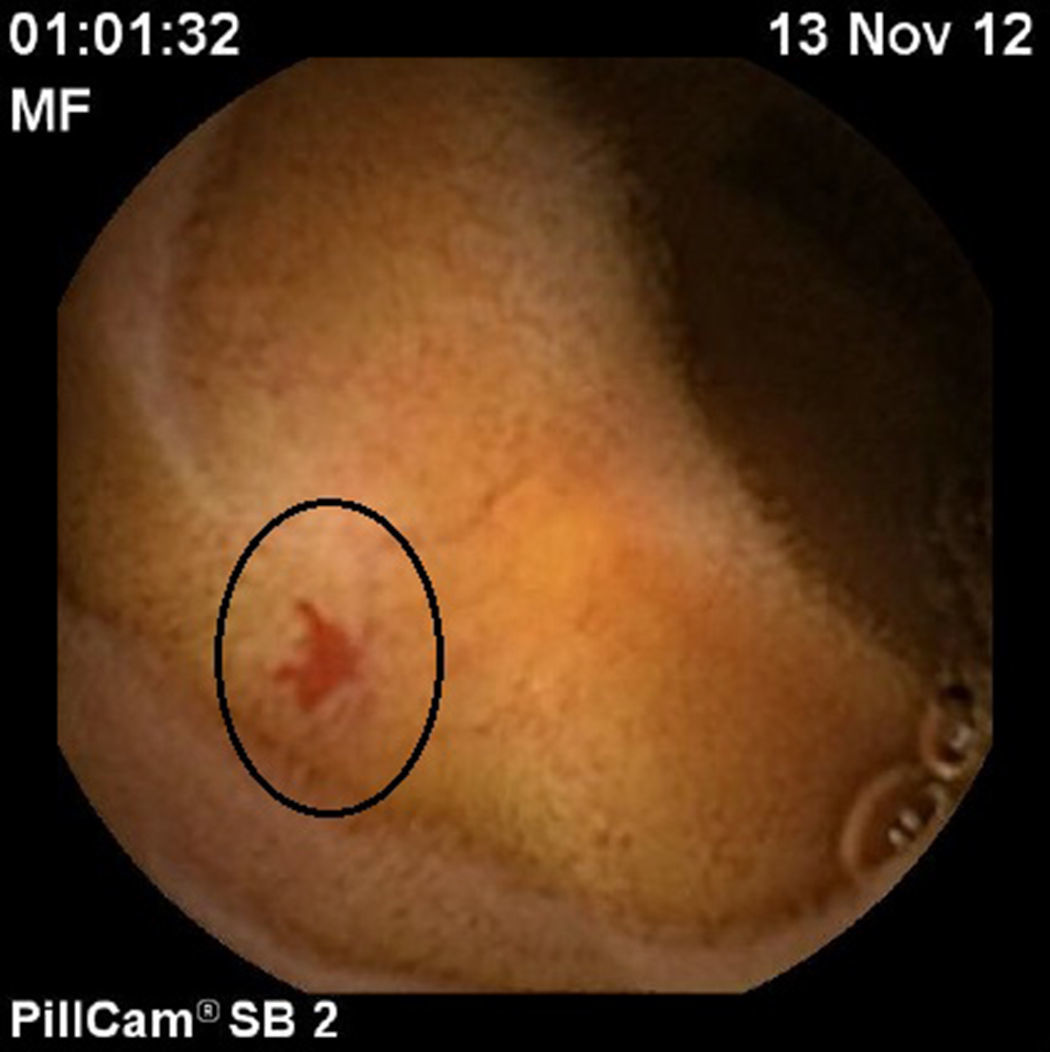
Caso 2Mujer de 84 años, diagnosticada de angiodisplasias yeyunoileales (fig. 1), que durante el tratamiento con octreótido LAR presentó 2 ingresos por melenas, transfusión de 3 concentrados de hematíes y la infusión intravenosa de hierro en varias ocasiones. Sin embargo, en los 10 meses posteriores al cambio a lanreótido la paciente no ha vuelto a presentar signos de sangrado digestivo, necesidad de transfusión sanguínea ni ferroterapia y se han normalizado sus cifras de hemoglobina.
Las dosis de fármaco utilizadas fueron de octreótido 20mg, con una periodicidad mensual y de lanreótido autogel 120mg cada 6 semanas.
En los otros 2 casos, el tiempo transcurrido desde el inicio de lanreótido es de 5 y 6 meses respectivamente, manteniendo cifras normales de hemoglobina.
La evidencia científica sobre la utilidad del tratamiento de las angiodisplasias con análogos de somatostatina se basa en estudios con pequeño número de pacientes. En la mayoría de ellos se empleó octreótido y en los que se utilizó indistintamente octreótido o lanreótido no se explica si hubo diferencias en la respuesta entre ambos. Tampoco la dosis y la pauta de administración están bien definidas.
Asimismo resaltar que no existen referencias que valoren la utilidad del cambio de un análogo por otro.
Los casos referidos, apoyan la eficacia del cambio de octreótido por lanreótido en los pacientes que el primero no es eficaz o ha perdido su eficacia. Estos hallazgos deben ser demostrados por estudios con mayor número de casos y mayor evidencia científica. Además, cabe destacar, que en los pacientes anticoagulados, la administración del octreótido intramuscular implica mayor riesgo de hematomas que la administración subcutánea de lanreótido.
Esta serie como la mayoría de las publicadas, tiene como limitaciones, la ausencia de grupo control y el pequeño tamaño muestral. Por otro lado es probable que la eficacia del fármaco dependa de la gravedad de la hemorragia y de los fármacos predisponentes al sangrado, especialmente la anticoagulación, por lo que son necesarios estudios equivalentes de eficacia de las distintas dosis disponibles.