Nilotinib es un inhibidor de la tirosina cinasa (ITK) aprobado como tratamiento la leucemia mieloide crónica (LMC). Nilotinib se ha asociado a un incremento del riesgo de enfermedad arterial periférica (EAP)1-3, enfermedad coronaria y eventos cerebrovasculares4-6. Presentamos a 3 pacientes que padecieron ictus isquémico durante el tratamiento crónico con nilotinib. Dos de ellos presentaron también EAP y aterosclerosis intracraneal. El tercero sufrió una disección de la arteria carótida interna (ACI) sin evidencia de ateromatosis en el estudio vascular. En el momento del ictus, los 3 pacientes presentaban un riesgo cardiovascular (RCV) elevado a los 10 años según la valoración de la American Heart Association (AHA)7.
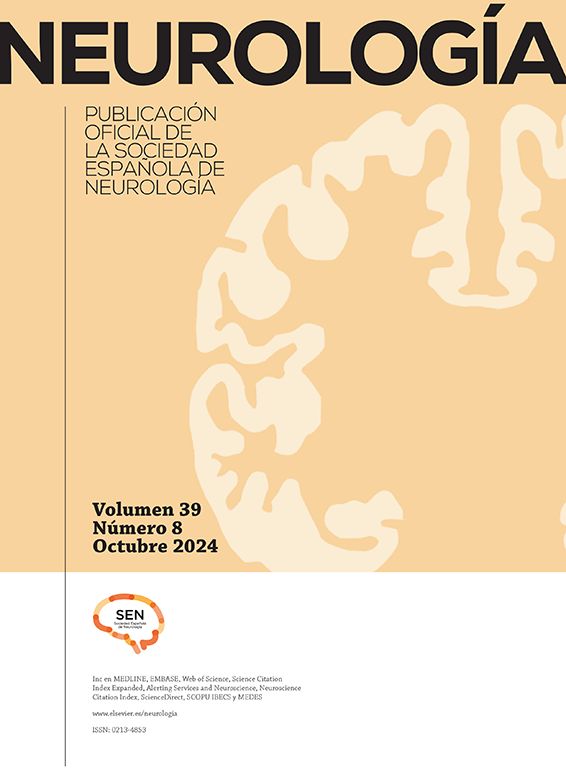
Descripción de los 3 casosCaso 1Varón de 66 años con antecedentes de hipertensión arterial y LMC en tratamiento con nilotinib 400mg 2 veces al día durante los 8 meses previos. El RCV a 10 años según la ASCVD era de 9,6%. El paciente consultó por un cuadro brusco de vértigo, diplopía, paresia facial central y ataxia de la marcha. La resonancia magnética (RM) mostró múltiples lesiones isquémicas agudas en mesencéfalo, protuberancia y córtex occipital. La angio-RM (a-RM) mostró oclusión de la arteria vertebral e importante aterosclerosis intracraneal (fig. 1 A). Se sustituyó el tratamiento por dasatinib y se inició anticoagulación por vía oral con acenocumarol. Ocho meses después, el paciente fue diagnosticado de EAP y requirió colocación de stent en la arteria femoral.
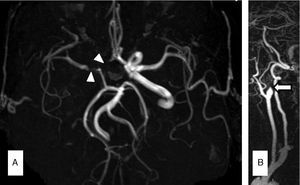
La angiografía por resonancia magnética (a-RM) del paciente 1 (A) mostró una oclusión de la arteria vertebral (AV) izquierda y aterosclerosis difusa intracraneal, especialmente en la AV derecha, la arteria cerebral media (ACM) izquierda y la arteria cerebral posterior (ACP) derecha. La a-RM del paciente 2 (B) mostró una ausencia de flujo en la arteria carótida interna (ACI) izquierda y la ACM izquierda, con aterosclerosis intracraneal de predominio en la ACM derecha y la ACP derecha.
Varón de 56 años de edad, fumador y con antecedente de hipertensión arterial y enfermedad coronaria. Fue diagnosticado de LMC 5 años antes del ingreso, por lo que realizó tratamiento con nilotinib 300mg 2 veces al día. Dieciséis meses antes del ingreso, el paciente presentó oclusión de la arteria central de la retina, por lo que se suspendió el tratamiento con nilotinib y se añadió tratamiento antiagregante e hipolipidemiante. Su riesgo ASCVD a los 10 años fue del 14,8%. El paciente ingresó tras presentar varios episodios autolimitados de disartria, hemiparesia y hemihipoestesia. El estudio vascular mostró una suboclusión de la ACI izquierda, así como estenosis de ACI derecha y ambas arterias cerebrales medias (ACM). Se inició tratamiento antiacoagulante con heparina sódica por vía intravenosa, a pesar del cual el paciente presentó recurrencia de la sintomatología en forma de hemiplejía y afasia por oclusión de la ACI izquierda. A pesar de angioplastia urgente y colocación de stent, no presentó mejoría clínica. Dos días después un control sonográfico mostró oclusión del stent. La a-RM confirmó ausencia de flujo en ACI y ACM izquierdas. Al alta se mantuvo tratamiento anticoagulante con acenocumarol. En el seguimiento a los 3 meses la puntuación en la escala NIHSS fue de 7. No había presentado nuevos eventos vasculares y se decidió sustituir el acenocumarol por aspirina.
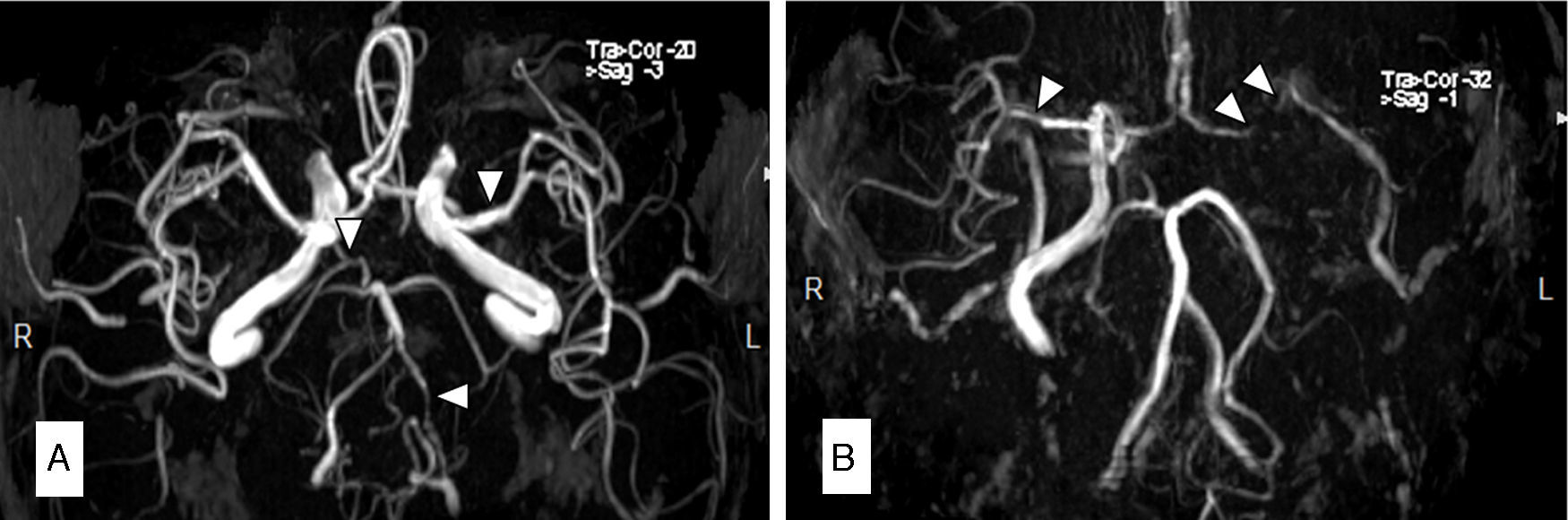
Caso 3Varón de 66 años con antecedente de LMC en tratamiento con nilotinib 300mg 2 veces al día durante los 7 años previos. El paciente consultó por 2 episodios transitorios de hemiparesia y hemihipoestesia izquierda. Su riesgo ASCVD a los 10 años fue del 9,3%. La RM reveló múltiples lesiones isquémicas en el córtex frontal y parietal derecho. La a-RM mostró una disección de la ACI y una estenosis > 50% de la ACM (fig. 2 A y B). Se suspendió el tratamiento con nilotinib y se inició tratamiento hipolipidemiante y anticoagulante con acenocumarol. A los 3 meses una angiotomografía computarizada de control mostró persistencia de oclusión de la ACI y se sustituyó el acenocumarol por aspirina.
DiscusiónNilotinib ha demostrado ser eficaz en el tratamiento de la LMC8. Los estudios de seguimiento a largo plazo han mostrado la aparición de complicaciones vasculares tales como la EAP, enfermedad coronaria o enfermedad cerebrovascular en una proporción de pacientes tratados9,10. Se han propuesto varios mecanismos para explicar esta asociación. Los efectos de nilotinib sobre células no hematopoyéticas, como células vasculares y perivasculares, mastocitos o células pancreáticas podrían predisponer al desarrollo de aterosclerosis, así como a hiperglucemia e hipercolesterolemia2. Además, ponatinib, otro TKI, se ha relacionado con eventos vasculares y cerebrales, lo que indica un potencial efecto de grupo1,11. Sin embargo, no se han descrito este tipo de eventos con imatinib o dasatinib.
Dos de nuestros pacientes presentaban marcada aterosclerosis intracraneal. Hallazgos similares se han descrito anteriormente en pacientes en tratamiento con nilotinib4 y ponatinib11. El tercer paciente presentó una disección de un gran vaso extracraneal. Esta afectación vascular no ha sido descrita previamente en pacientes en tratamiento con nilotinib.
Algunos expertos han sugerido que la evaluación del RCV mediante escalas validadas como las de la AHA7 o la European Society of Cardiology score12 puede ayudar a identificar los pacientes con un mayor riesgo de efectos adversos vasculares1,13.
Es importante que la asociación entre nilotinib y eventos cerebrovasculares sea conocida por los clínicos a fin de evitar este tratamiento en los pacientes con un RCV elevado o de controlar las alteraciones metabólicas que puedan surgir derivadas del tratamiento, como, por ejemplo, hipercolesterolemia o hiperglucemia. Asimismo, resulta aconsejable informar a los pacientes en tratamiento con nilotinib acerca de los síntomas del ictus para que consulten rápidamente.
Al Dr. Francisco Cervantes por su colaboración.