Evaluar la seguridad clínica y resultados audiológicos posoperatorios en pacientes de habla hispana con sordera postlingual, que recibieron implante coclear (IC) Nurotron™ modelo CS-10A (Nurotron Biotechnology Inc.; Hangzhou, Zhejiang, China).
Materiales y métodosEstudio descriptivo retrospectivo tipo serie de casos. Se hizo seguimiento de complicaciones y mediciones audiológicas antes y después del IC. Se incluyeron pacientes con pérdida auditiva neurosensorial bilateral severa a profunda o con sordera unilateral (SSD) con/sin tinnitus. Se realizaron medidas repetidas dentro de los sujetos para evaluar los umbrales de tonos puros y el rendimiento del habla (listados de bisílabas), así como seguimiento clínico para establecer la seguridad del dispositivo. En el análisis estadístico se utilizaron exámenes de la varianza y pruebas de medidas repetitivas.
ResultadosSe incluyeron 31 pacientes, 17 (54,8%) hombres y 14 (45,2%) mujeres. La edad media en el momento de la cirugía fue de 49,82 ± 18,8. El seguimiento medio fue de 31,56 ± 9,57 meses (mínimo = 19,6 y máximo = 52,50). Como complicación mayor uno (3,23%) tuvo un fallo técnico que requirió remoción y reimplantación. De estos, 25,8% presentaron complicaciones menores, siendo la más frecuente el vértigo/inestabilidad en 22,6%. La media de discriminación del habla (campo libre a 65 decibelios [dB] Sound Pressure Level [SPL]) fue de 62,19% ± 16,66; siendo de 69,82% ± 7,35 en el grupo de hipoacusia neurosensorial bilateral severa/profunda. Se observó una reducción estadísticamente significativa en los pacientes con tinnitus, evaluados mediante la escala visual analógica (EVA), preoperatorio = 7,2 ± 1,6 vs. posoperatorio (18 meses) = 1,7 ± 1,3 (p < 0,001).
ConclusionesEl IC Nurotron™ muestra resultados audiológicos satisfactorios, acordes con lo reportado en la literatura. Las complicaciones menores fueron similares a estudios previos, pero se debe continuar observando el porcentaje de fallo técnico que fue superior a otros reportes con seguimiento equiparable.
to assess clinical safety and postoperative audiological outcomes in postlingual deafness Spanish speaking patients, who underwent surgery with Nurotron™ cochlear implant.
Material and MethodsRetrospective descriptive case series study. We performed follow-up of complications and audiological measurements before and after cochlear implantation. Patients with bilateral severe to profound sensorineural hearing loss or patients with unilateral deafness with/without tinnitus were included. Repeated-measures within-subjects for assess pure tone thresholds and speech performance (bilingual test) with a detailed monitoring to establish security or adverse effects were performed. Analysis of variance tests, repetitive measures, were used for statistical analysis.
Results31 patients were included, 17 (54.8%) men and 14 (45.2%) women. Mean age at the time of surgery was 49.82 ± 18.8 years. The mean follow-up of the group was 31.56 ± 9.57 months (minimum = 19.6 months and maximum = 52.50months). As major complication one patient (3.23%) had a hard failure that required removal and re-implantation. 25.8% of the patients presented minor complications, the most frequent being vertigo/unsteadiness in 22.6%.
The mean of language discrimination (free field at 65 dB SPL) was 62.19% ± 16.66; being 69.82% ± 7.35 in the group of severe to profound bilateral sensorineural hearing loss. A statistically significant reduction was observed in patients with tinnitus, assessed using the visual analog scale, preoperative = 7.2 ± 1,6 vs postoperative (18 months postoperative) = 1.7 ± 1.3 (p < 0.001).
ConclusionsThe Nurotron™ cochlear implant shows satisfactory audiological results, in accordance with what has been reported in the literature. Minor complications were similar to previous studies, but the percentage of hard failure should continue to be observed, which was higher than other reports with comparable follow-up.
En adultos la hipoacusia se asocia con aislamiento social, depresión, pérdida de la autonomía, disminución en la capacidad productiva y alteraciones neurocognitivas1,2. Una parte de los pacientes pueden ser rehabilitados con prótesis auditiva1,3, pero, para aquellos con hipoacusia neurosensorial (HNS) severa/profunda, esto no es suficiente y la mejor opción de tratamiento es el implante coclear (IC)3. En ellos el principal objetivo es mantener el lenguaje hablado como principal forma de comunicación3.
La HNS severa/profunda bilateral fue la primera indicación para implantación coclear que aprobó la Food and Drug Administration (FDA) en adultos1. Posteriormente, las indicaciones se extendieron para pacientes con HNS severa/profunda unilateral con el otro oído sano (SSD) o con una HNS menor que severa en el otro oído (HNS asimétrica)1,3. En casos de SSD o HNS asimétrica los objetivos adicionales son control del tinnitus, restablecimiento de la audición binaural (localización de la fuente sonora, mejorar la discriminación del habla en fondo ruidoso) y mejoría en calidad de vida1,3–5.
A pesar de los reconocidos beneficios de la rehabilitación auditiva, su empleo sigue siendo bajo1,6. En una revisión sistemática sobre el tema, reportan que en los adultos los factores involucrados con una baja utilización de prótesis auditivas se podían agrupar en tres categorías: motivacionales, barreras de acceso y aquellos relacionados con el desempeño del dispositivo auditivo6. Entre las barreras de acceso más relevantes se describen: limitaciones por el costo del dispositivo y de cobertura por parte de las aseguradoras/sistemas de salud6. Para el caso específico del IC, un estudio estimó que menos de 10% de los adultos que son candidatos para IC lo reciben efectivamente7. Otros factores que explican el bajo uso del IC son el desconocimiento de sus beneficios y de los criterios de selección1,6–8.
Como el IC es un dispositivo de alta tecnología y fabricación compleja, existen pocas empresas que lo producen, manteniendo un costo elevado y que no ha disminuido en las últimas tres décadas8. Nurotron™ modelo CS-10A (Nurotron Biotechnology Inc.; Hangzhou, Zhejiang, China) es una marca de IC, que obtuvo aprobación para su uso en China en 2011, en la comunidad europea en 2012, en Colombia en 2013 y puede representar una alternativa de acceso para algunos pacientes8. En el ensayo clínico inicial, reportan una discriminación del lenguaje ∼ 80% a los seis meses (frases en mandarín) y de ahí en adelante un fenómeno de meseta8. Los autores también mencionan que el desempeño del IC Nurotron™ es comparable al de otras marcas disponibles en el mercado8.
El presente estudio lo realizamos con el fin de describir la seguridad clínica y los resultados audiológicos en pacientes adultos postlinguales hispanohablantes que recibieron un IC de marca Nurotron™.
Materiales y métodosDiseño del estudioEl presente es un estudio descriptivo de series de casos en el que se comparan los resultados antes y después de la implantación coclear. Se incluyeron pacientes operados desde marzo de 2014 hasta enero de 2020, quienes recibieron el IC en un centro de tercer nivel de referencia de Bogotá, Colombia.
SujetosSe incluyeron pacientes que recibieron implantación coclear con la marca Nurotron™. Los criterios adicionales fueron edad > 15, adquisición del lenguaje hablado antes de la implantación coclear, idioma nativo español y que tengan las mediciones de desenlaces por al menos 12 meses posoperatorios. Se excluyeron aquellos con IC contralateral o que tuvieran déficits neurológicos. Los elegibles fueron identificados a partir de los archivos de quienes contaban con IC del centro del estudio. La información demográfica, de cirugía y de seguimientos clínicos se obtuvo de forma retrospectiva. Los resultados audiológicos y de funcionamiento del IC se obtuvieron en el servicio de audiología encargado de la activación y programación de los dispositivos. La información preoperatoria fue tomada de los registros de los seis meses (±1 mes) previos a la cirugía y la información posoperatoria incluyó hasta el último seguimiento completo registrado.
Se utilizó un tamaño de muestra por conveniencia, incluyendo todos los pacientes que cumplen los criterios de inclusión y no tienen ninguno de exclusión; por lo cual no se hizo cálculo del tamaño de la muestra.
Dado que la investigación se hizo registrando información de las historias clínicas, es una investigación sin riesgo para el paciente y se acoge a las recomendaciones de la declaración de Helsinki9. Los incluidos en el estudio recibieron la implantación coclear como parte del tratamiento que les fue indicado por su médico tratante y no se registraron datos que puedan identificar a uno de forma individual, asegurando la confidencialidad y privacidad de los sujetos.
Protocolo de implantación coclear y seguimientoLos pacientes fueron implantados de acuerdo con el protocolo de implantación coclear de la institución participante. Para las evaluaciones del lenguaje se utilizaron listados de bisílabas, de acuerdo con lo descrito para el idioma español3. En la evaluación preoperatoria el porcentaje de discriminación del lenguaje (PDL) fue obtenido en las mejores condiciones de amplificación cuando el paciente usaba prótesis auditiva, de lo contrario se obtenía el PDL a la máxima salida del audiómetro (90 decibelios [dB] hearing level [HL]). Los adultos se consideran candidatos a IC si del lado a implantar presentan HNS severa/profunda definida como: promedio de tonos puros (PTP) de cuatro frecuencias (0,5-3Khz) por vía aérea ≥ 70 dB y PDL < 50% y se clasificaron en una de las siguientes tres indicaciones: 1) pacientes con SSD (Grupo 1); 2) pacientes con HNS severa/profunda bilateral (Grupo 2); 3) pacientes con HNS asimétrica (Grupo 3). La SSD se define como: oído enfermo con HNS profunda (PTP ≥ 90 dB y PDL ≤ 20%) y oído contralateral sano (PTP ≤ 20 dB). La HNS severa/profunda como: PTP ≥70 dB y PDL < 50% en los dos oídos. Y la HNS asimétrica: oído a implantar con PTP ≥ 70 dB y PDL < 50% y oído contralateral con HNS leve a severa (PTP = 21 dB-69 dB) con PDL ≥ 60%. El encendido del IC se hizo entre cuatro a seis semanas posoperatorias y los seguimientos son tres, seis, 12 meses y luego cada seis meses. En cada punto del seguimiento se realiza una evaluación del lenguaje, evaluación clínica, evaluación audiológica y reprogramación del IC. En cada visita se hace un interrogatorio sistemático acerca del uso y funcionamiento del dispositivo, así como de complicaciones con el uso de este.
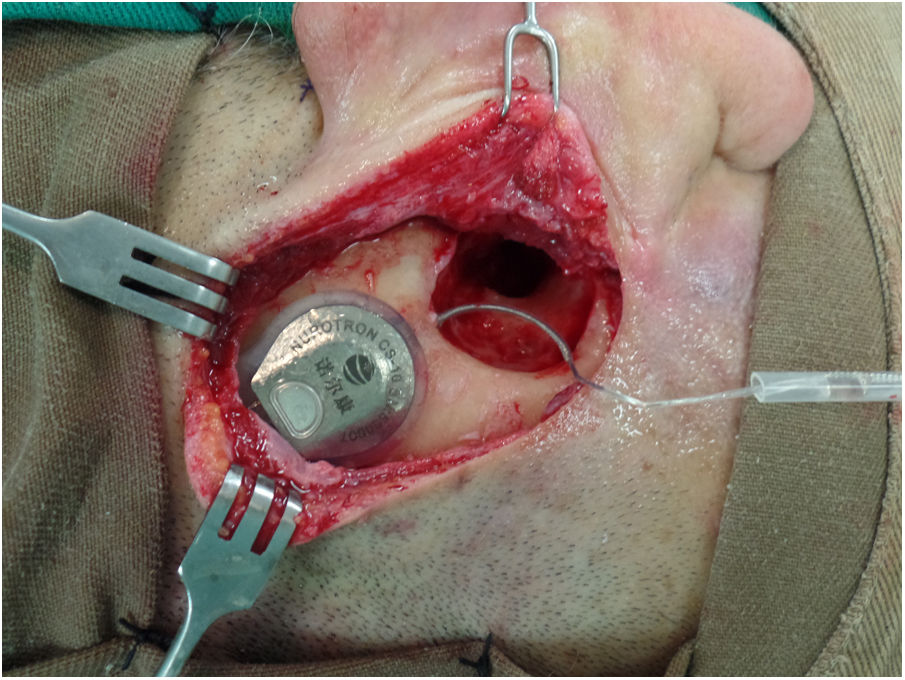
Técnica quirúrgica y dispositivo implantadoLa técnica quirúrgica es estándar buscando, siempre que sea posible, hacer la inserción de la serie de electrodos por ventana redonda (VR). Además, se intenta minimizar el trauma a los tejidos, como lo describen Almario et al.10. En todos los casos se hace un lecho para acomodar la antena-receptor y la serie de electrodos se pasa hacia la mastoides a través de un túnel/canal con el fin de aumentar la estabilidad del componente interno (fig. 1). Se utiliza antibiótico perioperatorio y se es exhaustivo con la asepsia/antisepsia durante la cirugía para disminuir el riesgo de infecciones tardías como biofilms11. Para disminuir el trauma coclear se emplean corticoides perioperatorios y tópicos antes de la apertura de la VR, el fresado del nicho de la VR se hace a baja velocidad (2.000 rpm), la inserción de la serie de electrodos se hace lentamente (> 30 seg) y se trata de evitar la reinserción del electrodo. En casos de obliteración/osificación coclear se hace un abordaje escalonado hasta encontrar la luz coclear o se realiza una cocleostomía radical, como lo describen Balkany et al.12.
Paciente con IC Nurotron™
En un oído derecho se observa la antena-receptor alojada en el lecho que se hace con el fin de aumentar su estabilidad. La serie de electrodos pasa desde el lecho hacia la mastoides a través de un túnel. Estas medidas buscan reducir el riesgo de desplazamiento/extrusión del componente interno del implante coclear.
El paciente tenía una cavidad de mastoidectomía con muro abajo (por secuelas de OMC colesteatomatosa) por lo cual, para la implantación coclear, se decidió hacer una petrosectomía subtotal con cierre del conducto auditivo externo en su tercio lateral, resección de todos los remanentes epiteliales, obliteración de la trompa de Eustaquio con injertos de músculo y hueso y obliteración de la cavidad con injertos de músculo y fascia temporal.
IC: implante coclear; OMC: otitis media crónica.
El IC utilizado de marca Nurotron™ fue el modelo CS-10A (Nurotron Biotechnology Inc.; Hangzhou, Zhejiang, China), que tiene un receptor/estimulador con una serie de 24 electrodos activos intracocleares y dos de referencia. Se usó en todos los casos un electrodo recto (estándar, que era el disponible al momento de las cirugías), que tiene 22 mm de longitud, distancia entre contactos de 0,8 mm y un área de 0,2 mm2 en cada contacto. A nivel de la punta la serie de electrodos mide 0,70 x 0,56 mm y a nivel de la base 0,93 x 0,68 mm8. Los pacientes recibieron el procesador de sonido Venus® (Nurotron Biotechnology Inc.; Hangzhou, Zhejiang, China), el cual es de diseño retroauricular y a través de la antena de radiofrecuencia establece la comunicación con el componente interno.
Mediciones audiológicasLa evaluación preoperatoria incluyó audiometría tonal, por vías aérea y ósea y se calculó el PTP de cuatro frecuencias para definir la severidad de la pérdida auditiva en cada oído. Estos resultados se confirman con potenciales auditivos de tallo cerebral o potenciales de estado estable. La logoaudiometría se hace por vía aérea con auriculares supra-aurales, buscando el máximo PDL en cada oído. Posteriormente, se evalúa el desempeño con prótesis auditiva en campo libre, con dos parlantes ubicados a 1 m frente al paciente (azimut 0° y elevación 0°), buscando umbrales auditivos y PDL a 65 dB Sound Pressure Level (SPL). Para el grupo 1 las mediciones se hicieron con prótesis auditiva en el oído enfermo y para los de los grupos 2 y 3 evaluando cada oído por separado con su respectiva prótesis auditiva. Para los de los grupos 1 y 3, el oído no revisado fue ocluido con un protector auditivo de inserción más enmascaramiento con ruido blanco a 45 dB a través de un auricular supra-aural.
Las evaluaciones posoperatorias se hicieron de forma similar a lo descrito para el preoperatorio, con el IC encendido y realizando oclusión más enmascaramiento del mejor oído para los pacientes de los grupos 1 y 3 y sin el uso de prótesis auditiva en el oído no implantado para los del grupo 2.
Evaluación del tinnitusEn pacientes con tinnitus, la severidad del síntoma se evaluó usando la escala visual analógica (EVA). Se les explicó que el tinnitus correspondía al «ruido/ruidos interno/s que percibían y que no tenía/n una fuente externa que lo/s genere» y se les pidió que califiquen su severidad de 0 a 10, siendo 0 = ausencia de tinnitus y 10 = «el peor tinnitus que puedan imaginar». En el preoperatorio se hizo sin el uso de ayuda auditiva y en las visitas de seguimiento se hizo con el IC encendido.
Evaluación y seguimiento de complicacionesEl protocolo de implantación coclear tiene un formato de historia clínica prediseñado que se debe diligenciar en cada visita. Dicho formato tiene un apartado en el que se registran específicamente la presencia o ausencia de complicaciones con el uso del dispositivo. Las complicaciones son clasificadas como mayores y menores. Una complicación mayor es aquella que necesita tratamiento médico intensivo, requiere revisión quirúrgica y/o causa morbilidad permanente en el paciente.
Análisis estadísticoLas variables cuantitativas (interválicas/proporcionales y ordinales) se describen mediante medidas de tendencia central y dispersión, y las variables nominales mediante frecuencias. Las comparaciones se hicieron con pruebas paramétricas o no paramétricas, según la naturaleza de las variables.
Para los desenlaces principales, las complicaciones se presentan mediante frecuencias. Las mediciones audiométricas y de evaluación del tinnitus fueron comparadas antes y después de la implantación coclear, utilizando un análisis de la varianza (ANOVA) de medidas repetidas, con significancia estadística en p < 0,05. Los análisis se hicieron con el programa SPSS versión 11.5 (SPSS, Inc., Chicago, IL, EE. UU.).
Los resultados del estudio se presentan siguiendo las recomendaciones para el reporte Strengthening the Reporting of Observational Studies in Epidemiology (STROBE)13.
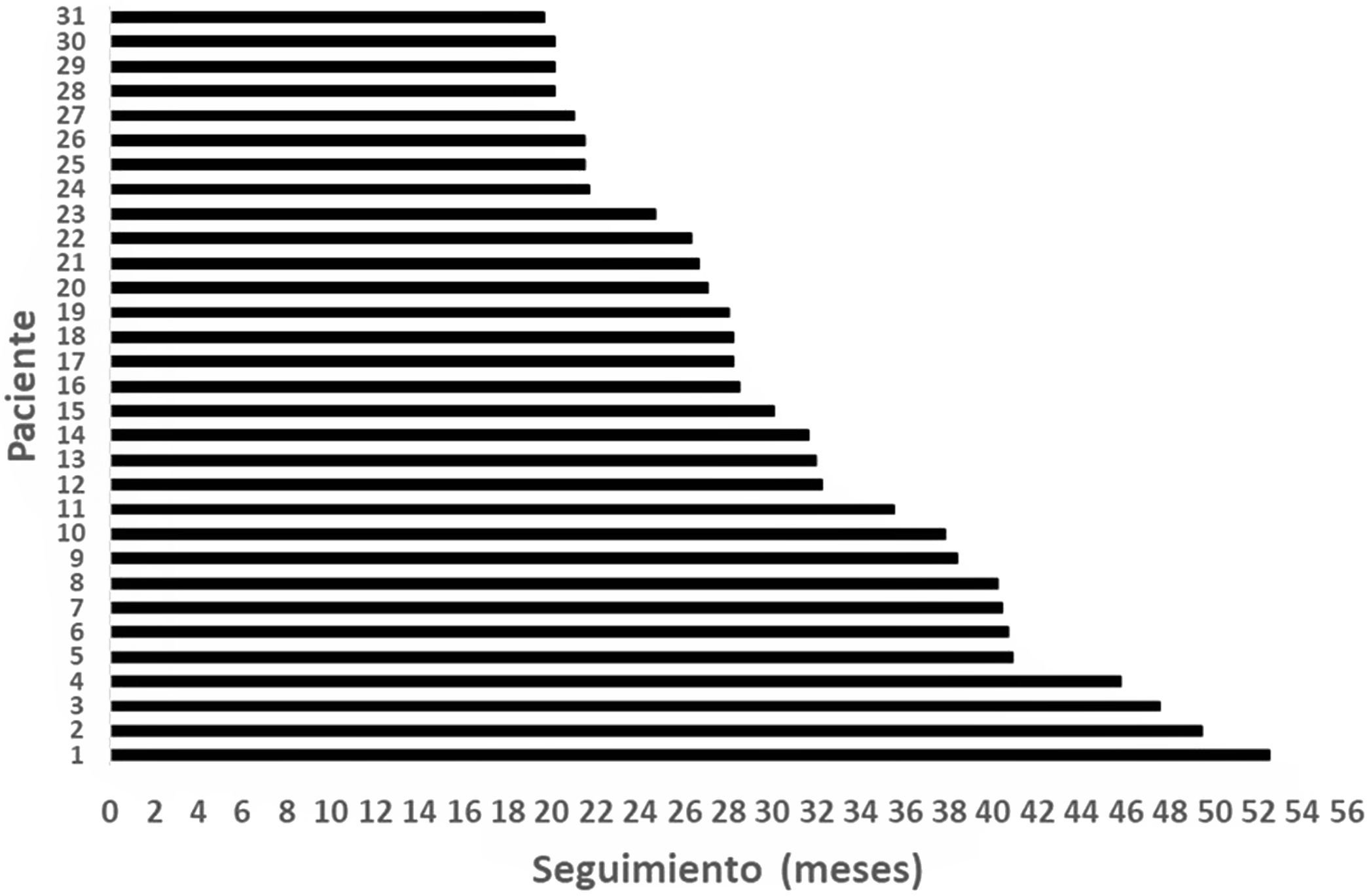
ResultadosSe identificaron 33 pacientes que recibieron IC Nurotron™, dos fueron prelinguales y sus resultados excluidos del análisis. Dos se perdieron del seguimiento (6,5%), uno por fallecimiento por patología no relacionada con el IC y otro por pérdida del aseguramiento al sistema de salud (fig. 2). El seguimiento del grupo fue de 31,56 ± 9,57 meses (mínimo = 19,6, máximo = 52,50) (fig. 3). Para los dos casos de pérdida de seguimiento se reportan sus resultados hasta el momento del último disponible. El paciente que falleció fue por cáncer de epiplón, tenía su implante funcionando adecuadamente (24 electrodos activos y PDL = 60%) y usándolo de forma rutinaria.
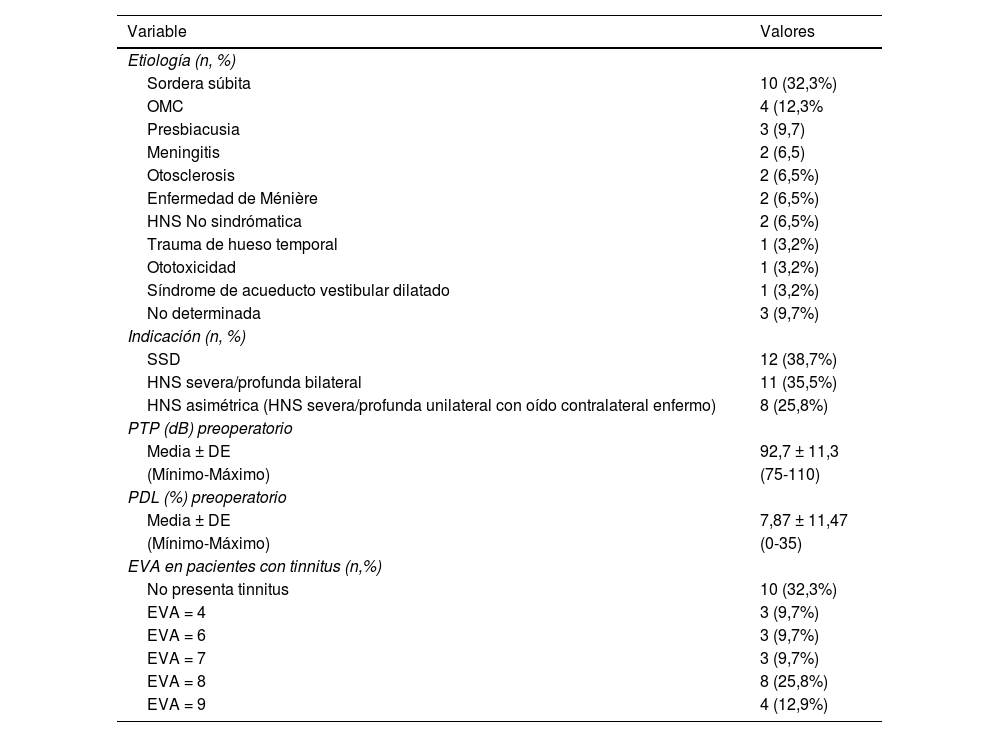
La tabla 1 muestra las características del grupo de estudio y en la tabla 2 se presentan los hallazgos clínicos de la población de estudio. Las cirugías fueron primarias y se realizaron de forma unilateral en todos los pacientes. La duración de la pérdida auditiva severa/profunda antes del IC fue 49,52 ± 46,64 meses. Un total de 14 (45,2%) usaron prótesis auditiva antes de recibir el IC y la utilizaron 122,14 ± 144,83 meses. La SSD fue la indicación más frecuente (38,7%, n = 12), lo cual se relaciona con la sordera súbita como causa más frecuente en nuestra serie. En general, el oído que recibió el IC presentaba HNS profunda (PTP = 92,7 dB ± 11,3; PDL = 7,87% ± 11,4). El tinnitus fue un síntoma frecuente presentándose en 21 de ellos (67,7%), siendo de intensidad moderada a severa (EVA = 4-9). En el estudio imagenológico preoperatorio a 15 (48,4%) se les hizo resonancia magnética + tomografía, a nueve (29%) solo tomografía y a siete (22,6%) únicamente resonancia magnética. En estos estudios se identificó a uno (3,2%) con acueducto vestibular dilatado y a dos con osificación coclear completa (6,5%).
Características de la población de estudio (n = 31)
| Edad (años)Media ± DE(Rango) | SexoHombre / Mujer(n, %) | Oído implantadoDerecho / Izquierdo(n, %) | Discapacidad adicional(n, %) |
|---|---|---|---|
| 49,82 ± 18,8(15,7-77,9) | 17 (54,8%) / 14 (45,2%) | 16 (51,6%) / 15 (48,4%) | Ninguna = 25 (80,6%)Pérdida visual = 3 (9,7%)Otras alteraciones de la voz = 1 (3,2%)Alzheimer = 1 (3,2%)Retraso mental leve = 1 (3,2%) |
DE: desviación estándar.
Hallazgos clínicos de la población de estudio (n = 31)
| Variable | Valores |
|---|---|
| Etiología (n, %) | |
| Sordera súbita | 10 (32,3%) |
| OMC | 4 (12,3% |
| Presbiacusia | 3 (9,7) |
| Meningitis | 2 (6,5) |
| Otosclerosis | 2 (6,5%) |
| Enfermedad de Ménière | 2 (6,5%) |
| HNS No sindrómatica | 2 (6,5%) |
| Trauma de hueso temporal | 1 (3,2%) |
| Ototoxicidad | 1 (3,2%) |
| Síndrome de acueducto vestibular dilatado | 1 (3,2%) |
| No determinada | 3 (9,7%) |
| Indicación (n, %) | |
| SSD | 12 (38,7%) |
| HNS severa/profunda bilateral | 11 (35,5%) |
| HNS asimétrica (HNS severa/profunda unilateral con oído contralateral enfermo) | 8 (25,8%) |
| PTP (dB) preoperatorio | |
| Media ± DE | 92,7 ± 11,3 |
| (Mínimo-Máximo) | (75-110) |
| PDL (%) preoperatorio | |
| Media ± DE | 7,87 ± 11,47 |
| (Mínimo-Máximo) | (0-35) |
| EVA en pacientes con tinnitus (n,%) | |
| No presenta tinnitus | 10 (32,3%) |
| EVA = 4 | 3 (9,7%) |
| EVA = 6 | 3 (9,7%) |
| EVA = 7 | 3 (9,7%) |
| EVA = 8 | 8 (25,8%) |
| EVA = 9 | 4 (12,9%) |
dB: decibelios; DE: desviación estándar; EVA: escala visual analógica; HNS: hipoacusia neurosensorial; OMC: otitis media crónica; PDL: porcentaje de discriminación del lenguaje; SSD: sordera unilateral.
Con respecto a los hallazgos quirúrgicos, en 25 pacientes (80,6%) la anatomía de la VR y vuelta basal de la cóclea fue normal, en cuatro (12,9%) se encontró obliteración del nicho de la VR y/o segmento inferior de la vuelta basal de la cóclea y en dos (6,5%) hubo osificación coclear completa. En 27 (87,1%) la inserción se hizo por VR, en dos casos (6,5%) se debió fresar el segmento inferior de la vuelta basa de la cóclea por obliteración parcial y en dos se requirió cocleostomía radical (6,5%) por osificación completa de la cóclea. El cirujano reportó en cirugía inserción completa de la serie de electrodos (24) en 24 pacientes (77,4%) e inserciones parciales en los restantes siete. El menor número de electrodos activos se observó en los dos que requirieron cocleostomía radical: siete y 10, respectivamente.
Como complicaciones intraquirúrgicas, se presentaron dos casos (6,5%) de fístula de líquido cefalorraquídeo (LCR), que fueron los dos pacientes con osificación coclear completa que requirieron cocleostomía radical. En los dos casos la fístula de LCR se produjo por ingreso al conducto auditivo interno (CAI) durante el fresado coclear. Se manejaron obliterando el sitio de la fístula con un injerto de músculo-fascia temporal, sellando la trompa de Eustaquio con injertos óseos (cortical mastoidea) y músculo temporal, cerrando el conducto auditivo externo (parte de la técnica de cocleostomía radical), obliterando la cavidad timpanomastoidea con grasa abdominal (después de colocar el IC) y dejando un vendaje compresivo por tres días en el posoperatorio. En los dos casos hubo control de la fístula de LCR intraoperatoriamente y no se requirieron medidas adicionales en el posoperatorio. No se reportaron complicaciones intraoperatorias en los restantes 29 (93,5%).
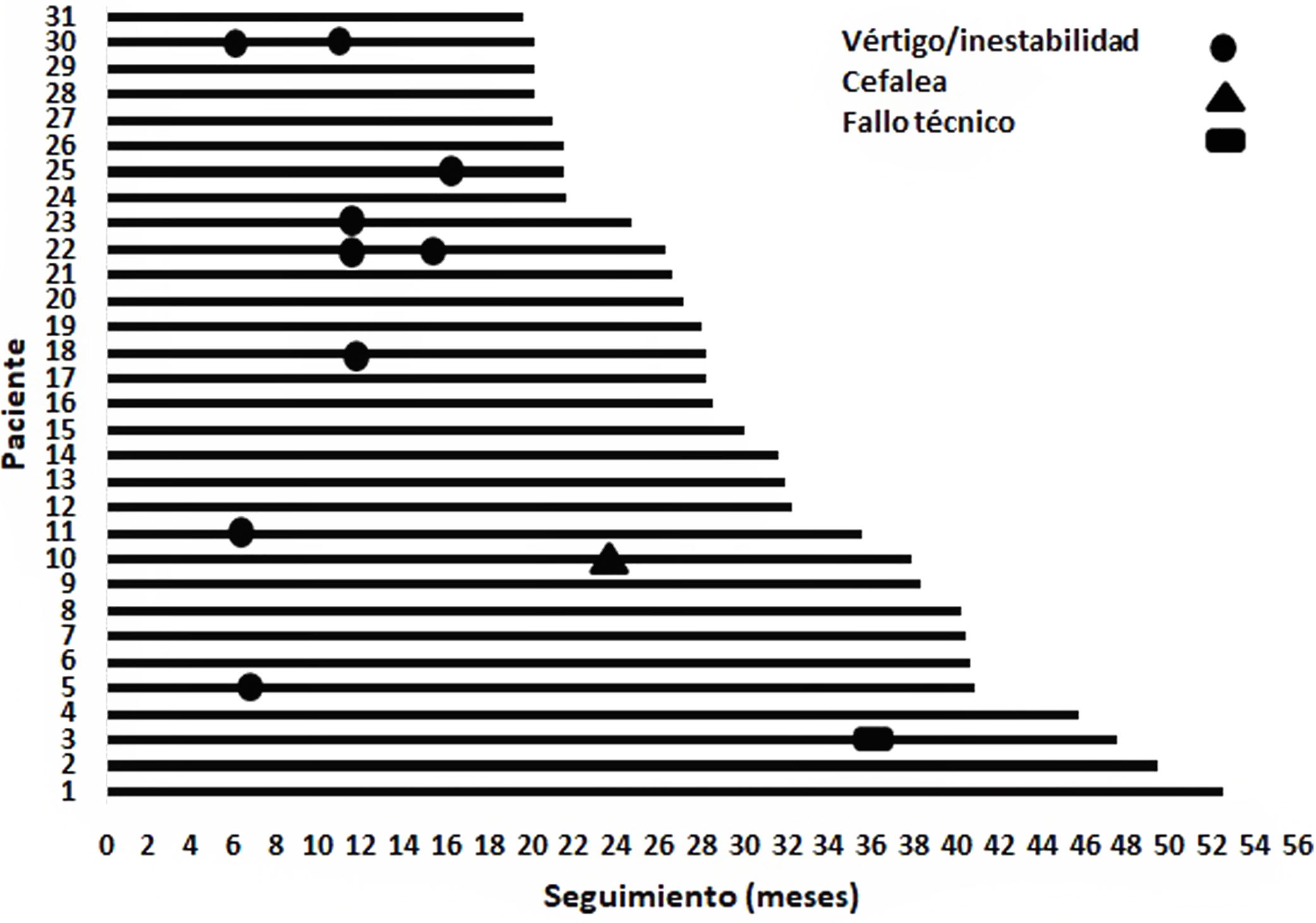
En el seguimiento, un paciente presentó fallo técnico (3,23%) que requirió explantación y reimplantación con un dispositivo nuevo en el mismo tiempo. En el reporte del fabricante se informa que el dispositivo explantado no tenía daños en su cobertura, pasó la prueba de hermeticidad (prueba de helio) y la alteración encontrada fue un fallo en la fuente de corriente compatible con daño por descarga electrostática (ESD). Una vez reemplazado dicho componente se comprobó adecuado funcionamiento del receptor estimulador, así como su comunicación con el procesador de sonido. Este fue un paciente de 75 años con HNS bilateral severa/profunda con un seguimiento de 48 meses, cuyo mejor PDL antes de la explantación fue 80% y posterior a la reimplantación el PDL fue 60% (seis meses post-reimplantación). Como complicaciones menores se reportan 10 eventos, de ellos nueve fueron vértigo/inestabilidad y uno cefalea (fig. 4). Los eventos de vértigo/inestabilidad fueron manejados con maniobras de reposicionamiento de Epley y/o terapia vestibular, el que reportó cefalea recibió acetaminofén; todos los eventos fueron resueltos satisfactoriamente desde el punto de vista sintomático.
Los resultados audiométricos se muestran en la tabla 3, tanto para el grupo total, como discriminado por los tres grupos según la indicación de cirugía. En la línea de base audiométrica preoperatoria se observó una diferencia significativa en el PDL entre grupo 1 (3,33 ± 7,79) vs. grupo 2 (14,45 ± 13,94), (p = 0,019, ANOVA); pero no entre el grupo 1 vs. grupo 3 (p = 0,641, ANOVA), ni entre grupo 2 vs. grupo 3 (p = 0,085, ANOVA). Los resultados de discriminación del lenguaje posoperatorio mostraron una clara mejoría con respecto al preoperatorio, tanto para el grupo total como para los tres subgrupos de indicación de cirugía (p < 0,001, para todas las comparaciones). No hubo diferencias en los resultados del PDL posoperatorios entre los tres grupos (p > 0,05, para todas las comparaciones).
Discriminación del lenguaje en pacientes del estudio
| Variable | Preoperatorio | Posoperatorio(última medición) | Diferencia(p) |
|---|---|---|---|
| PDL (%), Media ± DE | 7,87 ± 11,47 | 62,19 ± 16,66* | 54,32 ± 17,43 |
| (n = 31) | p < 0,001** | ||
| PDL (%), por grupo de indicación de cirugía | |||
| Grupo 1 (n = 12) | 3,33 ± 7,79 | 59,83 ± 17,89* | 56,50 ± 16,11 |
| p < 0,001*** | |||
| Grupo 2 (n = 11) | 14,45 ± 13,94 | 69,82 ± 7,35 | 55,36 ± 16,42 |
| p < 0,001*** | |||
| Grupo 3 (n = 8) | 5,63 ± 9,04 | 55,25 ± 21,28 | 49,63 ± 21,76 |
| p < 0,001*** |
Grupo 1: pacientes con sordera unilateral (SSD). Grupo 2: pacientes con HNS severa/profunda bilateral. Grupo 3: Pacientes con HNS asimétrica.
DE: desviación estándar; PDL: Porcentaje de discriminación del lenguaje, listado de bisílabas en campo libre a 65 decibelios (dB) Sound Pressure Level (SPL).
En cuanto a la supresión del tinnitus, el análisis se hizo con los 21 pacientes que lo presentaban en el preoperatorio (tabla 4). Se observó una marcada reducción del tinnitus con el uso del IC, estadísticamente significativa (p < 0,001) para todos los puntos del seguimiento analizados (hasta los 24 meses). Además, la reducción del tinnitus se incrementó significativamente (p < 0,05) con el paso del tiempo hasta los 18 meses, posterior a lo cual se observó un efecto de meseta.
Resultados respecto al tinnitus en la población de estudio
| Medida | Preoperatorio(n = 21) | 3 mes(n = 21) | 6 mes(n = 21) | 12 mes(n = 21) | 18 mes(n = 20) | 24 mes(n = 14) | 36 mes(n = 3) |
|---|---|---|---|---|---|---|---|
| EVA Media ± DE | 7,2 ± 1,6 | 3,7 ± 1,1 | 3 1 ± 0,9 | 2,5 ± 0,7 | 1,7 ± 1,3 | 1,6 ± 1,2 | 0,7 ± 1,2 |
| p* | < 0,001 | < 0,001 | < 0,001 | < 0,001 | < 0,001 |
DE: desviación estándar; EVA: escala visual analógica.
Análisis de la varianza (ANOVA) de medidas repetidas. Se compara cada punto del seguimiento con la medida preoperatoria. Los análisis post hoc (prueba de Bonferroni) mostraron que el efecto de supresión de tinnitus continuó incrementándose con el tiempo hasta los 18 meses y que estas diferencias fueron estadísticamente significativas: 3 mes vs. 6 mes p = 0,025, 6 mes vs. 12 mes p = 0,05, 12 mes vs. 18 mes p = 0,031. Luego de los 18 meses el efecto de supresión del tinnitus se estabilizó: 18 mes vs. 24 mes p = 0,41. Comparaciones realizadas con el número total de sujetos (n) disponible a cada punto del seguimiento.
Al momento de activación hubo en promedio 21,8 electrodos funcionales; a los tres meses = 21,9, seis = 21,9, 12 = 21,8, 18 = 21,3 y a los 24 = 21,3; diferencias que no fueron significativas (p > 0,05. ANOVA de medidas repetidas). En cuanto al rango dinámico de los electrodos activos se observó un incremento estadísticamente significativo hasta los seis meses (p < 0,05. ANOVA de medidas repetidas; análisis post hoc prueba de Bonferroni): a la activación = 42,9 ± 6,0 unidades internacionales (UI), tres meses = 55,8 ± 8,1 UI, seis = 60,1 ± 7,9 UI. A partir de los 12 meses se observó un efecto de meseta, con estabilización del rango dinámico: 12 = 62,7 ± 8,9 UI, 18 = 65,7 ± 8,7 UI, 24 = 62,9 ± 10,6 UI y 36 = 68,3 ± 7,6 UI (p > 0,05. ANOVA de medidas repetidas).
Dos casos que requieren una descripción especial son aquellos que tenían obliteración coclear completa, detectada en las imágenes preoperatorias. En los dos casos la causa de la pérdida auditiva fue secuelas de otitis media crónica (OMC), con historia de ∼ 4 y 5 años de pérdida profunda. En un caso la indicación fue por SSD (PTP oído sano = 13 dB, PDL = 100%) y el otro por HNS asimétrica (PTP mejor oído = 55 dB, brecha aéreo-ósea = 30 dB, PDL = 100%, usuario de prótesis auditiva). Los dos pacientes tenían tinnitus significativo (EVA = 6 y 8, respectivamente), laboralmente activos (el primer caso de profesión conductor) y luego de revisar las opciones de rehabilitación se consideró, en conjunto con los pacientes, que la mejor alternativa era el IC. Al momento de la cirugía el primero tenía 44 años y el segundo 47, hubo fístula de LCR que se controló intraoperatoriamente y al adaptar los procesadores de sonido se pudieron activar siete y 10 electrodos, respectivamente. Aunque en los dos casos el PDL fue bajo, 20 y 30%, la supresión del tinnitus fue significativa (EVA = 2 y 1, respectivamente), los dos pacientes usan el IC de forma rutinaria (> 12 hrs/día, todos los días de la semana) y permanentemente durante su trabajo.
DiscusiónLa implantación coclear en la población de estudio mostró un resultado bueno (PDL = 62-2% a 65 dB SPL) y equiparable a los publicados en la literatura para adultos postlinguales con indicaciones similares1,8. La serie de pacientes fue relativamente homogénea con respecto a factores pronósticos de resultado: no hubo malformaciones mayores del oído interno (solo un caso con acueducto vestibular dilatado), el tiempo medio de deprivación auditiva no fue prolongada = 49,5 meses (∼ 4 años) y no hubo casos con patología del nervio auditivo. Por otro lado, hubo dos casos de osificación coclear completa que requirieron cocleostomía radical para la colocación de la serie de electrodos. La necesidad de una cocleostomía radical puede afectar negativamente el resultado de la implantación coclear, ya que solo una parte de los electrodos queda en contacto con el nervio coclear, dicho contacto es poco estable y todo esto finalmente lleva a menos electrodos funcionales12,14. En nuestra serie estos dos pacientes con osificación coclear completa tienen valores de PDL posoperatorios extremos (PDL = 20% y PDL = 30%). Si excluimos estos dos casos del análisis, la discriminación del lenguaje para el grupo total se incrementa a 64,8% ± 13,8% (n = 29).
En el estudio clínico inicial con el IC Nurotron™, Zeng et al.8, reportaron un porcentaje de reconocimiento de frases de 68% a los cuatro meses postactivación, con un máximo de 89% a los 36 meses del seguimiento y con un efecto de meseta en el rendimiento a partir de los seis meses. Ese estudio incluyó 60 pacientes postlinguales con HNS severa/profunda bilateral, hablantes nativos de Mandarín8. En nuestro estudio el grupo de pacientes que tuvo una indicación similar (grupo 2, n = 11) mostró un porcentaje de reconocimiento de bisílabas de 69,8%, con un seguimiento medio de 31,6 meses. Aunque los resultados no son comparables directamente, ya que las frases tienen más redundancia de información que las bisílabas y por tanto es esperable porcentajes de reconocimiento mayor, las mediciones en estos dos estudios muestran un claro beneficio con el IC. En otra investigación con adultos postlinguales, se reporta un porcentaje de reconocimiento de monosílabas (consonat-nucleus-consonat [CNC]) de 58% a los 12 meses, en una población de 259 adultos (277 oídos) operados entre 2016 a 20191. En nuestra serie de 31 pacientes, el PDL = 62% es levemente superior al estudio de referencia, aunque debemos tener en cuenta que la redundancia de la información es mayor con bisílabas que con monosílabas. En un estudio cuya evaluación del habla se hizo con bisílabas (en coreano), se encontró un PDL = 70% a los 12 meses para 15 pacientes con sordera súbita15, valor ligeramente superior a 61,1% (± 19,1%) entre los 12 que fueron implantados por SSD en nuestro estudio (grupo 1). En un ensayo clínico entre pacientes con SSD, Galvin et al.5, reportan incrementos en el reconocimiento de CNC de 66,8, 76 y 84% a 1,3 y seis meses postactivación, respectivamente. Dicho estudio también mostró que los pacientes con SSD tenían claros beneficios en términos de localización del sonido, comprensión del habla, supresión del tinnitus y mejoría en la calidad de vida5; resultados que están en concordancia con otros estudios publicados al respecto4,16,17. En tanto a resultados en idioma español, en un reporte reciente usando IC Nurotron™, Pacheco et al.18, reportan un PDL = 50% entre siete pacientes mayores de 65 años que recibieron el dispositivo. Aunque el PDL de esta serie es inferior al que encontramos en la nuestra, debemos tener en cuenta que dicha serie solo incluyó población anciana y que hubo un caso de reimplantación coclear (en dos ocasiones), que también tuvo mal resultado con las dos marcas previas que utilizó. Encontramos un claro beneficio con el IC para suprimir el tinnitus (tabla 4). Aunque en candidatos a IC el tinnitus se puede presentar tanto en aquellos con SSD, como con HNS severa/profunda bilateral y con HNS asimétrica; los resultados de supresión del tinnitus son más frecuentemente reportados en pacientes con SSD. En el ensayo clínico de Galvin et al., entre pacientes con SSD, hubo una reducción estadísticamente significativa del tinnitus, evaluada mediante la EVA; hasta alcanzar un valor de 2,3 a los seis meses postactivación5. Resultados similares han sido publicados de forma consistente por otros autores16,17,19,20. En un estudio de evaluación de tecnologías entre adultos y niños con SSD (IC e implantes de conducción ósea), el beneficio fue mayor con la implantación coclear16. Aunque los dos sistemas mostraron beneficios en los umbrales auditivos (ganancia funcional), comprensión del lenguaje en fondo ruidoso y mejoría en la calidad de vida; solo el IC mostró una clara reducción del tinnitus y un perfil claramente favorable en los análisis de costo-efectividad al comparar IC vs. no tratamiento16. Dicho estudio reporta que, en promedio, el incremento en la relación costo-efectividad estuvo entre $17.783 y $18.148/año ajustado por calidad de vida (QALY) y con una disposición a pagar de $100.000 por QALY. Los autores encontraron que 70% de las simulaciones se consideraron rentables para la implantación coclear16.
En un dispositivo médico implantable, la seguridad clínica con su utilización y la replicabilidad de los resultados son aspectos muy importantes para los pacientes, los centros clínicos de atención y las autoridades regulatorias. El presente estudio tuvo un seguimiento medio = 31,6 meses, por lo que puede considerarse un reporte de mediano plazo. Se encontró que hubo dos pacientes con fístula de LCR (2/31 = 6,5%), que fue controlada de forma satisfactoria en la misma cirugía. Los dos casos tenían osificación coclear completa, requirieron cocleostomía radical y fue durante dicho fresado que se ingresó al CAI y se produjo la fístula. Por tanto, esta situación está en relación directa con la técnica quirúrgica que se requirió y no con la marca del dispositivo. Algunos autores consideran a esta como una complicación cuando se presenta en el posoperatorio y no en el transoperatorio. En un resumen de complicaciones entre investigaciones con más de 500 pacientes (10), se reporta una prevalencia de fístula de LCR posoperatorio = 0,2% (9/5.985)1. En cuanto a complicaciones posoperatorias menores (fig. 4), tuvimos 10 eventos en ocho pacientes, es decir una prevalencia = 25,8%; de ellos nueve eventos fueron vértigo/inestabilidad (en siete, prevalencia = 22,6%). Carlson en su resumen, reporta una prevalencia de complicaciones menores de 8,4% (482/5.771); siendo el vértigo/inestabilidad la más frecuente, en 102/4.664 (2,2%) pacientes1. En nuestro estudio, esta frecuencia fue mayor en parte porque se reportó como hallazgo positivo tanto el síntoma como el signo. En un metanálisis en el que se investigó específicamente este síntoma, se encontró que 9,3% de los pacientes (1.283/13.783) reportaron vértigo luego de la implantación coclear21. Sin embargo, como síntoma nuevo en el posoperatorio, en los 31 estudios que lo reportaron, el síntoma estuvo presente en 17,4%21; valor cercano al que encontramos en nuestra serie. Incluso al investigar el síntoma en el preoperatorio, los investigadores encontraron que, entre 32 reportes, 24,7% de los pacientes (451/1.827) refirieron vértigo21. Este hallazgo es interesante y puede ser explicado porque la misma patología que causa la hipoacusia, genera una lesión activa o daño permanente de los receptores vestibulares, llevando a síntomas vestibulares persistentes. Aunque no registramos el vértigo/inestabilidad preoperatoria, es de esperar que un grupo de los pacientes lo hayan tenido, ya que hubo casos de sordera súbita, enfermedad de Ménière y ototoxicidad; que pueden tener una lesión vestibular activa o un daño permanente a los receptores vestibulares. Otro factor que puede también explicar la alta frecuencia de vértigo/inestabilidad en nuestra serie, es que se trata de una población con edad media de implantación relativamente alta (49,8 ± 18,8); con 24 > 30 años y 18 > 50. En población adulta hay varios factores que contribuyen a la sintomatología vestibular luego de la implantación coclear, aparte del trauma quirúrgico, como son el daño previo de los receptores vestibulares por la patología otológica y la degeneración de los sistemas relacionados con el equilibrio (presbivértigo)21. En pacientes > 18 años, el metaanálisis de Hänsel et al., muestra una prevalencia de vértigo posoperatorio de 16,8% (446/2.651) y se encontró una clara correlación entre la presencia de vértigo y una mayor edad de implantación21; resultados que son comparables a los que encontramos en nuestra serie. Como complicación mayor posoperatoria encontramos un paciente con fallo técnico del implante (hard failure), equivalente a 3,23% (1/31). En la revisión de Carlson se reporta una prevalencia de complicaciones mayores de 2,7% (207/7.542); con una frecuencia media de fallo técnico del IC = 1,9% (125/6.461), entre los siete artículos que reportan esta información (rango = 0,2-6,0%)1. Al evaluar el fallo en IC el periodo de seguimiento es un factor relevante, ya que se esperará mayor frecuencia de fallos a medida que el seguimiento se prolongue. Por ejemplo, en un grupo de pacientes operados en un periodo de 30 años (mediana de seguimiento = 4,8), la frecuencia de fallos del IC fue 4,8% (136/2.827); siendo 3,9% fallos técnicos que no permiten el funcionamiento del implante (hard failure) y 0,9% fallos técnicos «suaves» (soft failures)22. Estos fallos se presentaron ∼ 5 años luego de la cirugía (niños = 5,5 años, adultos = 5,3)22, lo que refuerza la importancia del periodo de seguimiento a la hora de valorar esta complicación. Por lo tanto, vemos que con el seguimiento de mediano plazo que reportamos, la frecuencia de fallo técnico de 3,23% es superior a lo reportado en estudios con seguimiento equiparable y es un aspecto que debe seguir observándose.
Con respecto a complicaciones usando la marca específica Nurotron™, no se dispone de información clara ni suficiente, dado que es una marca relativamente nueva en el mercado (11 años de utilización clínica) y los estudios publicados son limitados. Zeng et al., no registraron información acerca de complicaciones ni fallos del dispositivo8. Li et al.23 y Yu et al.,24 refieren de forma difusa que durante el seguimiento (dos y tres años, respectivamente), no hubo infección, ni extrusión ni complicaciones ni efectos adversos relacionadas con el IC Nurotron™; sin embargo, no se observa en estos sistematicidad metodológica para recolectar información sobre complicaciones. Rebscher et al., solo mencionan complicaciones durante la inserción del electrodo en pruebas en huesos temporales, con una frecuencia de trauma severo con la inserción de 12,5% (ocho especímenes)25. Otras investigaciones clínicas tampoco describen complicaciones con el uso de esta marca de IC, ni mencionan fallos del dispositivo18,26–30. El análisis del implante que presentó fallo técnico por parte del fabricante reportó un daño electrónico. En la revisión de 136 implantes cocleares que presentaron fallos, Wang et al.22, encontraron daños en los componentes electrónicos en 19,5% de los 77 dispositivos que tuvieron análisis por parte del fabricante. En dicho estudio la causa más frecuente de fallo del dispositivo fue daño en la serie de electrodos con 48,1%.
La disponibilidad de una marca adicional de IC genera una mayor oferta y puede mejorar el acceso, en especial en países en desarrollo donde el costo del tratamiento en un factor importante para su consecución. Esto se ejemplifica bien en un proceso de licitación, usado con frecuencia para la compra de estos dispositivos, en donde «la puja» con un oferente más puede llevar a que para una cantidad fija de dinero se consigan más dispositivos. En nuestro país que tenemos la opción de usar cinco marcas de IC (Advanced Bionics™ [Advanced Bionics LLC, Valencia, CA, Estados Unidos], Cochlear™ [Cochlear LTD, Sydney, NSW, Australia], Medel™ [MED-EL Medical Electronics, Innsbruck, Austria], Nurotron™ y Oticon™ [Oticon Medical/Neurelec SAS, Vallauris, Francia]); encontramos que Nurotron™ tiene un costo ∼ 20% inferior al promedio de las otras marcas.
Como conclusiones encontramos que entre pacientes adultos postlinguales hispanohablantes, el IC Nurotron™ presenta unos resultados audiológicos satisfactorios y concordantes con los reportados con otras marcas de IC en grupos poblacionales similares. Nuestros hallazgos replican los resultados de estudios con hablantes nativos de mandarín que se han publicado con Nurotron™. También encontramos una importante reducción del tinnitus con el uso del IC. En cuanto a seguridad clínica, con un seguimiento de mediano plazo, encontramos que las complicaciones menores son concordantes a las reportadas en la literatura, aunque se debe seguir con atención el porcentaje de fallo técnico que fue superior a lo reportado en otras series con periodo de seguimiento equiparable. El vértigo/inestabilidad posoperatoria fue un poco más frecuente, debido en parte a las características clínicas de la población de estudio. Como limitantes del presente debemos mencionar la naturaleza descriptiva de su diseño, la falta de mediciones audiológicas en fondo ruidoso y de mediciones de calidad de vida; que actualmente son muy importantes a la hora de evaluar un tratamiento como el IC. Se requieren estudios en otros grupos poblacionales y con periodos de seguimiento más prolongados, que corroboren los resultados audiológicos y de seguridad clínica, tanto del nuestro como de los reportados con pacientes hablantes nativos de mandarín.
FinanciaciónLa presente investigación no ha recibido ayudas específicas provenientes de agencias del sector público, sector comercial o entidades sin ánimo de lucro. El estudio fue aprobado por el comité de ética e investigación de la institución participante (código: CEIFUS 3300-22; acta Núm. 045-22).
Conflictos de interesesLos autores declaran no tener ningún conflicto de intereses.
Al Doctor Jorge Medina del departamento de investigación de Unisanitas-Clínica Universitaria Colombia por su apoyo durante el proceso de preparación de este trabajo.
Resultados preliminares presentados en: 11th Asia Pacific Symposium on Cochlear Implants and Related Sciences. Cyprus – September 19 -22, 2017. Resumen publicado en: Ordóñez-Ordóñez LE, Angulo-Martínez ES, Rodriguez SR, Vanegas SC. Clinical Safety and Outcomes with Nurotron™ Cochlear Implant in Spanish Speaking Patients. J Otolaryngol ENT Res. 2017;9(2): 00280. DOI:10.15406/joentr.2017.09.00280.