INTRODUCCION
En una publicación anterior, se demostró que los antígenos de las heces del murciélago (Tadarida brasiliensis) eran capaces de inducir la síntesis de anticuerpos específicos IgG en conejos e IgE en humanos a los que se les atribuyó algún papel en el 25 % de los que sufrían el síndrome rinitis/asma1.
En este trabajo se presenta la inducción de una neumonitis por hipersensibilidad en cobayos con dichos antígenos para valorar la respuesta inmune específica por la vía inhalatoria habida cuenta de las limitaciones éticas para emplear un antígeno nuevo en la prueba desencadenante bronquial (challenge) y valorar los hallazgos en el BAL de asmáticos atópicos.
MATERIALES Y MÉTODOS
Antígeno
Las heces de los murciélagos (BAT) se obtuvieron de los taparrollos o de las partes internas de las persianas de enrollar de las viviendas de los pisos altos de las casas de departamentos habitados por nuestros pacientes. Su aspecto macroscópico es el de granitos de arroz de color negro con un olor desagradable. Cada partícula fue tomada con una pinza metálica y guardada en un recipiente estéril a 20 °C. Cuando se obtuvieron 20 g, el material fue procesado según la técnica de Frugoni-Hansen para los aero-alergenos, con ligeras modificaciones. Así, en vez de emplear la solución de Coca (ClNa: 5 g; CO3HNa: 2,75 g; fenol: 4 g; agua destilada 1.000 ml) se utilizó la de Stier-Hollister (ClNa: 7 g; glicerina: 46 ml; agua destilada 47 ml, a razón de 5 g del extracto por cada 100 ml de la solución extractora) para evitar un posible efecto deletéreo del fenol sobre las proteínas del extracto a obtener2. Con la técnica de Bradford se valoraron las proteínas mientras que las hexosas fueron determinadas por el método del indol empleando una mezcla de galactosa y manosa como estándar al medir en el espectrofotómetro a 470 nm de densidad óptica3,4.
Fraccionamiento por columna de Sephadex
Se utilizó una columna de Sephadex G-150 de 780 mm por 22 mm que se equilibró y se eluyó con buffer fosfato y ClNa 0,15 M a pH 8 y a 4 °C. Tres y medio mililitros del BAT (70 mg de proteínas) fueron sembrados y alícuotas de un mililitro del eluído fueron recogidas en el colector de fracciones con una velocidad de 20 ml/min. Las proteínas de cada eluído fue determinadas por absorbancia a 280 nm en el espectrofotómetro4.
Técnicas inmunológicas
La presencia de IgG e IgM en los cobayos aerosolizados se detectó por las técnicas de Ouchterlony y de Boyden. En la primera, los sueros no se diluyeron mientras que en la segunda fueron diluídos hasta 1:1024. El BAT fue concentrado hasta 10 mg/ml de proteínas puras por perevaporación. El MIF diagnosticó LT sensibilizados realizando los experimentos por duplicado y empleando concentraciones variables del BAT (10, 100 y 500 μg/ml). Todos los animales fueron testificados con 100 μg del BAT en 0.10 ml de PBS en una zona rasurada del dorso 48 hs antes de su sacrificio midiéndose la induración producida. El Ovary-Bier determinó la presencia de anticuerpos citofílicos en los sueros sin diluir de los cobayos mientras que el BAT (10 mg/ml) se empleó con el azul de Evans por la vía venosa5-9.
Animales de experimentación
Treinta y seis cobayos adultos de 250-300 g de peso, vírgenes de todo tratamiento, fueron aerosolizados durante 12 semanas con el BAT. Cada grupo de 6 animales fue colocado en una cámara de vidrio de un volúmen de 6.000 cm3 conectada a un nebulizador ultrasónico que aerosolizaba los 10 ml del antígeno en partículas de 3 μen 30 minutos. El antígeno estaba compuesto por 1 ml del concentrado (11 mg) diluído en 9 ml de PBS esterilizado por filtros Millipore de 0.22μ. Este procedimiento se repitió 6 veces para completar los 36 cobayos del grupo experimental. El grupo control recibió la aerosolización diaria de 10 ml de PBS estéril. Semanalmente, una hora después de finalizada la aerosolización, un grupo de 3 animales fue sacrificado bajo anestesia profunda con éter etílico, sangrados a blanco, extraídos sus órganos para el estudio histopatológico, fraccionados los sueros en tubos a 20 °C y los linfocitos separados con un gradiente de Ficoll-Hypaque. Idéntico procedimiento se desarrolló con los cobayos del grupo control.
Histopatología
Se realizó sobre los cortes de pulmón, riñón, bazo e hígado de los cobayos de los grupos experimental y control. Los órganos fijados con Bouin, se montaron en parafina, se cortaron en secciones de 6 μy se colorearon con hematoxilina-eosina, PAS, azul de toluidina al 1 % y tricrómico de Mallory. La evidencia histopatológica de una alveolitis alérgica extrínseca se basó en el trípode constituído por la bronquiolitis celular, los infiltrados intersticiales y los granulomas solitarios no caseosos. Se valoró la presencia de células gigantes multinucleadas, de células espumosas intraalveolares, de neumonía organizada, de bronquiolitis obliterante y de fibrosis intersticial, clasificando la intensidad de la inflamación desde 1 + hasta 5 + .
Así, el grupo de 1 + involucró a la bronquiolitis celular con infiltrados de linfocitos y plasmocitos de intensidad diversa a lo largo de los bronquiolos sin invadir los sacos alveolares mientras el epitelio bronquiolar permaneció intacto con escaso exudado en la luz. Las lesiones codificadas con 2 + mostraron infiltrados intersticiales linfoplasmocitarios que variaron desde moderados a densos con paredes alveolares engrosadas.
El tipo de 3 + agregó los granulomas solitarios, no necrotizantes repartidos desordenadamente en el parénquima, en las paredes bronquiolares y alveolares; nunca éstos granulomas involucraron a los vasos sanguíneos. Las lesiones rotuladas con 4 + presentaron acúmulos de histiocitos en los alvéolos que imitaban granulomas (histiocitos epitelioides) con o sin células gigantes, cristales de colesterol, cuerpos de Schaumann e inclusiones asteroides. Por fin, las lesiones de 5 + asociaron neumonía organizada, bronquiolitis obliterante y fibrosis intersticial.
Las microfotografías obtenidas y expuestas fueron tomadas con un fotomicrosocopio con aumentos de 100X, 400X y 1000X y con una película Kodakcolor de 100° Asa.
RESULTADOS
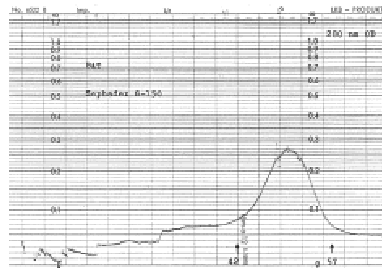
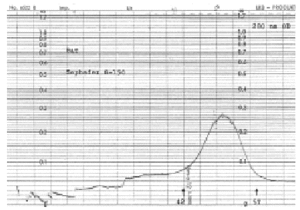
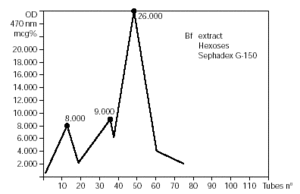
El fraccionamiento por columna de Sephadex G-150 del BAT permitió obtener un pico proteico entre los tubos 42 y 57 y tres picos de hexosas en los tubos 13, 36 y 48. El Bradford determinó los siguientes contenidos proteicos: el BAT: 20 mg/ml y los tubos 42-57: 15 mg/ml.
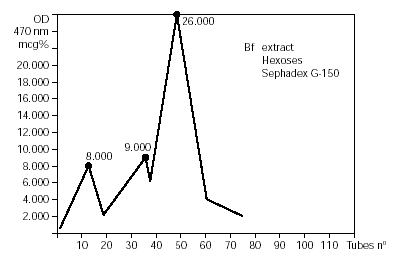
El indol estableció los siguientes contenidos de azúcares: el BAT: 50 mg %; el tubo 13: 13,8 mg %; el tubo 36: 9 mg % y el tubo 48: 26 mg % (figs. 1 y 2).
Figura 1.--Fraccionamiento del BAT por columna de Sephadex G-150. Se observa un pico proteico entre los tubos 42 y 57.
Figura 2.--Gráfico de las concentraciones de hexosas en los diferentes tubos del fraccionamiento.
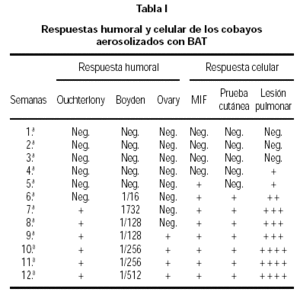
Los resultados del Ouchterlony, Boyden, Ovary-Bier, intradermorreacción tardía e histopatología pulmonar se resúmen en la tabla I (figs. 3 y 4).
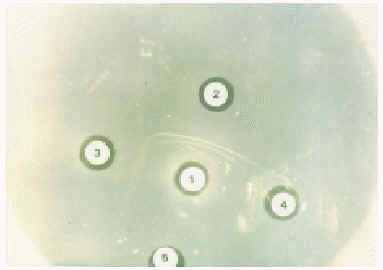
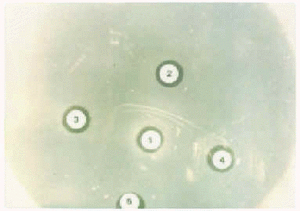
Figura 3.--Prueba de Ouchterlony. 1) suero de cobayo anti-BAT; 2) BAT; 3) fracción 42-57; 4) pelo de murciélago; 5) pelo de rata. Se observan bandas de precipitación entre el suero y sus antígenos con identidad total.
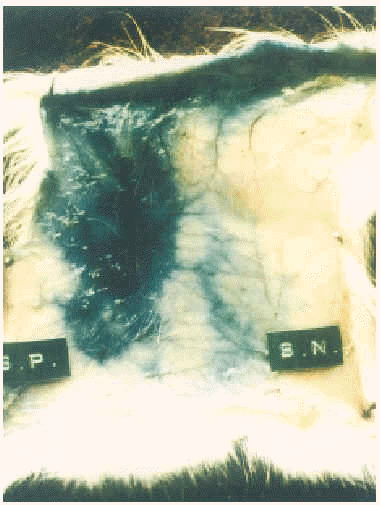
Figura 4.--Test de Ovary-Bier. SP: suero de cobayo anti-BAT; SN: suero normal de cobayo. Se observa una reacción positiva (manchas azules) con el suero anti-BAT.
No se observaron lesiones en los pulmones, riñones, bazo e hígado de los animales controles. En el grupo experimental, no se observaron cambios durante las 2 primeras semanas de aerosolización aunque aumentó el patrón descamativo de los bronquiolos. A partir de la 3.ª semana se observó una bronquiolitis celular con predominio linfoplasmocitario. Este infiltrado intersticial varió desde moderado a denso (2 +) con engrosamiento de las paredes alveolares incrementándose desde la 6.ª hasta la 9.ª semanas. Desde la 10.ª semana hasta el final del experimento, las lesiones pulmonares empeoraron progresivamente. Los infiltrados se hicieron más densos (3 + y 4 +) con la aparición de los granulomas solitarios no caseosos (tabla I).
El azul de toluidina no reveló células metacromáticas (mastocitos) tanto en los pulmones del grupo experimental como del control; el PAS evidenció un engrosamiento de las membranas basales, especialmente, en los pulmones y en los riñones (figs. 5-7).
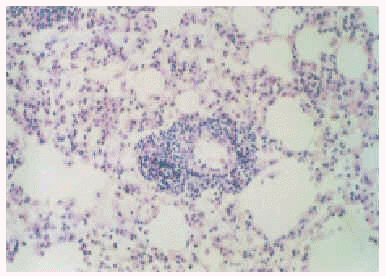
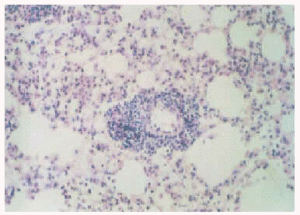
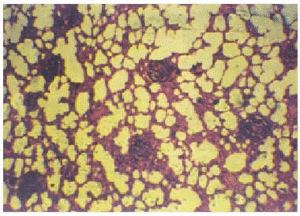
Figura 5.--Histopatología del pulmón de cobayo con infiltrados celulares en los tabiques interalveolares y alrededor de los bronquiolos (HE x 100).
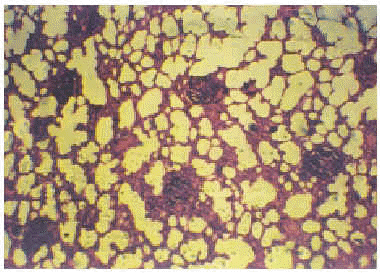
Figura 6.--Histopatología del pulmón de cobayo donde se observan granulomas solitarios no caseosos e infiltrados intersticiales (HE x 400).
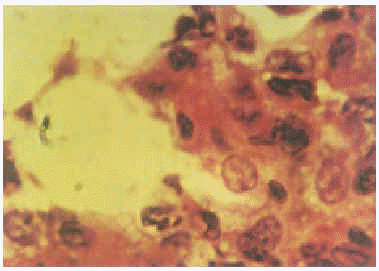
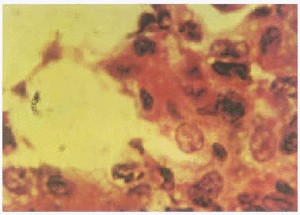
Figura 7.--Histopatología del pulmón del cobayo donde se observan células espumosas ("foamy") en el infiltrado de los tabiques alveolares (HE x 1000).
DISCUSION
Los extractos de heces están involucrados en varias condiciones inmunopatológicas, tales como, el pulmón del colombófilo, aunque los epitopes antigénicos precisos que gatillan la hipersensibilidad no estén muy bien precisados aún. En este caso, las heces de los murciélagos que se refugian en los taparrollos de las ventanas de los departamentos de Buenos Aires demuestra poseer inmunogenicidad en un modelo animal, así como, en los humanos atópicos que sufren de rinitis perenne y de asma bronquial.
Estos asertos están avalados por la detección de anticuerpos específicos IgG y de linfocitos y macrófagos en el modelo animal y de IgE en los pacientes estudiados y no en los animales o humanos de los grupos controles. Por otra parte, este antígeno no experimentó ninguna reactividad cruzada con el pelo del murciélago, el suero y los pelos y escamas de las ratas y las heces de las palomas. Se está desarrollando el análisis del antígeno por SDS-PAGE, Western-blot e isoelectroenfoque al igual que el estudio de sus propiedades proteásicas y gelatinolíticas y su posible vinculación con la inmunogenicidad. El suero del murciélago es muy dificil de conseguir por su escasa cantidad en el mamífero, pero se hace imprescindible el lograrlo para valorar si la IgA, que pudiera haber en esas heces (IgA-secretoria) pudiera jugar un papel en la antigenicidad y/o contaminación del extracto total18.
El BAT mostró un único pico proteico con un elevado contenido de azúcares, tal como, reveló el estudio cromatográfico. Esta composición glucoproteica refuerza nuestra sospecha que las proteínas del suero del murciélago podrían jugar algún papel en su inmunogenicidad, al igual que, otras estructuras o sustancias pertenecientes al intestino del quiróptero tal como se sostiene con la tropomiosina. El papel de las endotoxinas de la flora intestinal del murciélago debería evaluarse en atención a recientes hallazgos vinculados con su influencia en el paradigma TH1-TH2. Su rol en el desarrollo de lesiones pulmonares por inhalación crónica (modelo animal) se presta para una mayor profundización de la investigación.
Estos datos confirman que el BAT podría comportarse como un antígeno inhalatorio de ciertos habitats domiciliarios, que, en el 25 % de una población de atópicos respiratorios sería capaz de producir anticuerpos IgE cuya especificidad fuera asegurada por el RAST-inhibición.
Las pruebas desencadenantes nasales y bronquiales (challenge) no se realizaron por razones eticas hasta conocer más acabadamente las propiedades fisicoquímicas del antígeno.
Como fuere, el epitelio, la orina y la saliva de los murciélagos deberán ser estudiados para valorar su participación en la generación de anticuerpos específicos, pensando en aquellos laboratoristas que están expuestos permanentemente en la confección de los cultivos celulares para las vacunas antirrábicas8.
Es posible que esta sea la primera comunicación mediante la cual se documentan los hallazgos obtenidos luego de la exposición crónica de cobayos al BAT con la producción de una típica alveolitis alérgica extrínseca (neumonitis por hipersensibilidad) y pruebas cutáneas tardías positivas con induración.
La síntesis de anticuerpos específicos del isotipo IgG y la eventual formación de complejos inmunes BAT- IgG- anti- BAT podrían incrementar la activación de los macrófagos a través de sus receptores para los Fc (CD16, CD32 y CD64), y, así contribuir a la formación de los granulomas solitarios no caseosos típicos de la lesión avanzada de la 10.ª semana del experimento.
La ausencia de células metacromáticas (mastocitos) en esta inflamación pulmonar resulta llamativa habida cuenta de su participación en otros modelos inflamatorios crónicos y autoinmunes conocidos (v.g. artritis reumatoidea, encefalomielitis alérgica experimental y enfermedades desmielinizantes) como elemento perpetuador y amplificador de la respuesta a través de la liberación de mediadores vasoactivos y citoquinas proinflamatorias10-17.
Los atópicos con hobbies o profesiones ecológicas como espeleólogos, arqueólogos y naturalistas se hallan en riesgo de sufrir un ataque de asma ante la inhalación brusca de grandes cantidades del antígeno en las cuevas de las montañas, si estuvieran sensibilizados previamente19.