Puntos clave
La lactoferrina (Lf) es una glucoproteína bilobulada de la familia de las transferrinas de 78kDa presente en la leche de mujer1. También se encuentra en otros fluidos orgánicos, como en las secreciones pancreáticas y bronquiales. La concentración de Lf en la leche de mujer es de 1-2g/l, mientras que en la leche de vaca es de 20-200mg/l.
Las funciones (estudiadas in vitro y en animales) que se atribuyen a la Lf son:
- —
Facilita la absorción intestinal de hierro y otros metales: al ser una proteína que pertenece a la familia de las transferrinas, su función principal es la unión a moléculas de hierro, y puede unir de forma reversible 2 moléculas de hierro, con mayor afinidad que la transferrina2–5.
- —
Estimula el crecimiento: en ratas se ha demostrado que promueve el crecimiento de la mucosa intestinal y de los hematíes6,7.
- —
Inmunomodulación: induce la producción de citocinas antiinflamatorias (interleucina [IL] 4, IL-10) y la formación de anticuerpos. Disminuye la producción de citocinas proinflamatorias (factor de necrosis tumoral alfa, IL-1β)8.
- —
Actividad antibacteriana, antiviral y antifúngica: inhibe el crecimiento de agentes patógenos9.
- —
Regula la flora intestinal: algunas bacterias anaerobias (Clostridium y Bacteroides) precisan el hierro para realizar reacciones de oxidación-reducción intracelulares. La unión del hierro a la Lf favorece un descenso en los valores de hierro disponibles para estas bacterias, regulando la flora intestinal dependiente de hierro10.
- —
Actividad antioxidante: su capacidad de ligar moléculas de hierro disminuye la concentración libre de Fe y su poder oxidativo11.
La Lf es una de las proteínas más abundantes en la leche de mujer, mientras que la concentración en la leche de vaca es más baja y es prácticamente nula en las fórmulas de inicio. En los Ultimos años, se ha pensado la posibilidad de añadir Lf a las fórmulas de inicio, para de este modo poder proporcionar los posibles efectos beneficiosos de esta proteína. La adición de Lf se realiza mediante Lf bovina, que presenta una secuencia similar a la humana en un 69%. Tanto la Lf humana como la bovina sobreviven a la acción digestiva del jugo gástrico y fermentos pancreáticos, ya que se detectan en las heces12. La digestión parcial de Lf bovina dentro del tracto gastrointestinal conduce a la liberación de péptidos catiónicos, como la lactoferricina, que presenta una alta actividad antimicrobiana mayor que la Lf humana13.
se han realizado algunos ensayos clínicos para evaluar los beneficios de la adición de Lf bovina a las fórmulas de inicio (tabla 1). El objetivo de este trabajo es realizar una revisión de la bibliografía médica disponible al respecto, para determinar si hay alguna ventaja en añadir esta proteína a las fórmulas infantiles.
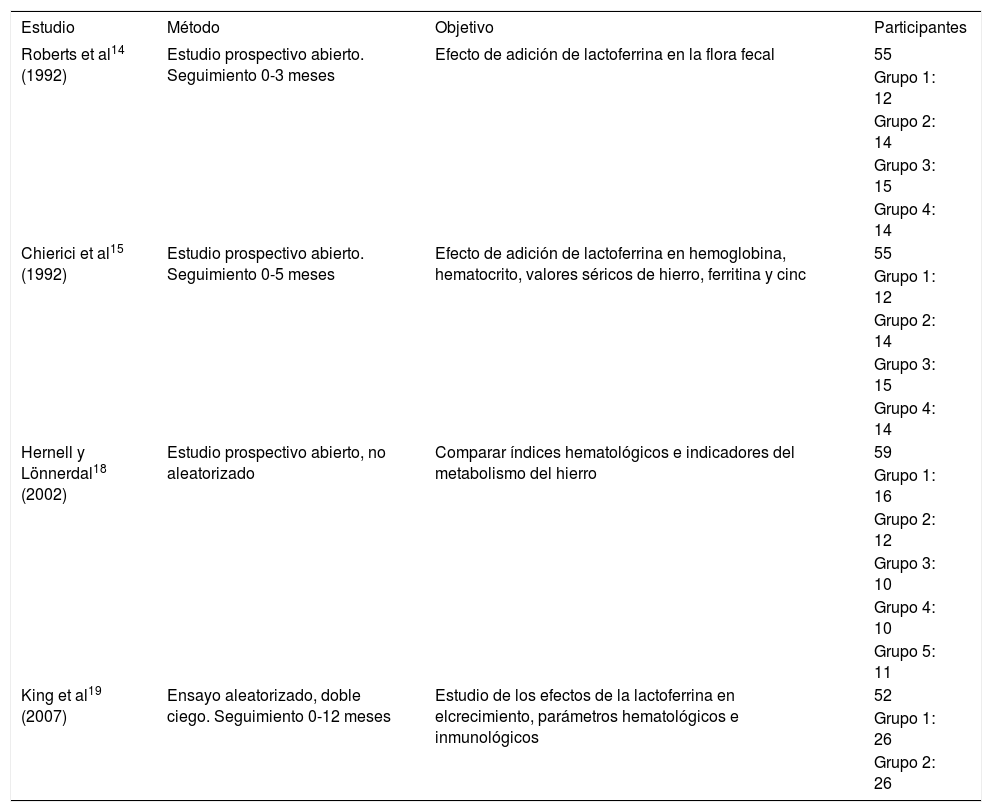
Resumen de los trabajos realizados con adición de lactoferrina bovina a las fórmulas infantiles
| Estudio | Método | Objetivo | Participantes |
|---|---|---|---|
| Roberts et al14 (1992) | Estudio prospectivo abierto. Seguimiento 0-3 meses | Efecto de adición de lactoferrina en la flora fecal | 55 |
| Grupo 1: 12 | |||
| Grupo 2: 14 | |||
| Grupo 3: 15 | |||
| Grupo 4: 14 | |||
| Chierici et al15 (1992) | Estudio prospectivo abierto. Seguimiento 0-5 meses | Efecto de adición de lactoferrina en hemoglobina, hematocrito, valores séricos de hierro, ferritina y cinc | 55 |
| Grupo 1: 12 | |||
| Grupo 2: 14 | |||
| Grupo 3: 15 | |||
| Grupo 4: 14 | |||
| Hernell y Lönnerdal18 (2002) | Estudio prospectivo abierto, no aleatorizado | Comparar índices hematológicos e indicadores del metabolismo del hierro | 59 |
| Grupo 1: 16 | |||
| Grupo 2: 12 | |||
| Grupo 3: 10 | |||
| Grupo 4: 10 | |||
| Grupo 5: 11 | |||
| King et al19 (2007) | Ensayo aleatorizado, doble ciego. Seguimiento 0-12 meses | Estudio de los efectos de la lactoferrina en elcrecimiento, parámetros hematológicos e inmunológicos | 52 |
| Grupo 1: 26 | |||
| Grupo 2: 26 |
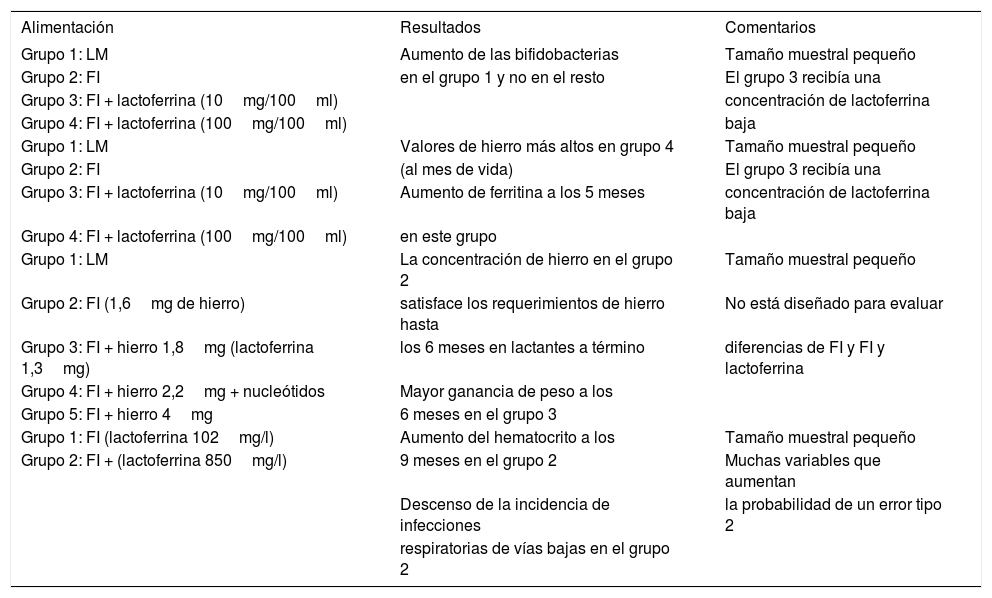
FI: fórmula de inicio; LM: lactancia materna
Se trata de un estudio prospectivo, abierto, realizado en neonatos durante los 3 primeros meses de vida. se realizaron 4 grupos: 12 lactantes alimentados con lactancia materna, 14 con fórmula de inicio, 15 con fórmula de inicio suplementada con 10mg/100ml de Lf bovina, y 14 lactantes con fórmula de inicio suplementada con 100mg/100ml de Lf bovina. Se recogieron coprocultivos y se midió el pH fecal a la primera semana, al mes de vida y a los 3 meses. En los resultados se observó un aumento de las bifidobacterias y un descenso de los anaerobios facultativos en los niños alimentados con lactancia materna al mes de vida, sin observarse en el resto de los grupos. El grupo de lactantes que recibió suplemento con 100mg/100ml de Lf bovina presentó en el 57% de los niños una flora fecal bifidógena al tercer mes de vida, aunque los gérmenes Clostridium sp. y Bacteroides sp. eran comunes en las heces de los niños que recibían ambas fórmulas que contenían Lf.
| Alimentación | Resultados | Comentarios |
|---|---|---|
| Grupo 1: LM | Aumento de las bifidobacterias | Tamaño muestral pequeño |
| Grupo 2: FI | en el grupo 1 y no en el resto | El grupo 3 recibía una |
| Grupo 3: FI + lactoferrina (10mg/100ml) | concentración de lactoferrina | |
| Grupo 4: FI + lactoferrina (100mg/100ml) | baja | |
| Grupo 1: LM | Valores de hierro más altos en grupo 4 | Tamaño muestral pequeño |
| Grupo 2: FI | (al mes de vida) | El grupo 3 recibía una |
| Grupo 3: FI + lactoferrina (10mg/100ml) | Aumento de ferritina a los 5 meses | concentración de lactoferrina baja |
| Grupo 4: FI + lactoferrina (100mg/100ml) | en este grupo | |
| Grupo 1: LM | La concentración de hierro en el grupo 2 | Tamaño muestral pequeño |
| Grupo 2: FI (1,6mg de hierro) | satisface los requerimientos de hierro hasta | No está diseñado para evaluar |
| Grupo 3: FI + hierro 1,8mg (lactoferrina 1,3mg) | los 6 meses en lactantes a término | diferencias de FI y FI y lactoferrina |
| Grupo 4: FI + hierro 2,2mg + nucleótidos | Mayor ganancia de peso a los | |
| Grupo 5: FI + hierro 4mg | 6 meses en el grupo 3 | |
| Grupo 1: FI (lactoferrina 102mg/l) | Aumento del hematocrito a los | Tamaño muestral pequeño |
| Grupo 2: FI + (lactoferrina 850mg/l) | 9 meses en el grupo 2 | Muchas variables que aumentan |
| Descenso de la incidencia de infecciones | la probabilidad de un error tipo 2 | |
| respiratorias de vías bajas en el grupo 2 |
Este estudio forma parte del anterior, y prolonga la adición de Lf y los controles hasta los 5 meses. Se realizaron controles analíticos al nacimiento, a la semana, al mes, a los 3 meses y a los 5 meses. Se determinaron: hemoglobina, hematocrito, valores séricos de hierro, ferritina y cinc. En los resultados se observaron diferencias estadísticamente significativas en los valores de hierro al mes de vida, siendo más elevados en los niños alimentados con fórmula infantil suplementada con 100mg/100ml de Lf (p = 0,04) y un incremento en los valores de ferritina en este grupo de lactantes a los 5 meses de vida (p = 0,02).
El diseño de este trabajo fue abierto, no aleatorizado, e incluyó a 59 lactantes, nacidos a término, que recibieron lactancia materna hasta una edad de 4 ± 2 semanas. Los objetivos del trabajo fueron comparar los índices hematológicos y los indicadores del metabolismo del hierro en lactantes con lactancia materna, o alimentados con fórmula infantil, con concentraciones de hierro de 2-4mg/l, así como evaluar los efectos de administrar parte del hierro en forma de Lf bovina o de adicionar nucleótidos. Se realizaron 5 grupos: 16 lactantes con lactancia materna exclusiva, 12 con fórmula de inicio experimental con contenido de hierro 1,6mg/l, 10 con fórmula de inicio experimental conteniendo 1,8mg/l de hierro, del cual 1,3mg era Lf bovina, 10 que recibieron fórmula de inicio experimental con 2,2mg/l de hierro fortificada con nucleótidos y, por último, 11 con fórmula de inicio con 4mg/l de hierro. Se tomaron medidas antropométricas mensuales y se determinaron índices hematológicos, valores de hierro, cinc, cobre y ácidos grasos en hematíes al mes, a los 4 y a los 6 meses. Los autores concluyen que una concentración de 1,6mg/l de hierro en las fórmulas infantiles satisface los requerimientos de los lactantes a término hasta los 6 meses, por lo que resulta innecesaria la adición de una aportación mayor de hierro. La fortificación con Lf bovina o nucleótidos no aumentó los valores de hierro y ácidos grasos de los hematíes, pero sí se observó más ganancia de peso (estadísticamente significativa) a los 6 meses en el grupo con Lf.
Se trata de un ensayo aleatorizado, doble ciego. Incluye neonatos con ≥ 34 semanas de gestación y ≥ 2.000g de peso con ≤ 4 semanas de edad seguidos por un período de 12 meses. Se distribuyeron para recibir fórmula suplementada con Lf 850mg/l (grupo de tratamiento) o fórmula adaptada con 102mg/l de Lf (grupo control) durante 12 meses. Se recogieron variables antropométricas al mes, a los 2, 4, 6, 9 y 12 meses. Se valoró la presencia de enfermedades en el primer año de vida, como diarrea, infección respiratoria de vías altas, otitis media aguda e infección respiratoria de vías bajas. Se realizó analítica de sangre a los 9 y 12 meses de edad, en la que se determinaron parámetros hematológicos (hemoglobina, hematocrito y volumen corpuscular medio) e inmunológicos (anticuerpos de difteria, tétanos, Haemophilus influenzae tipo B y hepatitis B). De los 79 niños que iniciaron el estudio, 52 lo completaron (26 en grupo control y 26 en grupo de tratamiento). Los resultados obtenidos mostraron en el grupo de tratamiento un menor índice de infecciones respiratorias bajas en el primer año de vida y un incremento del hematocrito en el control analítico de los 9 meses, que fue estadísticamente significativo con respecto al grupo control (p < 0,05). No se observaron diferencias significativas en las variables antropométricas, aunque sí una tendencia a un aumento en el peso a los 6 meses de edad en el grupo de tratamiento (p = 0,06). No hubo diferencias en las variables inmunológicas estudiadas.
DiscusiónLa existencia de Lf en grandes cantidades en la leche de mujer y sus propiedades biológicas han sido el principal estímulo para estudiar el efecto de añadir Lf a las fórmulas infantiles. Los estudios publicados en la bibliografía son escasos, todos de pequeño tamaño muestral, que dificulta obtener resultados estadísticos fiables. Por otro lado, los objetivos estudiados sobre la adición de Lf a las fórmulas infantiles han sido diversos: parámetros hematológicos, flora fecal, parámetros antropométricos, inmunológicos o disminución de las infecciones en el primer año de vida.
En el trabajo de Roberts et al14, se investigó, in vivo, la capacidad bacteriostática de la Lf bovina añadida a fórmulas infantiles, a diversa concentración. Para ello, estudiaron intensivamente la flora fecal de lactantes, a la semana de vida, al mes y a los 3 meses. El método de referencia era la flora fecal de los lactantes con lactancia materna. Encontraron que a la semana de vida no había una clara preponderancia de ningún microorganismo en todos los grupos. Los lactados al pecho tenían bifidobacterias, enterococos y enterobacterias, patrón que cambiaba radicalmente al mes de vida en que la mayoría de este grupo presentaban una flora fecal dominada por bifidobacterias. Este cambio no se observó en los grupos de fórmula infantil ni en los grupos de fórmula suplementadas con Lf. En los que recibieron fórmula con suplemento de Lf bovina a 100mg/100ml se observó que, a los 3 meses, aproximadamente la mitad de los niños tenía un alto porcentaje de flora bifidógena, lo que implica una supresión de organismos facultativos, aunque con un alto porcentaje de colonización por Bacteroides sp. Los autores comentan la tardía respuesta, de dudoso efecto beneficioso para el lactante en la flora fecal. No obstante, en este trabajo se utiliza Lf bovina en concentraciones inferiores a las existentes en la leche madura humana, lo que unido a las diferencias de especie puede haber alterado los resultados.
El trabajo de chierici et al15 se trata de un estudio abierto, con los mismos grupos del anterior. Los objetivos fueron valorar los efectos de la adición de Lf bovina en los valores de cinc sérico, hierro sérico y ferritina, debido a que esta proteína permite valorar los depósitos de hierro. Al nacer, todos los grupos presentaron valores de cinc, hierro, hematocrito, hemoglobina y ferritina similares. En el grupo de lactancia materna, la ferritina sérica era significativamente mayor que el grupo que recibió fórmula infantil no suplementada con Lf bovina, tanto al mes como a los 3 meses. Los niños que recibieron fórmula infantil suplementada con Lf a 100mg/100ml presentaban valores de ferritina elevados, comparables con los lactados al pecho a los 3 meses y se mantuvieron elevados a los 150 días, desgraciadamente no pudieron compararse con los que recibieron lactancia materna, grupo que había disminuido en este período. Los valores de cinc no mostraron diferencias en todos los grupos, lo que indica, al igual que en otros trabajos realizados en ratas, que la absorción de cinc no está influida por la Lf bovina o humana.
Los valores altos de ferritina en el grupo suplementado con Lf a 100mg a los 3 y 5 meses apoya la hipótesis de que la Lf no es solamente una molécula transportadora del hierro, sino que favorece la absorción de éste. Hay trabajos realizados en niños recién nacidos a los que se administró fórmula con Lf bovina marcada con isótopo estable Fe58, frente a recién nacidos a los que se dio una fórmula estándar con cloruro férrico, y en los que se valoró la retención estimada del hierro, por el hierro excretado en las heces, sin encontrarse diferencias entre los 2 grupos, por lo que la Lf bovina no mejoró la biodisponibilidad del hierro16; en otro trabajo realizado en lactantes alimentados al pecho, a los que se administró leche humana intacta y leche humana a la que se había retirado la Lf, tampoco se encontró mayor incorporación del hierro en los hematíes en el grupo de lactantes que recibió leche materna sin modificar17. Estos resultados son discrepantes del trabajo de chierici et al15, los cuales, no obstante, comentan que sus resultados dejan abierta, mediante otros estudios, la necesidad de incorporación de Lf bovina a las fórmulas infantiles.
Hernell y Lönnerdal18 investigaron si la Lf bovina mejoraba los índices hematológicos y los indicadores del estado del hierro en niños que recibieron fórmulas infantiles de contenido bajo de este metal. La principal conclusión que se obtiene de este trabajo es que el suplemento de las fórmulas infantiles con aportes bajos de hierro son suficientes para los lactantes hasta los 6 meses de edad. Los inconvenientes de este estudio son que no está específicamente diseñado para valorar el efecto de adición de Lf bovina a las fórmulas, y que el escaso número de lactantes en cada grupo puede afectar a las conclusiones con un error estadístico de tipo 2. El estudio realizado por King et al19 es un estudio bien planteado, doble ciego, controlado con placebo, que presenta el inconveniente de la pérdida de un 34% de los lactantes inicialmente incluidos en el estudio; esto, unido a las numerosas variables estudiadas, hacen susceptible que los resultados pierdan significación estadística, por un error tipo 2. Los objetivos de este estudio piloto fueron valorar el impacto de la alimentación a largo plazo (1 año) de una fórmula suplementada con Lf bovina (850mg/l) en el crecimiento, los parámetros hematológicos y la frecuencia de enfermedades comunes en la primera infancia. En el grupo suplementado con Lf se encontró una tendencia estadística a un incremento de peso a los 6 meses, hecho reseñado en el estudio de Hernell y Lönnerdal18, menores episodios de enfermedades del tracto respiratorio inferior y aumentos significativos del hematocrito a los 9 meses, en relación con el grupo control que recibió una fórmula infantil estándar. La discusión realizada por los autores es excelente y rigurosa, en la que se indican cuáles son los puntos débiles y fuertes del trabajo, y se concluye diciendo que se precisan estudios más amplios y puntuales para indicar los posibles beneficios de añadir Lf bovina a las fórmulas infantiles.
ConclusionesPor el momento, los trabajos disponibles en la bibliografía no demuestran claros beneficios de la adición de Lf bovina a las fórmulas de inicio, aunque sí presentan datos prometedores para investigar las ventajas de la adición de Lf bovina a las fórmulas infantiles con grupos más amplios.