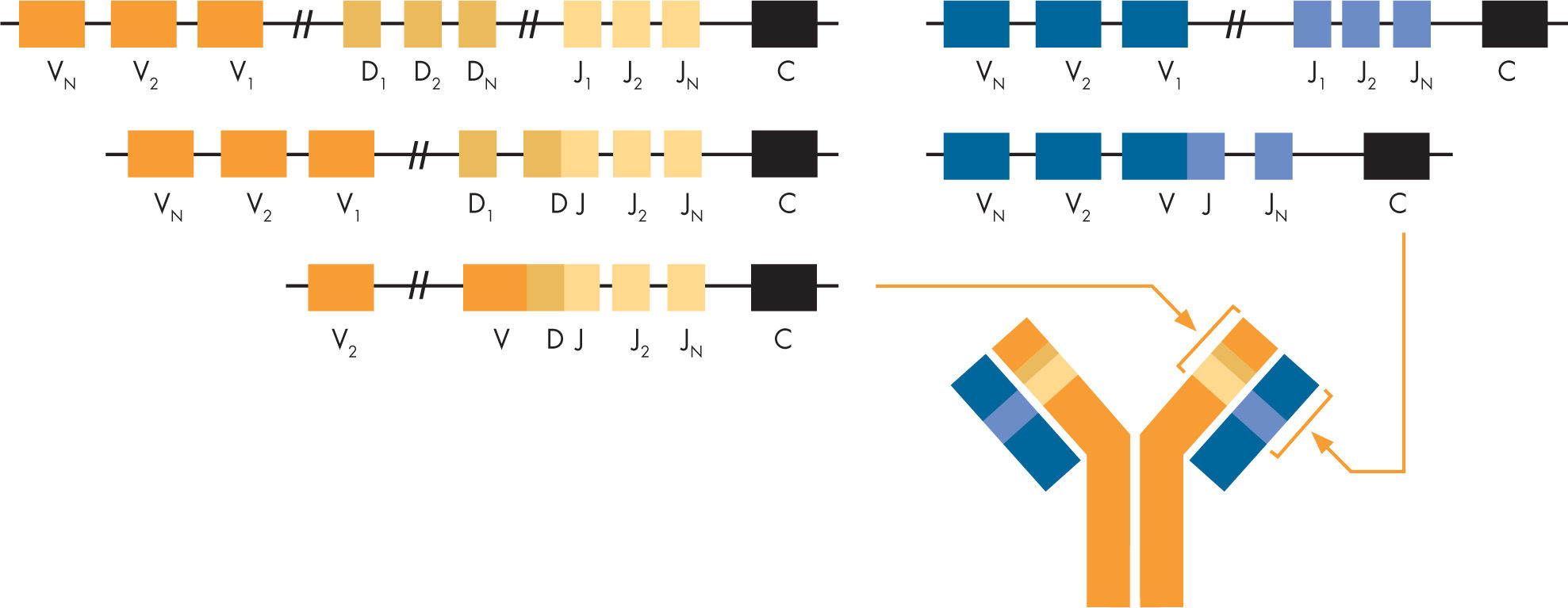Puntos clave
El cáncer es un grupo de aproximadamente unas 100 enfermedades caracterizadas por un hecho común: la expansión territorial de una clona de células mutada. La mutación de una sola célula y la subsiguiente expansión de la progenie —con la sucesiva acumulación de mutaciones y selección clonal— dan lugar al fenómeno clínico conocido como cáncer1. La diversidad de tipos de cáncer, la heterogeneidad de las alteraciones moleculares en el mismo tipo de tumor y entre las células de un mismo tumor y las múltiples combinaciones de mutaciones descritas en un número creciente de genes hacía prever una gran dificultad para explicar el fenómeno del cáncer en función de unos principios biológicos comunes. Sin embargo, se han descrito estos principios fundamentales o alteraciones mínimas de los mecanismos de regulación de la célula humana para adquirir el fenotipo tumorigénico2. Estos conocimientos permiten hoy afirmar que la célula tumoral, sea cual sea su origen, presenta un conjunto de cambios en su fisiología que son comunes a todos los tumores.
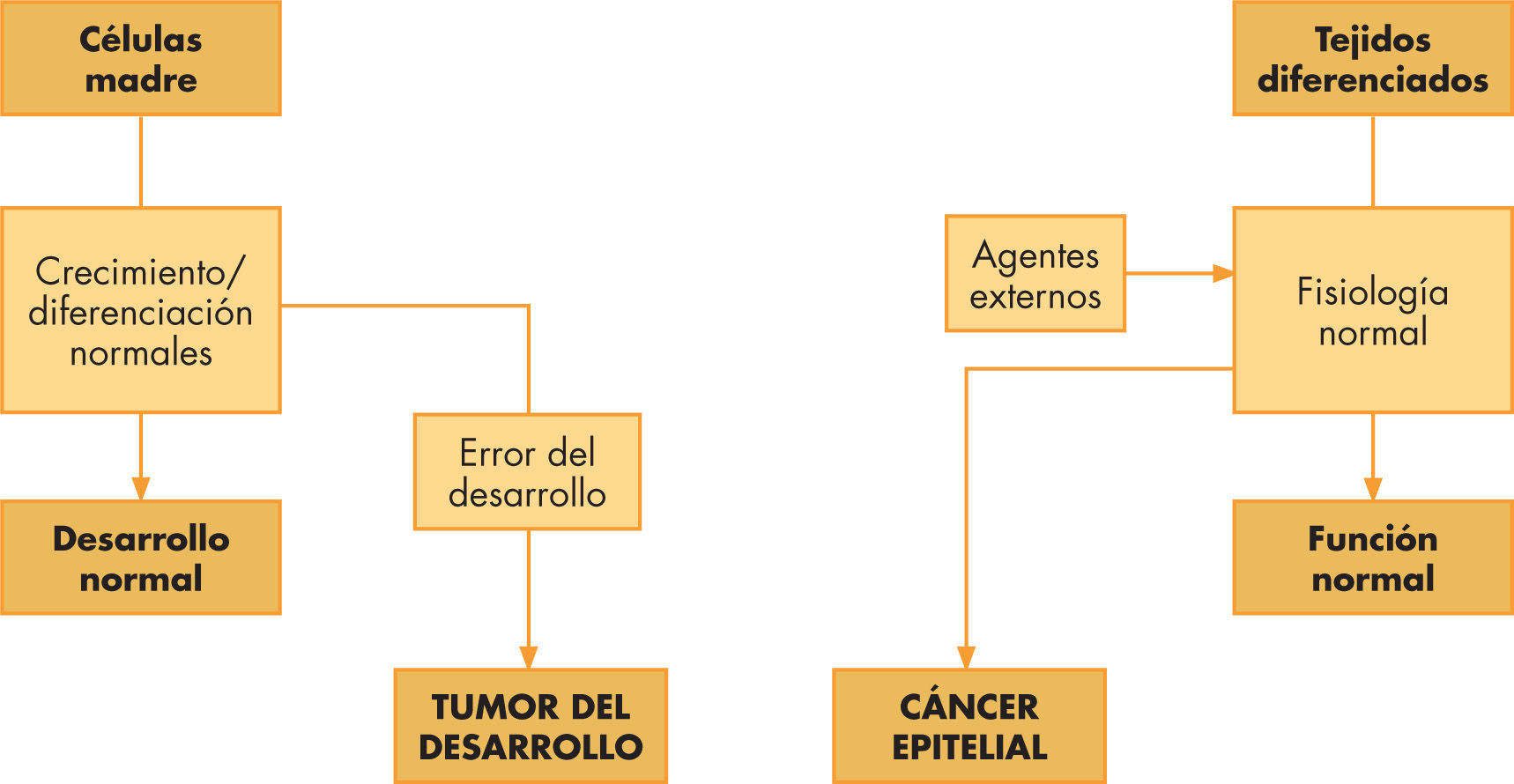
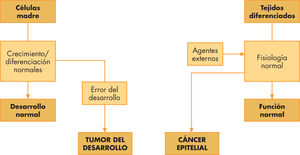
El término cáncer del desarrollo se refiere a los raros tumores que aparecen como consecuencia de las desviaciones del proceso normal de crecimiento y desarrollo de los tejidos3. Los tumores del desarrollo vienen determinados por el medio propicio que supone la transformación y proliferación del período del desarrollo, lo que explica las características únicas y diferenciales de estos tumores (fig. 1). Su incidencia es más elevada en el período posnatal y declina progresivamente hasta los 10 años de edad, lo que refleja sobre todo el comportamiento del subgrupo de tumores del desarrollo calificados como embrionarios. El tumor embrionario es aquel que se origina de poblaciones celulares que no han acabado el proceso de diferenciación durante el período del desarrollo fetal o posnatal. Estas células son conocidas como células blásticas, o blastémicas, y los tumores que se derivan se conocen como blastomas. Desde el punto de vista histológico estos tumores se caracterizan por células inmaduras, sin elementos morfológicos propios de los tejidos diferenciados, lo que hace que se los califique como primitivos o embrionarios.
El cáncer es un grupo de aproximadamente unas 100 enfermedades caracterizadas por un hecho común, la expansión territorial de una clona de células mutada. El término cáncer del desarrollo se refiere a los raros tumores que aparecen como consecuencia de desviaciones del proceso normal de crecimiento y desarrollo de los tejidos.
El cáncer que afecta a los niños y adolescentes es, en su gran mayoría, cáncer del desarrollo. A pesar de que la mayoría de los tumores del desarrollo responden a la quimioterapia, la curación, utilizando sólo quimioterapia, es imposible para la mayoría de los tumores. Curiosamente, sin embargo, para algunos tumores, como los tumores germinales, o los derivados de las células hematopoyéticas, la quimioterapia es curativa en la mayoría de casos, incluso para las presentaciones metastásicas.
Desde los años 1950, la quimioterapia se ha utilizado con éxito para tratar el cáncer y para algunos tumores permite su curación. Por ejemplo, el uso de únicamente metotrexato ha permitido curaciones hasta del 90% para los pacientes con coriocarcinoma4. Niveles de curación similares pueden obtenerse en pacientes con cáncer germinal con combinaciones de quimioterápicos. Las probabilidades de curación para los pacientes con enfermedad de Hodgkin tratados sólo con quimioterapia son aproximadamente del 80%5 y hasta un 70%, en conjunto, para los pacientes con linfomas no hodgkinianos (NHL)6.
La sensibilidad a la quimioterapia y el potencial de curación con el uso exclusivo de ésta en estos tumores contrasta con la situación de la mayoría de los tumores sólidos. A pesar de los descubrimientos de las últimas décadas, la lista de las neoplasias avanzadas que pueden curarse sólo con quimioterapia sigue sin cambios. Para los tumores sólidos metastásicos del adulto y del niño, la mayoría de los protocolos de quimioterapia combinada han conseguido prolongar los intervalos libres de enfermedad pero, en general, las posibilidades de curación siguen bajas7.
Los tumores quimiocurables se originan a partir de células que de manera fisiológica sufren reordenamientos genéticos y que retienen una gran sensibilidad a la inducción de apoptosis por daño del ADN, propio de las células de origen. La curabilidad de estos tumores depende, fundamentalmente, de su intrínseca sensibilidad a los estímulos proapoptóticos.
Aunque el tratamiento actual para la mayoría de los tumores potencialmente curables es la combinación de quimioterápicos, los primeros estudios en los años 1960-1970 demostraron que hay tumores que pueden curarse con el uso de un solo fármaco. La demostración más clara son las altas probabilidades de curación observadas en mujeres con enfermedad trofoblástica tratadas sólo con metotrexato4, y los casos de seminoma en el que sólo con carboplatino se puede curar hasta el 70% de los casos8. En los años 1960, el tratamiento del teratoma testicular sólo con actinomicina conseguía respuestas en el 23% de los casos, y alguna curación. En el caso de la enfermedad de Hodgkin, los primeros ensayos clínicos demostraron que fármacos como la ciclofosfamida, vinblastina, adriamicina, dacarbacina o bleomicina eran capaces de conseguir respuestas hasta en el 50% de los casos cuando eran utilizados como terapia única, y en algunos pacientes incluso conseguir la curación. Los tratamientos actuales, como la pauta ABVD (adriamicina, bleomicina, vinblastina y dacarbacina), son capaces de conseguir curaciones en más del 75% de los casos de enfermedad de Hodgkin avanzada9. En el caso de los NHL, el tratamiento con un único quimioterápico en los años 1960 conseguía respuestas en 10-15% de los casos, aunque estas respuestas eran generalmente muy breves. Cuando se combinó la ciclofosfamida, la vincristina y la prednisona, se prolongó significativamente la duración de las respuestas hasta conseguir la curación10. Con la progresiva incorporación de la adriamicina, y más recientemente el rituximab, hoy el 85% de los niños y adolescentes con NHL pueden curarse.
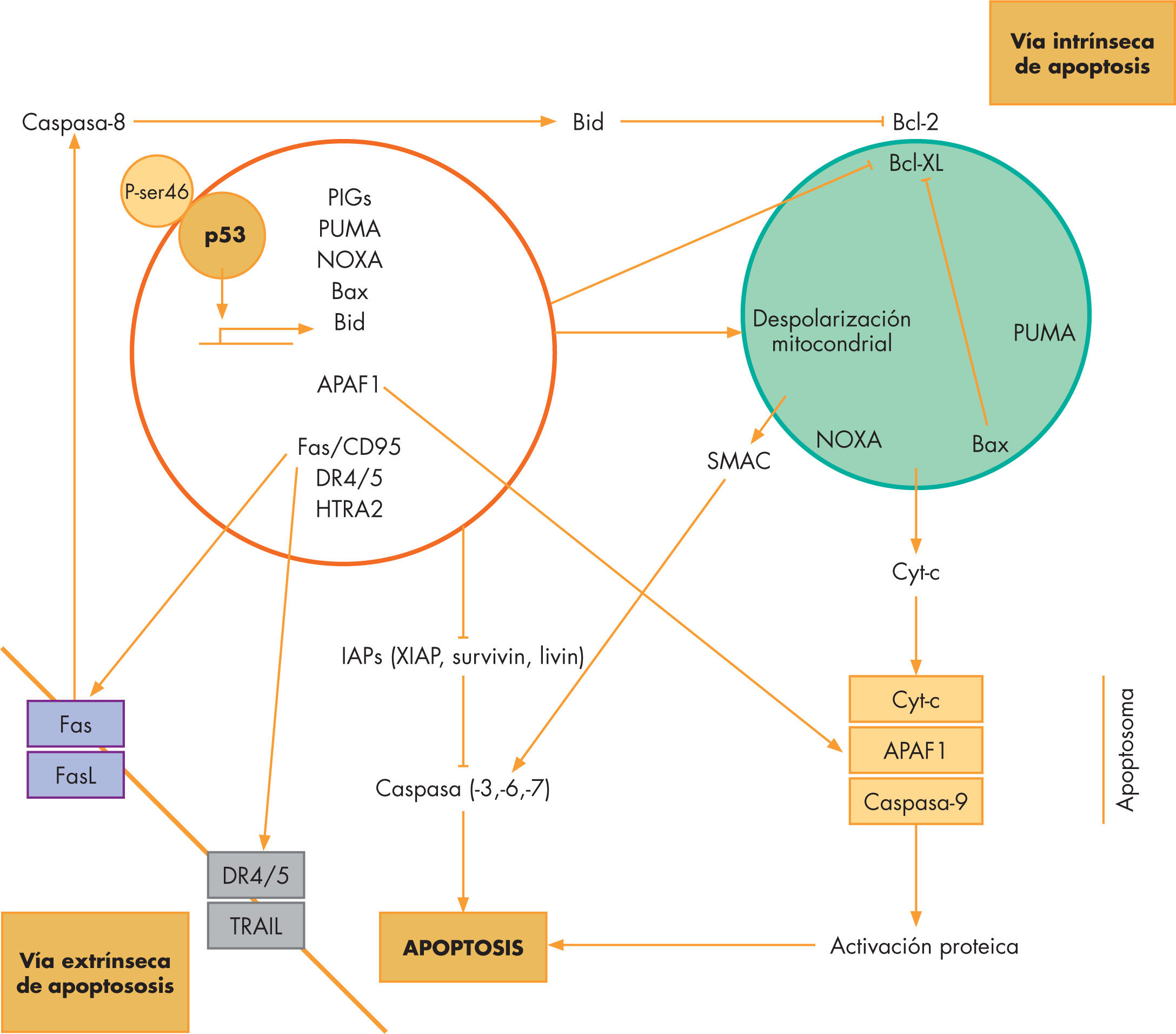
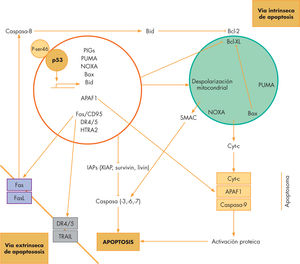
QuimiosensibilidadDadas las radicales diferencias en cuanto a la respuesta a la quimioterapia entre un grupo relativamente infrecuente de neoplasias comparado con la mayoría de los tumores, la pregunta es: ¿cuánto influyen las propiedades de los fármacos en el resultado final de la acción de la quimioterapia? La mayoría de los quimioterápicos citotóxicos actúan como venenos intracelulares, corrompiendo los procesos celulares más esenciales. Estos procesos inducen una respuesta de muerte celular (apoptosis) (fig. 2)11. ¿Existen evidencias para demostrar que los tumores quimiocurables retienen la capacidad de inducir apoptosis cuando se exponen a los fármacos citotóxicos en la misma medida que los tumores incurables presentan mecanismos de resistencia relacionados con la imposibilidad de responder al daño genotóxico con apoptosis?11.
Esquema de las vías moleculares de apoptosis. La vía intrínseca es la que se desencadena por señales que se originan en el interior de la célula, por ejemplo, por señales que provienen del daño al ADN (mediados por p53), como el que causan los citotóxicos. La vía extrínseca es la que se desencadena directamente por señales que provienen de receptores de muerte celular situados en la membrana celular (Fas o DR4/5) por mediadores de señales externos (FasL o TRAIL). El cuadro rojo representa el núcleo celular y el verde la mitocondria. De las múltiples proteínas involucradas en la apoptosis cabe resaltar la familia de Bcl-2 de las que hay miembros con actividad antiapoptótica (el mismo Bcl-2 o Bcl-XL) y otros con actividad proapoptótica (Bax, Bid).
Las claves de los mecanismos que subyacen a la quimiosensibilidad intrínseca y duradera de algunos tipos de tumores pueden obtenerse a partir de la observación del desarrollo fetal. Al inicio de la embriogénesis las células fetales presentan una extraordinaria sensibilidad a la quimioterapia, como se demuestra por la capacidad del metotrexato a muy bajas dosis para producir una muerte muy rápida del feto en embarazos ectópicos o conseguir un aborto en las primeras 8 semanas de gestación12. La quimioterapia administrada a las madres durante el primer trimestre de la gestación, durante la organogénesis, muestra una clara asociación con la pérdida del feto y un riesgo aumentado de malformaciones. Durante el segundo y tercer trimestres, sin embargo, cuando la organogénesis está completada, el feto y la placenta muestran una resistencia a la quimioterapia similar a la de los tejidos adultos. Estas observaciones indican que los tejidos más indiferenciados tienen una quimiosensibilidad intrínseca que se pierde luego con la maduración13.
Numerosos estudios han demostrado que los tumores quimiocurables presentan una mayor sensibilidad intrínseca a la inducción de apoptosis por sustancias que causan daño al ADN comparado con los tumores más comunes y no quimiosensibles. Si así fuera, deberíamos encontrar características comunes en los tumores quimiocurables que los distingan de los tumores no quimiosensibles y que pudieran explicar los mecanismos de la quimiosensibilidad.
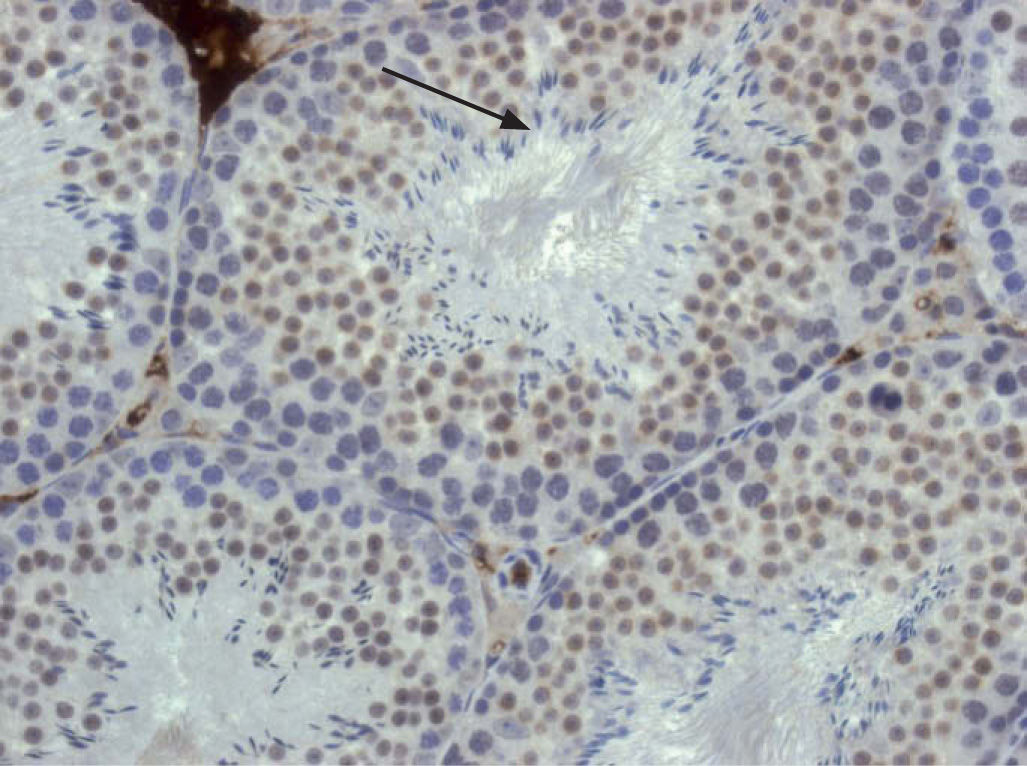
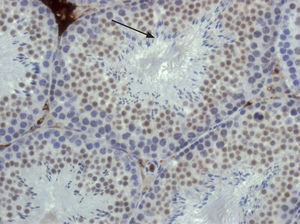
Vías de tumorigénesis que retienen la quimiosensibilidadTumores germinalesLos tumores germinales testiculares, tanto el seminoma como el no seminoma, se originan a partir de espermatogonias. En el testículo las espermatogonias sufren diversas mitosis y maduran hacia el tipo B de espermatogonia, que son las células que sufrirán el proceso de meiosis para producir las espermátides (fig. 3). Las espermatogonias normales que dan lugar a las espermátides presentan un elevado ritmo de apoptosis fisiológica, una característica que vemos en los tumores germinales14. En estos tumores la transformación maligna ocurre en una célula que sobreexpresa de manera fisiológica la proteína p53 no mutada y por lo tanto muy sensible a reconocer los puntos de recombinación genética que activan la apoptosis cuando se producen roturas de las cadenas de ADN. La transformación maligna se cree que ocurre por intercambio cromosómico aberrante durante las fases del desarrollo del cigoto. Este proceso desemboca en una reiniciación aberrante del ciclo celular asociada a inestabilidad genómica genética y epigenética, la cual a su vez facilita la transformación maligna15.
Fotomicrografía de un testículo de ratón generado en nuestro laboratorio para el estudio de la maduración de las espermatogonias (Dra. C. Lavarino). En el testículo, las espermatogonias (células grandes en azul) sufren diversas mitosis y maduran hacia el tipo B de espermatogonia (en marrón en el túbulo seminífero) que son las células que sufrirán el proceso de meiosis para producir las espermátides (flecha; células azules alargadas de menor tamaño).
En conjunto, estas y otras alteraciones resultan en un fenotipo tumoral que tiene un elevado potencial maligno, con una elevada capacidad para el rápido crecimiento y metástasis, aunque reteniendo intacta la facilidad para iniciar la apoptosis en respuesta al daño del ADN como el que produce la quimioterapia. La mayoría de los tumores germinales retienen intactas las vías de apoptosis, incluyendo una expresión normal de p53 y los pacientes responden muy bien a la quimioterapia. Por el contrario, los tumores germinales que adquieren mutaciones que comportan la pérdida de función de p53 son los más resistentes a la quimioterapia, y los pacientes son raramente curables16.
Leucemias y linfomasEl sistema inmunitario normal tiene una gran capacidad para una rápida replicación combinada con una poderosa fuerza efectora que obliga a que el sistema se proteja de las células con receptores no funcionales eliminándolos rápidamente. El resultado es que el sistema inmunitario posee una rápida capacidad proliferativa y un elevado nivel de apoptosis que son los elementos clave en su desarrollo y homeostasia17.
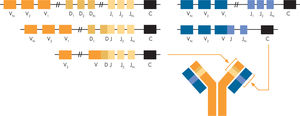
Los linfocitos llevan a cabo reordenamientos del ADN (fig. 4) mediante la combinación de las regiones génicas V, D y J del gen de la cadena pesada de las inmunoglobulinas (linfocitos B) y de la cadena beta del receptor T (linfocitos T). La recombinación de las regiones génicas V y J también ocurre en las cadenas ligeras de las inmunoglobulinas y cadenas alfa de los receptores T18. Después de estos reordenamientos iniciales, subsiguientes recombinaciones permiten el cambio de isotipo en los linfocitos B antes de su proceso de diferenciación final. La recombinación V(D)J ocurre en los linfocitos B y T primitivos y se inicia en la fase de célula progenitora linfoide común. El complejo enzimático V(D)J recombinasa rompe el ADN reconociendo las secuencias de recombinación pero los reordenamientos génicos se producen al azar y sólo una tercera parte produce un nuevo receptor con ADN que puede leerse adecuadamente. Así, de manera fisiológica, estas células retienen unas vías de apoptosis muy activas para asegurar su eliminación si se produce un receptor anormal, no funcionante18. En los linfocitos B el siguiente paso es la hipermutación, que ocurre en los centros germinales de los ganglios linfáticos y tejidos linfáticos periféricos19. Sólo las células que tienen una mutación selectiva que produce un receptor funcional continuarán con la maduración definitiva puesto que aquellas células que no reciben o no responden a estímulos de crecimiento selectivos, los procesos proapoptóticos desencadenarán una respuesta de muerte celular.
Esquema representando los segmentos de los genes con los exones que codifican para las regiones variable (V), diversidad (D), unión (joining o J) de las inmunoglobulinas o receptores de los linfocitos T. La C se refiere al centrómero del cromosoma representado. Las regiones variables de las cadenas β y δ del receptor T y de las cadenas pesadas (IgH) de las inmunoglobulinas se obtienen a partir de la recombinación de segmentos de los exones de V, D y J (panel de la izquierda) mientras que las cadenas α y γ de los receptores T y las cadenas κ y γ de las cadenas ligeras de las inmunoglobulinas se obtienen de la recombinación de exones de los segmentos V y J exclusivamente (panel derecho).
Si la transformación maligna ocurre en los estadios más precoces del desarrollo del linfocito B durante la fase de reordenamiento V(D)J de las cadenas pesadas, el resultado es la leucemia aguda linfoblástica (LAL), la forma de cáncer más frecuente en el niño, y el linfoma linfoblástico. La LAL se caracteriza por su rápido crecimiento y la quimioterapia por sí sola consigue índices de curación cercanos al 80%20. De los linfomas que afectan a los niños y adolescentes encontramos el linfoma de Burkitt (40%), el linfoma difuso de célula grande B (DLBCL) (20%), el linfoma linfoblástico (30%) y el linfoma anaplásico de célula grande (10%)6. La mayoría de los linfomas de Burkitt y DLBCL derivan de linfocitos de los ganglios periféricos de las regiones de los centros germinales donde los linfocitos inmaduros rápidamente proliferantes (centroblastos) sufren los procesos de diferenciación a centrocitos después de los fenómenos de hipermutación.
El linfoma de Burkitt (BL) se caracteriza en el 70-80% de los casos por la translocación t(8;14)(q24.1;q32). Esta translocación yuxtapone el oncogén c-myc (en 8q24) junto al gen de la cadena pesada (IgH) de las inmunoglobulinas en 14q32, lo que comporta la sobreexpresión de c-myc y determina la transformación maligna. Con los tratamientos actuales de quimioterapia, los índices de curación se aproximan al 90% en niños y al 50-60% en adultos6. El DLBCL se origina tanto en los centros germinales de células que están llevando a cabo el proceso de hipermutación, como de linfocitos B maduros ya en circulación periférica21. La importancia del estado de las vías proapoptóticas en el momento en el que ocurre la transformación neoplásica se refleja claramente en las diferencias de curación entre los DLBCL. Los linfomas que se originan a partir de los centros germinales durante la hipermutación somática tienen unos índices de curación del 75%, mientras que los que derivan de células maduras tienen unos índices de curación de sólo el 16%21.