Puntos clave
La profilaxis con vitamina D es nuevamente objeto de estudio y controversia en la comunidad científica internacional. El papel de esta vitamina en el mantenimiento de un metabolismo mineral adecuado es bien conocido; el descubrimiento de su receptor nuclear en múltiples tejidos del organismo ha generado hipótesis sobre nuevas funciones1. Su implicación en procesos no ligados al metabolismo del calcio, la preocupación por el déficit subclínico, la falta de consenso respecto al umbral de suficiencia en niños y la escasez de ensayos clínicos que aclaren la auténtica relación de sus niveles y el efecto de los suplementos con los marcadores de salud ósea y la prevalencia de determinadas enfermedades, motivan lagunas que sólo la continuidad en investigación podrá solventar. Algunas sociedades científicas han modificado recientemente sus recomendaciones de profilaxis, a la espera de mejor evidencia y extrapolando en ocasiones a la población infantil los datos obtenidos de estudios en adultos2.
EpidemiologíaLa primera edición del tratado sobre raquitismo de Glisson data de 1650 y ya ofrece una descripción precisa de esta enfermedad que en el siglo XIX fue epidémica en las ciudades del norte de Europa, debido a los cambios sociales propiciados por la revolución industrial. La observación de las condiciones de vida en los afectados apuntó a la ausencia de luz solar o de algún nutriente esencial como factores etiológicos, constatándose mejoría en la mineralización tras la exposición a la radiación ultravioleta (RUV). En 1936 Windaus sintetizó el 7-dehidrocolesterol y por irradiación lo convirtió en vitamina D3. El hallazgo posterior de su producción cutánea hizo posible la síntesis, su adición a los alimentos y su uso en presentación farmacéutica1.
Metabolismo de la vitamina DEl término engloba 2 sustancias liposolubles (colecalciferol y ergocalciferol) con capacidad de prevenir y curar el raquitismo. La molécula precursora se convierte en colecalciferol por exposición a la RUV. Existe un intermediario que se acumula en la piel y puede constituir una fuente sostenida de vitamina1. La vitamina D se transporta ligada a una proteína específica (DBP) y requiere 2 hidroxilaciones (hepática y renal) para activarse biológicamente. El metabolito activo es la 1–25 (OH)2D o calcitriol, la mayoría de cuyas acciones están mediadas por su receptor nuclear (VDR). La hipocalcemia, hipofosforemia y la parathormona (PTH) son un potente estímulo para la síntesis de calcitriol; la acidosis y el FGF23 (factor regulador del metabolismo del fósforo) pueden suprimirla1. Los valores del metabolito hepático (25OHD o calcidiol) determinan el estatus de vitamina D.
FisiopatologíaLa función clásica de la vitamina D es el mantenimiento de los valores de calcio y fósforo en el rango fisiológico normal que permita mineralización ósea, transmisión neuromuscular y funciones metabólicas. Para ello, favorece su absorción intestinal y puede promover su liberación del hueso al torrente sanguíneo. Si hay mucho calcio disponible su transporte será menos dependiente de vitamina D. En situaciones de déficit, el aumento de PTH (mediado por el sensor de calcio en paratiroides) favorece la movilización de calcio del hueso, su reabsorción renal y la síntesis de calcitriol, causando fosfaturia. Esta situación, inicialmente compensadora, conllevará si se cronifica un cociente calcio/fósforo inadecuado para la mineralización1. La producción de calcitriol en células ajenas a este sistema y la existencia de VDR en más de 30 tejidos2 ha suscitado hipótesis sobre nuevas funciones. Se ha publicado que niveles “adecuados” de vitamina D podrían disminuir la incidencia de ciertos tumores del adulto y participar en la modulación inmunológica3,4. Estas publicaciones generan gran interés, pero será necesario esperar estudios prospectivos a largo plazo que evalúen los efectos de los suplementos en la prevención de estas enfermedades2.
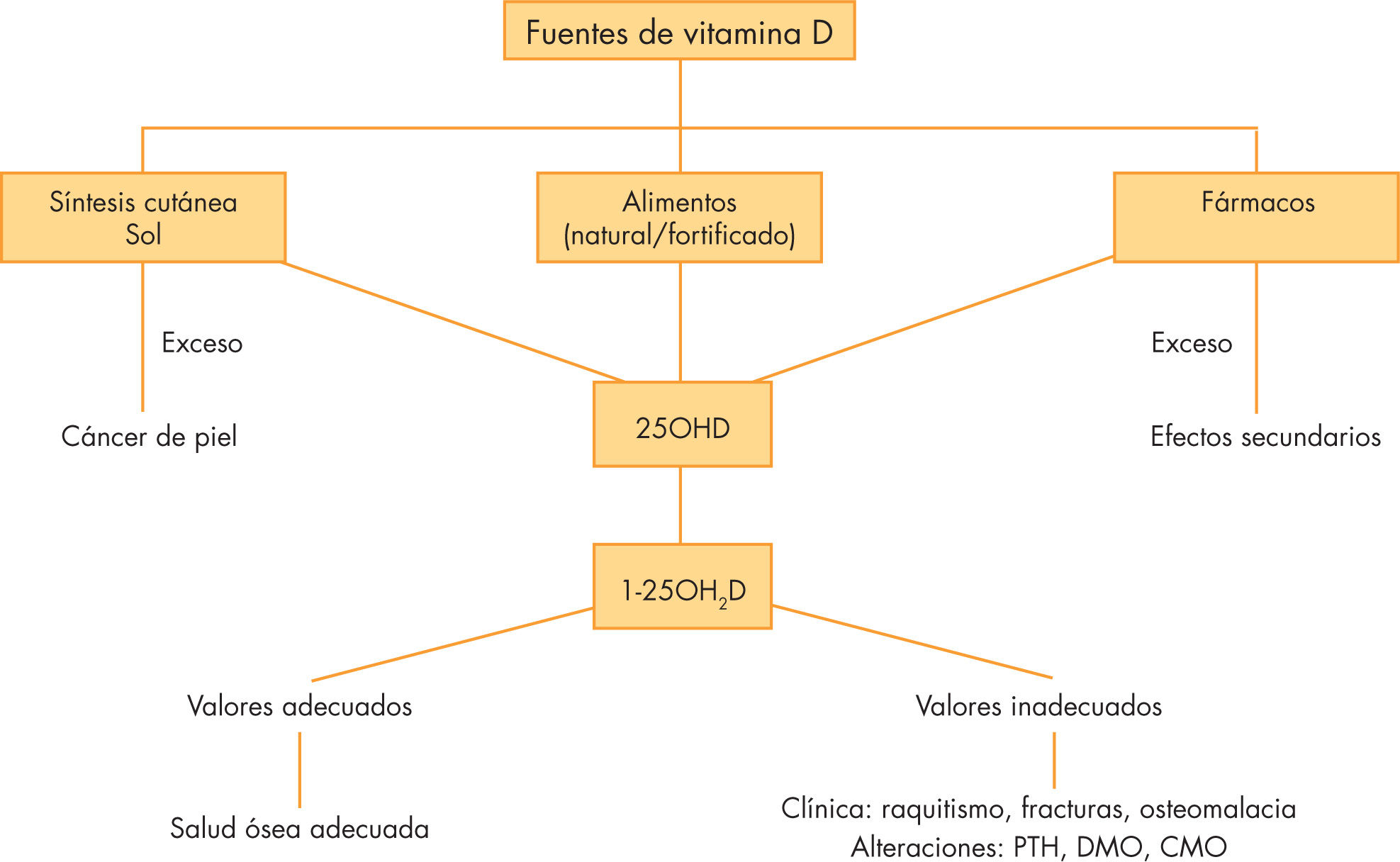
Fuentes de vitamina DLa principal es la síntesis cutánea mediada por el sol. Menos del 10% puede obtenerse de alimentos que la contienen o han sido fortificados y de preparados farmacológicos (fig. 1). El polémico balance “beneficio/riesgo” de la exposición solar dificulta la elaboración de mensajes de salud pública no contradictorios. Ninguna revisión sistemática aclara si hay un grado de exposición suficiente y seguro para mantener un óptimo estatus de vitamina D5, pero su exclusión habitual es un riesgo de deficiencia6. Según Specker, 30 min/ semana en pañal y 2 h vestido, sin gorro, permitiría valores de 25OHD > 11 ng/ml7. Ho (Asia) encontró que exponer la cara 24 min/día sería suficiente para eso8. Holick publica que 1/3-1/6 del MED (mínimo eritema dosis) en cara y extremidades superiores permitiría los valores recomendados actualmente1. Muchos factores condicionan la producción de vitamina D (tabla 1) pero ningún estudio ha podido aún determinar el impacto de cada uno5.
Factores que condicionan la producción de vitamina D
| Piel | La melanina regula la RUV que penetra en las capas epidérmicas con más alta concentración de 7-dehidrocolesterol; piel oscura menor producción |
| Edad | La edad disminuye la disponibilidad de 7-dehidrocolesterol. La mayor superficie corporal por talla de los niños favorece la síntesis |
| Indice de masa corporal | La obesidad parece asociar niveles de 25OHD más bajos |
| Cremas protectoras | El uso de protectores solares en todos los paseos del niño puede limitar la producción de vitamina D |
| Hora del día, estación año, latitud | Condicionan el ángulo cenital solar y la radiación efectiva para la síntesis de vitamina D. El sol del mediodía tiene más RUV-B en el espectro adecuado (280–320 nm) |
| Polución, nubosidad, ozono | Dificulta la penetrabilidad de la RUV-B eficaz para la síntesis de vitamina D |
25OHD: 25-hidroxivitamina D o calcidiol; RUV: radiación ultravioleta; RUV-B: radiación ultravioleta tipo B.
Los hábitos culturales y la propia legislación del país pueden condicionar el aporte de vitamina D en la dieta. La fortificación de alimentos es mayor en Norteamérica que en Europa, pero ocurre lo contrario con el aporte de calcio en la dieta9. En España las fórmulas adaptadas, los cereales y otros alimentos de consumo en niños están fortificados (tabla 2). El contenido final de vitamina D o el aporte de calcio puede modificarse por el tipo de dieta: freír el pescado disminuye su vitamina D; los fitatos, el exceso de proteínas o sodio y el ácido oxálico tienden a producir hipocalcemia por distintos mecanismos2,10. Todo esto es sólo una pequeña parte de las dificultades existentes para extrapolar o comparar datos en investigación.
Alimentos fortificados en España
| Alimento | Vitamina D |
|---|---|
| Fórmula adaptada inicio | 1-1,4 μg/100 ml |
| Fórmula adaptada continuación | 1,7-1,8 μg/100 ml |
| Fórmula de prematuros | 1,7 μg/100 ml |
| Cereales infantiles | 300 U/100 g |
| Yogur de leche adaptada | 72 U /unidad |
| Yogur natural | 30 U/unidad |
| Yogur desnatado | 50 U/unidad |
| Leche semidesnatada | 0,75 μg/100 ml |
| Margarina vegetal | 240 U/100 g |
5 μg = 200 U.
Su producción endógena impide establecer una dosis diaria recomendada (RDA) para la vitamina D, pero 5 μg/día se considera aporte adecuado (AI) en la infancia11. El Food and Nutrition Board revisa en la actualidad esta cifra y se prevé su informe en mayo de 2010. No existe consenso, sin embargo, respecto al umbral de suficiencia en niños. La escasez de estudios, la falta de estandarización de la metodología y de la interpretación de resultados de éstos, lo dificulta5. Los rangos ofrecidos varían de 5 a 20 ng/ml para la deficiencia y de 15 a 30 ng/ml para la suficiencia12,13. Esto genera estimaciones de prevalencia de hipovitaminosis D entre 1% -78%14. El Instituto de Medicina de EE.UU. en su Dietary Reference Intakes define la deficiencia como una concentración de 25OHD < 11 ng/ml15. En adultos, este umbral se ha establecido en 20 ng/ml, nivel de 25OHD a partir del cual la PTH deja de bajar16, pero en lactantes y neonatos esta correlación inversa 25OHD/PTH no es tan clara. Se requieren estudios adicionales y actualmente se sugiere que este punto podría estar en algún lugar por encima de 10,8 ng/ml5. Algunos autores consideran que el rango de suficiencia de vitamina D en niños debe adaptarse al aporte de calcio en la dieta17.
Vitamina D y salud óseaMuy pocos estudios en lactantes relacionan los valores séricos de 25OHD con la densidad mineral ósea (bone mineral density, BMD) y algunos que intentan evaluarlo presentan un importante factor de confusión, al haber sido realizados en países con escaso aporte de calcio dietético5. El Centro de Medicina Basada en la Evidencia de la Universidad de Ottawa ha revisado recientemente la literatura médica y concluye que los datos son inconsistentes18–20.
Profilaxis farmacológica. Recomendación actualHay gran variabilidad entre países: universal (EE.UU., Suecia y Canadá), condicionada por factores de riesgo (Australia, Reino Unido y Nueva Zelanda), o ninguna profilaxis. En España han coexistido durante décadas diversas pautas, sin guías claras al respecto. En los últimos años, la literatura sobre vitamina D se ha saturado de trabajos que la vinculan con otras enfermedades y que alertan de la posibilidad de déficit subclínico, especialmente en la lactancia materna exclusiva12,13,21 o en países muy soleados que no utilizan profilaxis22. Todo ello, sumado a la sombra del raquitismo, aún presente (aunque generalmente en niños con factores de riesgo), ha llevado a algunas sociedades científicas a modificar sus recomendaciones previas. Hasta este momento, el Comité de Lactancia Materna de la Asociación Española de Pediatría23, la Sociedad Española de Gastroenterología y Nutrición24 y el Grupo Previnfad (www.aepap.org/previnfad) de la Asociación Española de Pediatría de Atención Primaria recomendaban la profilaxis (200–400 U/día) en situaciones de riesgo específico (tabla 3). En agosto de 2009, Previnfad suscribe la nueva Guía de la AAP21, que desde 2008 aboga por la profilaxis universal, recomendando la administración de 400 U/día a todos los lactantes que no consuman al menos 1 l de leche suplementada al día, y a los niños y adolescentes con factores de riesgo que no adquieran este aporte por la dieta o una adecuada exposición solar. Esta recomendación descansa en el umbral de suficiencia en adultos (el cual parece que no alcanzarían los niños amamantados con menor dosis) y la escasa toxicidad histórica de la vitamina D, añadiendo que los preparados en EE.UU. dispensan por ml/gota esta dosis21. La leche materna contiene menor cantidad de vitamina D que la fórmula adaptada (previamente suplementada); los niños amamantados tienen por lo general valores inferiores de vitamina D, por el mismo motivo, pero no hay una evidencia clara de que esto se relacione con una salud ósea deficiente en ellos, ya que la biodisponibilidad del calcio podría ser diferente y el transporte menos dependiente de vitamina D24. No se ha demostrado en ensayos clínicos que lactantes amamantados con y sin profilaxis tengan valores de PTH o contenido mineral óseo significativamente diferentes, pese a serlo sus valores de 25OHD18,19. Otros estudios no encuentran diferencia significativa en estos parámetros entre niños alimentados con leche materna y fórmula adaptada25.
Factores de riesgo específicos para el déficit de vitamina D
| Prematuridad |
| Etnias específicas con pigmentación oscura de la piel |
| Exclusión de luz solar por razones culturales, religiosas o de cualquier tipo |
| Enfermedad orgánica subyacente crónica o con riesgo aumentado de déficit de absorción de calcio o de producción de vitamina D (insuficiencia renal, trastornos de la absorción intestinal, desnutrición, fibrosis quística de páncreas, enfermedad endocrinológica o metabólica) |
| Enfermedad crónica de la piel que requiera el uso frecuente de corticoides tópicos |
| Dietas con alto contenido en fitatos |
| Lactantes que tomen exclusivamente pecho, y cuyas madres no se expongan a la luz solar habitualmente, sigan dietas específicas (vegetarianas estrictas, alto contenido en fitatos) o enfermedad crónica que condicione riesgo de déficit en ellas |
Los múltiples factores que condicionan el estatus de vitamina D, el desconocimiento del umbral de suficiencia en lactantes, la falta de estudios a largo plazo sobre efectos secundarios20 y la escasez de ensayos clínicos que evalúen el efecto de la profilaxis, dificultan la unificación de criterios y la extrapolación de datos entre países, etnias y tramos etarios. La Cochrane Collaboration recomienda en 2007 realizar estudios en distintos grupos. Es preciso supervisar la alimentación y la exposición solar de madres y lactantes amamantados (sobre todo en períodos de poca RUV), detectar situaciones de riesgo (tabla 3) y determinar incluso en casos concretos el estado de la vitamina D; pero el uso indiscriminado de la profilaxis, o etiquetar la lactancia materna exclusiva como “factor de riesgo”, requiere prudencia.