Las infecciones de endoprótesis de aorta torácica suponen una complicación infrecuente. Su incidencia varía según las publicaciones, oscilando en torno al 1% según Cernohorsky et al.1 y entre el 0,2 y el 0,7% según Hobbs et al.2. Su escasa frecuencia explica el hecho de que en la literatura médica se encuentren principalmente descripciones de casos clínicos singulares y series de casos cortas. Dada la severidad de dicha complicación, es fundamental que el cirujano vascular conozca cómo poder reconocerla y de qué opciones terapéuticas dispone para enfrentarse a ella.
Acude a nuestro centro un paciente de 68 años, dislipidémico, refiriendo episodio de hematemesis. Fue intervenido 53 días antes por un pseudoaneurisma de aorta torácica descendente roto, descubierto como hallazgo en angio-TC por estudio de dolor torácico de perfil pleuropericárdico persistente de un mes de evolución.
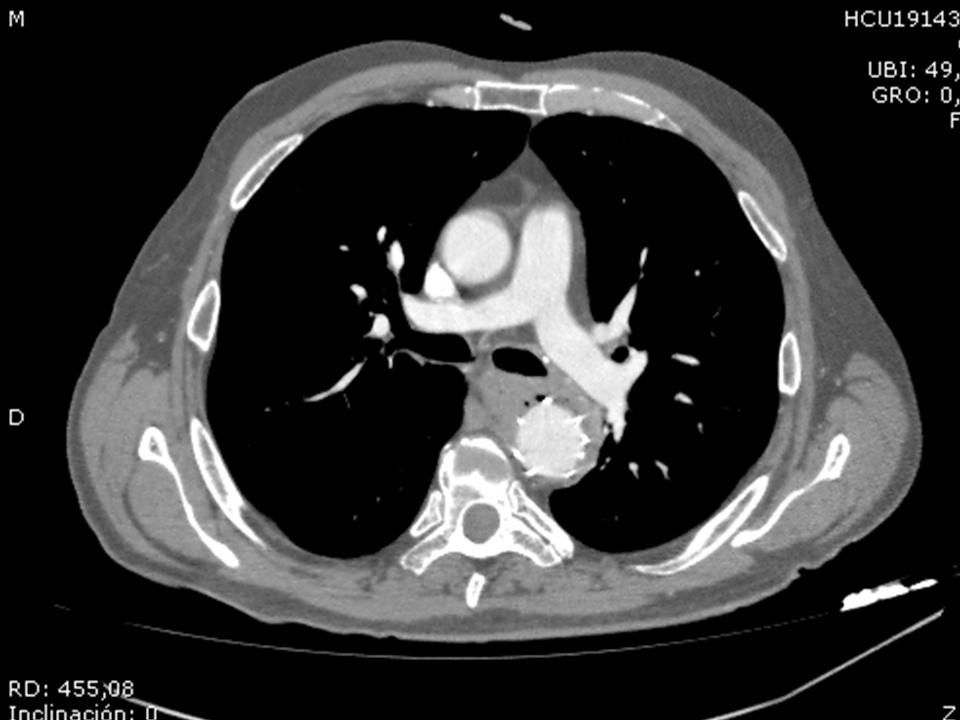
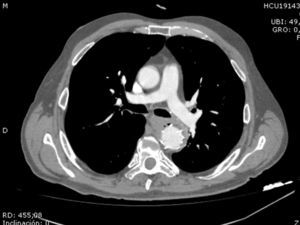
Trece días antes del episodio de hematemesis consulta en el servicio de urgencias por cuadro de fiebre, malestar general, disfagia y cefalea. Se obtienen hemocultivos para estudio y se prescribe tratamiento sintomático. Presenta 48 h antes fiebre en su domicilio, así como persistencia del dolor torácico. En el servicio de urgencias se detectan 14.500 leucocitos/μl, con neutrofilia de 90%, y una proteína C reactiva de 152,3mg/l y procalcitotina de 0,54ng/l. Se realiza endoscopia observando una lesión de 2cm de diámetro, sobreelevada y con material fibrinoide y hemático, sin sangrado activo en el momento de la exploración. Dados los antecedentes del paciente se realiza angio-TC para descartar fístula aortoesofágica. Se observa gas entre la pared aórtica y la endoprótesis sin evidencia de fístula aortoentérica. Ante los datos clínicos y radiológicos se establece el diagnóstico de infección endoprotésica, comenzando tratamiento antibiótico empírico con vancomicina y meropenem y programando el explante diferido de la endoprótesis dada la estabilidad clínica del paciente.
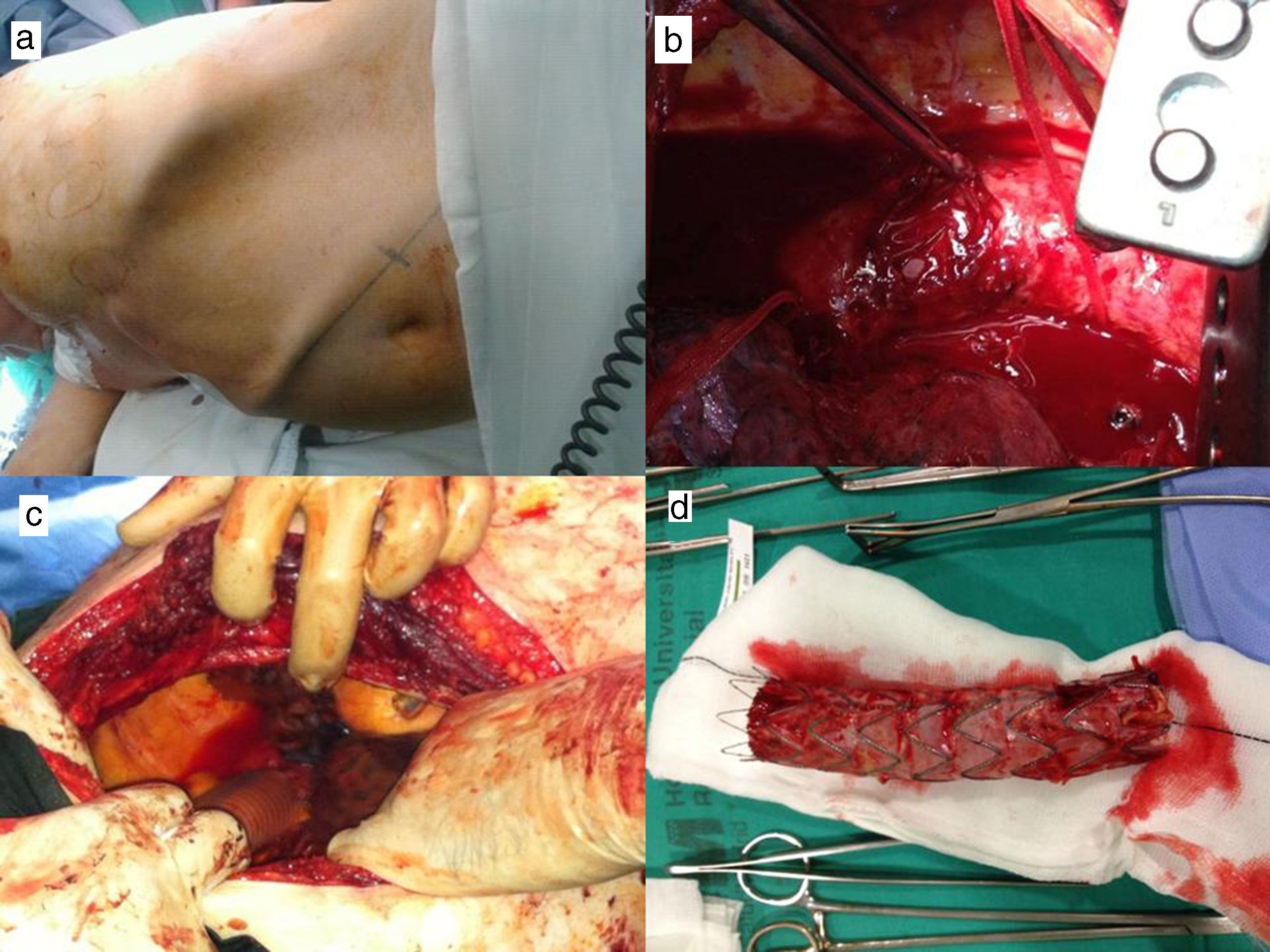
En el mismo acto quirúrgico, previo al explante de la endoprótesis, se realiza un bypass axilar derecho-femoral izquierdo de descarga, con tunelización subcutánea. Vía toracotomía lateral izquierda, a nivel del quinto espacio intercostal, se accede a la aorta torácica objetivando material purulento a nivel de la pared aórtica, así como múltiples adherencias en el pulmón izquierdo y una lesión inflamatoria del tercio medio del esófago en íntimo contacto con la aorta pero sin evidencia de fístula. Se realiza un clampaje proximal distal al origen de la subclavia izquierda y un clampaje distal proximal a las ramas viscerales. Explante de la endoprótesis y bypass terminoterminal con prótesis Silver Woven de Maquet de 26mm Finalmente, se coloca un parche de Tachosil entre la pared aórtica y el esófago y se dejan drenajes torácicos (figs. 1 y 2).
Se aisló en un hemocultivo y en la pared aórtica Streptococcus anginossus sensible a penicilina, y Candida glabratta (C. glabratta) resistente a azoles y Candida albicans (C. albicans) en el derrame pleural izquierdo encapsulado que se observa en el angio-TC de control y que requiere de drenaje percutáneo. Se solicita gammagrafía con leucocitos marcados un mes después de la intervención con resultado negativo. Alta a los 51 días con antifúngicos y antibióticos orales ajustados según antibiograma.
El diagnóstico de las infecciones endoprotésicas se basa en la clínica y en pruebas complementarias. Malestar general, dolor torácico, escalofríos, pérdida de peso, fiebre, o sepsis entre 4 y 12 meses, como mínimo2, tras el implante deben hacernos sospechar. Las pruebas de imagen confirman dicha sospecha diagnóstica. En la literatura médica se describen varias opciones para confirmar dicho diagnóstico: angio-TC, gammagrafía con leucocitos marcados y PET-TC. En el 68% de los casos se detecta el microorganismo causante2. Staphylococcus aureus es el que se aísla con mayor frecuencia. En nuestro caso se identificó tanto en hemocultivo como en la pared aórtica Streptococcus anginosus3, patógeno causante de abscesos viscerales y endocarditis, pero componente de la flora habitual del sistema gastrointestinal. Probablemente el origen del cuadro en este caso fue la lesión esofágica mediante un mecanismo de siembra hematógena que pudiera contaminar la prótesis, o mediante translocación bacteriana. La infección por C. glabratta y C. albicans detectada con posterioridad, responde probablemente a una sobreinfección secundaria al empleo de antibióticos de amplio espectro.
En cuanto al tratamiento, el planteamiento habitual consiste en el explante de la endoprótesis, seguido del desbridamiento amplio de los tejidos infectados y la reconstrucción arterial4,5 mediante bypass extraanatómico, axilobifemoral o axilofemoral, o mediante bypass in situ desde aorta ascendente hasta aorta descendente6. La reconstrucción in situ se puede realizar mediante el empleo de prótesis sintéticas impregnadas en antibiótico7, Dacron plata, o bien mediante la interposición de un injerto criopreservado. Se recomienda llevar a cabo medidas adicionales para prevenir recidivas, aislando el área afectada mediante colgajos pericárdicos, de músculo dorsal ancho, etc., o empleando tejidos biológicos, así como drenajes y mecanismos de irrigación de antibiótico. En determinados casos, especialmente en función de la gravedad, se puede optar por un planteamiento exclusivamente conservador, encontrando en la bibliografía argumentos tanto a favor como en contra de dicha actitud1,4,5.
Dada la dificultad para conseguir un tamaño muestral suficientemente grande como para obtener resultados extrapolables es recomendable valorar cada caso de manera individualizada, según sus particularidades, pudiendo apoyar nuestras decisiones en la experiencia recogida por el resto de la comunidad médica.
Responsabilidades éticasProtección de personas y animalesLos autores declaran que para esta investigación no se han realizado experimentos en seres humanos ni en animales.
Confidencialidad de los datosLos autores declaran que han seguido los protocolos de su centro de trabajo sobre la publicación de datos de pacientes y que todos los pacientes incluidos en el estudio han recibido información suficiente y han dado su consentimiento informado por escrito para participar en dicho estudio.
Derecho a la privacidad y consentimiento informadoLos autores declaran que en este artículo no aparecen datos de pacientes.
Conflicto de interesesLos autores declaran no tener ningún conflicto de intereses.