La isquemia mesentérica se caracteriza por una reducción del flujo sanguíneo a nivel intestinal, de forma brusca o de forma progresiva, con unas consecuencias potencialmente letales, sobre todo en los casos agudos.
La falta de evidencia científica ante una enfermedad poco frecuente, con una clínica y pruebas diagnósticas en ocasiones inespecíficas, y la gran heterogeneidad en los procedimientos de revascularización hacen difícil la toma de decisiones. Las sociedades científicas deben estimular el desarrollo de algoritmos diagnósticos y terapéuticos con el fin de mejorar el manejo y la supervivencia de estos pacientes y, por otro lado, avalar la actividad de sus miembros. Es, en este marco, donde la SOciedad Castellano Leonesa de Angiología y CIrugía VAScular (SOCLACIVAS) se propuso establecer un algoritmo diagnóstico y terapéutico en la isquemia mesentérica.
Mesenteric ischaemia is characterised by a sudden or gradual reduction in blood flow at intestinal level, with some potentially fatal consequences, particularly in acute cases.
The lack of scientific evidence of a rare disease, with a clinical picture and diagnostic tests that are occasionally non-specific, as well as a wide variation in revascularisation procedures, make it difficult to make decisions. The scientific societies must stimulate the development of diagnostic and therapeutic algorithms, with the aim of improving the management and survival of these patients, as well as to endorse the activities of their members. It is within this framework that the Angiology and Vascular Surgery Society of Castile and Leon (Sociedad Castellano Leonesa de Angiología y Cirugía Vascular) (SOCLACIVAS) proposes to establish a diagnostic and therapeutic algorithm for mesenteric ischaemia.
La isquemia mesentérica (IM) es la consecuencia de una reducción de flujo sanguíneo a nivel intestinal, producida por una oclusión, espasmo o hipoperfusión de la vasculatura esplácnica1. Las consecuencias pueden ser catastróficas, incluyendo sepsis, infarto intestinal y muerte (superior al 50% en los casos agudos y hasta el 15% en los casos crónicos)2,3, por lo que el rápido diagnóstico y tratamiento son decisivos4. El mejor conocimiento de esta dolencia, el aumento de la edad poblacional y la expansión de los procedimientos intervencionistas están incrementado el número de casos tratados. Sin embargo, la evidencia científica es escasa, lo que dificulta la estandarización de su manejo5.
Propongo una revisión del diagnóstico y tratamiento de la IM, e invito a los miembros de la Sociedad Española de Angiología y Cirugía Vascular (SEACV) a debatir el posible manejo de esta dolencia, con el fin de desarrollar algoritmos que pudieran mejorar la supervivencia y apoyar en la toma de decisiones.
Isquemia mesentérica agudaSe define como una situación de hipoperfusión intestinal de forma brusca. Puede ser producida por una embolia, generalmente a nivel de la arteria mesentérica superior (AMS), o por una trombosis de placa, más frecuentemente en pacientes con enfermedad aterosclerótica multinivel y con clínica previa de angina intestinal. Existen otras causas menos habituales como son las situaciones de bajo gasto o vasoconstricción en pacientes pluripatológicos, en tratamiento con aminas vasopresoras, conocida como isquemia mesentérica no oclusiva (IAMNO), o la trombosis venosa mesentérica (TVM) en pacientes jóvenes con diversas coagulopatías, en procesos sépticos u oncológicos6,7.
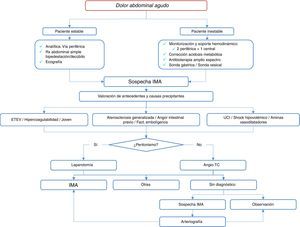
DiagnósticoSe necesita una alta sospecha clínica ante cuadros de dolor abdominal8, en pacientes con factores de riesgo conocidos, para iniciar rápidamente una batería de actuaciones y pruebas diagnósticas que suelen culminar con técnicas invasivas que permiten llegar al diagnóstico e, incluso, al tratamiento.
Su baja incidencia, menos de 1/1.000 de los ingresos hospitalarios, y la clínica tan común con otras enfermedades retrasan el diagnóstico y tratamiento4,9. Esta demora se traduce en aumento de la mortalidad, de un 36% en los casos tratados antes de las 24 h de inicio de los síntomas hasta un 76% en los tratados más allá de las primeras 24 h10.
El dolor abdominal está presente en casi todos los casos, pero su localización, duración y naturaleza son variables dependiendo de la etiología. Así, las embolias tienen una clínica más florida y una rápida progresión frente a los casos de trombosis venosa, en los que el paciente puede consultar tras días de inicio de la sintomatología. La forma más común es un dolor de aparición súbita, incapacitante, en epigastrio o mesogastrio, en ocasiones acompañado de vómitos o diarrea. La exploración inicial puede ser poco significativa, cierta distensión abdominal o disminución del peristaltismo que puede contrastar con la situación de postración del paciente. En los casos evolucionados, con necrosis intestinal, puede aparecer hematemesis o melena, signos peritoníticos, fiebre e incluso inestabilidad hemodinámica8,11.
Las pruebas de laboratorio no son concluyentes. Aparecen en otros cuadros de abdomen agudo y, además, resultan tardías, cuando ya reflejan situaciones de necrosis intestinal establecida. Así, podemos encontrar leucocitosis, elevación de los niveles séricos de láctico deshidrogensasa, creatinfosfocinasa, fosfatasa alcalina y acidosis metabólica8.
En cuanto a las pruebas de imagen, la radiografía simple tan ampliamente utilizada y la tomografía computarizada (TC) son normales hasta en un 25% de los casos y en situaciones avanzadas se pueden observar datos inespecíficos y comunes a otras enfermedades como íleo paralítico, engrosamiento de la pared, pneumatosis o falta de realce en pared tras contraste intravenoso en TC12. Sin embargo, son pruebas útiles para descartar otras enfermedades. Excepcionalmente, si la sospecha es una TVM, la TC es la prueba de elección, con una especificidad de hasta un 93% en alguna serie2.
La angiotomografía computarizada (angio-TC), con una sensibilidad del 94% y una especificidad del 95%8,13,14, es el test de elección en pacientes hemodinámicamente estables, con abdomen agudo y sospecha de isquemia mesentérica aguda (IMA). Permite valorar localización, extensión y características de la lesión del árbol arterial, el grado de afectación de la pared intestinal y los posibles accesos vasculares de cara a una intervención. Sin embargo, la arteriografía sigue siendo el gold standard en el diagnóstico y además permite el inicio de tratamiento. Por ello, en centros con gran experiencia en técnicas endovasculares, se plantea como primera opción en pacientes con alta sospecha con el fin de no retrasar la revascularización6,8,10,15.
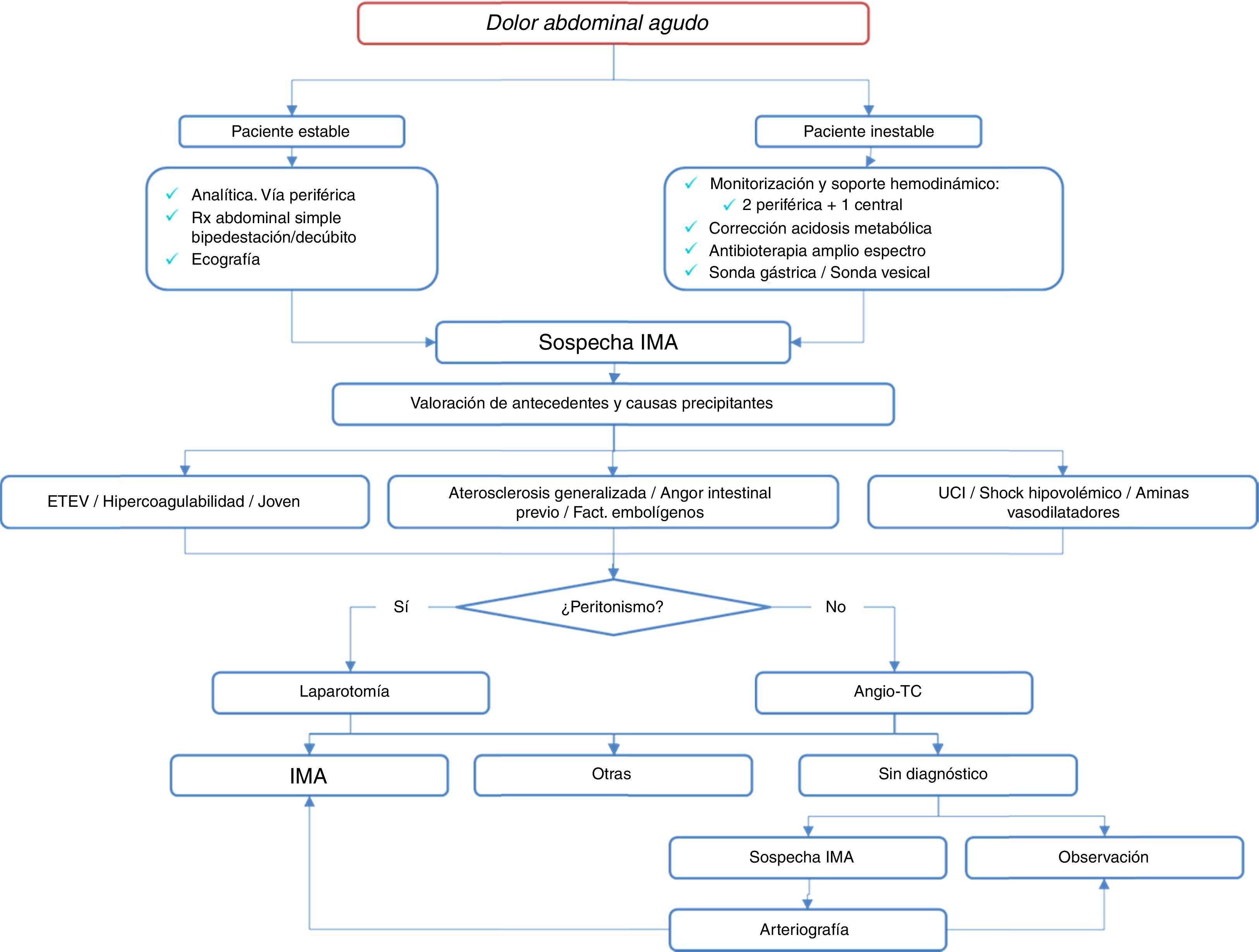
Desgraciadamente, el paciente inestable o con datos peritoníticos debe ser intervenido directamente mediante laparotomía: así se llega al diagnóstico de hasta el 20% de los casos de IMA16 (fig. 1).
TratamientoEl tratamiento inicial radica en un soporte hemodinámico agresivo, que corrija la hipovolemia y evite vasoconstrictores (especialmente alfa-agonistas), con el fin de mantener la perfusión en el territorio esplácnico. Se debe mejorar la acidosis metabólica y se debe iniciar antibioterapia de amplio espectro, para prevenir y tratar la translocación bacteriana. La anticoagulación es fundamental para evitar la progresión del trombo y para disminuir el riesgo de embolización en pacientes con fibrilación auricular, independientemente de los posibles sangrados durante el procedimiento posterior17,18.
En segundo lugar, siempre y cuando la situación clínica del paciente lo permita, se debe plantear una revascularización, teniendo en cuenta la etiología, duración de la clínica, comorbilidades del paciente y recursos técnicos.
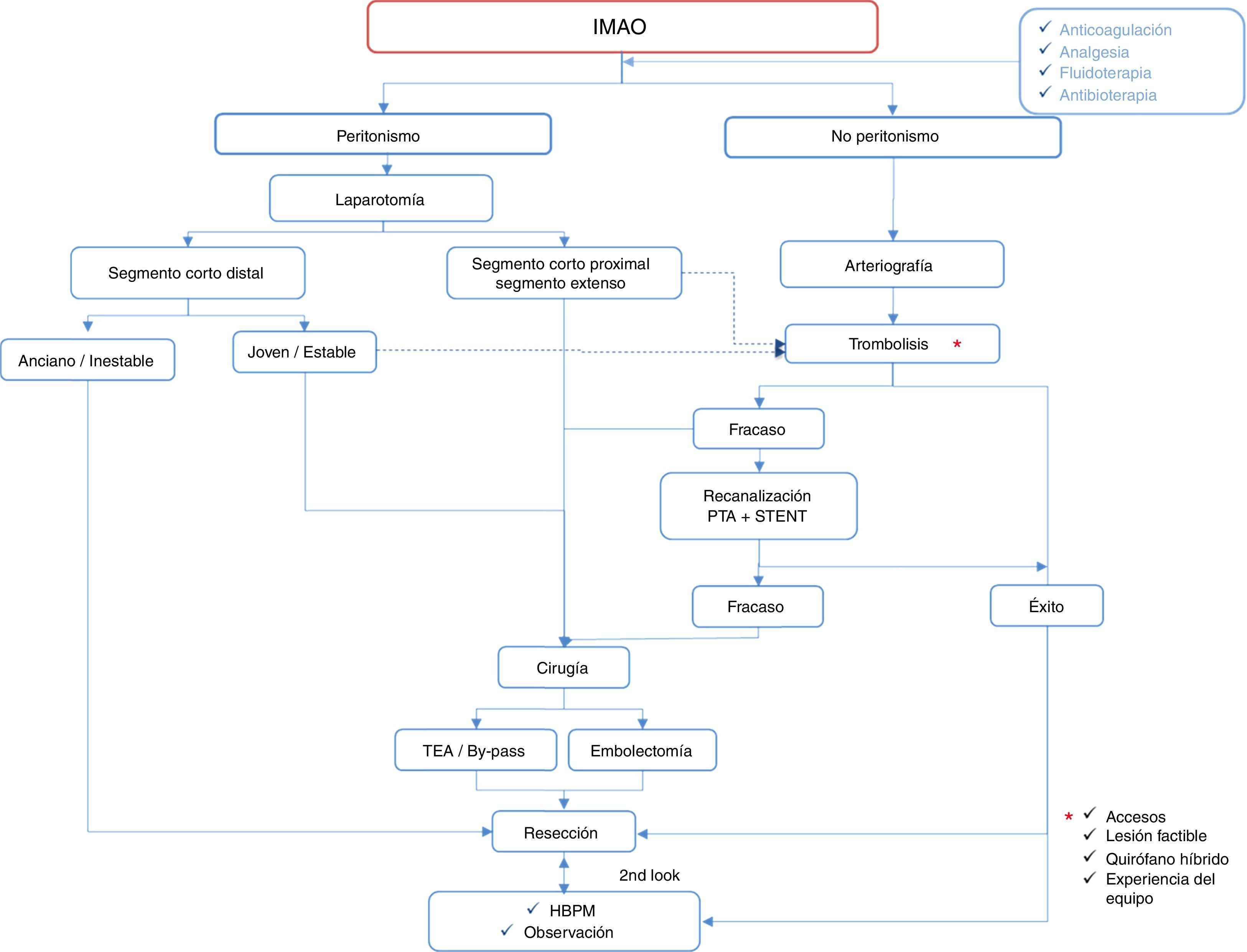
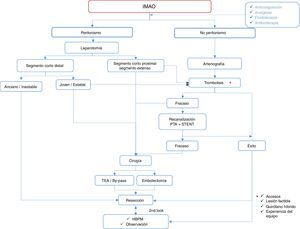
Aquellos pacientes con peritonismo o datos radiológicos de isquemia intestinal avanzada, serán tratados directamente con laparotomía. Se explorará extensión y localización del intestino afecto (color, distensión y peristalsis), pulso a nivel de AMS y arcadas mesentéricas, y posible ocupación de la VMS; algunos equipos recurren al doppler intraoperatorio e incluso a la inyección de fluoresceína para examinar la perfusión intestinal, aunque su utilidad es controvertida19,20. En los casos en los que no existe una necrosis masiva de todo el intestino delgado pero sí se objetivan zonas claramente no viables, se realiza una resección rápida y conservadora como control de daños y en el mismo tiempo quirúrgico se realiza una revascularización en los casos oclusivos. En pacientes muy inestables, de elevada edad y comorbilidad, con un segmento corto o muy distal, se puede realizar una extirpación aislada sin corrección de la lesión arterial o venosa13.
Las técnicas de revascularización quirúrgicas2,13, tanto la embolectomía como la tromboendarterectomía o diversos pontajes, son técnicas clásicas ampliamente descritas en la literatura y siguen siendo de primera elección en pacientes jóvenes o en casos de laparotomía abierta y sin medios técnicos ni humanos para realizar un abordaje híbrido. Sin embargo, la arteriografía intraoperatoria como complemento en la cirugía abierta puede ser útil en caso de dudas diagnósticas, ofrece un mapa de trabajo y además permite la infusión de vasodilatadores útiles para resolver el espasmo que persiste incluso después de la reperfusión21.
En un auge progresivo encontramos las técnicas endovasculares, de primera elección en pacientes estables y sin datos francos de peritonismo2,5,22–24. La trombólisis, mecánica o farmacológica, puede ser el primer escalón terapéutico9. En los casos de fallo, defecto parcial o clínica progresiva, se puede plantear la canalización de la lesión, realizar una preangioplastia e implantar un stent con sistemas de protección distal en algunos casos. La cirugía abierta se mantiene como último recurso cuando estas técnicas fallan o si aparecen datos de peritonitis o inestabilidad del paciente. Por ello, es importante desarrollarlas en salas donde se pueda realizar esta conversión técnica. Una opción alternativa es el stent retrógrado en pacientes con abdomen abierto. Parece reducir los tiempos quirúrgicos y presenta una alta tasa de éxito6.
Por último, tras una revascularización se debe plantear la necesidad de resección intestinal. En caso de realizarla, esta debe ser conservadora, y programar una segunda exploración, second look, en la que los márgenes de resección se encontrarán más definidos (fig. 2).
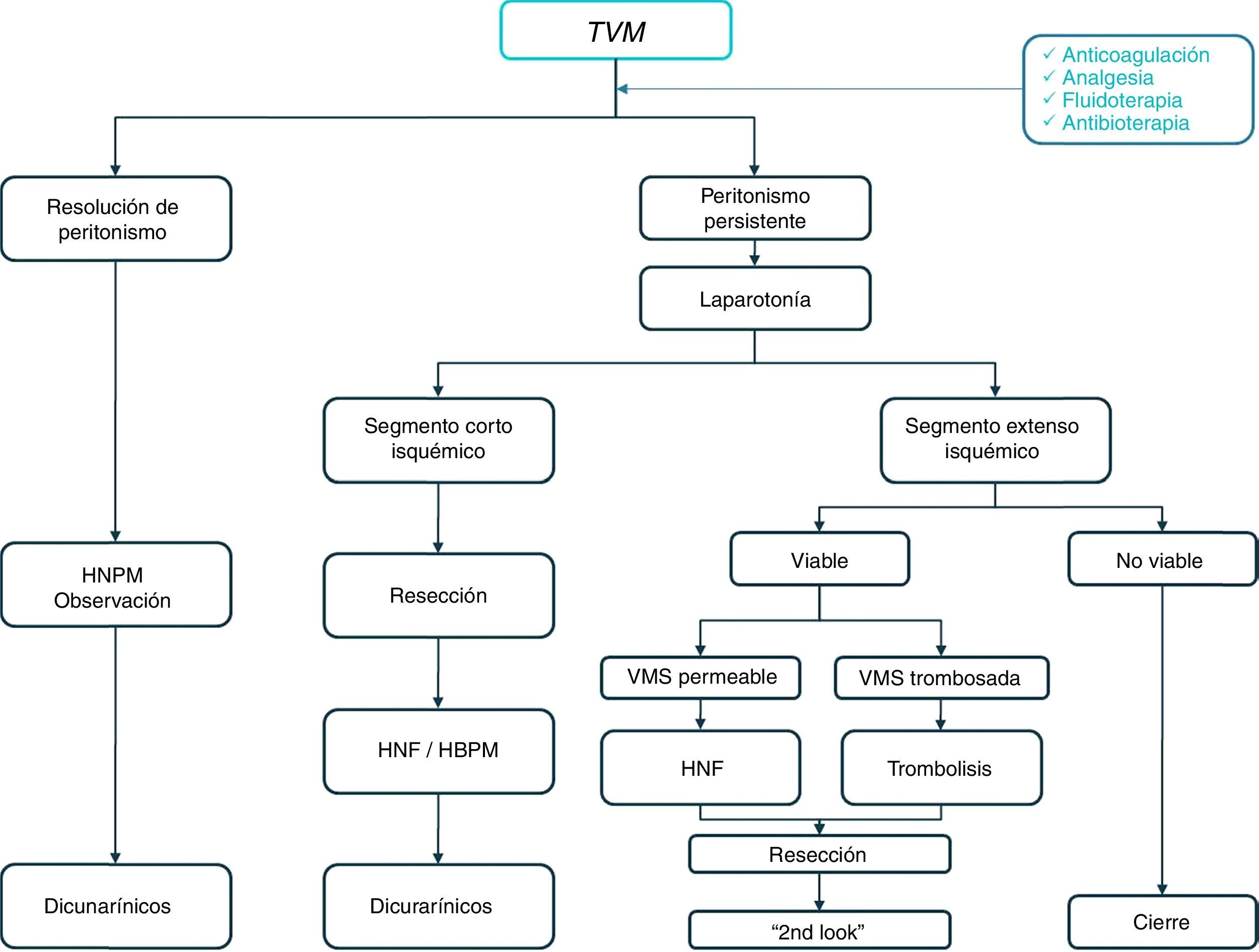
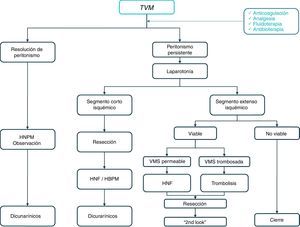
El tratamiento de la TVM y de la IAMNO es en principio médico. La clínica de la TVM se resuelve hasta en un 80% de los casos con anticoagulación25. En aquellos sin respuesta, con clínica progresiva y sin datos de isquemia intestinal avanzada se plantea la posibilidad de trombólisis26,27. La trombectomía quirúrgica no ha demostrado grandes beneficios ante las frecuentes retrombosis (fig. 3). En la IAMNO, los pilares de tratamiento son el soporte hidroelectrolítico, la retirada de vasoconstrictores (en caso de necesitar aminas se prefiere el uso de dobutamina o dopamina a bajas dosis) y, de forma especial, la corrección del desencadenante. La administración de vasodilatadores a nivel local en caso de realización de arteriografía, los inhibidores de la enzima convertidora de angiotensina o el glucagón también han demostrado su beneficio6,17.
Isquemia mesentérica crónicaConocida también como angina intestinal, se caracteriza por una hipoperfusión intestinal paulatina o episódica como consecuencia generalmente de lesiones ateroscleróticas en vasos viscerales a múltiples niveles1,28.
DiagnósticoLa clínica es bastante característica. Dolor abdominal posprandial que conlleva una aversión a la ingesta y pérdida progresiva de peso que puede culminar en un cuadro de IMA. Si ante este cuadro tenemos además a un paciente con factores de riesgo cardiovascular o enfermedad aterosclerótica a otros niveles, debemos pensar en una isquemia mesentérica crónica (IMC)29.
Sin embargo, en ocasiones la clínica se focaliza en una situación de pérdida de peso y con frecuencia el paciente es orientado hacia una posible causa oncológica. Por ello, existe una demora desde el inicio de la sintomatología hasta el tratamiento de hasta 10,7 y 15 meses en algunas series3,30.
Las pruebas de laboratorio, al igual que algunas pruebas de imagen como la radiografía simple, el enema opaco y la endoscopia, son inespecíficas, aunque fundamentales en el diagnóstico diferencial. El estudio del perfil nutricional nos ayudará a ponderar la severidad del cuadro y la necesidad de su corrección.
El ecodoppler, dada su disponibilidad, inocuidad y coste, puede ser la primera opción para identificar estenosis-oclusiones proximales con una sensibilidad que disminuye drásticamente para valorar lesiones distales. La velocidad de ascenso pico-sistólica >275cm/s en AMS y >200cm/s en tronco celiaco se ha correlacionado con estenosis >70% en arteriografía con una sensibilidad del 92% y una especificidad del 96%31.
La angio-TC es la prueba de elección. Permite valorar localización y extensión de la obstrucción, colateralidad, descartar otras posibles causas de abdominalgia y determinar posibles vías de acceso en caso de un tratamiento intervencionista32. La angio-RM, aunque poco disponible y costosa, presenta una gran sensibilidad en manos expertas para valorar estenosis ostiales o proximales, por lo que en ciertos centros recurren a ella como primera herramienta diagnóstica33.
Finalmente, cuando existen dudas diagnósticas o se quiere hacer un estudio dinámico de las vías de colateralidad para una mejor planificación de la revascularización, la arteriografía, siempre en al menos 2proyecciones, es definitoria.
Ante las pruebas de imagen, se define la IMC como la afectación de al menos 2de los 3vasos viscerales. La estenosis aislada de AMS no debe ser considerada como diagnóstica de IMC ya que más del 18% de la población general mayor de 65 años presenta estenosis significativas de tronco celiaco o AMS de forma asintomática. Sin embargo, sí se han descrito anginas intestinales con oclusión completa de AMS y permeabilidad del resto de los vasos viscerales hasta en un 5% de los casos34-36.
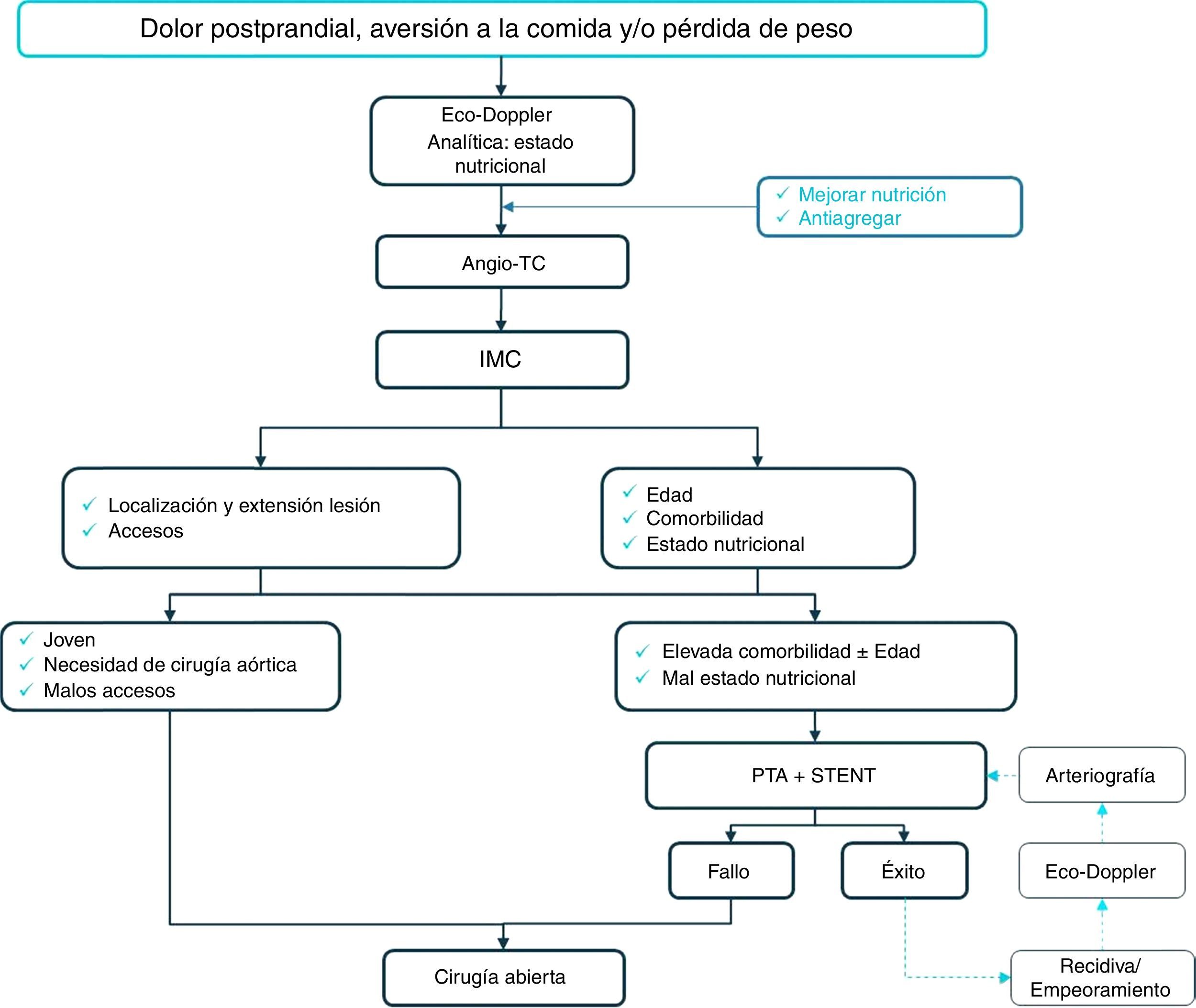
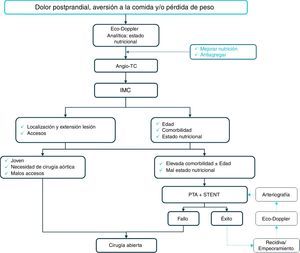
TratamientoEl tratamiento inicial en pacientes asintomáticos radica en el control de los factores de riesgo cardiovascular y en el inicio de antiagregación. En los pacientes sintomáticos, tras un soporte nutricional agresivo, incluso mediante alimentación enteral, se debe plantear una revascularización ante el potencial riesgo de evolución hacia un infarto intestinal o muerte por inanición37. De manera excepcional, en aquellos con clínica esporádica, añosos y de elevada comorbilidad, se puede plantear inicialmente un tratamiento conservador, mediante una dieta baja en grasas y rica en proteínas, con mayor número de ingestas, pero de menor cuantía.
Las técnicas endovasculares son actualmente el tratamiento de elección. Dado su carácter menos agresivo, son de especial interés en pacientes de mayor edad, comorbilidad o peor estado nutricional. Tienen una tasa de éxito técnico >95% y con mejoría de los síntomas en un 90-100% de los casos. Presentan mejores resultados frente a cirugía abierta, en mortalidad (3,5 vs. 7,23%), morbilidad (13,23 vs. 33%) y estancias hospitalarias (4 vs. 18 días) aunque, dada su peor permeabilidad, requieren de un seguimiento más estrecho, generalmente mediante ecodoppler, para solventar las posibles reestenosis3,5,38,39.
Desde el punto de vista técnico, la AMS es el vaso de elección en el procedimiento de revascularización y, en caso de imposibilidad, se trata el tronco celiaco. Sin claro consenso sobre si se debe tratar uno o 2vasos. Existen grupos en los que la tasa de reaparición de la sintomatología es mayor en los casos en los que se trata tan solo un vaso, mientras que en otros no existen diferencias y enfatizan en la mayor complejidad de tratamiento y mayores complicaciones40,41. Se realiza una predilatación y se implanta un stent, generalmente un balón expandible, pero sin datos suficientes para recomendar el uso del stent libre o recubierto. Algunos expertos abogan por el uso de filtros para evitar la embolización distal42.
La cirugía convencional se reserva, en algunos centros, como primera opción en pacientes jóvenes y en aquellos que precisan cirugía aórtica combinada y, como segunda opción, en casos de fallo, imposibilidad o recurrencia de los procedimientos endovasculares43 (fig. 4).
ConclusionesLa IM, en sus 2variantes, aguda y crónica, es una entidad rara en la que los antecedentes del paciente y una clínica muchas veces inespecífica debe poner en alerta a los clínicos para iniciar una batería de pruebas diagnósticas. La angio-TC se ha postulado como la prueba de elección, siempre y cuando el paciente se encuentre estable, aunque la arteriografía sigue siendo el gold standard cuando existen dudas o se plantea un tratamiento endovascular como primera opción terapéutica.
En la IMA, los datos de peritonitis son mandatorios y obligan a realizar una laparotomía inmediata, con el fin de revascularizar y realizar una resección conservadora del intestino afecto. En los casos en los que existe estabilidad del paciente, se plantean inicialmente diversas terapéuticas endovasculares que dependerán del tipo de lesión, tiempo de instauración y recursos técnicos.
En la IMC, la aparición de síntomas obliga a cuidar el estado nutricional del paciente y a plantear una revascularización. Los procedimientos intervencionistas son de elección, siempre que las lesiones sean factibles y accesibles, y especialmente en los pacientes de mayor comorbilidad. En centros de gran experiencia, la cirugía sigue siendo de referencia en pacientes jóvenes por su mayor duración.
Ante la falta de evidencia científica, debido a la escasa incidencia y a la creciente variedad y mejora de los procedimientos endovasculares, se hace importante la creación de algoritmos diagnósticos y terapéuticos por las sociedades científicas44, como es la SEACV, algoritmos que cada centro debe extrapolar a su experiencia y a sus recursos humanos y técnicos.
Responsabilidades éticasProtección de personas y animalesLos autores declaran que para esta investigación no se han realizado experimentos en seres humanos ni en animales.
Confidencialidad de los datosLos autores declaran que han seguido los protocolos de su centro de trabajo sobre la publicación de datos de pacientes.
Derecho a la privacidad y consentimiento informadoLos autores declaran que en este artículo no aparecen datos de pacientes.
Conflicto de interesesLos autores declaran no tener ningún conflicto de intereses.