En cardiología clínica y experimental, los inhibidores de fosfodiesterasa-5 (PDE-5) han atraído el interés científico en años recientes como herramienta terapéutica para el tratamiento de la HAP. Las fosfodiesterasas son una superfamilia de enzimas que inactivan el adenosín monofosfato cíclico y el guanosín monofosfato cíclico, los segundos mensajeros de la prostaciclina y del óxido nítrico. El razonamiento para utilizar los inhibidores de PDE-5 en HAP se basa en su relativa selectividad por la circulación pulmonar y en su capacidad para sobreexpresar la vía del óxido nítrico por inhibición de la hidrólisis del guanosín monofosfato cíclico e incrementar sus concentraciones, lo cual produce efectos vasodilatadores, antiproliferativos y proapoptóticos que pueden revertir el remodelado vascular pulmonar. Además, pueden aumentar el inotropismo ventricular derecho al incrementar el adenosín monofosfato cíclico mediado por la inhibición de la fosfodiesterasa tipo 3 sensible al guanosín monofosfato cíclico.
El sildenafil, el tadalafil y el vardenafil son 3 inhibidores de PDE-5 actualmente en uso clínico que comparten similar mecanismo de acción aunque presentan algunas diferencias significativas en potencia, selectividad por la PDE-5 y propiedades farmacocinéticas.
Para el tratamiento de la HAP en pacientes en clase funcional ii y iii (NYHA/WHO), el sildenafil fue aprobado por la Food and Drug Administration y la European Medicines Agency en 2005; y tadalafil por la Food and Drug Administration y la European Medicines Agency en 2009. En México, el sildenafil y el tadalafil recibieron la aprobación por parte de la Comisión Federal para la Protección contra Riesgos Sanitarios para la misma indicación en 2010 y 2011 respectivamente.
In experimental and clinical cardiology, phosphodiesterase type 5 (PDE-5) inhibitors have brought scientific interest as a therapeutic tool in pulmonary arterial hypertension (PAH) management in recent years. Phosphodiesterases are a superfamily of enzymes that inactivate cyclic adenosine monophosphate and cyclic guanosine monophosphate, the second messengers of prostacyclin and nitric oxide. The rationale for the use of PDE-5 inhibitors in PAH is based on their capacity to overexpresss the nitric oxide pathway pursued inhibition of cyclic guanosine monophosphate hydrolysis. By increasing cyclic guanosine monophosphate levels it promotes vasodilation, antiproliferative and pro-apoptotic effects that may reverse pulmonary vascular remodeling. There is also evidence that these drugs may directly enhance right ventricular contractility through an increase in cyclic adenosine monophosphate mediated by the inhibition of the cyclic guanosine monophosphate -sensitive PDE-3.
Sildenafil, tadalafil and vardenafil are 3 specific PDE-5 inhibitors in current clinical use, which share similar mechanisms of action but present some significant differences regarding potency, selectivity for PDE-5 and pharmacokinetic properties.
Sildenafil received approval in 2005 by the Food and Drug Administration and the European Medicines Agency and tadalafil in 2009 by the Food and Drug Administration and the European Medicines Agency for the treatment of PAH in patients classified as NYHA/WHO functional class II and III. In Mexico, sildenafil and tadalafil were approved by Comisión Federal de Protección contra Riesgos Sanitarios for this indication in 2010 and 2011, respectively.
La fisiopatología de la hipertensión arterial pulmonar (HAP) se caracteriza por fenómenos de vasoconstricción, trombosis, e hiperproliferación celular ocasionados por un estado de disfunción endotelial vascular pulmonar de aparición temprana en el curso de la enfermedad1. La vasoconstricción en su génesis está asociada con el desequilibrio entre los factores vasodilatadores derivados del endotelio (óxido nítrico [ON], prostaciclina) y los vasoconstrictores (endotelina-1, tromboxano) ocasionado por un endotelio vascular disfuncional. Conforme la hipertensión pulmonar avanza, habrá un proceso de remodelación vascular debido a proliferación y apoptosis celular anormal (células de músculo liso vascular, células endoteliales y fibroblastos), con la aparición eventual de lesiones plexiformes características de la enfermedad. Aun cuando las causas que la originan se desconocen, la HAP podría sobrevenir como consecuencia de un fenómeno de «doble repercusión», debido por una parte a anomalías genéticas (v.gr. mutación del gen BMPR2) y por otra a factores ambientales o enfermedades asociadas tales como colagenopatías, hiperflujo pulmonar, medicamentos, virus o toxinas2–4.
En su fisiopatología, se ha señalado entre otros mecanismos, una producción disminuida de ON y aumento en la expresión y actividad de la enzima fosfodiesterasa-5 (PDE-5) en las células de músculo liso vascular y del miocardio ventricular derecho5,6.
Las fosfodiesterasas son una superfamilia de enzimas compuesta de 11 isoenzimas (PDE-1 a PDE-11) que inactivan al adenosín monofosfato cíclico (AMPc) y al guanosín monofosfato cíclico (GMPc), los segundos mensajeros de la prostaciclina y del ON respectivamente, los cuales promueven vasorrelajación. Las fosfodiesterasas tienen diferente afinidad de sustrato y distribución tisular, tal es el caso de la PDE-5, ampliamente investigada, expresada en células de músculo liso, plaquetas, fibroblasto de pulmón y cerebelo, y de la cual se conocen 3 isoformas, A1, A2 y A3. Su principal función es acelerar el proceso de degradación del GMPc y limitar los efectos vasodilatadores del ON y de los péptidos natriuréticos auriculares mediados por la guanilato ciclasa soluble. En cardiología clínica y experimental los inhibidores de la PDE-5 han atraído el interés científico en la última década como herramienta terapéutica para el manejo de la HAP, siendo el sildenafil el más extensamente investigado. El razonamiento para utilizarlos se basa en su relativa selectividad por la circulación pulmonar y en su capacidad para sobreexpresar la vía del ON al inhibir la hidrólisis del GMPc e incrementar sus concentraciones, lo que produce efectos vasodilatadores, antiproliferativos y proapoptóticos que pueden revertir el remodelado arterial pulmonar. Sin embargo, debido a que PDE-5 es expresada también en otros tejidos como la vasculatura arterial coronaria, y vasculatura venosa, músculo esquelético, visceral y traqueobronquial así como en las plaquetas, los efectos de su inhibición resultan complejos. Además, pueden incrementar el inotropismo ventricular derecho mediante el incremento en el AMPc mediado por la inhibición de la fosfodiesterasa tipo 3 sensible al GMPc6–8.
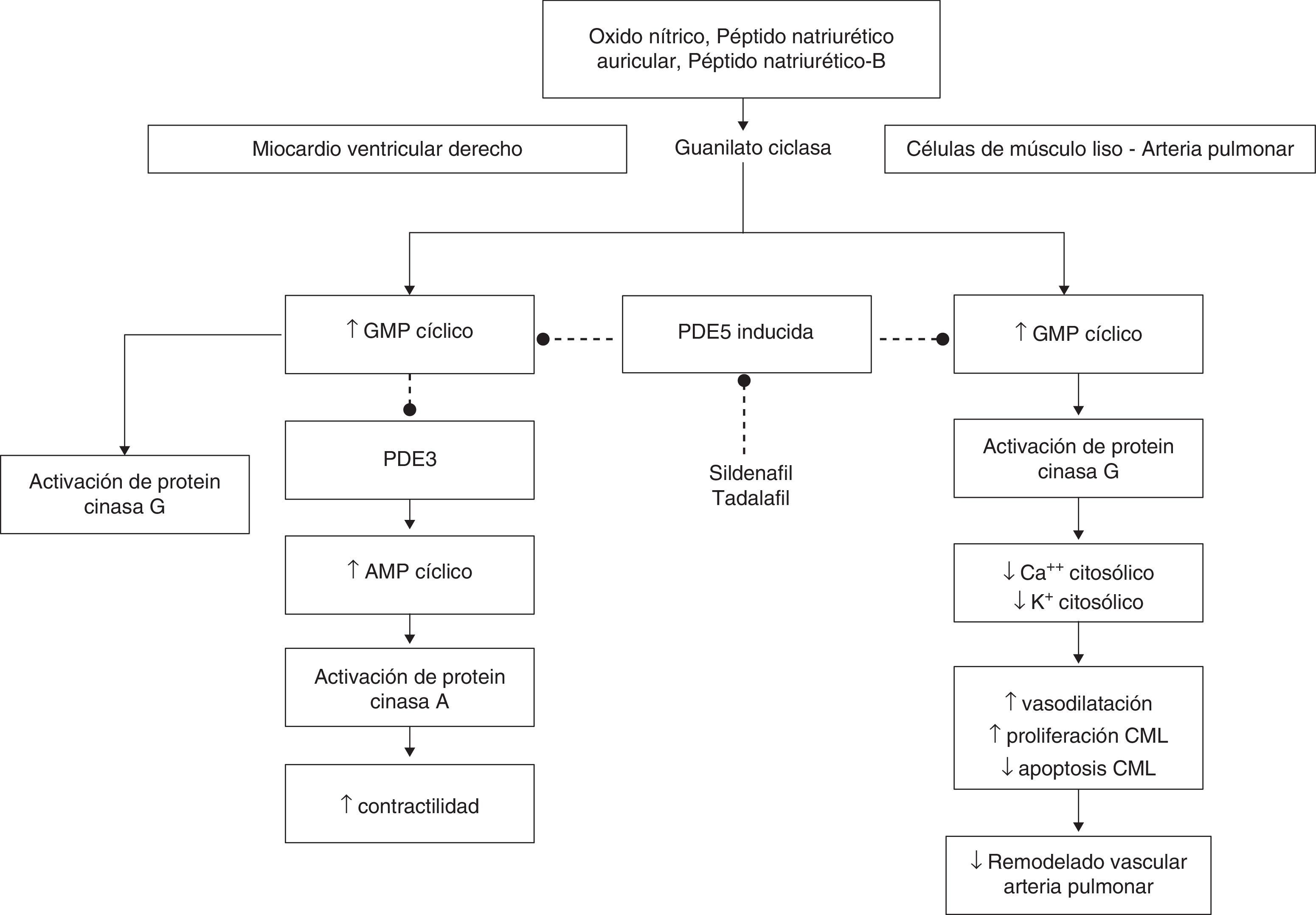
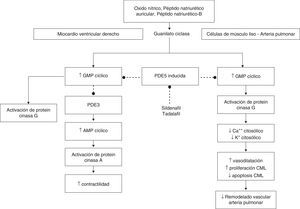
Aunque la PDE-5 no está expresada en el miocardio del ventrículo derecho (VD) normal, el mRNA y la proteína están marcadamente sobreexpresadas (upregulated) en el miocardio del VD hipertrofiado. La PDE-5 está sobreexpresada también en el miocardio hipertrofiado del VD en la rata. La inhibición de PDE-5 (con MY-5445 o con sildenafil) aumenta de manera significativa la contractilidad en el VD hipertrofiado pero no en el VD normal. La inhibición de PDE-5 conduce a aumentos en GMPc y AMPc en VD hipertrofiado pero no en VD normal. La actividad de la proteincinasa G está suprimida en la hipertrofia del VD explicando por qué el incremento de GMPc inducido por la PDE-5 no conduce a inhibición de la contractilidad. Más bien conduce a la inhibición de la PDE-3 GMPc sensible, explicando el aumento del AMPc y de la contractilidad8 (fig. 1).
Efectos de los inhibidores de PDE-5 en la vasculatura pulmonar y el ventrículo derecho.
Los inhibidores de PDE-5 al disminuir la poscarga del ventrículo derecho y aumentar el inotropismo tienen ventaja sobre aquellos fármacos que actúan solo en la vasculatura pulmonar. Al inhibir PDE-5 aumenta el GMPc y el AMPc en el VD hipertrofiado pero no en el VD normal. La actividad de la proteincinasa G está suprimida en HVD y explica por qué el incremento de GMPc inducido por la PDE-5 no inhibe la contractilidad. Más bien conduce a la inhibición de PDE-3 GMPc sensible con aumento del AMPc y de la contractilidad.
En células de músculo liso de la arteria pulmonar incrementa GMPc su efecto, mediado por la activación de proteincinasa G, produce vasodilatación, reducida proliferación celular y aumento en la apoptosis. Ello, disminuye el remodelado vascular y la resistencia vascular pulmonar.
Los inhibidores de la PDE-5 al disminuir la poscarga del VD y aumentar el inotropismo tienen una ventaja sobre aquellos fármacos que actúan solo en la vasculatura pulmonar. Por otra parte, existe evidencia creciente experimental y clínica de los efectos fisiológicos y estructurales favorables en el corazón obtenidos al inhibir la PDE-5 en pacientes con insuficiencia cardíaca de diversa etiología, atribuible a la activación de la proteincinasa G en los miocitos ventriculares y cuyo efecto es dosis-dependiente9–13.
Los 3 inhibidores de la PDE-5 disponibles para uso clínico aprobados inicialmente para el tratamiento de la disfunción eréctil (sildenafil, tadalafil y vardenafil) causan vasodilatación pulmonar significativa. Las principales diferencias están relacionadas con la rapidez y duración de acción, y en menor grado con los efectos indeseables, lo que se atribuye a la capacidad inhibitoria y reactividad cruzada que cada uno tiene sobre las diferentes fosfodiesterasas. La vida media promedio es de 3 a 4h para el sildenafil y el tadalafil y aproximadamente de 18h para el vardenafil.
En 2005, el sildenafil obtuvo la aprobación por parte de la Food and Drug Administration (FDA) y la Agencia Europea de Medicamentos (EMEA) para el tratamiento de la HAP. En el 2009 el tadalafil consiguió su aprobación para esta misma indicación. El vardenafil aún no ha sido aprobado para el tratamiento de la HAP. En México, el sildenafil y el tadalafil recibieron la aprobación de la Comisión Federal para la Protección contra Riesgos Sanitarios (COFEPRIS) para la misma indicación en 2010 y 2011 respectivamente.
A pesar de la similitud en su mecanismo de acción, los inhibidores de la PDE-5 sildenafil, tadalafil y vardenafil presentan algunas diferencias estructurales, farmacológicas y clínicas14.
El sildenafil es un inhibidor preferencial de la PDE-5 con una concentración inhibitoria del 50% (CI50) de 3.5nmol/L, en tanto que para la PDE-6 es de 37nmol/L y para la PDE-1 de 280nmol/L. Una dosis única de 100mg de sildenafil alcanza concentraciones plasmáticas de 1.2μmol, suficiente para inhibir la PDE-1, aumentada en HAP7 lo cual explica en parte su efecto benéfico antiproliferativo al incrementar el AMPc.
Para el tadalafil, la concentración inhibitoria eficaz (CI50) de la PDE-5 es 6.7nmol/L y tiene menos efecto inhibitorio sobre la PDE-6 cuya CI50 es 1,260-1,300nmol/L lo que podría tener importancia relacionada con los efectos secundarios oftalmológicos (descritos abajo), en tanto que el valor de la CI50 para inhibir la PDE-1 es>30,000nmol/L.
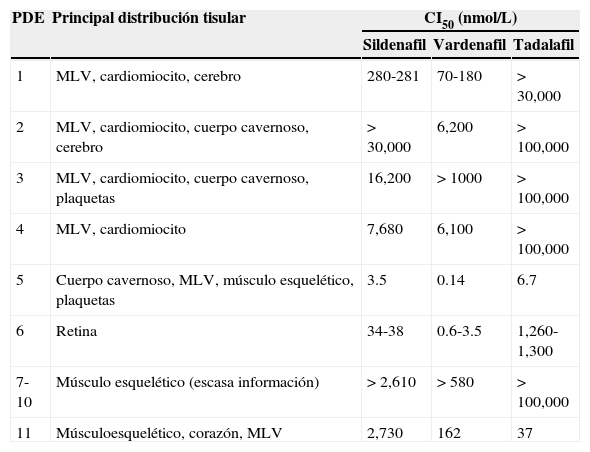
El vardenafil requiere una concentración absoluta menor para inhibir PDE-5 (0.14nmol/L), sin embargo, la selectividad relativa para esta es similar a la de sildenafil. Los valores de la CI50 para inhibir a la PDE-6 son 0.6-3.5nmol/L y para PDE-1 son de 70-180nmol/L (tabla 1).
Características de distintas isoenzimas PDE
| PDE | Principal distribución tisular | CI50 (nmol/L) | ||
|---|---|---|---|---|
| Sildenafil | Vardenafil | Tadalafil | ||
| 1 | MLV, cardiomiocito, cerebro | 280-281 | 70-180 | >30,000 |
| 2 | MLV, cardiomiocito, cuerpo cavernoso, cerebro | >30,000 | 6,200 | >100,000 |
| 3 | MLV, cardiomiocito, cuerpo cavernoso, plaquetas | 16,200 | >1000 | >100,000 |
| 4 | MLV, cardiomiocito | 7,680 | 6,100 | >100,000 |
| 5 | Cuerpo cavernoso, MLV, músculo esquelético, plaquetas | 3.5 | 0.14 | 6.7 |
| 6 | Retina | 34-38 | 0.6-3.5 | 1,260-1,300 |
| 7-10 | Músculo esquelético (escasa información) | >2,610 | >580 | >100,000 |
| 11 | Músculoesquelético, corazón, MLV | 2,730 | 162 | 37 |
CI50: concentración inhibitoria del 50%: MLV: músculo liso vascular; PDE: fosfodiesterasa.
Estas diferencias en selectividad, capacidad inhibitoria y distribución tisular de las diferentes isoenzimas fosfodiesterasas podrían explicar el perfil de efectos secundarios ligeramente diferente que muestra cada uno de ellas15. Así por ejemplo, las alteraciones visuales (discriminación de colores) y el aumento en la sensibilidad a la luz son debidas a la inhibición retiniana de la PDE-6, enzima responsable de la fototransducción. Este efecto secundario es menos frecuente con el tadalafil que con el sildenafil (0.1 vs. 11%, respectivamente). Se ha informado pérdida súbita de la visión con el uso de sildenafil en pacientes tratados por disfunción eréctil. En estos, se ha diagnosticado neuropatía óptica isquémica anterior no arterítica sin que se haya establecido una relación causal con la utilización de dicho fármaco. Las mialgias y el dolor de espalda se relacionan con inhibición de la PDE-5 localizada en el músculo esquelético, en tanto que la rubicundez, cefalea y la epistaxis se atribuyen a la inhibición de PDE-5 localizada en células de músculo liso vascular de pequeños vasos. Cabe mencionar que la tendencia a la hipotensión con la utilización de inhibidores de PDE-5 es una preocupación latente. Sin embargo, la magnitud de la disminución de la presión arterial sistémica depende del grado de activación de la vía de la guanilato ciclasa-ON (sGC-ON), efecto que puede ser potenciado por el uso combinado con los nitratos al ocasionar la acumulación de GMPc con el riesgo potencial de causar hipotensión refractaria. Por lo tanto, estos no deben utilizarse en combinación. Lo mismo sucede con los estimuladores de la guanilato ciclasa (p. ej., riociguat) una nueva generación de fármacos para el tratamiento de la HAP, que aumenta la sensibilidad y la actividad de la vía sGC-ON y su uso combinado está contraindicado. Por otra parte, en pacientes con hipotensión arterial basal y/o presíncope se recomienda iniciar con dosis baja. Utilizados como monoterapia el sildenafil, el tadalafil y el vardenafil tienen un efecto leve sobre la presión arterial; Zusman et al. informaron una reducción en la presión sistólica-diastólica de 7 a 10mmHg después de la administración de sildenafil, efecto que no fue dosis-dependiente16. En pacientes hipertensos se ha demostrado que la combinación de sildenafil con una amplia gama de antihipertensivos es bien tolerada. Por último, el sildenafil no tiene efecto teratogénico, a diferencia de los antagonistas de los receptores de le endotelina, lo cual es relevante en una enfermedad que es común en mujeres aún en edad reproductiva17.
En un estudio prospectivo, Ghofrani et al.18 compararon los efectos clínicos agudos de los 3 inhibidores de PDE-5 sobre la hemodinámica sistémica y pulmonar y de los parámetros de intercambio gaseoso en 60 pacientes con HAP. El sildenafil en dosis oral única de 50mg causó disminución en la presión arterial pulmonar media (PAPm) de −16.2% (IC −11.6 a −21.5) y aumento en el índice cardíaco del 13.2% (IC 9.9 a 17.1). El efecto vasodilatador máximo se obtuvo a los 60min. La selectividad pulmonar del efecto vasodilatador se observó al alcanzar una reducción máxima de la PVRI de −28% (IC −26.1 a −31.2) y reducción del cociente PVR/SVR de −15.5% (IC −11.1 a −21.3). También se pudo observar un incremento significativo en la pO2 arterial del 8.9% (IC 1.2 a 22.9) y no se reportaron eventos adversos.
El vardenafil en dosis de 10 y 20mg por vía oral causó disminución de la PAPm de −14.3% (IC −5.6 a −23.1) y −12.1% (IC −7.3 a −15.8) respectivamente. El índice cardíaco aumentó un 9.3% (IC 1.8 a 18.7) con 10mg y un 18.4% (IC 9.8 a 25.1) después de 20mg en tanto que la reducción de la PVRI fue de −21.6% (IC −10.2 a −32.3) y de −26.3% (IC −22.8 a −29.2) respectivamente. El efecto vasodilatador máximo se alcanzó a los 41.3min con 10mg y a los 45min con 20mg. Una observación interesante fue la reducción equipotente de las SVR y PVR con cocientes de PVR/SVR de −6.9 (IC −24.8 a 15.2) con 10mg y −0.1 (IC −8.2 a 4.2) con 20mg. La saturación arterial de oxígeno se mantuvo inalterada. No obstante su falta de selectividad vascular pulmonar, solo se reportaron eventos adversos menores en el 30% de los casos (rubicundez y cefalea leve).
El tadalafil por vía oral, en dosis de 20, 40 y 60mg disminuyó la PAPm −12.6% (IC −3.6 a −24.2), −18.3% (IC −13.9 a −21.8) y −10% (IC −22.1 a 1.1) respectivamente; a la vez se observó un incremento en el índice cardíaco del 9.3% (IC −4.8 a 15.4), 7.5% (IC −4 a 20.7) y 18.8% (IC 3.3 a 36.7). El efecto vasodilatador máximo se alcanzó a los 75, 90 y 86.3min con 20, 40 y 60mg de tadalafil, en tanto que las PVRI disminuyeron −18.6% (IC −14 a −28.4), −27.1% (IC −14.2 a −39.8) y −26.7% (IC −19.9 a −39.8) respectivamente. Cabe señalar la disminución significativa incluso hasta con la dosis de 60mg en las PVR/SVR de −11.4% (IC −2.8 a −33.9) reflejo de la selectividad del tadalafil sobre la circulación pulmonar. La PaO2 permaneció sin cambio con cualquiera de las dosis. No se reportaron eventos adversos.
En resumen, la expresión de fosfodiesterasas por el tejido pulmonar es abundante, en particular los tipos 1, 3, 4 y 5, lo cual explica el efecto vasodilatador pulmonar preferente mostrado por sildenafil al disminuir casi un 30% las PVRI y un 15% el cociente PVR/SVR además de mejorar la relación ventilación–perfusión al incrementar la oxigenación arterial. En contraposición y a pesar de su similitud estructural y farmacológica, el vardenafil en dosis de 10 y 20mg mostró reducciones equipotentes de la PVRI y PVR/SVR reflejo de su falta de selectividad pulmonar en respuesta a ambas dosis y sin cambios en la oxigenación arterial. Por último, el tadalafil mostró selectividad por la circulación pulmonar al reducir PVRI y el cociente PVR/SVR pero sin modificar de manera favorable la relación ventilación-perfusión al no modificar la oxigenación arterial. Debido a que el sildenafil fue el único que mejoró la oxigenación arterial, se especula que quizás el sildenafil sea un vasodilatador pulmonar muy selectivo que amplifica procesos de señalización vasorreguladora local mediante GMPc, lo cual optimiza la perfusión con relación a la distribución de la ventilación18.
El sildenafil y el tadalafil son metabolizados predominantemente por la enzima hepática citocromo P450 3A4 y parcialmente por la isoenzima 2C9 por lo que su depuración se afecta con el uso concomitante de inhibidores o inductores de dichas isoenzimas (v.gr. antifúngicos, retrovirales, antibióticos, antagonistas de los receptores de la endotelina)19–21. Tal es el caso del bosentán, inductor de la CYP3A4 y 2C9 que disminuye la concentración plasmática del sildenafil en más del 50%, aunque al parecer esta interacción es menor con el uso del tadalafil20. Por el contrario, la exposición en plasma de sildenafil aumenta con el empleo de inhibidores de proteasas como el ritonavir y el saquinavir, con sus implicaciones inherentes en el tratamiento de la HAP asociada a infección por VIH. Por otra parte, el metabolismo hepático del vardenafil es mediante la enzima CYP3A4 con alguna contribución de la CYP3A5.
En presencia de disfunción renal leve a moderada no es necesario modificar la dosis del sildenafil ni del vardenafil; en cambio, se recomienda disminuir la dosis del tadalafil a 20mg/día. Hacen falta estudios en pacientes con daño renal y hepático grave.
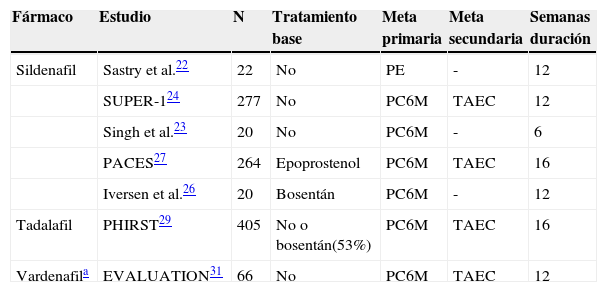
Evidencia clínicaSildenafilEl sildenafil es un compuesto activo por vía oral con gran selectividad por la PDE-5, administrado 3 veces/día. Cinco estudios aleatorizados, controlados, en pacientes con HAP tratados con sildenafil han reportado mejoría en síntomas, capacidad al ejercicio y hemodinámica22–27 (tabla 2).
Características de los estudios aleatorizados con inhibidores de PDE-5
| Fármaco | Estudio | N | Tratamiento base | Meta primaria | Meta secundaria | Semanas duración |
|---|---|---|---|---|---|---|
| Sildenafil | Sastry et al.22 | 22 | No | PE | - | 12 |
| SUPER-124 | 277 | No | PC6M | TAEC | 12 | |
| Singh et al.23 | 20 | No | PC6M | - | 6 | |
| PACES27 | 264 | Epoprostenol | PC6M | TAEC | 16 | |
| Iversen et al.26 | 20 | Bosentán | PC6M | - | 12 | |
| Tadalafil | PHIRST29 | 405 | No o bosentán(53%) | PC6M | TAEC | 16 |
| Vardenafila | EVALUATION31 | 66 | No | PC6M | TAEC | 12 |
PC6M: prueba de caminata de 6min; PE: prueba de esfuerzo; TAEC: tiempo a empeoramiento clínico.
En el estudio multicéntrico, aleatorizado, doble-ciego Sildenafil use in pulmonary arterial hypertension (SUPER) que incluyó a 278 pacientes con HAP idiopática, asociada a enfermedad del tejido conectivo, y cardiopatías congénitas en clase funcional ii-iii (NYHA/WHO), se comparó la terapia con sildenafil 20, 40 y 80mg por vía oral cada 8h frente a placebo. El objetivo primario fue el cambio con relación al basal en la prueba de caminata de 6min (PC6M) a las 12 semanas de seguimiento. En sus resultados se pudo observar un incremento de +45, +46 y +50m en los grupos que recibían sildenafil (p<0.001), respectivamente. Las 3 dosis lograron reducir la PAPm −2.1, −2.6 y −4.7mmHg (p<0.001); las resistencias pulmonares −122, −143 y −261dyn.sec.com−5 (p<0.001); y también aumentó el índice cardíaco 0.21, 0.24 y 0.27l/min/m2 (p<0.001), respectivamente. También hubo mejoría en la clase funcional. El tiempo a empeoramiento clínico (muerte, trasplante, hospitalizaciones por empeoramiento de HAP, o inicio de terapia adicional para HAP) con el uso del sildenafil comparado con placebo no fue estadísticamente significativo pero las hospitalizaciones por empeoramiento de la HAP fue mayor en el grupo placebo (p=0.02). La mayoría de los eventos adversos reportados con las 3 dosis fueron de leve a moderada intensidad (rubicundez, dispepsia y diarrea) y no hubo cambios clínicamente significativos en las variables de laboratorio. En el estudio de extensión a un año en el que utilizaron 80mg por vía oral 3 veces/día, se observó un incremento sostenido en la PC6M de +51m, con disminución de resistencias vasculares pulmonares y de la PAPm.
El Pulmonary arterial hypertension combination study of epoprostenol and sildenafil (PACES) evaluó los efectos de agregar sildenafil a la terapia con epoprostenol en 264 pacientes y demostró mejoría en la PC6M +28m (objetivo primario) a las 16 semanas de seguimiento, en particular en aquellos que caminaban>325m desde la basal, además de la hemodinamia y en el tiempo a empeoramiento clínico comparado con placebo27.
En la actualidad, el sildenafil 20mg 3 veces/día por vía oral es la dosis aprobada por la FDA y la EMEA, basándose en los resultados del estudio SUPER, cuyo beneficio en la PC6M no fue dosis-dependiente pero sí en las variables hemodinámicas con un beneficio creciente en las dosis de 40 y 80mg. Por otra parte, en estudios de titulación de dosis, se ha mostrado mejoría incluso en la capacidad funcional con dosis mayores aunque limitada por sus efectos secundarios atribuibles a vasodilatación (cefalea, rubicundez, congestión nasal y epistaxis).
Debido a sus características farmacocinéticas, una forma de administración intravenosa fue aprobada por la FDA y EMEA, para pacientes en tratamiento a largo plazo con dificultad para deglutir como terapia temporal de sustitución28.
TadalafilEl tadalafil es un compuesto activo por vía oral administrado una vez al día, con elevada selectividad por la PDE-5. El estudio Pulmonary arterial hypertension and response to tadalafil (PHIRST) doble ciego controlado con placebo incluyó a 405 pacientes (HAP idiopática y asociada) en clase funcional ii-iii (NYHA/WHO), previamente tratados o no con bosentán (53%) aleatorizados a placebo o tadalafil 2.5, 10, 20 y 40mg vía oral una vez al día. La meta primaria fue el cambio a las 16 semanas con relación a la basal en la distancia caminada en 6min. Evaluó también la clase funcional, empeoramiento clínico y calidad de vida. El tadalafil incrementó la distancia recorrida de manera dosis-dependiente pero solo la dosis de 40mg alcanzó significación estadística (p<0.01) preespecificada; el efecto global fue +33m (corregido con placebo). El tadalafil 40mg, mejoró el tiempo a empeoramiento clínico (p=0.041). Los cambios en la clase funcional no fueron estadísticamente significativos y los efectos secundarios más frecuentes fueron cefalea, mialgias y rubicundez29 (tabla 2).
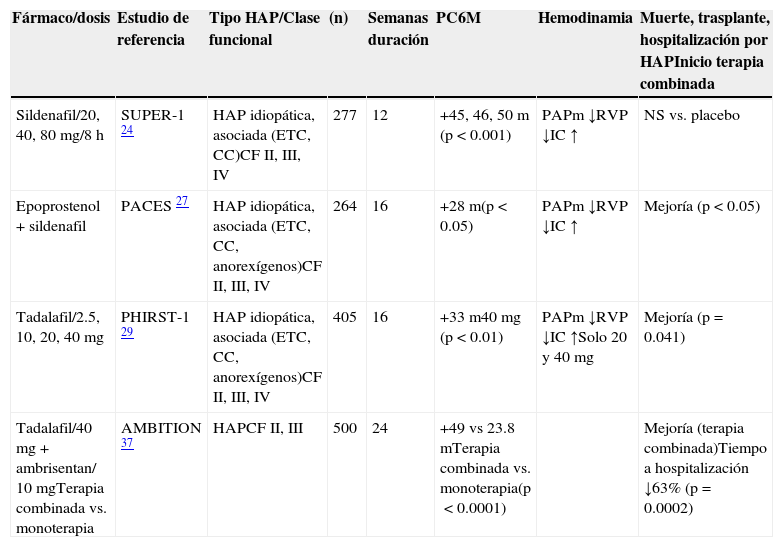
Los pacientes del estudio PHIRST (n=357) fueron elegidos para participar en el estudio PHIRST-2, una fase de extensión de 52 semanas, doble-ciego, no controlado, para evaluar durabilidad de la eficacia y seguridad a largo plazo con tadalafil 20 y 40mg. Se utilizó la PC6M en la evaluación de la durabilidad de la eficacia. También el tiempo a empeoramiento clínico y cambio en la clase funcional fueron evaluados. En sus resultados el tadalafil fue bien tolerado a largo plazo, además, los pacientes que recibían 20 y 40mg mostraron un efecto sostenido de mejoría en la PC6M (415±80 y 410±78m, respectivamente) al final del estudio comparado con el basal (PHIRST). El evento adverso más común fue cefalea, reportada en el 14% y en el 16% en pacientes con 20mg y con 40mg, comparado con el 32% y el 42% reportado en PHIRST, lo que muestra que cede con el tiempo. En 91 pacientes (25.5%) ocurrieron efectos adversos serios, incluyendo 11 muertes, en su mayoría relacionados con la HAP. En un análisis relacionado (post-hoc), los pacientes que recibían terapia de respaldo con bosentán y con mejor capacidad funcional (PC6M) en el estudio PHIRST, tuvieron menor incidencia de eventos de empeoramiento clínico. Entre aquellos que recibieron 20mg y 40mg desde el principio, solo el 9% y el 6% respectivamente mostraron deterioro en la clase funcional (NYHA/WHO), en tanto que el 34% de los pacientes con ambas dosis tuvo mejoría en comparación con la basal en PHIRST. En la actualidad, tadalafil 40mg es la dosis recomendada por la FDA29,30(tabla 3).
Resultados de los principales estudios aleatorizados
| Fármaco/dosis | Estudio de referencia | Tipo HAP/Clase funcional | (n) | Semanas duración | PC6M | Hemodinamia | Muerte, trasplante, hospitalización por HAPInicio terapia combinada |
|---|---|---|---|---|---|---|---|
| Sildenafil/20, 40, 80mg/8h | SUPER-1 24 | HAP idiopática, asociada (ETC, CC)CF II, III, IV | 277 | 12 | +45, 46, 50m (p<0.001) | PAPm ↓RVP ↓IC ↑ | NS vs. placebo |
| Epoprostenol+sildenafil | PACES 27 | HAP idiopática, asociada (ETC, CC, anorexígenos)CF II, III, IV | 264 | 16 | +28m(p<0.05) | PAPm ↓RVP ↓IC ↑ | Mejoría (p<0.05) |
| Tadalafil/2.5, 10, 20, 40mg | PHIRST-1 29 | HAP idiopática, asociada (ETC, CC, anorexígenos)CF II, III, IV | 405 | 16 | +33m40mg (p<0.01) | PAPm ↓RVP ↓IC ↑Solo 20 y 40mg | Mejoría (p=0.041) |
| Tadalafil/40mg+ambrisentan/ 10mgTerapia combinada vs. monoterapia | AMBITION 37 | HAPCF II, III | 500 | 24 | +49 vs 23.8mTerapia combinada vs. monoterapia(p<0.0001) | Mejoría (terapia combinada)Tiempo a hospitalización ↓63% (p=0.0002) |
CF: clase funcional; ETC: enfermedad tejido conectivo; CC: cardiopatías congénitas; HAP: hipertensión arterial pulmonar; IC: índice cardíaco; PAPm: presión arterial pulmonar media; PC6M: prueba de caminata de 6min; RVP: resistencia vascular periférica.
El vardenafil es un inhibidor de PDE-5 de gran selectividad, activo por vía oral, administrado 2 veces/día. En el estudio aleatorizado y controlado Efficacy and safety of vardenafil in the treatment of pulmonary arterial hypertension (EVALUATION) 66 pacientes recibieron vardenafil 5mg 2 veces/día, y mostraron efectos favorables en capacidad al ejercicio, hemodinámica y tiempo a deterioro clínico. El vardenafil aún no ha sido aprobado para el tratamiento de la HAP. El perfil de efectos secundarios es similar al del sildenafil31.
RecomendacionesLa era moderna del tratamiento específico para la HAP comienza a finales de la década de los noventa con la introducción del epoprostenol y 9 años más tarde es aprobado el primer inhibidor de PDE-5, sildenafil. Sin duda, se han logrado avances significativos en el tratamiento de la enfermedad al mejorar la capacidad funcional, el tiempo a empeoramiento clínico y la calidad de vida de los enfermos. Por desgracia, no hay estudios reales de supervivencia con este grupo de fármacos y solo existen estudios comparativos con controles históricos (registro NIH)32 excepto con el epoprostenol y más recientemente macitentan (antagonista de receptores de endotelina); además, la falta de estudios comparativos fármaco-fármaco hace virtualmente imposible recomendar el de primera elección por lo que la selección del fármaco debe basarse en el estado de aprobación (registro sanitario), clase funcional, comorbilidad, disponibilidad, costo y experiencia del médico.
Las guías para el tratamiento de la hipertensión pulmonar de la American Heart Association y el American College of Cardiology publicadas en 2009, recomiendan sildenafil y tadalafil (nivel de evidencia I-A y I-B, respectivamente) en pacientes con HAP (grupo i) en clase funcional ii y iii (NYHA/WHO)33.
En el quinto simposio mundial de hipertensión pulmonar celebrado en 2013, el panel de expertos recomendó entre otras opciones, como monoterapia, la utilización del sildenafil o del tadalafil en pacientes con HAP en clase funcional ii-iii (NYHA/WHO) con un nivel de evidencia I-A34. El sildenafil o el tadalafil están indicados además en pacientes en clase funcional iv (NYHA/WHO). Sin embargo, el número de pacientes incluidos en los estudios aleatorizados para su aprobación es reducido por lo que la mayoría de los expertos considera estos tratamientos como segunda opción en pacientes gravemente enfermos (IIa-C). En este contexto, los prostanoides parenterales deben ser la terapia de inicio debido a que estos fármacos mejoran el pronóstico a corto plazo34.
La experiencia con inhibidores de PDE-5 en terapia combinada para el tratamiento de HAP es limitada pero promisoria. En pacientes con HAP grave y deterioro clínico a pesar del tratamiento con prostanoides, la adición del sildenafil al iloprost inhalado tuvo un efecto hemodinámico favorable y mejoría de la clase funcional35. Resultados similares con sildenafil 50mg administrado 3 veces/día asociado a treprostinil36 o epoprostenol27 han sido descritos en estudios pequeños. En cambio, la combinación de sildenafil y bosentán no fue superior a la monoterapia con bosentán con respecto a la PC6M (meta primaria) y solo mejoró la saturación arterial de oxígeno en reposo en pacientes con HAP debida a cardiopatía congénita26. En fecha reciente el estudio multicéntrico aleatorizado, controlado con placebo, doble ciego, A randomized, multicenter study, of first-line of ambrisentan and tadalafil combination therapy in subjects with pulmonary arterial hypertension (AMBITION) comparó el tadalafil 40mg y el ambrisentan 10mg en monoterapia en comparación con la combinación de ambos fármacos para evaluar la eficacia y seguridad de la terapia combinada inicial, en pacientes con HAP en clase funcional ii-iii (NYHA/WHO). La meta primaria fue el tiempo al primer evento de falla clínica, definido como el tiempo desde la aleatorización a la primera incidencia de muerte, hospitalización, o empeoramiento clínico. La terapia combinada logró reducir un 50% el riesgo de falla clínica en comparación con la monoterapia (RR=0.502; IC 95%: 0.348, 0.724; p=0.0002). El efecto del tratamiento observado sobre la meta primaria fue debido principalmente a la reducción en hospitalizaciones. El tiempo a la primera hospitalización fue retrasado un 63% (RR=0.372; IC95%: 0.217, 0.639; p=0.0002). La terapia de combinación también tuvo resultados estadísticamente significativos en diversas metas secundarias comparada con la monoterapia, al demostrar el cambio de la basal a la semana 24 en la concentración de N-terminal propéptido natural tipo-B (−67.4% vs. −49.7%; p<0.0001), el porcentaje de pacientes con respuesta clínica satisfactoria a las 24 semanas (39% vs. 29%; p=0.026) y un cambio promedio en la PC6M de la basal a la semana 24 de seguimiento (49 vs. 23.8m; p<0.0001). La clase funcional (NYHA/WHO) basal y a la semana 24 no mostró diferencia entre grupos. Aun cuando los eventos adversos fueron más frecuentes con la combinación (edema periférico 46%, cefalea 42%, congestión nasal 21%, y anemia 15%), la tasa de eventos adversos serios y los que llevaron a la suspensión del tratamiento fue similar para todos los grupos37.
Aspectos relevantes a considerarDesde el punto de vista epidemiológico, la hipertensión pulmonar asociada a enfermedad cardíaca izquierda por disfunción diastólica o sistólica es, con mucho, la forma más común de hipertensión pulmonar38. En algunos pacientes este diagnóstico se confunde con el de HAP y son tratados de manera errónea en consecuencia. Aun cuando hay información preliminar con el uso del sildenafil en pacientes con insuficiencia cardíaca crónica que muestra que puede ser seguro e incluso benéfico, la recomendación para su aplicación en la práctica diaria debe esperar resultados de ensayos clínicos aleatorizados39–41. Cabe agregar que aunque algunos estudios han sugerido que los inhibidores de PDE-5 pueden ser utilizados en hipertensión pulmonar secundaria, la aprobación de la FDA no incluyó esta indicación, y la evidencia que lo sustenta es limitada.
El uso indiscriminado del sildenafil en pacientes con elevación de la presión pulmonar como criterio diagnóstico aislado de HAP determinado solo por ecocardiografía, se ha vuelto una práctica común en nuestro medio y en diferentes partes del mundo. Utilizar este método de estudio de manera sistemática para la confirmación diagnóstica es un error metodológico, por omisión, que tiene implicaciones en el costo-beneficio de la terapéutica vasodilatadora, no carente de riesgo, y que no se justifica. Si bien el ecocardiograma forma parte integral en la detección y evaluación de los pacientes con hipertensión pulmonar, las guías para el diagnóstico y tratamiento de la HAP establecen como requisito indispensable para la confirmación diagnóstica y evaluación de la gravedad la realización del cateterismo cardíaco derecho con mediciones de la PAP diastólica, PAPm, PCWP, diferencia de presión diastólica (PAPd-PCWP), PVR, RAP y gasto cardíaco42,43. Además, permite realizar el reto farmacológico con un vasodilatador pulmonar selectivo de acción ultracorta (p. ej., ON), para detectar a pacientes con vasorreactividad que tienen mejor pronóstico y son susceptibles de ser tratados con un bloqueador de los canales de calcio. Finalmente, es importante recordar que los pacientes con diagnóstico de hipertensión pulmonar deben ser estudiados de manera exhaustiva que permita por eliminación, descartar formas secundarias de hipertensión. Por lo tanto es recomendable que aquellos pacientes con HAP, candidatos a recibir tratamiento (p. ej., inhibidores de la PDE-5), se sometan previamente a una cuidadosa evaluación clínica realizada por un experto en hipertensión pulmonar.
FinanciaciónNo se recibió patrocinio de ningún tipo para llevar a cabo este artículo.
Conflicto de interesesLos autores no tienen ningún conflicto de interés relacionado a este artículo.