Introducción
El cuidado intensivo perioperatorio del paciente sometido a un procedimiento cardiovascular es sumamente complejo, aún más en el paciente de alto riesgo. El riesgo quirúrgico elevado en cirugía cardiovascular es un tema muy vasto e incluye procedimientos de revascularización coronaria, valvulares, aórticos, congénitos o de remodelación ventricular, que no podrían abarcarse de manera exhaustiva en el presente trabajo, si bien en este capítulo se describe en cierta medida la intervención coronaria dado que se trata de la operación cardiaca más frecuente.
Por lo regular, el alto riesgo se ha relacionado con uno o más de los siguientes factores: edad avanzada, sexo femenino, trastornos concomitantes como hipertensión arterial, diabetes mellitus, enfermedad pulmonar obstructiva crónica, insuficiencia renal crónica, infarto agudo del miocardio, operación cardiaca previa, disección aórtica aguda, o bien con alguna enfermedad agregada de riesgo elevado como la insuficiencia renal aguda, choque cardiogénico o comunicación interventricular posterior a un infarto.
Algunos datos señalan que se ha incrementado el riesgo en la cirugía cardiovascular en las últimas décadas y se han identificado como causas la edad avanzada, el sexo femenino y la obesidad, en la cuales existe escasa o ninguna posibilidad de intervención por parte del paciente o el médico.
Protección miocárdica
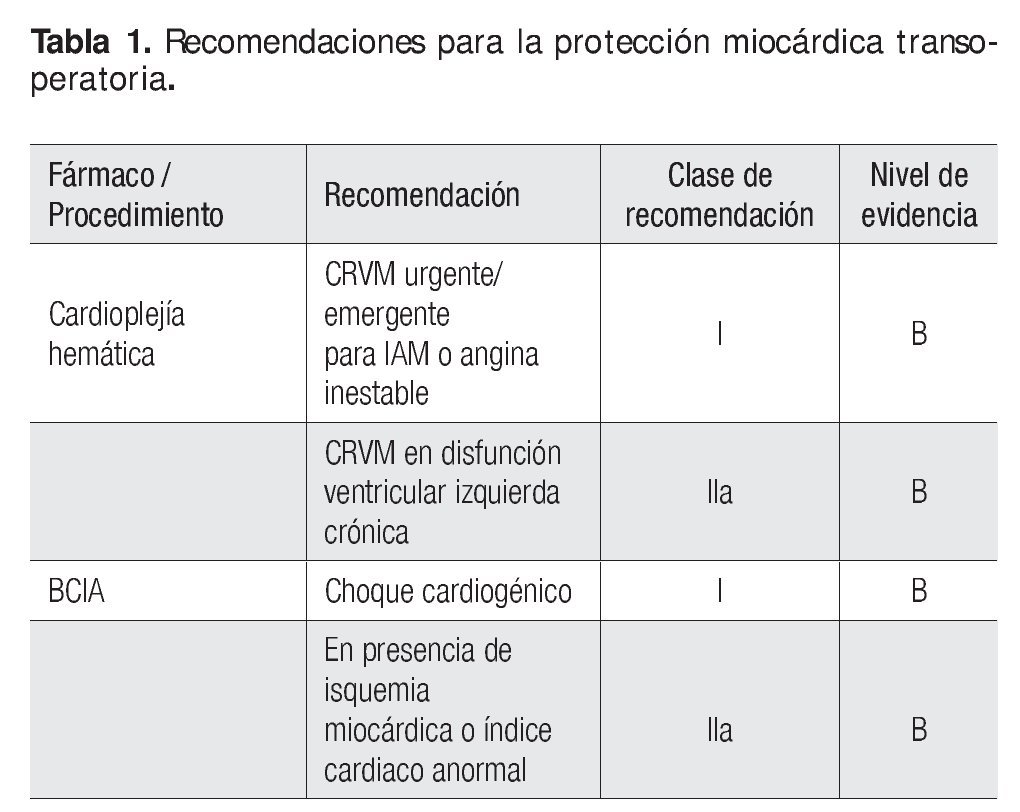
Durante el procedimiento de cirugía de corazón siempre se presentan (en diversos grados) diferentes mecanismos de lesión miocárdica, muchos de ellos relacionados con el uso de la bomba de circulación extracorpórea y otros con la anomalía misma; pueden mencionarse también la isquemia miocárdica, el daño por reperfusión o el aturdimiento miocárdico. Es por ello que desde hace varias décadas se han diseñado medidas que intentan minimizar este daño: la denominada protección miocárdica. Existe una amplia variedad de medios y forma de protección miocárdica, pero en los pacientes con función cardiaca normal es difícil encontrar en los estudios algunos que registren una mejoría significativa. Esto no ocurre en aquellos en quienes existe evidencia de insuficiencia cardiaca, ya sea aguda o crónica (Tabla 1).
Edad avanzada
En el paciente de edad avanzada, la mortalidad calculada es de 1.65% para el grupo etario de 50 a 60 años y se eleva en grado considerable en los mayores de 80 años, aunque se consigue una notable mejoría en la calidad de vida, lo cual debe llevar a valorar la relación riesgo-beneficio en estos individuos. Su atención es similar respecto de los pacientes más jóvenes y la morbimortalidad sólo se incrementa por enfermedades concomitantes. En este sentido, los pacientes mayores se benefician más de una cirugía de revascularización miocárdica (CRVM) y menos de una angioplastia (ACTP) en ausencia de falla cardiaca, enfermedad pulmonar o vascular periférica, por lo que debe considerarse en primer instancia en personas > 80 años de edad.
Se ha observado que los individuos > 65 años, así como las personas más jóvenes pero de sexo femenino, tienden a recibir bloqueadores β en menor cantidad o menos veces que los pacientes < 65 años o de sexo masculino, lo que predispone a mayores complicaciones posquirúrgicas (Tabla 2).
Obesidad
En un estudio de Engel y colaboradores efectuado en el Hospital del Buen Samaritano en Cincinnati, Ohio, se notificó la inexistencia de un riesgo adicional entre los pacientes con sobrepeso, obesidad y peso adecuado, de acuerdo con el índice de masa corporal (IMC), incluidos los pacientes obesos mórbidos (IMC > 40). No ocurre así entre los enfermos con bajo peso, para los cuales se encontró un riesgo mayor de morbilidad y mortalidad. Sin embargo, el estudio de Prabhakar de la base de datos de la Sociedad de Cirujanos de Tórax de Estados Unidos registra un incremento de la morbilidad en sujetos mórbidamente obesos (IMC > 40), si bien este estudio tiene la desventaja de que no incluyó a pacientes con bajo peso para su análisis. No se dispone aún de datos procedentes de estudios controlados y aleatorizados en el aspecto de obesidad para inferir conclusiones, por lo que resulta necesaria la conducción de mayores estudios (Tabla 3).
Sexo femenino
De acuerdo con estadísticas de Estados Unidos, de las intervenciones coronarias percutáneas practicadas en 2006, sólo 35% se realizó en mujeres, sobre todo en aqéllas con síndrome isquémico coronario agudo (SICA) de alto riesgo; más aún, la mortalidad no ajustada y las complicaciones fueron mayores respecto del sexo masculino. Además de estos datos, también se observa mayor frecuencia de edad avanzada, de SICA NST (SICA sin elevación del segmento ST), más comorbilidades, menor acceso al laboratorio de cateterismo y por ende menos intervenciones de revascularización; asimismo es más frecuente la presencia de choque cardiogénico. Como ya se mencionó, se ha observado que los sujetos > 65 años, o personas más jóvenes pero de sexo femenino, tienden a recibir menor cantidad de bloqueadores β; esto ha llevado a considerar que el sexo femenino no es específicamente un factor de riesgo independiente para la CRVM, sino que su relación se atribuye a la falta de oportunidad en tiempo y forma de dicho procedimiento.
Arritmias
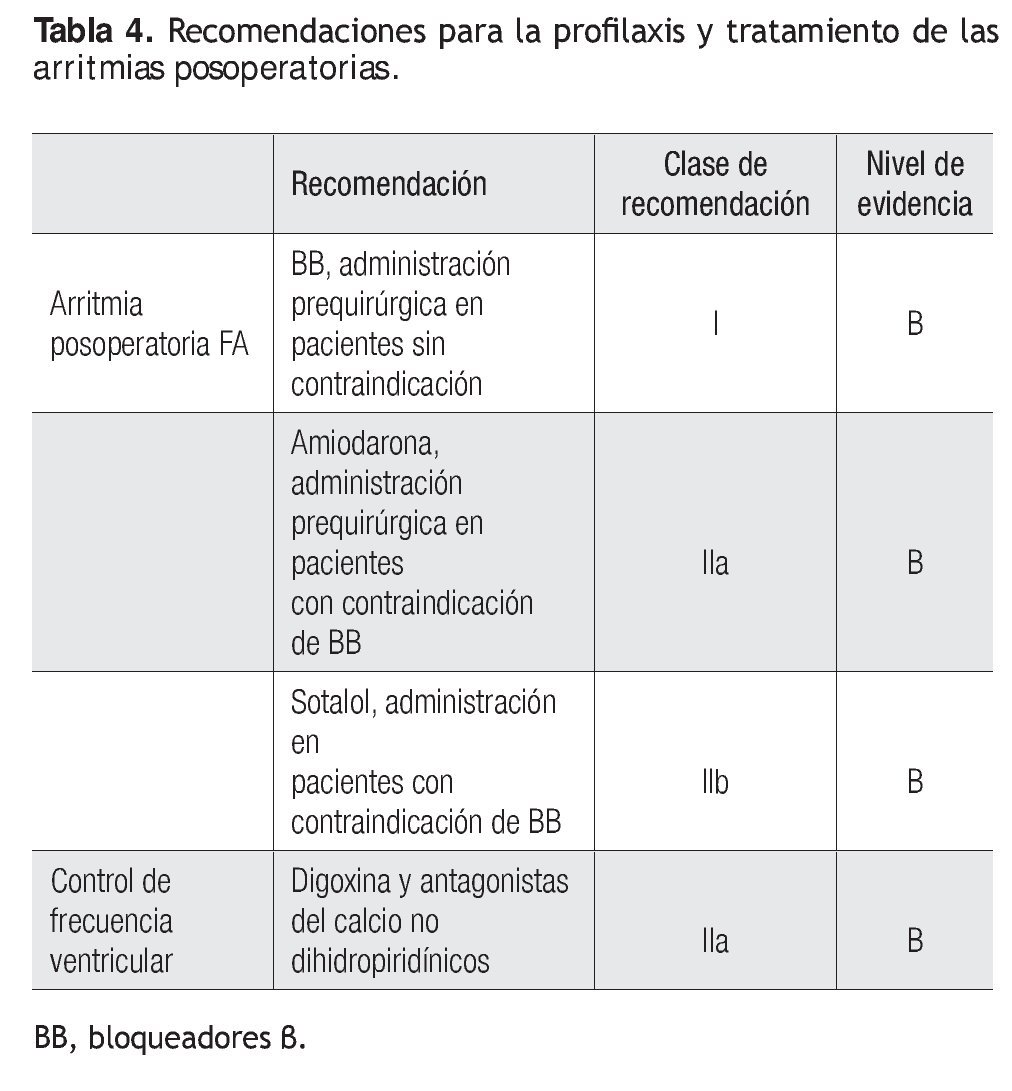
Por mucho, la arritmia posquirúrgica más frecuente es la fibrilación auricular. En los pacientes valvulares constituye con frecuencia el ritmo preoperatorio de base, aunque se presenta también en sujetos programados para CRVM, particularmente personas que consumen bloqueadores β de manera crónica y que los suspenden en el posoperatorio inmediato; por consiguiente, en diversos estudios se ha señalado la necesidad de iniciar o continuar el procedimiento antiarrítmico (Tabla 4).
Infarto agudo del miocardio
Se ha demostrado que la cirugía de revascularización coronaria conlleva no sólo una mejoría de la sobrevida del paciente, sino también una mejoría significativa de la clase funcional y con ello de la calidad de vida posterior a un infarto agudo del miocardio (IAM). Sin embargo, no se ha demostrado el tiempo óptimo para la realización de la intervención. Se ha postulado la espera de un tiempo "prudente" para la operación por considerar el incremento del riesgo de transformar la zona infartada en una hemorrágica, pero no se ha determinado con precisión el tiempo de espera para el cuadro agudo (las publicaciones indican desde 6 h hasta ocho días). Diversos estudios han señalado que la mortalidad de una revascularización coronaria dentro de la primera semana del infarto es siete veces mayor que en un paciente con angina estable, por lo que se debe considerar, si las condiciones hemodinámicas lo permiten, un plazo no menor de ocho días para llevar a cabo el procedimiento (Tabla 5).
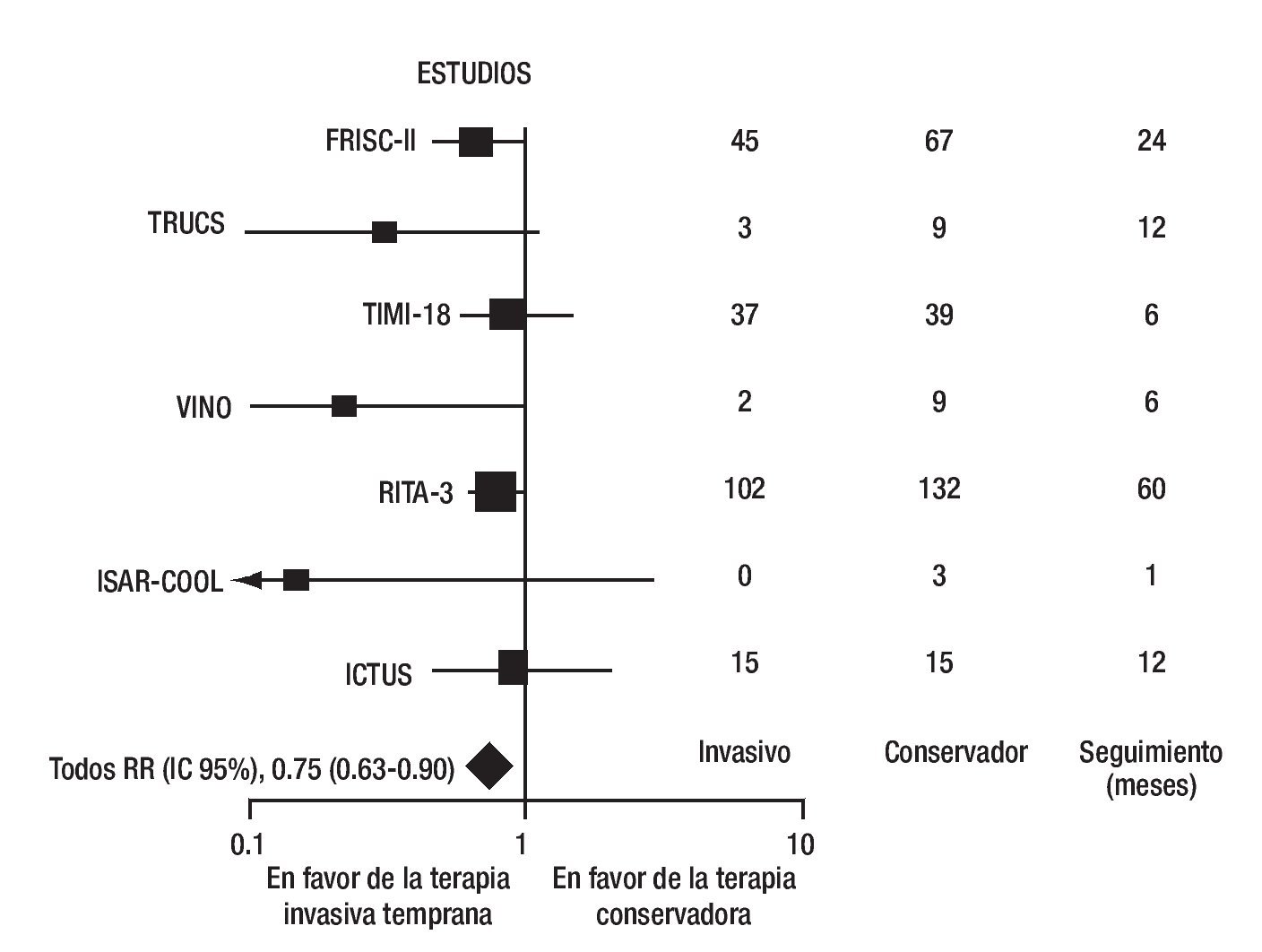
La revascularización coronaria debe realizarse antes de los cuatro meses para obtener las mejorías del proceso de revascularización; en diversos estudios han resultado evidentes los beneficios de una terapia invasiva temprana cuando se controlan los síndromes coronarios agudos con respecto al tratamiento médico conservador; en la mayor parte de los estudios los pacientes se programan para CRVM o ACTP (Figura 1).
Figura 1. Disminución de la mortalidad por una terapia invasiva temprana (CRVM/ACTP) en los síndromes coronarios agudos. J Am Coll Cardiol 2006;48(7):1319-25.
Choque cardiogénico
En los pacientes con infarto agudo del miocardio (IAM), el choque cardiogénico se desarrolla de 7% a 10% y su mortalidad ha permanecido elevada a través del tiempo (50% a 60%) a pesar del tratamiento óptimo que incluye inotrópicos, fluidoterapia, balón de contrapulsación intraaórtico (BCIA), angioplastia e incluso posterior a la implantación de un dispositivo de asistencia ventricular (DAV), que aún hoy en día es una opción controversial. Si bien es cierto que se ha incrementado la sobrevida posterior a la implantación DAV, todavía la evidencia existente es escasa y relacionada con mayores complicaciones. Por lo general, los sobrevivientes se programan para trasplante cardiaco o implantación de un dispositivo de larga estadía. En la actualidad existen 17 estudios importantes en las publicaciones sobre IAM con choque cardiogénico y DAV y muestran que no existe una mejoría significativa si la colocación del DAV no se vincula con algún procedimiento de reperfusión temprana, por lo que en las guías de la ACC/AHA para el tratamiento del IAM con elevación del segmento ST se recomienda la revascularización en los pacientes con IAM ST complicado con choque cardiogénico < 75 años mediante CRVM o ACTP (en los mayores de esta edad está indicada la CRVM). En un estudio de Hochman y colaboradores, la mortalidad del IAM ST con choque cardiogénico no mostró beneficio en la sobrevida a 30 días entre los pacientes sometidos a revascularización pronta o en aquellos en quienes se retrasó el procedimiento, aunque se registró una diferencia significativa en el punto final a seis meses en favor de la revascularización pronta. Por lo tanto, es altamente recomendable llevar a cabo dicho procedimiento en estos pacientes. Se sugiere la espera de la estabilización en la mayoría de los pacientes no complicados con choque cardiogénico o mecánico.
En la planeación quirúrgica de un paciente con un infarto de gran tamaño, y que ha desarrollado un aneurisma ventricular, se debe insistir en la resección de la cicatriz posterior al IAM con la reducción consecuente del volumen telediastólico final del VI, lo que permite la restauración de la geometría ventricular y con ello la función miocárdica global. Este procedimiento no sólo mejora la función sistólica, sino que también disminuye de manera significativa las arritmias y los mediadores neurohumorales que determinan la cardiorremodelación posterior al infarto; en consecuencia, con esta medida se observa una mejoría general y sostenida de la insuficiencia cardiaca posterior al episodio isquémico.
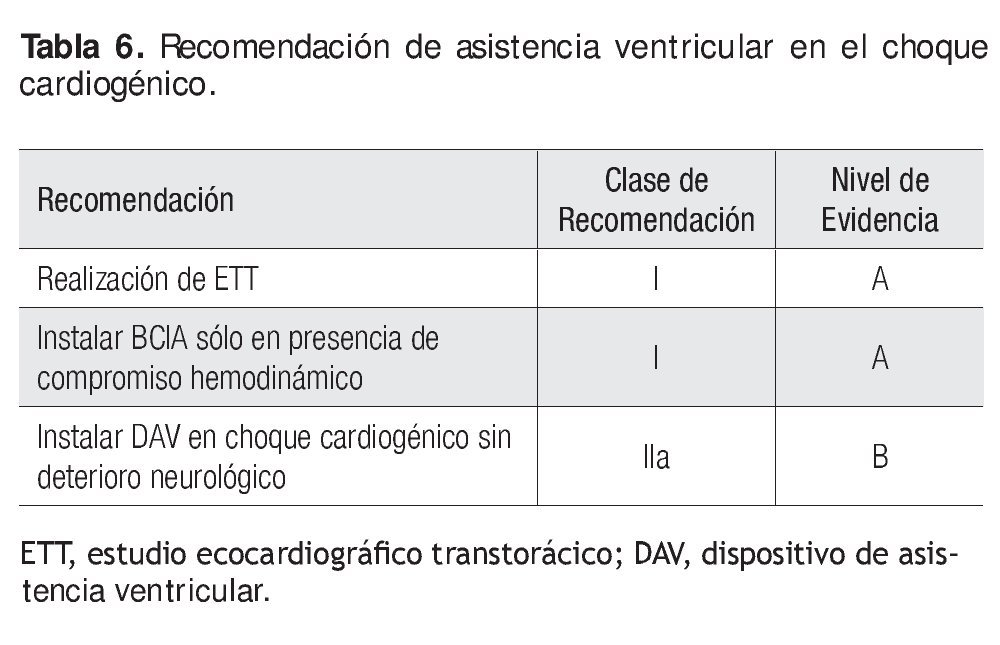
En cuanto a la realización de procedimientos adyuvantes, debe insistirse en la necesidad de realizar siempre un estudio ecocardiográfico transtorácico (ETT) y colocación de BCIA cuando exista compromiso hemodinámico. Pese a que la información es contradictoria cuando el paciente desarrolla choque cardiogénico sin daño neurológico, está indicada la colocación de DAV, lo cual hace posible ampliar la terapéutica a opciones como el puente a trasplante o la recuperación ventricular. No existe un consenso en la actualidad para su instalación y, pese a que ha mejorado los parámetros hemodinámicos, no ha sido así con la sobrevida a 30 días (Tabla 6).
Alteraciones de la coagulación
Existe una gran cantidad de informes inconsistentes acerca de la suspensión o no del ácido acetilsalicílico (ASA) antes de la CRVM. La Sociedad de Cirujanos de Tórax realizó una recopilación de estudios en este sentido. De 21 estudios identificados, seis eran aleatorizados y controlados con nivel de evidencia A y de ellos cinco identificaron este fármaco como un factor que favorece el sangrado posoperatorio (sólo uno no lo hizo). De 16 estudios con nivel de evidencia B, siete reconocieron un mayor sangrado posoperatorio y en nueve el ácido acetilsalicílico no provocó mayor sangrado posoperatorio. Curiosamente, en esta recopilación se observa una tendencia longitudinal, es decir, los estudios anteriores a 1994 muestran sangrado posoperatorio, mientras que los posteriores no; este hallazgo hace posible incluso determinar la cantidad del incremento de sangrado por el ácido acetilsalicílico (200 a 400 cm3 de drenaje torácico y 0.5 a 1 unidad de sangre transfundida por este hecho). Asimismo, esto se correlaciona con otro hecho en cardiología: a menor dosis de este fármaco mayor reducción de episodios cardiovasculares (19% de reducción de la dosis, de 500 a 1 500 mg, en comparación con 32% de reducción de la dosis, de 75 a 150 mg diarios). De igual modo, en el estudio de Muhammad y colaboradores no se encontró mayor sangrado en el posoperatorio, aunque su estudio incluyó en realidad un número muy reducido de pacientes. En general, se ha evidenciado que si bien el ASA incrementa el sangrado posoperatorio, no aumenta la mortalidad final, por lo que no se recomienda su suspensión en pacientes de alto riesgo (véase más adelante). En los sujetos con terapia antiplaquetaria dual (ASA + tienopiridinas) debe evaluarse el riesgo; en pacientes con situaciones de emergencia debe continuarse con la operación (en individuos seleccionados se suspende el tratamiento).
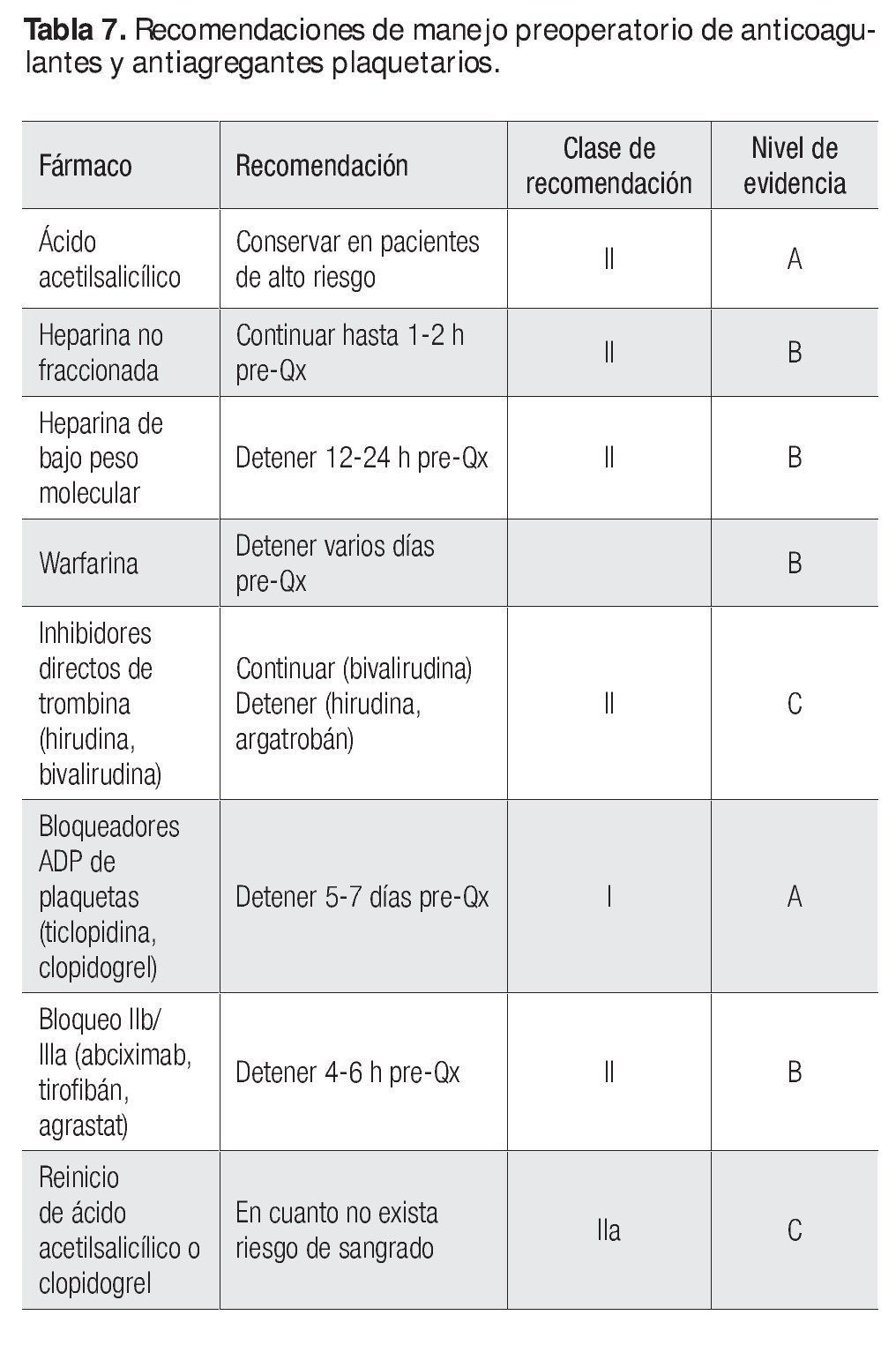
Respecto del uso de los inhibidores fibrinolíticos, se ha descrito una gran cantidad de estudios en favor o en contra de su uso; en el protocolo de Greilich se estudió a tres grupos, uno con aprotinina, otro con ácido aminocaproico y el tercero con placebo. No se evidenció diferencia significativa entre los grupos de fármacos y sí con el placebo en cuanto a sangrado, lo cual establece que no hay diferencia respecto de estos fármacos. Otro aspecto estudiado, además del sangrado, es su nexo con la insuficiencia renal y episodios vasculares cerebrales relacionados con anomalías trombóticas; en términos generales, sólo se recomienda su uso en cirugía de alto riesgo de sangrado, como las reoperaciones, hepatopatías o bien cuando la CRVM se acompaña de valvulopatías complejas. En la actualidad se dispone en el mercado sólo del ácido ε aminocaproico ε y el ácido tranexámico que en estudios contralados no implica el riesgo trombótico mostrado por la aprotinina (Tabla 7).
Diabetes
Los pacientes con cardiopatía isquémica y diabetes corresponden cada vez más a una mayor proporción de aquellos que tan sólo padecen cardiopatía isquémica. Además, tienen un riesgo mayor del doble de padecer un IAM que aquellos que no son diabéticos.
Después de un episodio agudo de infarto del miocardio debe pensarse en una revascularización pronta, en los primeros 14 días posteriores al episodio agudo, ya sea angioplastia o CRVM. Esto supone una reducción de la mortalidad de un 64% en pacientes diabéticos frente a 53% en los no diabéticos Asimismo, parece razonable sugerir la utilización de bloqueadores β en todos los individuos diabéticos y aún más la administración de un antagonista β1
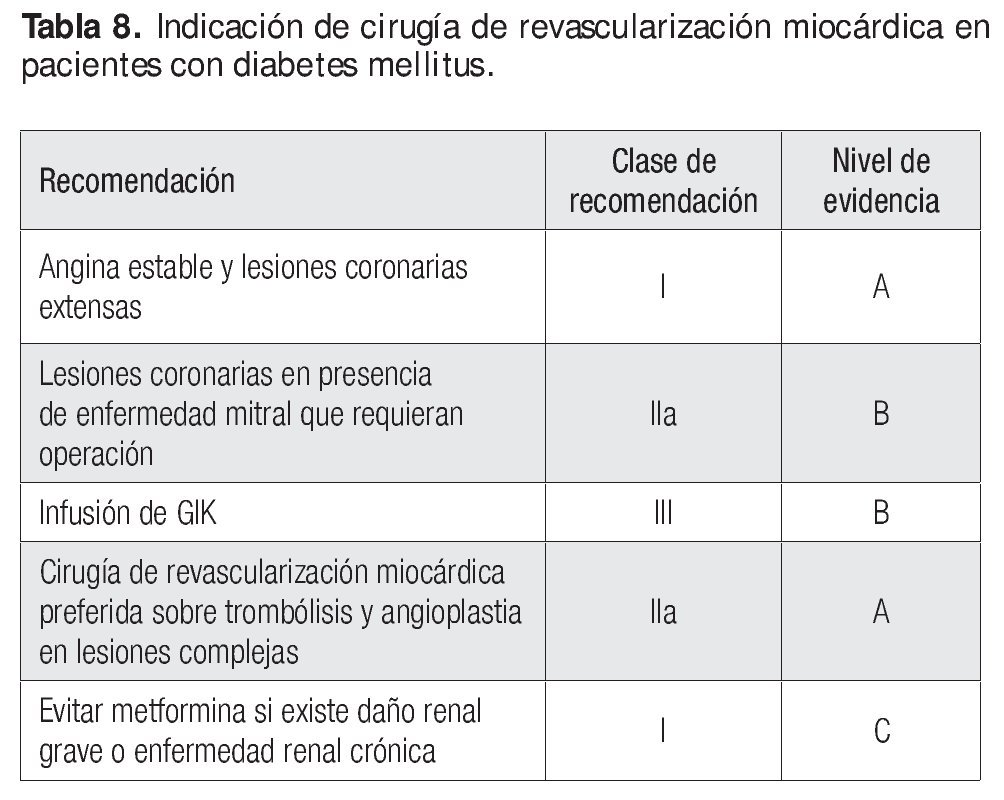
específico en pacientes con insulina y α1 en aquéllos con enfermedad vascular periférica o resistentes a la insulina. En cuanto a la posibilidad de angioplastia o CRVM en estos sujetos, es preferible la operación dada la mejoría de la sobrevida y sobre todo en relación con las múltiples lesiones coronarias. En los estudios multicéntricos EAST y CABG, Patch observó una mejoría en la sobrevida de los individuos sometidos a operación y angioplastia más que al tratamiento médico óptimo. Más aún, en el estudio SOS se observó a seis años una mejoría de la sobrevida de los enfermos diabéticos sometidos a CRVM. El control crónico de la diabetes debe ser similar al de los pacientes con DM sin enfermedad cardiaca, por ejemplo HbA1C de 7 (cifras mayores representan un riesgo mayor) (Tabla 8).
Insuficiencia renal
El primer problema en pacientes con alteraciones de la función renal es la definición de falla renal o insuficiencia renal. Existen más de ocho definiciones, lo cual tiende a complicar más que a facilitar el estudio de ésta y esto se torna en verdad crítico cuando se agrega CRVM. La enfermedad cardiovascular es la principal causa de mortalidad en pacientes nefrópatas, en particular cuando se acompaña de diabetes mellitus. La CRVM mejora definitivamente la sobrevida de estos enfermos, pero el requerimiento de la angiografía diagnóstica es la principal causa de daño renal en sujetos hospitalizados.
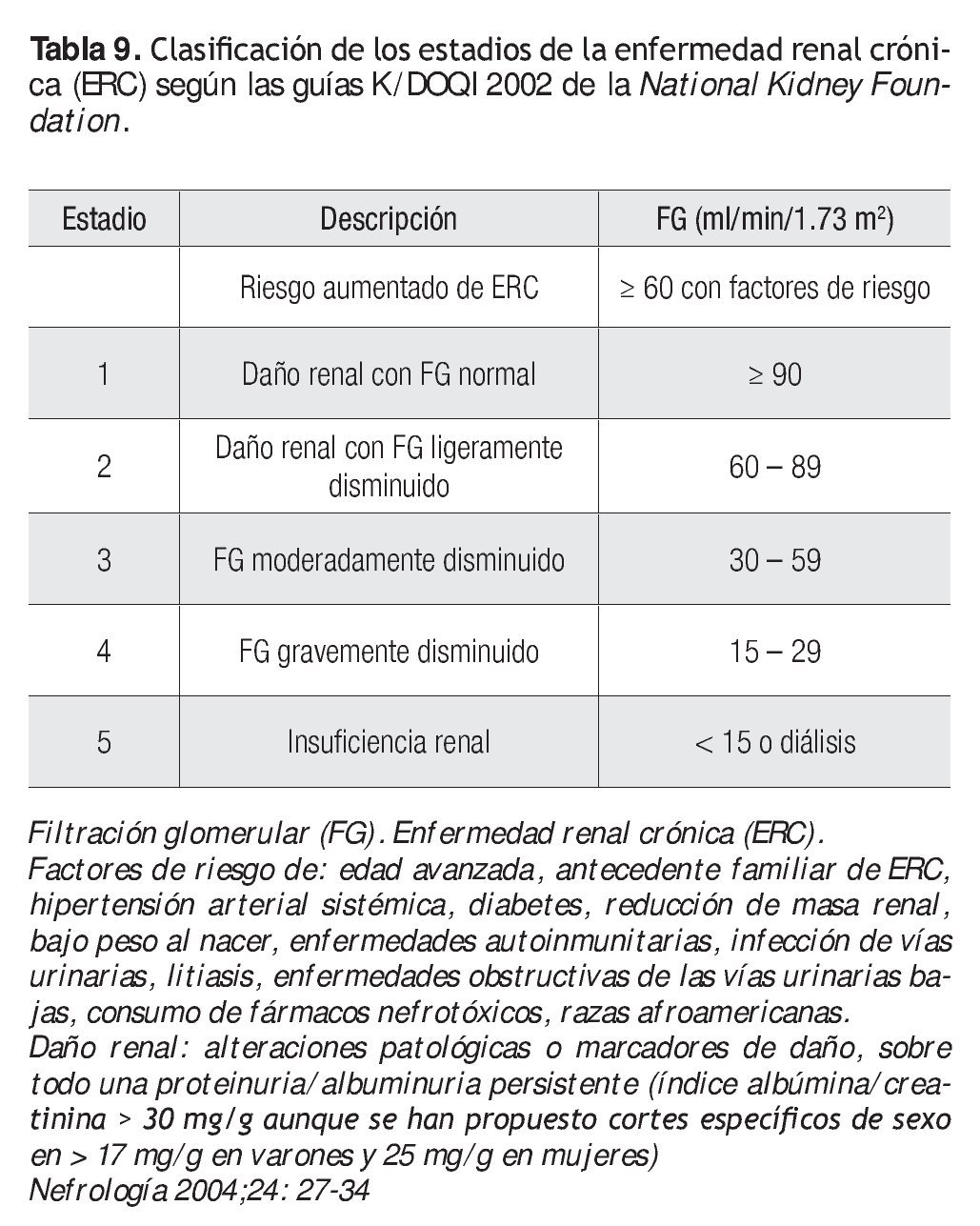
La National Kidney Foundation ha definido la enfermedad renal crónica (ERC) como el daño renal o la presencia de un filtrado glomerular (FG) disminuido durante un periodo mayor de tres meses. Se reconocen cinco estadios de ERC y se aplica el término de insuficiencia renal cuando el filtrado glomerular es < 60 ml/min/1.73 m2. El daño renal o el nivel de función renal determinan el estadio de la clasificación independientemente de la causa (Tabla 9).
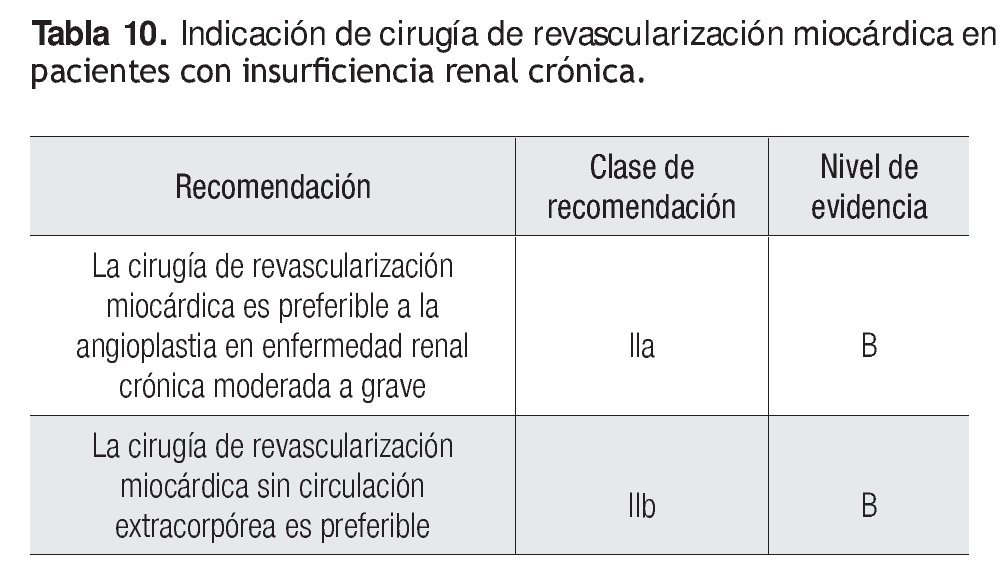
En las etapas 2 y 3 es claro el beneficio de la CRVM y aún más cuando se relaciona dicha afección con diabetes mellitus; no es tan evidente en cuanto a las etapas 4 y 5 (terminal). La CRVM confiere una mejor evolución a largo plazo, pero con una mortalidad perioperatoria mayor (lo contrario ocurre para la angioplastia). En definitiva, la mejor terapéutica es la prevención, esto es, mantener el estado hídrico y volémico del paciente en estado óptimo, lo cual se evalúa mejor por ETT en la dimensión de la vena cava inferior, más que con el catéter de flotación y mucho más que con la mera evaluación de la PVC (Tabla 10).
Transfusión sanguínea y métodos conservadores
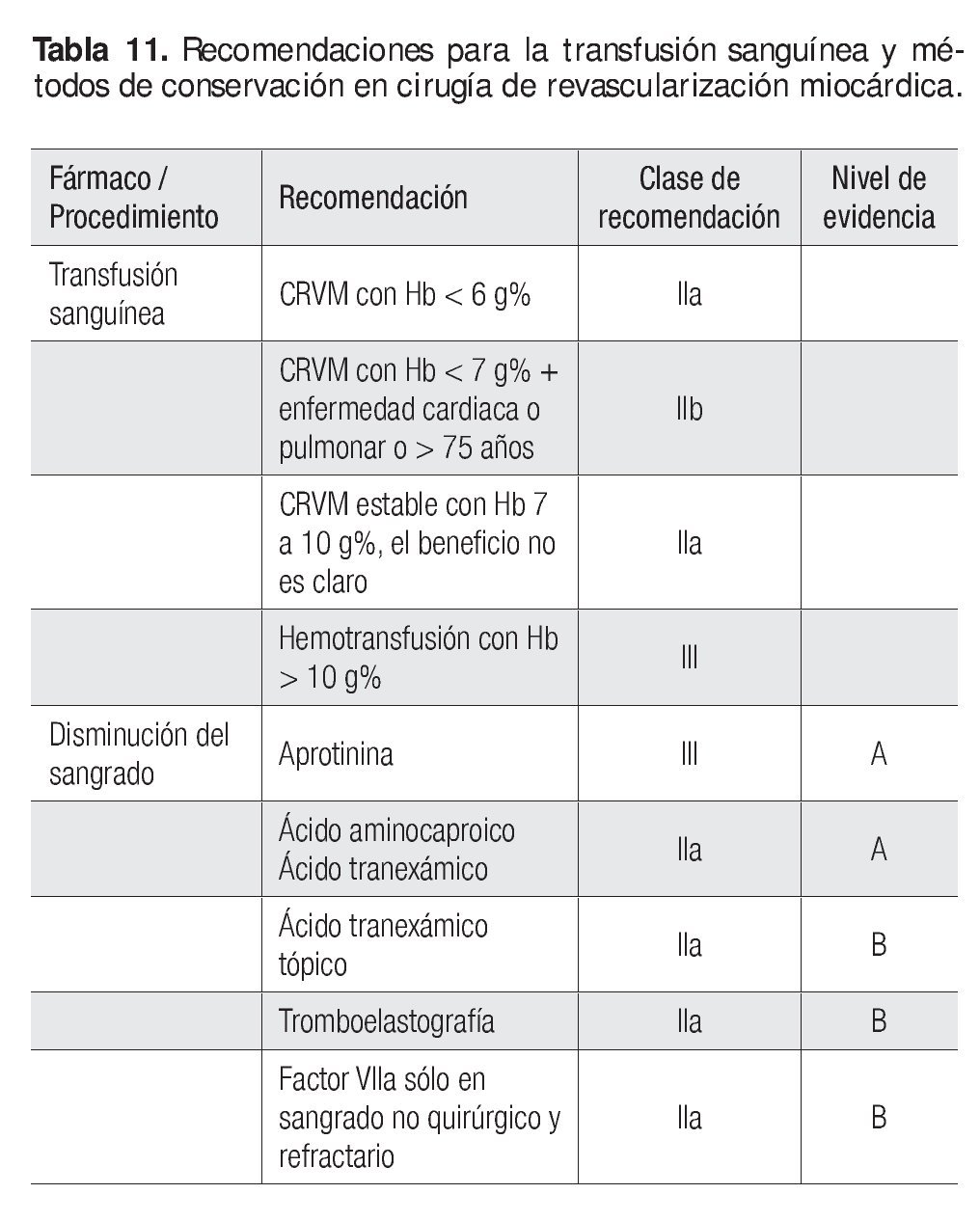
La hemotransfusión en pacientes sometidos a CRVM es un tema ampliamente revisado y con posiciones incluso contradictorias. El sangrado posoperatorio en el episodio isquémico puede tener diversas causas; de las médicas, las más frecuentes son alteraciones cualitativas por antiagregación y cuantitativas por anticoagulación y los objetivos en el nivel del hematócrito para la corrección de la anemia todavía no son universales y la evidencia actual no es concluyente para iniciar o indicar el momento exacto de la transfusión. Por lo regular se ha utilizado 10 g/dl de hemoglobina, pero al parecer esto no es cierto en todos los casos e incluso puede ser perjudicial para la sobrevida del sujeto. Es más razonable guiarse para los productos derivados por métodos como el tromboelastógrafo (Tabla 11).
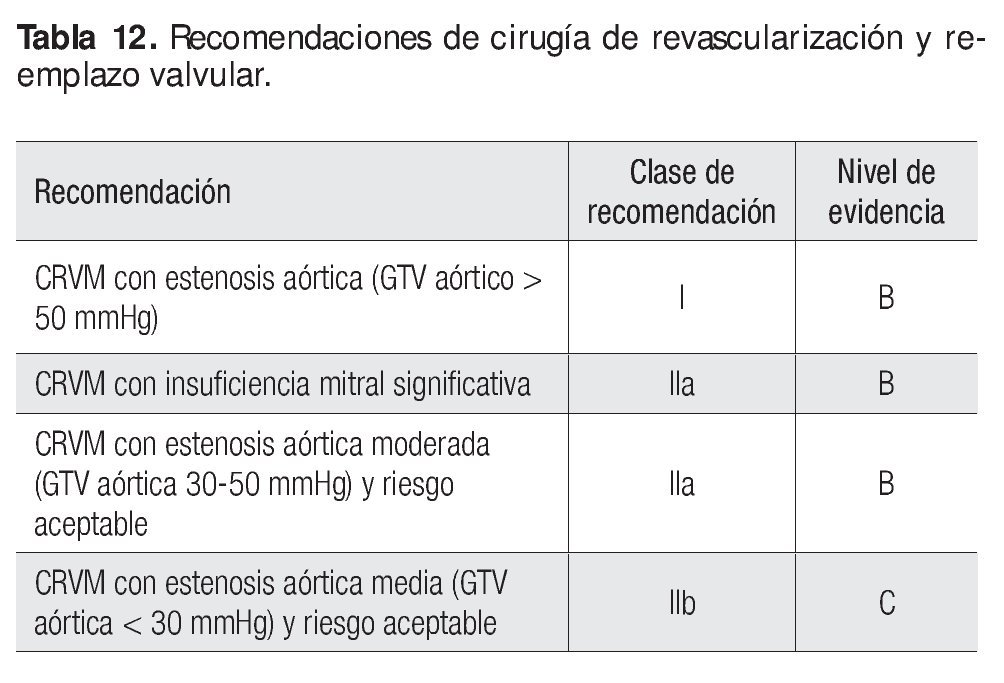
Cirugía de revascularización y reemplazo valvular
La coexistencia de CRVM con un procedimiento de cambio valvular es un contexto clínico que se presenta con mayor frecuencia en poblaciones > 60 años, ya que el nexo entre la cardiopatía isquémica y la estenosis aórtica degenerativa es cada vez más importante. Asimismo, el grado de disfunción valvular es el que determina cuando realizar su cambio (Tabla 12).
BCIA en pacientes de alto riesgo sin choque cardiogénico
Desde hace varios años se ha estudiado el efecto real que tiene la utilización preoperatoria del balón de contrapulsación intraaórtico (BCIA) en el paciente de alto riesgo y sólo ha sido hasta los últimos años que se dispone de una creciente evidencia de que su uso reduce la mortalidad posoperatoria, la morbilidad y la duración de la estancia hospitalaria. Un reciente meta-análisis reveló que el BCIA preoperatorio se vinculó con la reducción del riesgo absoluto del 3.6% en la mortalidad y una reducción del 59% de las probabilidades de mortalidad en pacientes de alto riesgo sometidos a CVRM. Con esta evidencia existe cada vez más un consenso en el uso del BCIA preoperatorio; donde no lo existe es en la definición de los factores de alto riesgo. En fecha reciente, Miceli y colaboradores del Bristol Heart Institute propusieron una calificación para identificar a los pacientes que podrían beneficiarse de la inserción de BCIA; entre los factores que lograron identificar figuran los siguientes:
• Baja fracción de expulsión (< 30%)
• Edad avanzada (> 70)
• Enfermedad del tronco coronario izquierdo (> 50%)
• Reintervención
• Infarto agudo del miocardio reciente (< 30 días)
• Clase funcional baja (NYHE III-IV o CCS III-IV)
• Cirugía de emergencia
Para evaluar el momento óptimo de inserción preoperatoria del BCIA, Christenson y colaboradores evaluaron a pacientes de alto riesgo con al menos dos de los siguientes factores de riesgo: baja fracción de expulsión (< 30%), angina inestable, reoperación o enfermedad de tronco coronario izquierdo (> 70%), y no encontraron diferencia significativa en los resultados en la instalación entre las 2 o las 24 h anteriores a la operación.
Dyub y colaboradores concluyeron en un meta-análisis que existe una reducción significativa de la mortalidad en los pacientes de alto riesgo sometidos a un BCIA preoperatorio. Rubino y colaboradores analizaron la evolución clínica, bioquímica y ecocardiográfica de 30 pacientes sometidos a CRVM e inserción de BCIA intraoperatorio o posoperatorio y compararon los resultados del posoperatorio inmediato; observaron una disminución de la mortalidad inmediata, pero no en el seguimiento a dos años.
En otro estudio, Christenson encontró una mejoría de la sobrevida y estancia en la UCI con la instalación del dispositivo preoperatorio. Asimismo, Craver y colaboradores utilizaron BCIA preoperatorio en pacientes de alto riesgo (que incluían insuficiencia renal y enfermedad cerebrovascular documentada, entre otras) en CRVM sin circulación extracorpórea y encontraron una disminución del uso de inotrópicos y mejor estabilidad hemodinámica en el transoperatorio a la dislocación del corazón para realizar las anastomosis distales.
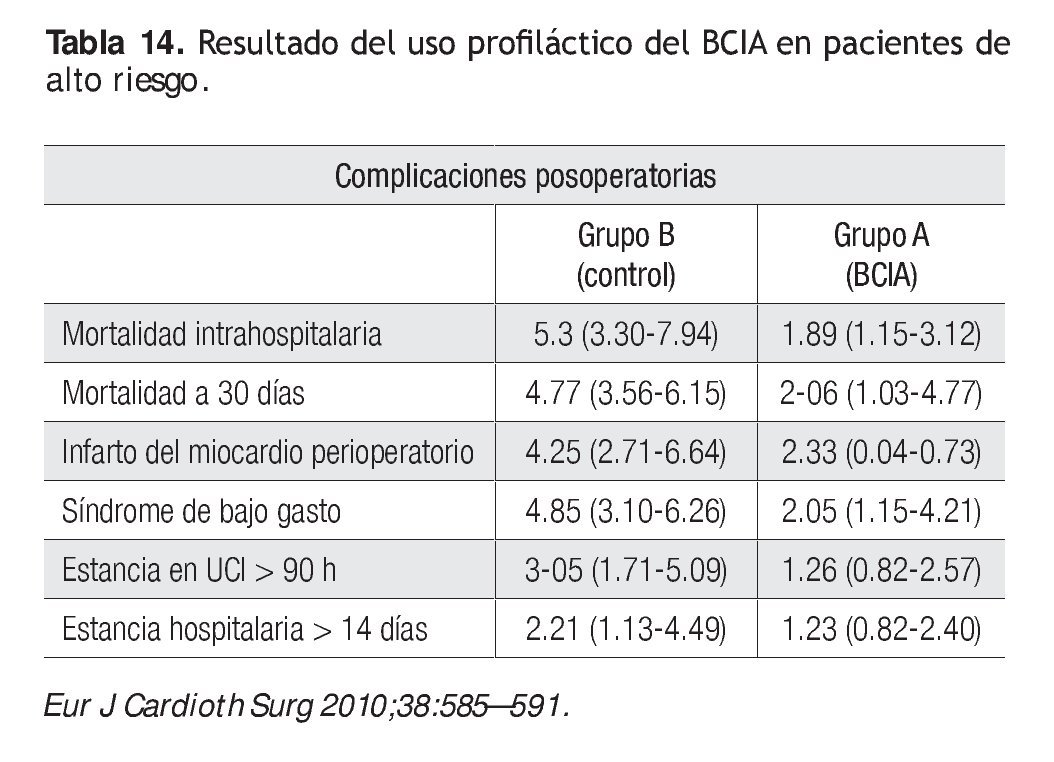
Lorusso y colaboradores llevaron a cabo un estudio prospectivo multicéntrico en 2010 en el cual se insertó de manera profiláctica un BCIA preoperatorio a pacientes de alto riesgo y que incluyó a 956 pacientes. Se reconoció una mejoría de la sobrevida intrahospitalaria, la sobrevida a 30 días, menor tasa de IAM posoperatorio, menor estancia en la UCI y mejoría en la fracción de expulsión, pero no en la sobrevida a cinco y ocho años. Ramnarin y colaboradores sugieren en su estudio que el mejor tiempo para su inserción es el preoperatorio, si bien adolece del tiempo exacto, esto es, no difiere si es una hora o un día; pese a ello, es clara la disminución de las complicaciones inmediatas en el grupo con BCIA (Tablas 13 y 14).
Bibliografía
Abizaid A, Costa MA, Centemero M, et al. Clinical and economic impact of diabetes mellitus on percutaneous and surgical treatment of multivessel coronary disease patients: insights from the Arterial Revascularization Therapy Study (ARTS) Trial. Circulation 2001;104:533-538.
Alonso-Martín JJ, Cursio-Ruigómez A, Cristóbal-Varela C, et al. Indicaciones de American Diabetes Association. Standards of medical care in diabetes 2010. Diabetes Care 2009;33:S11-S61.
Antman EM, Anbe DT, Armstrong PW, et al. ACC/AHA guidelines for the management of patients with ST-elevation myocardial infarction: a report of the American College of Cardiology/American Heart Association Task Force on Practice Guidelines (Committee to Revise the 1999 Guidelines for the Management of Patients With Acute Myocardial Infarction). Circulation 2004;110;e82-e293.
Bavry A, Kumbhani D, Rassi A, et al. Benefit of early invasive therapy in acute coronary syndromes. A meta-analysis of contemporary randomized clinical trials. J Am Coll Cardiol 2006;48:1319-1325.
Booth J, Clayton T, Pepper J, et al. Randomized, controlled trial of coronary artery bypass surgery versus percutaneous coronary intervention in patients with multivessel coronary artery disease: six-year follow-up from the Stent or Surgery Trial (SoS). Circulation 2008;118:381-388.
Bridges CR, Edwards FH, Peterson ED, et al. Cardiac surgery in nonagenarians and centenarians. J Am Coll Surg 2003;197:347-56; discussion 356-357.
Cheng JM, den Uil CA, Hoeks SE, et al. Percutaneous left ventricular assist devices vs. intraaortic balloon pump counterpulsation for treatment of cardiogenic shock: a meta-analysis of controlled trials. Eur Heart J 2009;30:2102-2108.
Christenson J, Simonet F, Badel P, et al. Evaluation of preoperative intra-aortic balloon pump support in high risk coronary patients. Eur J Cardiothorac Surg 1997;11:1097-1103.
Christenson JT, Simonet F, Badel P, et al. Optimal timing of preoperative intraaortic balloon pump support in high-risk coronary patients. Ann Thorac Surg 1999;68(3):934-939.
Craver JM, Murrah CP. Elective intraaortic balloon counterpulsation for high-risk off-pump coronary artery bypass operations. Ann Thorac Surg 2001;71:1220-1223.
Dunning J, Versteegh M, Fabbri A, et al. Guideline on antiplatelet and anticoagulation management in cardiac surgery. Eur J Cardiothorac Surg 2008;34:73-92.
Dyub AM, Whitlock RP, Abouzahr LL, et al. Preoperative intra-aortic balloon pump in patients undergoing coronary bypass surgery: a systematic review and meta-analysis. J Cardiac Surg 2008;23(1):79-86.
Eagle KA, Guyton RA, Davidoff R, et al. ACC/AHA 2004 guideline update for coronary artery bypass graft surgery: a report of the American College of Cardiology/American Heart Association Task Force on Practice Guidelines (Committee to Update the 1999 Guidelines for Coronary Artery Bypass Graft Surgery). J Am Coll Cardiol 2004;44;e213-e310.
Engel AM, McDonough S, Smith JM, et al. Institute for Research and Education, Good Samaritan Hospital, Department of Surgery, and Cardiac, Vascular, and Thoracic Surgery Inc, Cincinnati, Ohio. Does an obese body mass index affect hospital outcomes after coronary artery bypass graft surgery? Ann Thorac Surg 2009;88:1793- 800.
Ferraris VA, Ferraris SP, Saha SP, et al. Perioperative blood trans-fusion and blood conservation in cardiac surgery: the Society of Thoracic Surgeons and The Society of Cardiovascular Anesthesiologists clinical practice guideline. Ann Thorac Surg 2007;83:S27.
Ferraris VA. Ferraris SP, Moliterno DJ, et al. The Society of Thoracic Surgeons Practice Guideline Series: aspirin and other antiplatelet agents during operative coronary revascularization (executive summary). Ann Thorac Surg 2005;79:1454-1461.
Garatti A, Russo C, Lanfranconi M, et al. Mechanical circulatory support for cardiogenic shock complicating acute myocardial infarction: an experimental and clinical review. ASAIO J 2007;53:278-287.
Gheorghiade M, Goldstein S. Beta-Blockers in the post-myocardial infarction patient. Circulation 2002;106:394-398.
Greilich PE, Jessen ME, Satyanarayana N, et al. The effect of epsilon-aminocaproic acid and aprotinin on fibrinolysis and blood loss in patients undergoing primary, isolated coronary artery bypass surgery: a randomized, double-blind, placebo-controlled, noninferiority trial. Anesth Analg 2009;109:15-24.
Guilfoyle MR, Drain AJ, Khan A, et al. Cardiac surgery in nonagenarians: single-centre series and review. Gerontology 2010;56(4):378-84. Epub 2009 Dec 23. Review X.
Hajjar LA, Vincent JL, Galas FR, et al. Transfusion requirements after cardiac surgery: the TRACS randomized controlled trial. JAMA 2010;304(14):1559.
Hammoud T, Tanguay J, Bourassa MG. Management of coronary artery disease: therapeutic options in patients with diabetes. J Am Coll Cardiol 2000;36(2):355-365.
Hochman JS, Buller CE, Dzavik V, et al. Early revascularization and long-term survival in cardiogenic shock complicating acute myocardial infarction; overall results of the SHOCK Trial Registry. JAMA 2006;295:2511-2515.
Hochman JS, Buller CE, Dzavik V, et al. Early revascularization in acute myocardial infarction complicated by cardiogenic shock; overall results of the SHOCK Trial Registry. N Engl J Med 1999;341:625-634.
Jacobs AK. Coronary intervention in 2009: are women no different than men? Circ Cardiovasc Interv 2009;2:69-78. Review.
Jacobs AK. Coronary revascularization in women in 2003: sex revisited. Circulation 2003;107;375-377.
K/DOQI clinical practice guidelines for chronic kidney disease: part 4. Definition and classification of stages of chronic kidney disease. 2002;39:S46-S75.
Kamran M. Effect of aspirin on postoperative bleeding in coronary artery bypass grafting. Ann Thorac Cardiovasc Surg 2008;14:224-229.
Levey A. Definición y clasificación de la enfermedad renal crónica: propuesta de KDIGO (Kidney Disease: Improving Global Outcomes). Kidney Inter (Edición español) 2005;1:135-146.
Lorusso R, Gelsomino S, Carella R, et al. Impact of prophylactic intra-aortic balloon counterpulsation on postoperative outcome in high-risk cardiac surgery patients: a multicentre, propensity score analysis. Eur J Cardiothorac Surg 2010;38:585-591.
Marín R. Guía de la Sociedad Española de Nefrología sobre riñón y enfermedad cardiovascular. Versión abreviada. Nefrología 2006;26:31-44.
Mezzano AS, Aros EC. Enfermedad renal crónica: clasificación, mecanismos de progresión y estrategias de renoprotección. Rev Méd Chile 2005;133.
Miceli A, Duggan SM, Capoun R, et al. A clinical score to predict the need for intraaortic balloon pump in patients undergoing coronary artery bypass grafting. Ann Thorac Surg 2010;90:522-526.
Murphy GJ, Reeves BC, Rogers CA, et al. Increased mortality, postoperative morbidity, and cost after red blood cell transfusion in patients having cardiac surgery. Circulation 2007;116:2544-2552.
Nguyen HL, Goldberg RJ, Gore JM, et al. Age and sex differences, and changing trends, in the use of evidence-based therapies in acute coronary syndromes: perspectives from a multinational registry. Coronary Artery Dis 2010;21:336-344.
Prabhakar G, Haan CK, Peterson ED, et al. The risks of moderate and extreme obesity for coronary artery bypass grafting outcomes: a study from The Society of Thoracic Surgeons' Database. Ann Thorac Surg 2002;74:1125-1131.
Raghavan R, Benzaquen BS, Rudski L. Timing of bypass surgery in stable patients after acute myocardial infarction. Can J Cardiol 2007;23:976-982.
Ramnarine IR, Grayson AD, Dihmis WC, et al. Timing of intra-aortic balloon pump support and 1-year survival. Eur J Cardiothorac Surg 2005;27:887-892.
Reddy RC, Stone GW, Urban PM. Trends in intraaortic balloon counterpulsation complications and outcomes in cardiac surgery. Ann Thorac Surgrevascularización: aspectos clínicos. Rev Esp Cardiol 2005;58:198-216.
Rubino AS, Onorati F, Santarpino G, et al. Early intra-aortic balloon pumping following perioperative myocardial injury improves hospital and mid-term prognosis. Interact Cardiovasc Thorac Surg 2009;8:310-315.
Rydén L, Standl E, Bartnik M, et al. Guidelines on diabetes, pre-diabetes, and cardiovascular diseases: executive summary. Eur Heart J 2007;28:88-136.
Sami S, Willerson JT. Contemporary treatment of unstable angina and non-ST-segment elevation myocardial infarction (part 1). Tex Heart Inst J 2010;37:262-275. Review.
Sami S, Willerson JT. Contemporary treatment of unstable angina and non-ST-segmentelevation myocardial infarction (part 2). Tex Heart Inst J 2010;37:262-75. Review.
Sedlis SP, Morrison DA, Lorin JD, et al. Percutaneous coronary intervention versus coronary bypass graft surgery for diabetic patients with unstable angina and risk factors for adverse outcomes with bypass: outcome of diabetic patients in the AWESOME randomized trial and registry. J Am Coll Cardiol 2002;40:1555-1566.
Shander AS, Goodnough LT. Blood transfusion as a quality indicator in cardiac surgery. JAMA 2010;304:1610-1611.
Sheridan BC, Stearns SC, Rossi JS, et al. Three-year outcomes of multivessel revascularization in very elderly acute coronary syndrome patients. Ann Thorac Surg 2010;89:1889-1895.
Sjauw KD, Engström AE, Vis MM, et al. A systematic review and meta-analysis of intra-aortic balloon pump therapy in ST-elevation myocardial infarction: should we change the guidelines? Eur Heart J 2009;30:459-468.
Soriano-Cabrera S. Definición y clasificación de los estadios de la enfermedad renal crónica. Prevalencia. Claves para el diagnóstico precoz. Factores de riesgo de enfermedad renal crónica. Nefrología 2004;24: 27-34.
Thiele H, Sick P, Boudriot E, et al. Randomized comparison of intra-aortic balloon support with a percutaneous left ventricular assist device in patients with revascularized acute myocar-dial infarction complicated by cardiogenic shock. Eur Heart J 2005;26:1276-1283.
Thiele H, Smalling RW, Schuler GC. Percutaneous left ventricular assist devices in acute myocardial infarction complicated by cardiogenic shock. Eur Heart J 2007;28(17):2057-63. Epub 2007 num 22. Review.
Whang W, Bigger JT, The CABG Patch Trial Investigators and Coordinators. Diabetes and outcomes of coronary artery bypass graft surgery in patients with severe left ventricular dysfunction: results from The CABG Patch Trial database. J Am Coll Cardiol 2000;36:1166-1172.
Wijns W, Kolh P, et al. Guidelines on myocardial revascularization. The Task Force on Myocardial Revascularization of the European Society of Cardiology (ESC) and the European Association for Cardio-Thoracic Surgery (EACTS). European Heart J 2010;31:2501-2555.