Se presenta un varón de 78 años con antecedentes de hipertensión arterial, dislipidemia, enfermedad renal crónica, cardiopatía isquémica y diabetes de larga evolución tratada con metformina 850mg/d a la que se había añadido linagliptina 6 meses antes por mal control glucémico.2
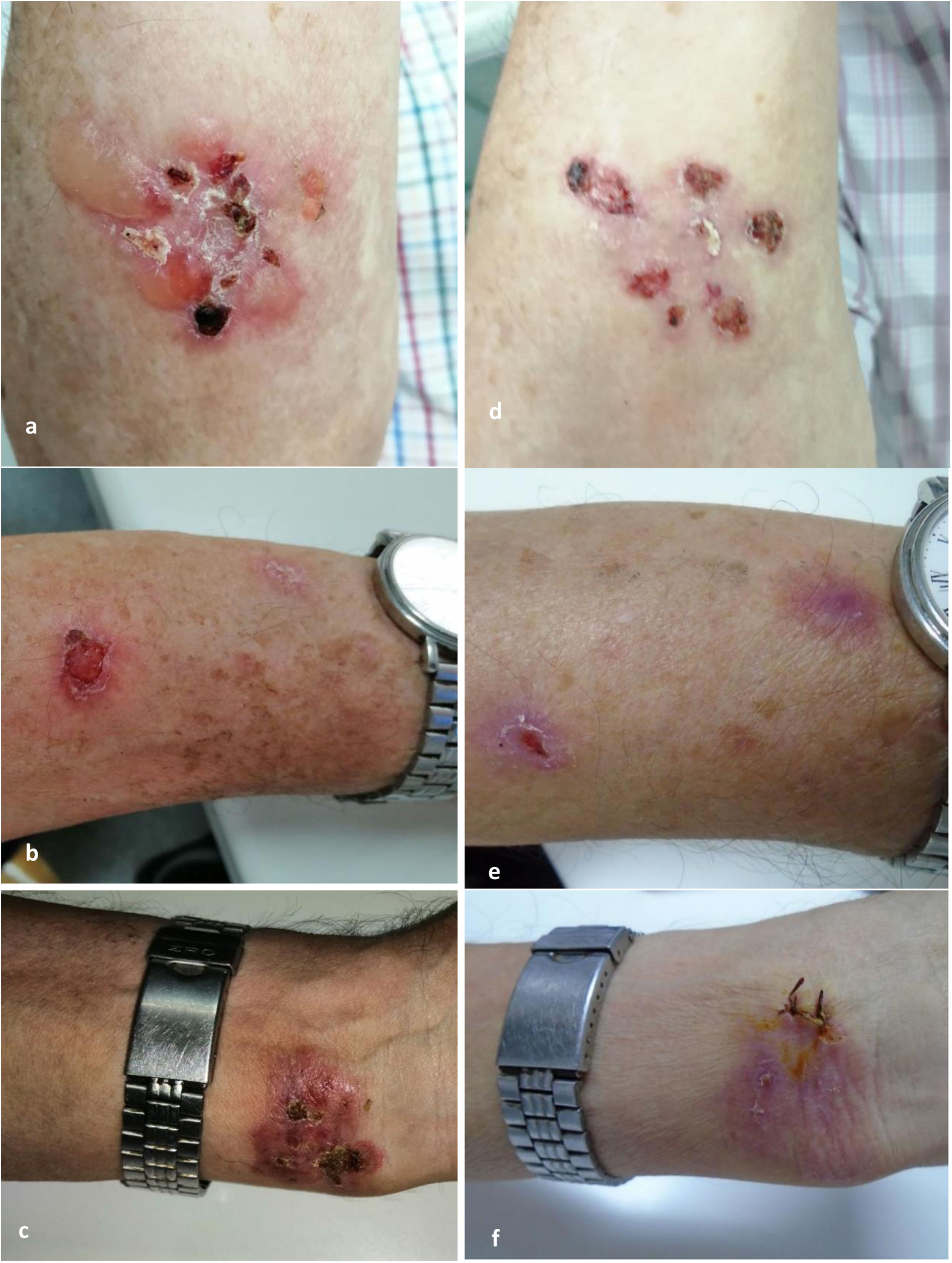
Consulta por la aparición de lesiones eritematosas con ampollas cutáneas y costras serohemáticas en el tronco y las extremidades (fig. 1a-c), levemente pruriginosas y sin afectación mucosa, de un mes de evolución.
a-c) Lesiones en el momento del diagnóstico: antebraquial derecha, antebraquial izquierda y muñeca, respectivamente. d-f) Lesiones tras un mes de evolución: antebraquial derecha, antebraquial izquierda y muñeca, respectivamente. En f se aprecian los puntos de sutura tras la biopsia cutánea.
La aparición de ampollas tensas con/sin afectación mucosa apunta a un diagnóstico de penfigoide ampolloso (PA), el trastorno bulloso más frecuente.
En las últimas décadas ha aumentado su incidencia en relación con distintos fármacos, asociándose recientemente al uso de inhibidores de la dipeptidil peptidasa 4 (iDPP4)1. Los iDPP4 (gliptinas) están indicados para el tratamiento de la diabetes tipo 2, en combinación o en monoterapia, considerándose uno de los principales tratamientos de segunda línea.
A principios de la década de 2010 se describió la asociación de PA con sitagliptina y vildagliptina, no siendo hasta 2016 cuando se reportó el primer caso por linagliptina. La incidencia de PA estimada en pacientes diabéticos tratados con iDPP4 es de 0,86/1.0002.
Los datos actuales describen un mayor riesgo relativo con vildagliptina, seguida por linagliptina, sitagliptina y saxagliptina1,3,4.
El PA clásico se caracteriza por la aparición de autoanticuerpos IgG contra la membrana basal (antígenos proteicos BP230 y BP180) que condicionan una pérdida de adherencia de los queratinocitos (acantólisis) a nivel subepidérmico.
Parece que el tratamiento con iDPP4 induce la generación de dichos autoanticuerpos frente a las mismas proteínas, pero con un epítopo distinto3,5.
La clínica del PA inducido por iDPP4 coincide con el clásico: ampollas tensas negativas para Nikolsky sobre piel sana o eritematosa que se puede acompañar de afectación mucosa (30%)4.
Atendiendo a los estudios de farmacovigilancia españoles, no se han encontrado diferencias entre sexos ni etnias1 y la edad mediana de aparición se sitúa por encima de los 70 años1,3.
La latencia entre el inicio del fármaco y la aparición de síntomas es de 7 meses de mediana: 3,5 en linagliptina y 12 para sitagliptina1,4.
Se requiere confirmación anatomopatológica mediante biopsia cutánea. Típicamente se hallan depósitos lineales de IgG y C3 en la membrana basal por inmunofluorescencia directa. La inmunofluorescencia indirecta puede mostrar autoanticuerpos IgG en suero4,5. Dichos hallazgos no presentan diferencias respecto al PA clásico; tampoco cuando comparamos subgrupos de población diabética5.
Tras diagnosticarlo se debe retirar el fármaco causante y prescribir corticoides tópicos. Cuando no se retira el fármaco, la respuesta es discreta o reaparece al poco tiempo4,6.
Se recomienda añadir corticoides sistémicos para evitar la recidiva. Se aconseja una dosis inicial de cortisona oral de 1mg/kg/d en casos moderados-severos, siendo inferior la dosis en casos leves (0,2-0,5mg/kg/d), disminuyéndose paulatinamente una vez estabilizada la enfermedad en ausencia de lesiones nuevas4.
Al mes de tratamiento suele evidenciarse mejoría, habiendo remitido a los 4 meses en el 83% de los casos3,4. Lo esperable es que remita sin lesiones residuales.
No disponemos de información a largo plazo, pero con los estudios disponibles no se ha descrito ninguna recidiva a los 12 meses tras la retirada del tratamiento5,6.
Volviendo a nuestro paciente, se sustituye la linagliptina por dapaglifozina y se inicia corticoterapia sistémica y tópica.
Se realiza la biopsia cutánea para histología e inmunofluorescencia directa, que confirman nuestra sospecha, y se notifica el caso al servicio de farmacovigilancia.
A los 30 días se evidencia la mejoría de las lesiones (fig. 1a-f), ajustando la corticoterapia hasta la resolución completa.
Se considera importante conocer el PA asociado a iDPP4 para identificarlo y abordarlo desde las consultas de Atención Primaria, así como describir los sujetos con mayor predisposición para adecuar su prescripción.
Consideraciones éticasLas fotografías presentes en el artículo, a pesar de no ser identificativas, cuentan con el consentimiento informado del paciente. Se ha accedido a la información clínica del paciente sin vulnerar el protocolo vigente de confidencialidad, y con una única finalidad divulgativa para la comunidad científica.
FinanciaciónLa presente investigación no ha recibido ayudas específicas provenientes de agencias del sector público, sector comercial o entidades sin ánimo de lucro.
Conflicto de interesesNinguno.