La ecografía es una herramienta de gran valor para el diagnóstico y el manejo de una gran variedad de situaciones clínicas cotidianas. El médico de familia como especialista generalista debe ser competente para el abordaje de prácticamente cualquier problema de salud que afecte a su población, por lo que, en sus manos, esta herramienta puede proporcionar un elevado impacto sobre la calidad y la eficacia del proceso asistencial. Este es el último artículo de una serie dedicada a mostrar la aplicabilidad de la ecografía clínica en nuestras manos, en la que hemos revisado la mayoría de sus aplicaciones, como la ecografía clínica abdominal, la nefrourológica, la musculoesquelética, la cardiaca o la pulmonar. Queremos terminar con escenarios como la afección del cuello o su uso en situaciones de urgencia, en las que proporciona datos definitivos para la orientación diagnóstica, el manejo clínico e incluso la supervivencia del paciente, tales como el paciente con sospecha de trombosis venosa profunda en miembros inferiores, traumatismo toracoabdominal, compromiso hemodinámico o parada cardiaca.
Ultrasound is a very useful tool for diagnosis and to handle a great sort of daily affaires. The family Doctor, as general specialist, must be competent to carry out almost all kind of wealthy situations that can potentially affect to his population. Because of that, with this tool in his hand, the Doctor can get a higher level of quality in the efficiency of the assistant procedure. This is the last paper of a serial dedicated to show the different applications of clinical ultrasound, in which most of them have been reviewed, such as abdominal, nephrourological, musculoskeletal, cardiac or pulmonary focused ultrasound. We want to finalize with scenarios like neck pathology or applications in urgencies in which we can provide the definitive data to get the right diagnosis orientation, the clinic use, or even patient live, such as the patient under deep vein thrombosis in lower members, thoracoabdominal trauma, hemodynamic compromise situation or cardiac arrest.
Las masas cervicales referidas por el paciente o como hallazgo en la exploración física constituyen un proceso frecuente en las consultas de atención primaria (AP). Generalmente se trata de enfermedades benignas, pero en ocasiones son el primer signo de enfermedades graves. La edad del paciente, la anamnesis, la exploración física y las pruebas de laboratorio pueden orientar el proceso, pero la ecografía clínica realizada en AP, casi inmediata, aporta información sobre la naturaleza y la localización de la lesión, disminuye la incertidumbre diagnóstica en este nivel asistencial y mejora de forma muy importante la atención a estos procesos.
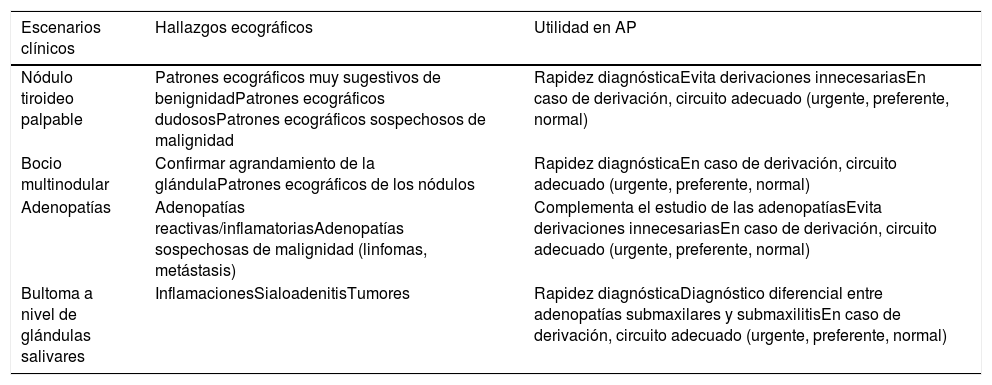
Las causas más frecuentes de masas cervicales son las que asientan sobre el tiroides (bocio y nódulo tiroideo [NT]), las adenopatías y el crecimiento de las glándulas salivales. En la tabla 1 se resumen los escenarios clínicos más habituales de la ecografía del cuello en AP, los hallazgos ecográficos esperables y la utilidad de la técnica en este nivel asistencial.
Escenarios clínicos para la ecografía del cuello en atención primaria
| Escenarios clínicos | Hallazgos ecográficos | Utilidad en AP |
|---|---|---|
| Nódulo tiroideo palpable | Patrones ecográficos muy sugestivos de benignidadPatrones ecográficos dudososPatrones ecográficos sospechosos de malignidad | Rapidez diagnósticaEvita derivaciones innecesariasEn caso de derivación, circuito adecuado (urgente, preferente, normal) |
| Bocio multinodular | Confirmar agrandamiento de la glándulaPatrones ecográficos de los nódulos | Rapidez diagnósticaEn caso de derivación, circuito adecuado (urgente, preferente, normal) |
| Adenopatías | Adenopatías reactivas/inflamatoriasAdenopatías sospechosas de malignidad (linfomas, metástasis) | Complementa el estudio de las adenopatíasEvita derivaciones innecesariasEn caso de derivación, circuito adecuado (urgente, preferente, normal) |
| Bultoma a nivel de glándulas salivares | InflamacionesSialoadenitisTumores | Rapidez diagnósticaDiagnóstico diferencial entre adenopatías submaxilares y submaxilitisEn caso de derivación, circuito adecuado (urgente, preferente, normal) |
AP: atención primaria.
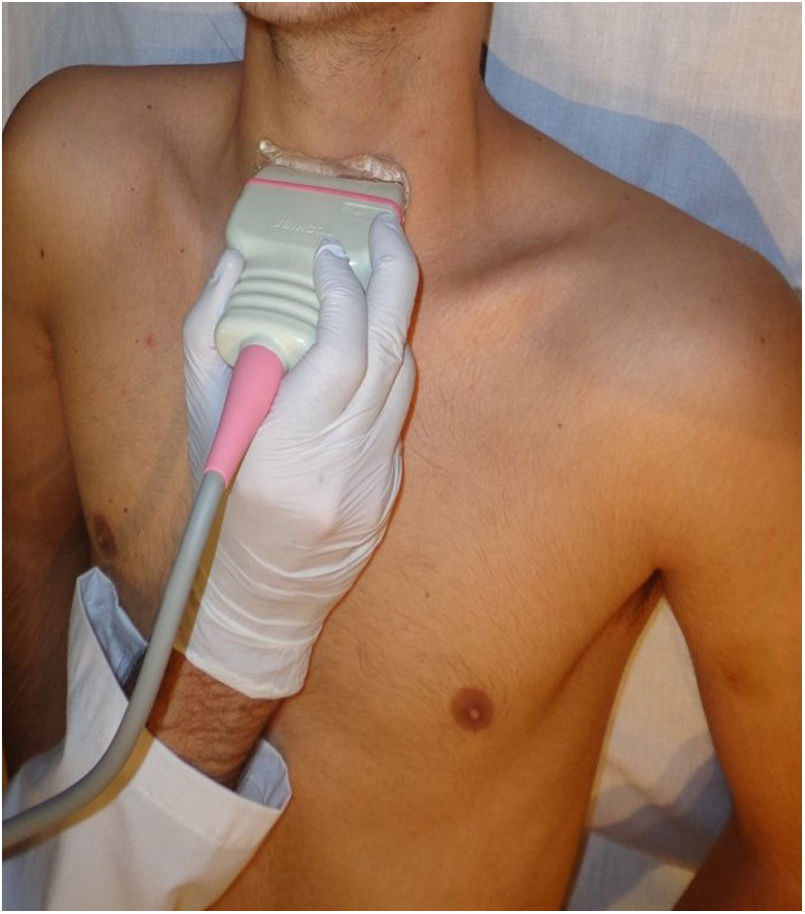
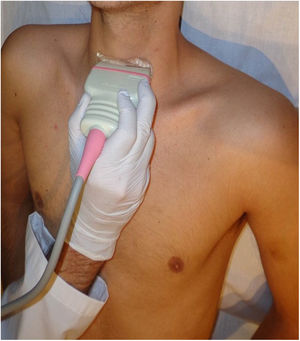
La glándula tiroides, superficial en el cuello, es muy accesible a la exploración ecográfica que se realiza con sonda lineal de alta frecuencia. El paciente debe hiperextender el cuello, en decúbito supino o sentado (fig. 1), y no precisa preparación.
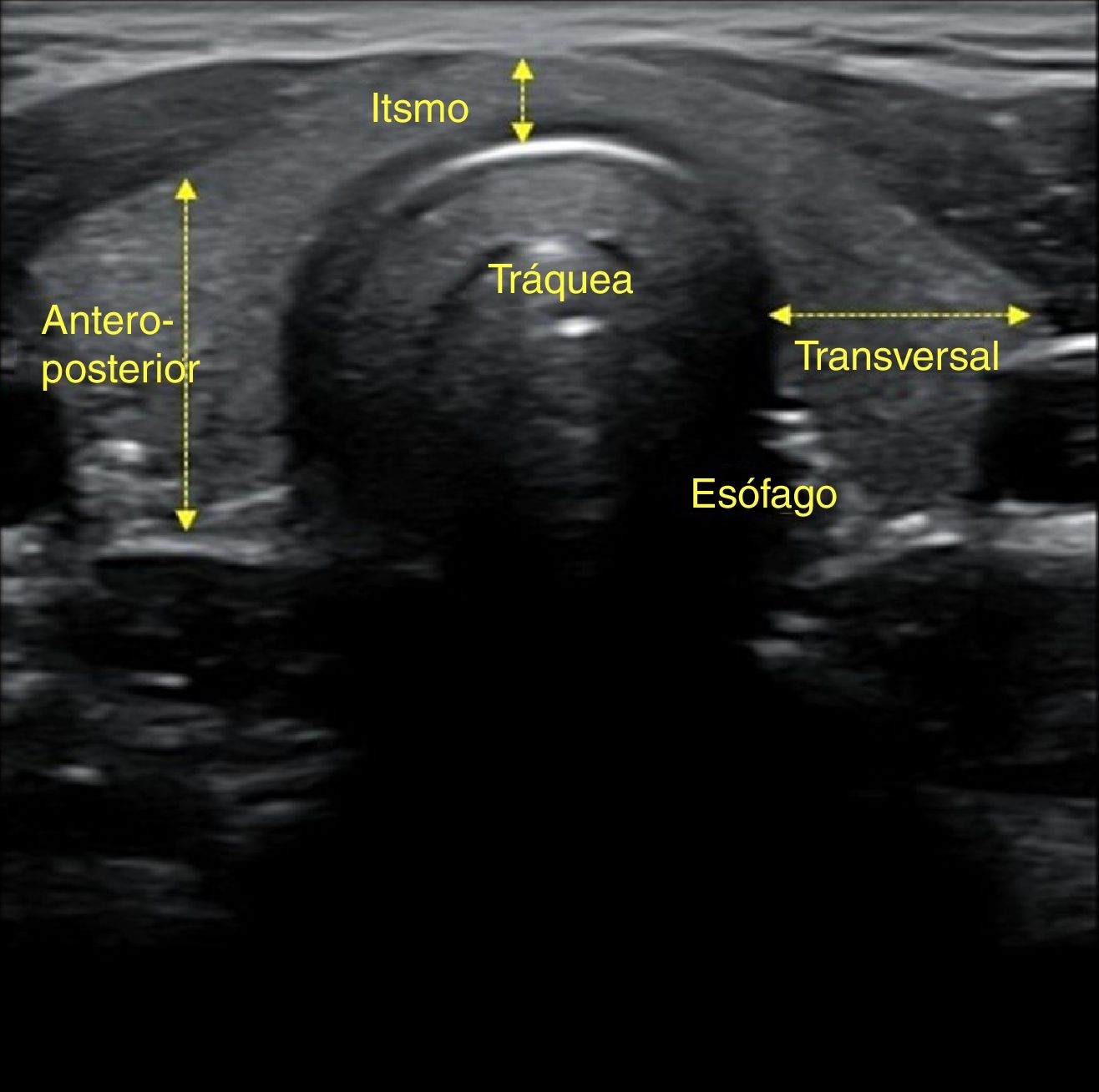
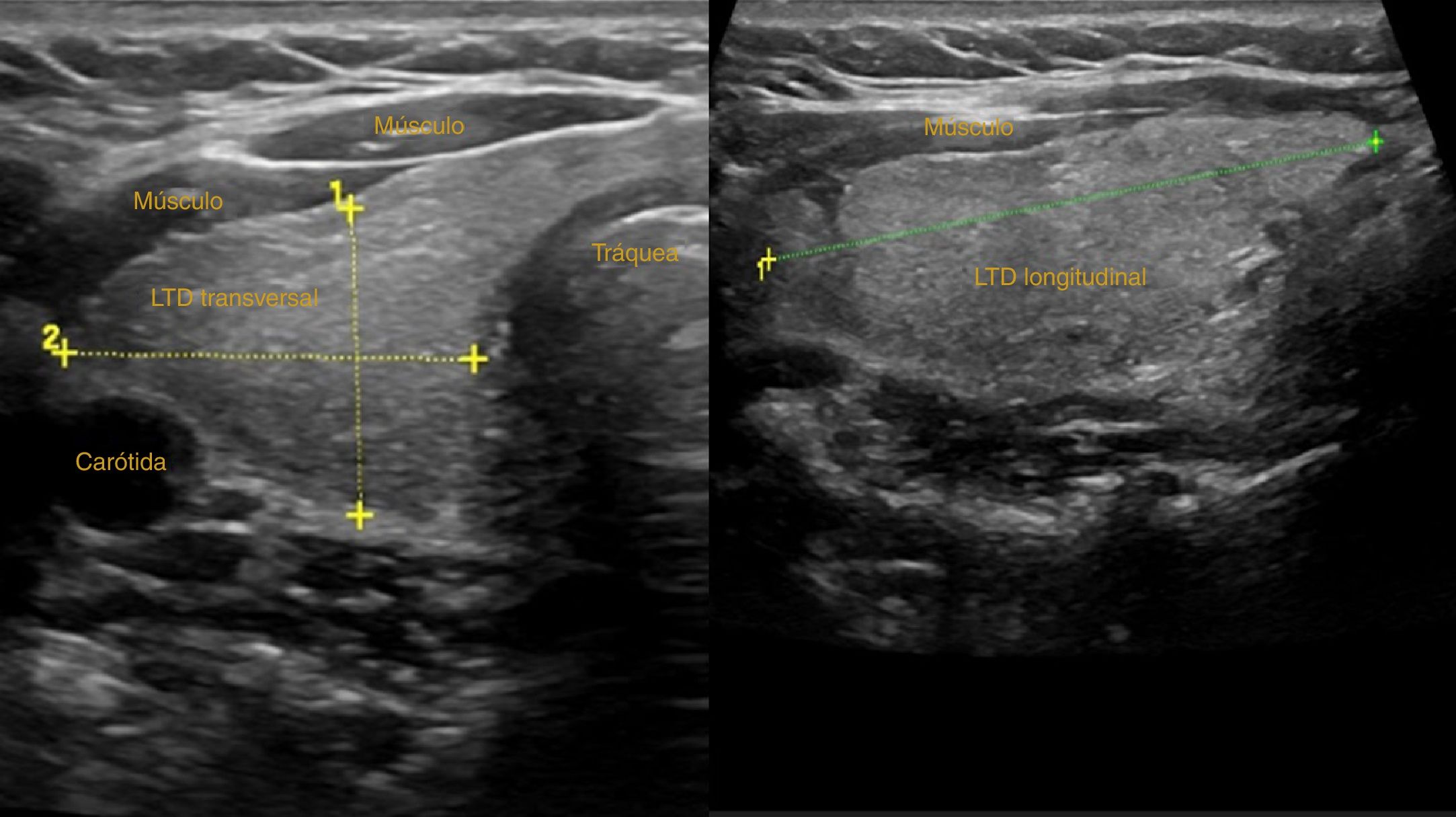
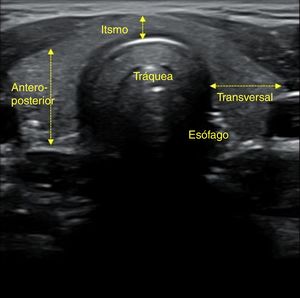
En un corte transversal del cuello, por debajo del cartílago tiroides, localizaremos la glándula como una estructura granular de ecogenicidad homogénea, hiperecogénica en relación a los músculos adyacentes que se ven como bandas hipoecoicas (fig. 2). El estudio continuará explorando cada lóbulo por separado, comenzando por el derecho, mediante cortes transversales y longitudinales del mismo (fig. 3). Posteriormente estudiaremos el istmo, también en cortes transversales y longitudinales. El lóbulo izquierdo se explora con la misma sistemática, con la particularidad de que en su corte transversal se suele apreciar el esófago en situación paratraqueal izquierda, pegado al estroma tiroideo. A ambos lados, y por fuera de la glándula, identificaremos la arteria carótida común y la vena yugular interna, así como posibles adenopatías si las hubiera. El estudio doppler color muestra la vascularización del tiroides y de las posibles lesiones que asienten sobre la glándula.
Escenarios clínicos en atención primaria y evidenciaLos 2 principales escenarios clínicos para el uso de la ecografía tiroidea en AP son el bocio y el NT.
BocioEl bocio es el aumento de tamaño de la glándula tiroides. Puede deberse a defectos de biosíntesis, deficiencia de yodo, enfermedad autoinmune o enfermedades nodulares.
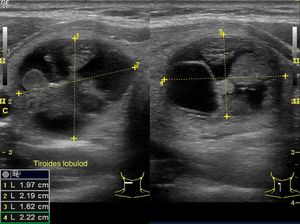
De todos los parámetros lineales, el diámetro anteroposterior del lóbulo tiroideo es el más preciso para confirmar el crecimiento de la glándula, por ser relativamente independiente de la talla del paciente. Cuando este es mayor de 2cm se confirma el aumento del tamaño glandular. El crecimiento tiroideo difuso se puede sospechar también por un aumento del istmo, con un diámetro anteroposterior mayor de 1cm. Un volumen tiroideo mayor de 25cm3 en varones y de 20cm3 en mujeres también es indicativo de bocio.
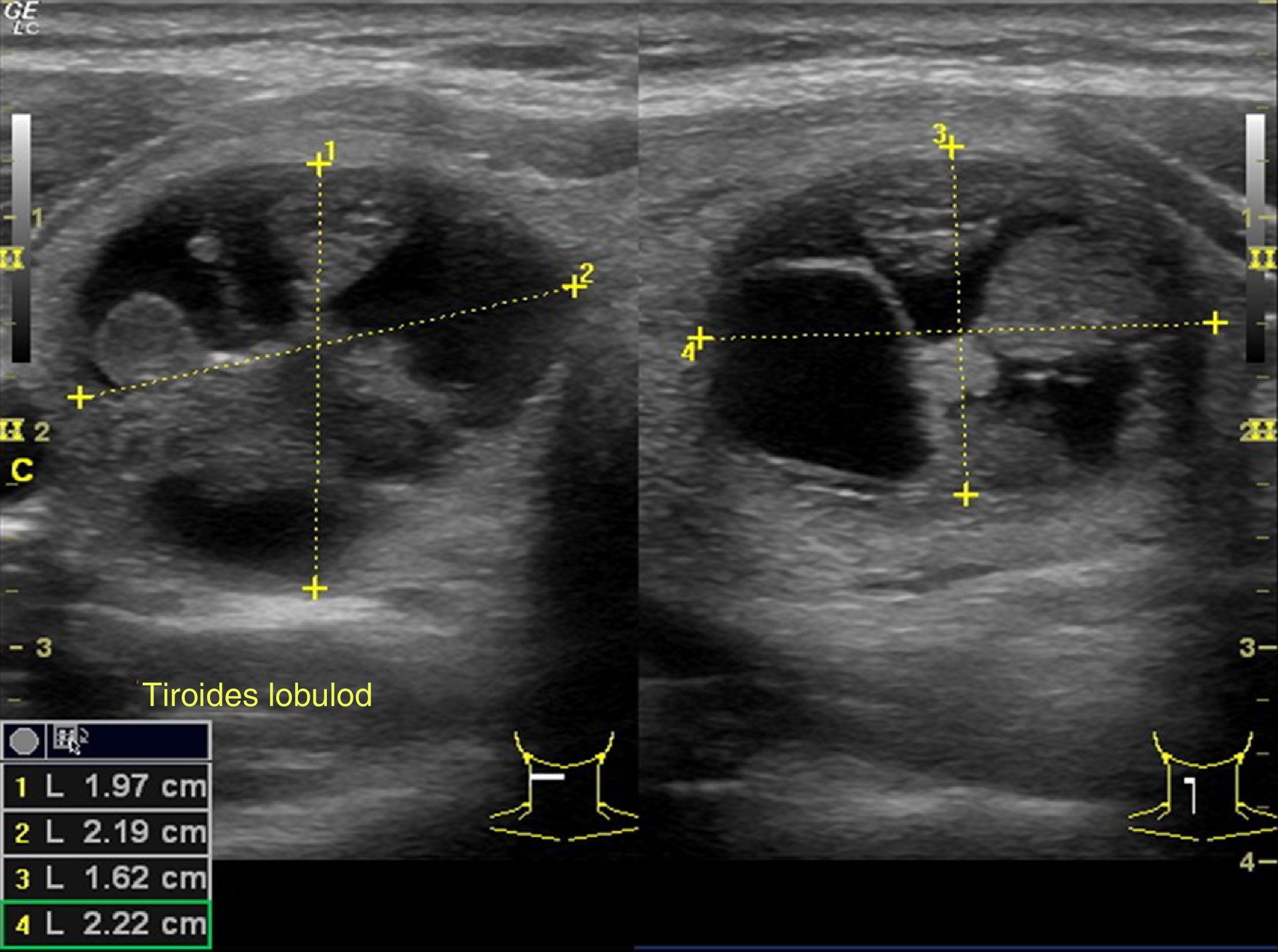
La ecografía en el bocio difuso muestra únicamente una glándula aumentada de tamaño. En el bocio multinodular puede apreciarse un aumento de tamaño glandular, con múltiples nódulos en los que se observa tejido tiroideo abigarrado y heteroecogénico. Se debe investigar si existen criterios ecográficos de malignidad en cualquiera de los nódulos. En la enfermedad de Graves se suele advertir un aumento homogéneo (a veces heterogéneo) de la glándula, característicamente hipervascularizado, objetivable con el doppler color. En la tiroiditis de Hashimoto veremos una glándula agrandada que puede ser multinodular, característicamente hipoecogénica y con tabicaciones groseras debidas a bandas fibrosas en estadios evolucionados.
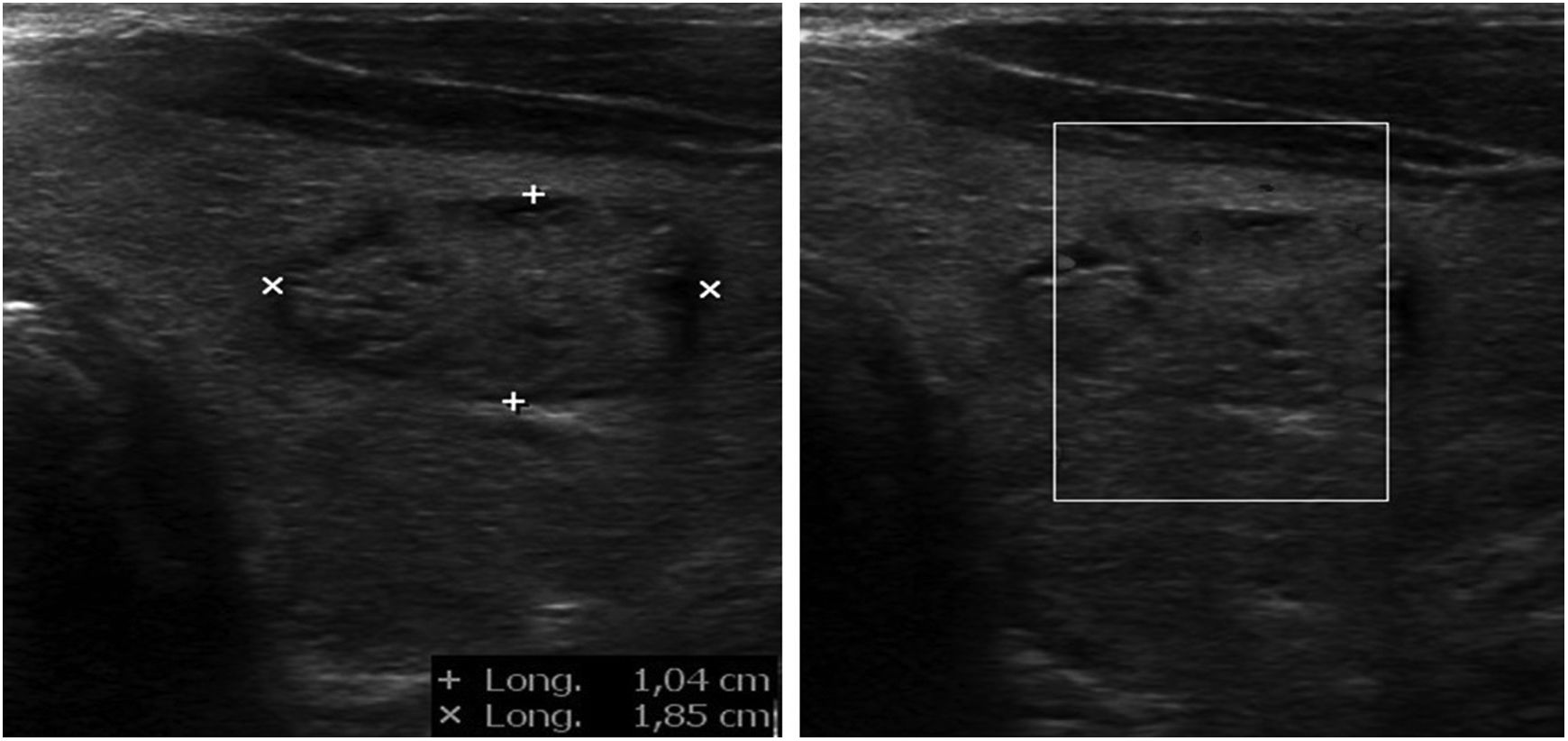
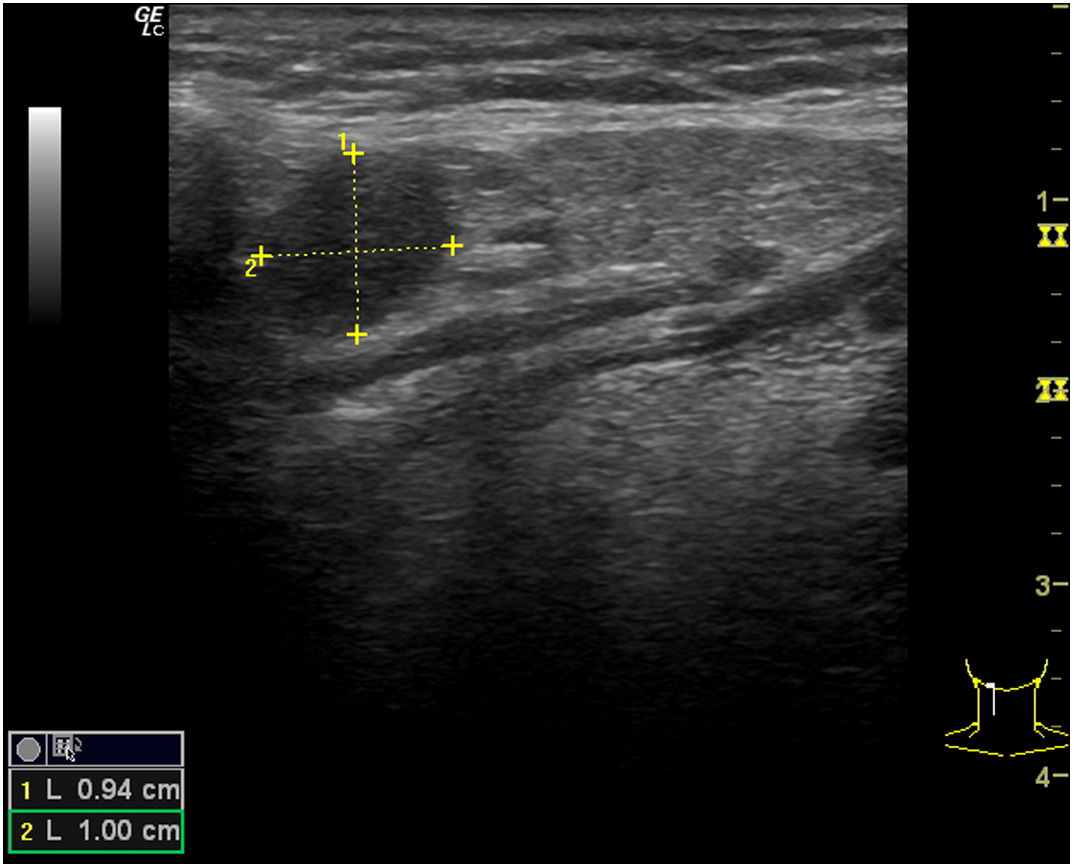
Nódulo tiroideo (figs. 4 y 5)El NT es un motivo frecuente de consulta en AP, ya que la prevalencia de los que son palpables se sitúa entre el 4 y el 7% de la población1, siendo más frecuente en mujeres. La prevalencia de los no palpables es muy superior, situándose por encima del 50% en mayores de 50años2. La importancia clínica de estudiar un NT radica en la necesidad de descartar un cáncer de tiroides, lo que ocurre el 5-10% de ellos3.
No se recomienda la ecografía como método de cribado de cáncer tiroideo en poblaciones asintomáticas, salvo en pacientes con factores de riesgo (antecedente de exposición a radiación cervical antes de los 15-18años, presencia de síndrome genético asociado a alta probabilidad de cáncer tiroideo y, probablemente, en pacientes con antecedentes de cáncer diferenciado de tiroides en 2 o más familiares de primer grado)4.
La ecografía de tiroides está indicada en todos los pacientes con sospecha de un NT o de un bocio nodular en el examen físico, en los nódulos incidentalmente observados en otros estudios de imagen y en el estudio de pacientes con adenopatías cervicales patológicas. Su empleo fuera de estas indicaciones, dada su elevada prevalencia y su carácter generalmente benigno, contribuye a la incidentalografía y a la realización de derivaciones y pruebas innecesarias.
Para mejorar el manejo del NT disponemos de un sistema de evaluación estandarizado (clasificación TI-RADS), que utiliza una categorización de riesgo de malignidad según las características ecográficas de los nódulos, con el fin de establecer los grupos que precisan ser estudiados por citología5. Los criterios ecográficos sugestivos de malignidad se exponen en la tabla 2.
Criterios ecográficos sugestivos de malignidad en el nódulo tiroideo
| Hipoecogenicidad |
| Microcalcificaciones |
| Nódulo parcialmente quístico con localización excéntrica del componente líquido y lobulación del componente sólido |
| Bordes irregulares |
| Invasión del parénquima tiroideo perinodular |
| Configuración taller thanwide (más alto que ancho) |
| Vascularización intranodal |
| Adenopatías sospechosas |
La ecografía es una técnica observador-dependiente y la evaluación ecográfica del NT puede ser compleja, por lo predictivo que los médicos de familia que realicen ecografía tiroidea deben disponer de formación en este escenario clínico. Existen estudios que evalúan la valoración ecográfica de los NT por no radiólogos, demostrando que el uso de manera rutinaria de la ecografía en la consulta permite agilizar el manejo de la enfermedad nodular tiroidea6, o que la ecografía de tiroides realizada por endocrinólogos tiene un valor predictivo positivo (VPP) y un valor predictivo negativo (VPN)>85% para el diagnóstico del cáncer de tiroides7. Recientemente se ha publicado un consenso para el estudio y el manejo de los NT por médicos no radiólogos4.
Utilidad de la ecografía clínica de tiroides en atención primariaLa primera utilidad de la ecografía tiroidea en AP es la de confirmar la localización de un nódulo en la región anterior del cuello. La exploración clínica suele aportar datos al respecto, pero siempre es de utilidad confirmar su ubicación en el tiroides.
No se debe realizar ecografía tiroidea fuera de las indicaciones aceptadas, pero en el contexto de estos escenarios clínicos su uso casi inmediato, realizado en AP, permitirá una aproximación a las características ecográficas del nódulo (composición, ecogenicidad, forma, márgenes, presencia o ausencia de calcificaciones y características de las mismas, vascularización), así como detectar posibles adenopatías cervicales patológicas, lo cual, junto con la historia clínica y las pruebas de función tiroidea, posibilitarán una adecuada valoración del proceso y, en el caso de ser necesaria, una derivación más orientada y con la prioridad más adecuada.
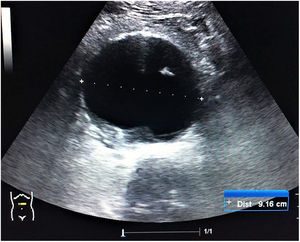
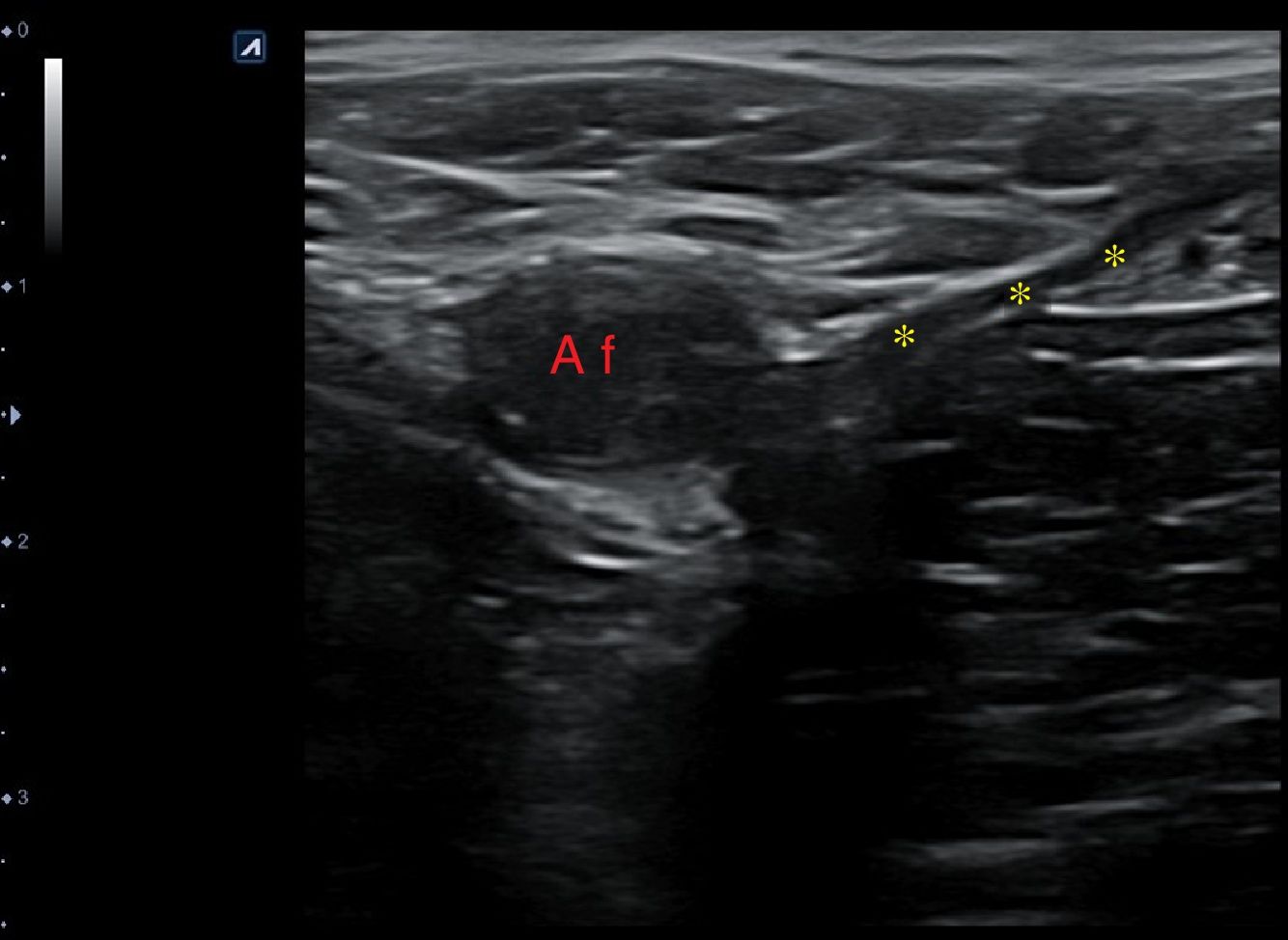
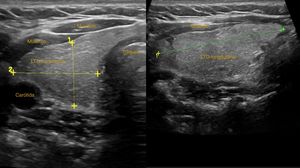
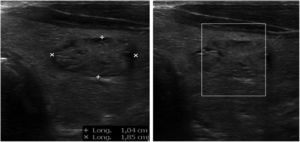
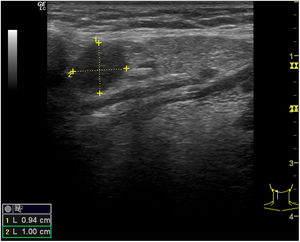
Adenopatías cervicalesUn nódulo o nódulos localizados en territorios ganglionares cervicales pueden ser debidos a adenopatías. No suelen ser patológicas las adenopatías menores de 1cm, al contrario que las mayores de 1cm, muchas de ellas de carácter benigno, de causa inflamatoria o reactiva. Solo el 1% de las adenopatías palpables son malignas8 (fig. 6), pero constituyen un motivo de preocupación frecuente en pacientes y médicos de familia. La edad del paciente, el tiempo de evolución, la clínica acompañante, las características de la adenopatía (localización, tamaño, consistencia, movilidad, presencia o ausencia de dolor) y la analítica, si es necesaria, pueden orientar a la etiología. No obstante, la ecografía clínica, en el caso de adenopatías con características clínicas sospechosas, aporta información adicional de gran valor, lo cual permitirá una mejor orientación del proceso.
Técnica de exploraciónLos territorios ganglionares, dada su situación superficial en el cuello, son de fácil acceso ecográfico, y esta técnica se ha demostrado útil para la evaluación de las adenopatías9. Para ello utilizaremos una sonda lineal de alta frecuencia. No es necesaria preparación previa. Realizaremos cortes longitudinales y transversales de la adenopatía o adenopatías, midiendo tanto el diámetro mayor como el menor. Utilizaremos el doppler color para estudiar la vascularización de estas. Si existen adenopatías sospechosas, siempre se debe ampliar el estudio ecográfico a la glándula tiroides, así como al resto de territorios ganglionares cervicales.
Escenarios clínicos en atención primariaCualquier nódulo o nódulos localizados en territorios ganglionares cervicales, sobre todo los sospechosos de malignidad (>1cm, duros, no dolorosos, adheridos a planos profundos), así como en el estudio de un NT, para confirmar o descartar adenopatías sospechosas, constituye el escenario de aplicación en AP.
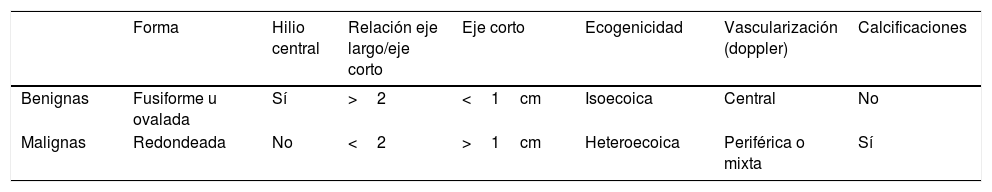
En la tabla 3 se resumen los criterios ecográficos sugestivos de benignidad o malignidad de las adenopatías9-14 y, aunque ninguno de los criterios es patognomónico, deben valorarse en conjunto. Las adenopatías de localización supraclavicular siempre se deben considerar patológicas.
Criterios ecográficos sugestivos de adenopatías cervicales benignas y malignas
| Forma | Hilio central | Relación eje largo/eje corto | Eje corto | Ecogenicidad | Vascularización (doppler) | Calcificaciones | |
|---|---|---|---|---|---|---|---|
| Benignas | Fusiforme u ovalada | Sí | >2 | <1cm | Isoecoica | Central | No |
| Malignas | Redondeada | No | <2 | >1cm | Heteroecoica | Periférica o mixta | Sí |
En el caso de adenopatías clínicamente sospechosas, la ecografía realizada en AP posibilita el estudio de la ecoestructura lesional, permitiendo una aproximación precisa a la gravedad del proceso y mejorando la toma de decisiones y la derivación, en caso de ser necesaria, más orientada y por el circuito más adecuado.
Glándulas salivalesEl aumento de tamaño o las masas localizadas a nivel de las glándulas salivales es un hallazgo ocasional en las consultas de AP. El tiempo de evolución de las lesiones, los factores desencadenantes, la afectación unilateral o bilateral, la palpación de la glándula y los signos y síntomas acompañantes pueden orientar su etiología. No obstante, en lesiones sospechosas o recidivantes la ecografía clínica realizada en AP puede aportar datos muy relevantes para la correcta evaluación del proceso.
Técnica de exploraciónPara explorar con ecografía las glándulas salivales utilizamos una sonda lineal de alta frecuencia sin preparación previa. Se deben realizar cortes longitudinales y transversales de las mismas y se completa la exploración con el estudio de las cadenas ganglionares cervicales. El doppler color permitirá estudiar la vascularización de la glándula y las lesiones que asienten sobre la misma. La parótida se localiza en la fosa retromandibular y su lóbulo profundo se explora parcialmente con ecografía. La glándula submandibular se localiza en la región posterior del triángulo submandibular y suele tener morfología casi triangular. La glándula sublingual está rodeada por los músculos de la cavidad oral y tiene una morfología ovoidea.
Las glándulas salivales mayores presentan una ecogenicidad homogénea que aumenta con la edad debido a su mayor contenido en grasa.
Escenarios clínicos en atención primariaSe consideran escenarios adecuados para la realización de ecografía clínica en AP las tumefacciones persistentes o recidivantes de las glándulas salivales y el hallazgo de masas a este nivel. También es útil para el diagnóstico diferencial de una masa a nivel submandibular, permitiendo realizar el diagnóstico diferencial entre la submaxilitis y las adenopatías submandibulares. En caso de enfermedad unilateral siempre es útil la comparación de la glándula afectada con la contralateral.
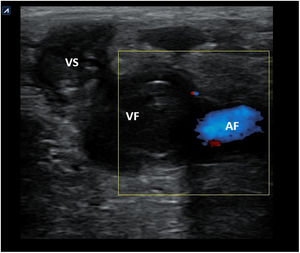
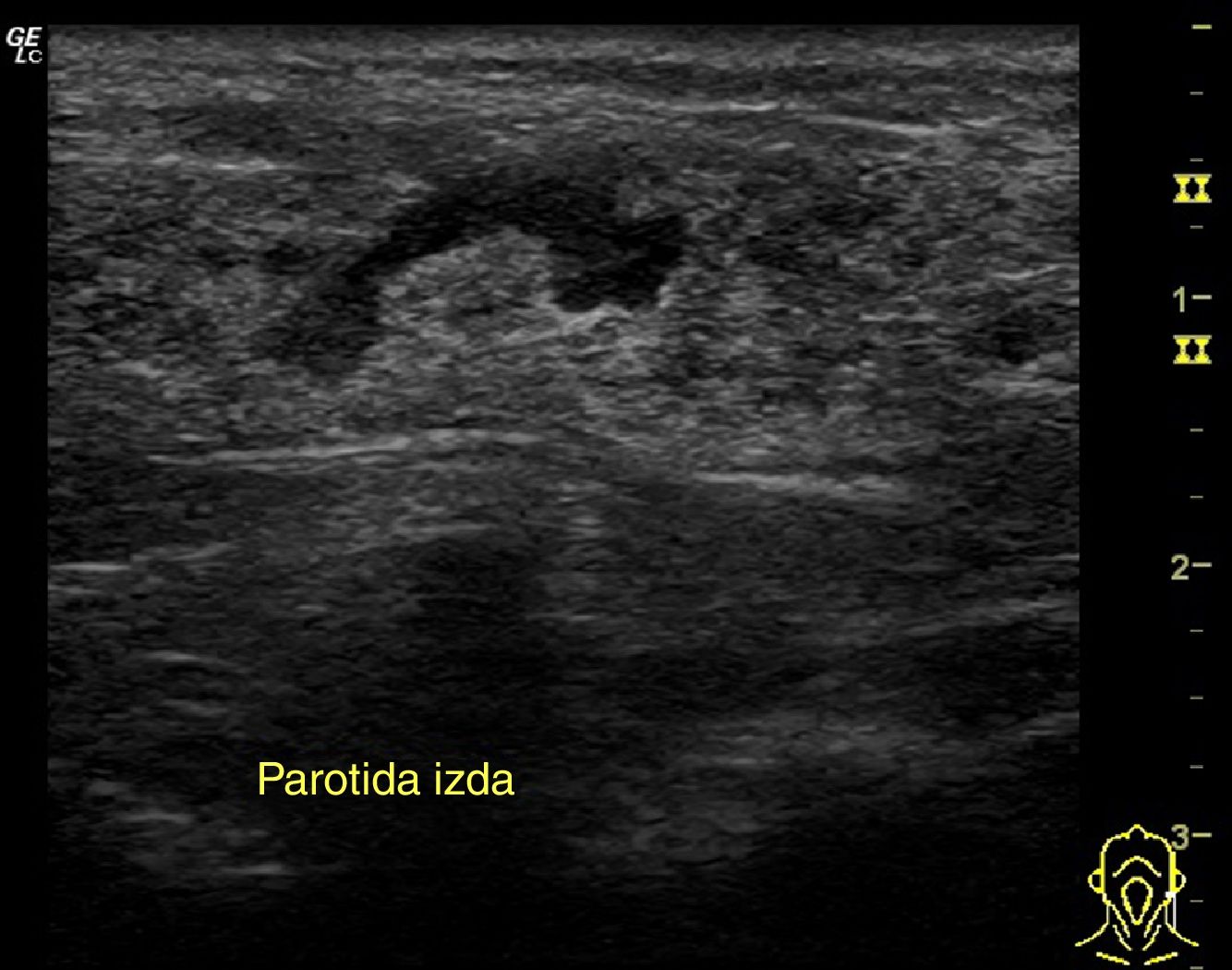
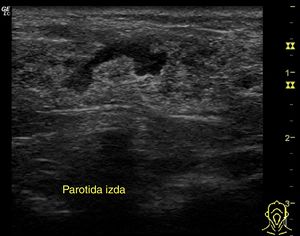
Utilidad de la ecografía de las glándulas salivales en atención primariaEn los escenarios comentados, la ecografía casi inmediata realizada en AP permitirá comprobar la afectación de la glándula y visualizar su ecoestructura, orientando las etiologías más frecuentes de enfermedad a ese nivel (inflamatoria [fig. 7], litiásica o tumoral), permitiendo integrar la información clínica con los hallazgos ecográficos, disminuyendo así la incertidumbre diagnóstica y mejorando la atención a estos procesos.
Ecografía clínica en situaciones de urgenciaCribado de trombosis venosa profunda en la extremidad inferiorLa trombosis venosa es una causa importante de morbimortalidad. La ecografía del trayecto venoso de las extremidades inferiores complementada con maniobras de compresión ha demostrado ser una técnica altamente sensible y específica para el reconocimiento de la trombosis venosa profunda (TVP) de extremidades inferiores, sin la necesidad de exposición a la iatrogenia, que puede inducir la irradiación o la inyección de contraste de otras exploraciones angiográficas15. Cuando el estudio de la extremidad inferior lo efectúa un técnico en radiología, y los interpreta un radiólogo, el tiempo hasta el diagnóstico y el tratamiento potencial de una TVP puede retrasarse hasta 2h16.
Las actuales recomendaciones para el diagnóstico ecográfico de la TVP en el territorio proximal de la extremidad inferior consisten en una técnica de compresión de 2puntos: la vena femoral común y la vena poplítea. Esta técnica se puede realizar en apenas 5min, y proporciona una elevada sensibilidad y especificidad. En concreto, el estudio de Poley et al.17 halló una sensibilidad del 91% (IC95%: 70-98%) y una especificidad del 97% (IC95%: 92-99%). Ante la sospecha clínica de TVP, una ecografía con compresión negativa significa que con un alto grado de necesidad no es preciso iniciar la terapia de anticoagulación. El examen de compresión de TVP de 2puntos se ha evaluado en múltiples estudios aleatorizados controlados, y es una técnica bien aceptada cuando se usa adecuadamente con las evaluaciones de probabilidad pretest. El aprendizaje por parte de un médico es posible realizarlo en una sesión de 10min de entrenamiento.
La incorporación de esta técnica redujo la necesidad de realización de la prueba de dímeroD en un 66%, y el tiempo medio para llegar al diagnóstico de certeza en 5h. Sin embargo, los trabajos de investigación revisados comentan en sus discusiones que, dada la baja sensibilidad de la técnica, esta no debe usarse de forma aislada.
En una revisión sistemática y metaanálisis, Pomero et al.18 compararon la ecografía de emergencia realizada por un médico clínico en urgencias mediante un ecógrafo sencillo con la realizada por un radiólogo mediante un ecógrafo equipado con doppler dúplex de flujo de color, y con la angiografía para diagnosticar la TVP. La sensibilidad media ponderada de la ecografía realizada por el médico clínico en urgencias en comparación con la prueba de imagen de referencia fue del 96,1% (IC95%: 90,6-98,5%) y la especificidad media fue del 96,8% (IC95%: 94,6-98,1%).
La seguridad, la facilidad de uso, la rapidez, el bajo costo y la accesibilidad hacen que la ecografía de cabecera para la TVP sea especialmente útil para los médicos de los centros de AP y de urgencias.
Técnica de estudioSe precisa un sistema de ultrasonido preferiblemente portátil con un transductor lineal de alta resolución: 5,0-7,0MHz y gel de ultrasonido. El paciente debe estar en posición supina con la pierna a explorar expuesta hasta el ligamento inguinal. Si se dispone de una camilla basculante, sería ideal colocarla en posición de 30-40grados de Trendelenburg inverso.
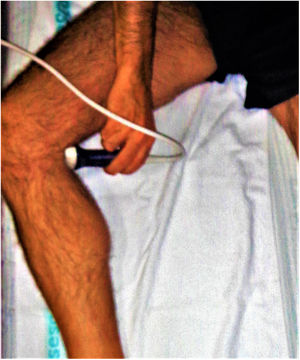
Tal como se ha comentado, se precisa explorar 2puntos. El primer punto es el examen de la vena femoral común (fig. 8). El paciente debe estar en posición supina con la cadera girada y flexionada externamente, como se muestra a continuación. Por convención, esta exploración se realiza con orientación abdominal con el marcador de la sonda apuntando hacia la cabeza o el lado derecho del paciente.
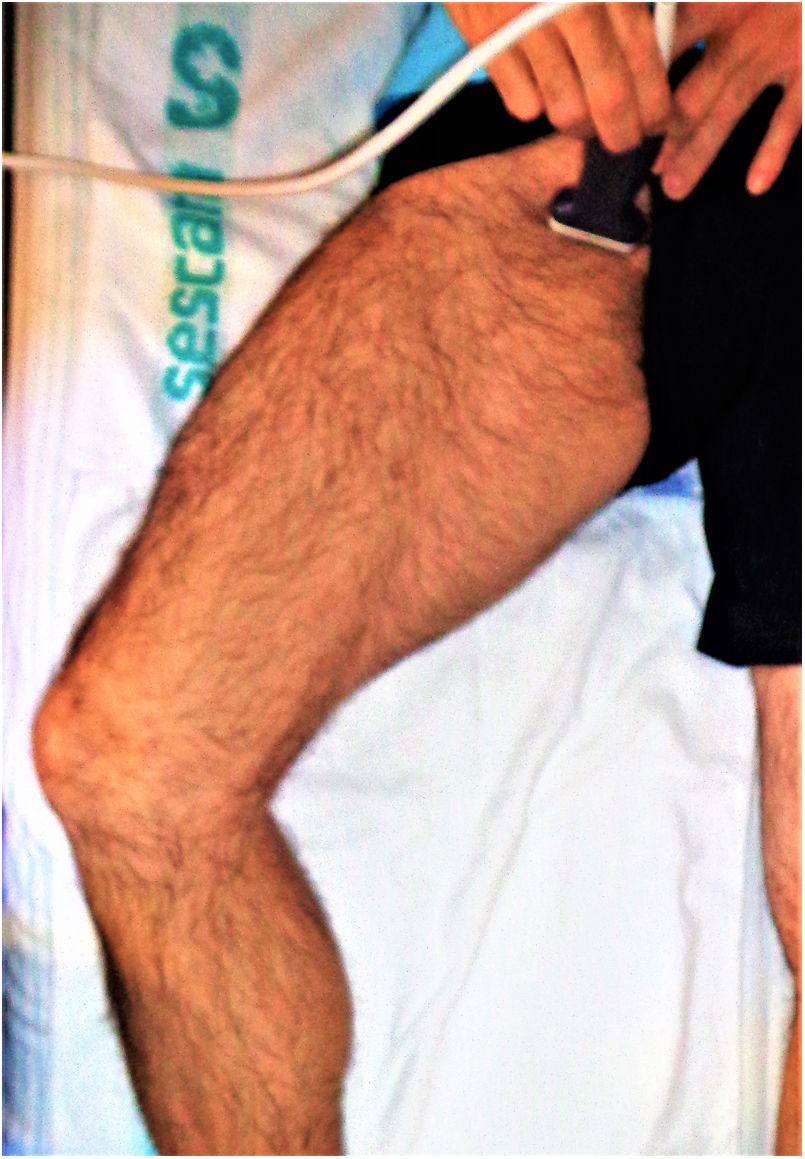
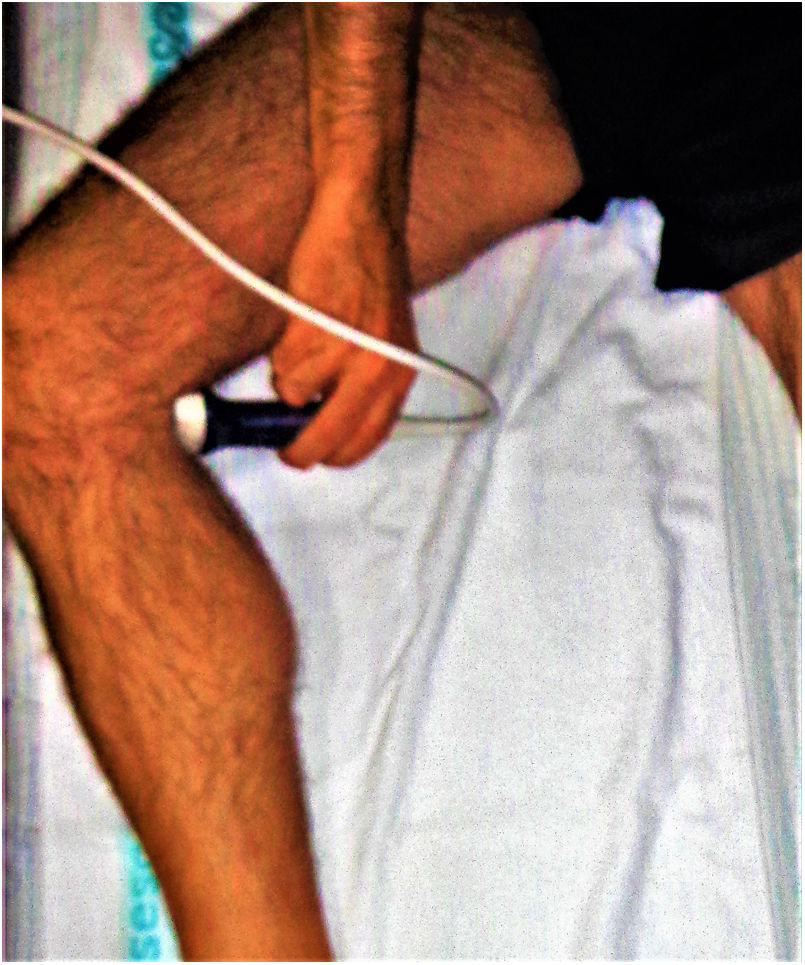
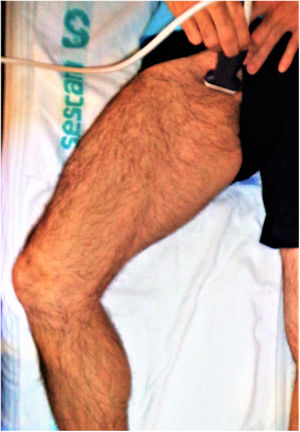
Al examinar la vena poplítea necesitamos acceder a la fosa poplítea posteromedial de la rodilla. El paciente puede colgar la pierna del borde de la cama o doblar la rodilla y rotar externamente la cadera, como se muestra en la figura 9. Si es necesario, el paciente también puede colocarse de costado o en posición prona. Aunque las imágenes mostradas representan posiciones ideales, el estado y la cooperación del paciente, en última instancia, determinarán la posición del paciente.
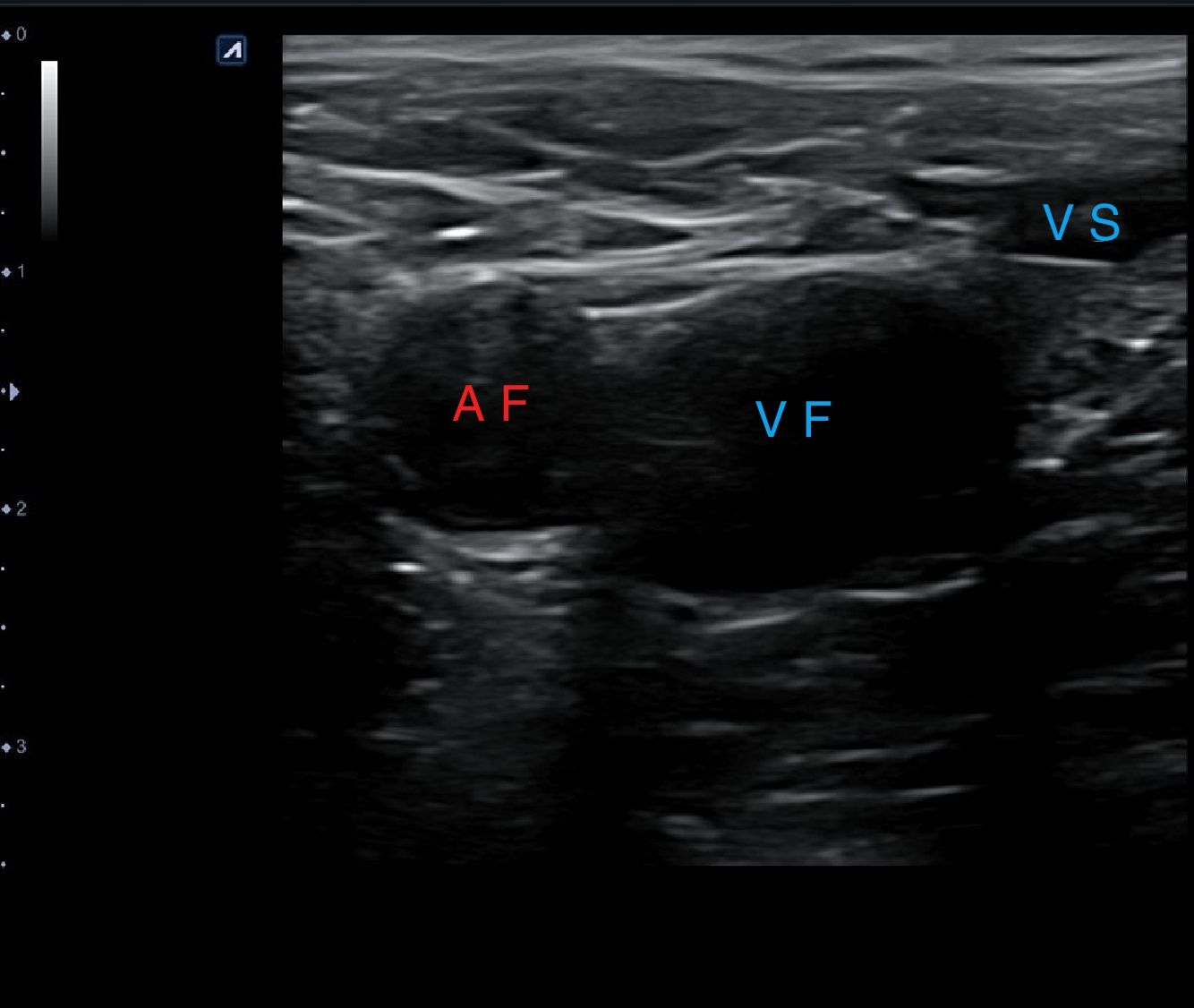
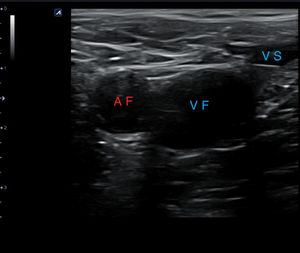
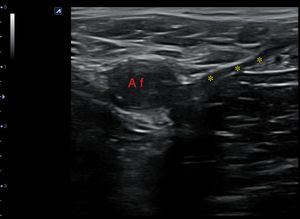
Una vez localizadas las estructuras venosas (fig. 10), usando el transductor, se aplica presión directa para comprimir completamente la vena. Si la vena se comprime por completo, se puede descartar una TVP en la localización que se está explorando (fig. 11). Hay que asegurarse de que se aplica suficiente presión y que esta se aplica de manera uniforme.
La ecografía se está constituyendo en una herramienta imprescindible en cualquier entorno clínico, siendo en muchos de ellos la primera prueba exploratoria a realizar. Si eso es cierto, no lo es menos en el paciente con trauma toracoabdominal grave. La utilización de la ecografía por médicos que trabajan en los servicios de urgencias se remonta a 198819, y específicamente en el trauma abdominal, a 199520. El e-FAST o Extended Focused Assessment with Sonography in Trauma (FAST extendido), que amplía la búsqueda de líquido intraabdominal/torácico al cribado de neumotórax masivo, dada su habitual coexistencia en este tipo de traumas, constituye, hoy en día, un protocolo tan básico de manejo en los servicios de urgencias como lo puede ser la misma resucitación cardiopulmonar (RCP), pudiéndose realizar de forma concomitante.
La ecografía portátil y portable tiene su origen en la guerra de Irak para atender a los soldados heridos, incluso en el frente, y facilitar el manejo del «blast injury». En el trauma toracoabdominal va camino de constituirse, por medio del protocolo e-FAST, en un «acto reflejo» para el médico que atiende pacientes politraumatizados en cualquier ámbito. Ha demostrado una sensibilidad mayor que el lavado peritoneal para detectar líquido intraperitoneal21. Realizada en el servicio de urgencias, adelanta la cirugía inmediata en el hemoperitoneo grave en 20min frente a la realizada por radiólogos en servicios centralizados (donde, con frecuencia, puede no estar disponible de forma presencial durante las 24h del día), disminuyendo de manera importante la morbimortalidad. La rapidez del diagnóstico (un médico experimentado tarda entre 3 y 5min en realizarlo) en estos pacientes es fundamental, porque si hay un sangrado intraabdominal la probabilidad de muerte asciende, aproximadamente, en un 1% cada 3min que se demora la intervención22. Se ha estimado la eficacia diagnóstica de la ecografía para la detección de líquido libre, ofreciendo una sensibilidad del 92,8%, una especificidad del 80%, un VPP del 92,8% y un VPN del 80%21.
La creciente disponibilidad de equipos portables de gran calidad posibilita que el examen e-FAST en el paciente con lesiones agudas pueda generalizarse, garantizando la adecuada capacitación profesional. Esta ha de estar sujeta a criterios de garantía de calidad, tal como establecieron el Instituto Americano de Ultrasonido en Medicina (AIUM) y el Colegio Americano de Médicos de Emergencia (ACEP)23. El Council of Emergency Medicine Residency Directors recomienda que los programas de entrenamiento en emergencias tengan una extensión de 2semanas (80h) y 150 valoraciones en situaciones críticas, incluyendo 40 exámenes FAST, 30 de TVP y 10 de procedimientos24. Nos consta que en España se realizan trabajos para establecer criterios de calidad, formación y niveles de competencia en ese sentido.
Técnica de estudio y utilidad clínica (tabla 4)Con sonda de baja frecuencia (3,5-5MHz), utilizando cortes longitudinales y transversales, buscamos líquido libre en los distintos espacios toracoabdominales, cuya presencia compromete la vida del enfermo (hemotórax, hemopericardio, hemoperitoneo y, en el e-FAST, neumotórax masivo). Deberá realizarse en 3-5min, pudiéndose completar y repetir a la vez que se van adelantando otras técnicas (toma de vías periféricas o centrales) o las propias maniobras de RCP. Los cortes se realizarán según el siguiente protocolo:
- 1.
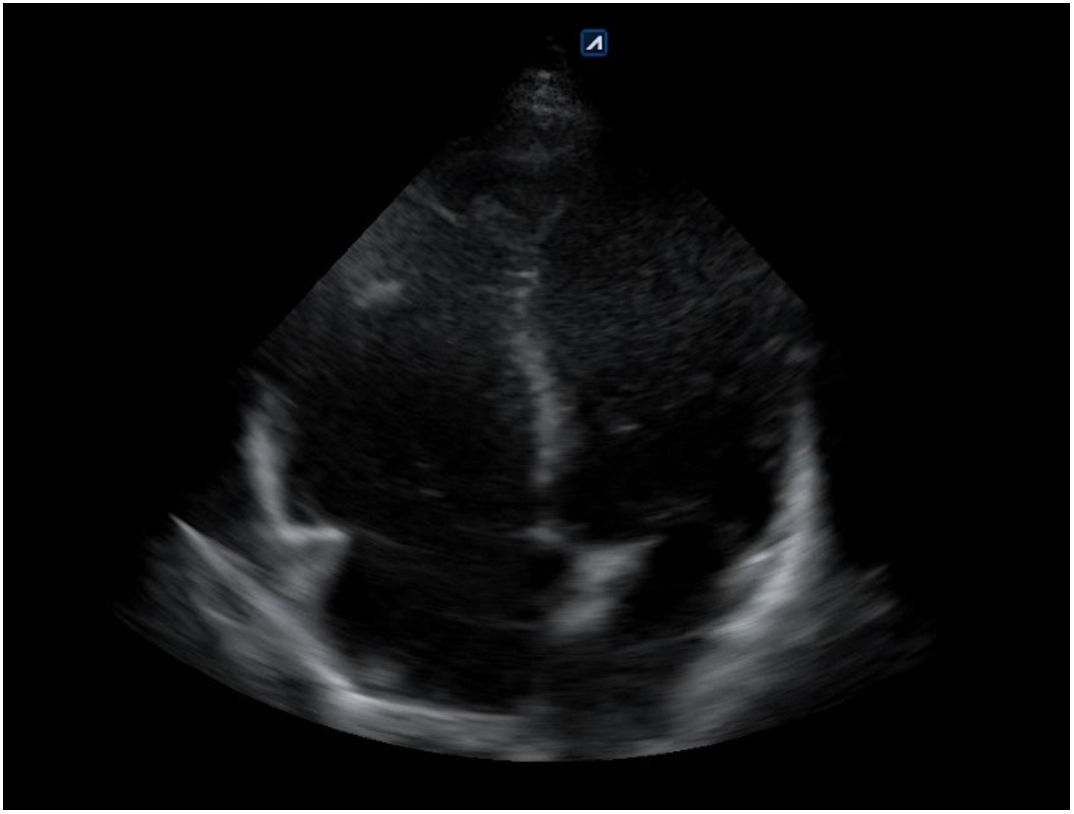
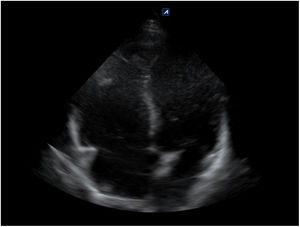
Subxifoideo, transversal para descartar derrame pericárdico (fig. 12) o hemopericardio.
- 2.
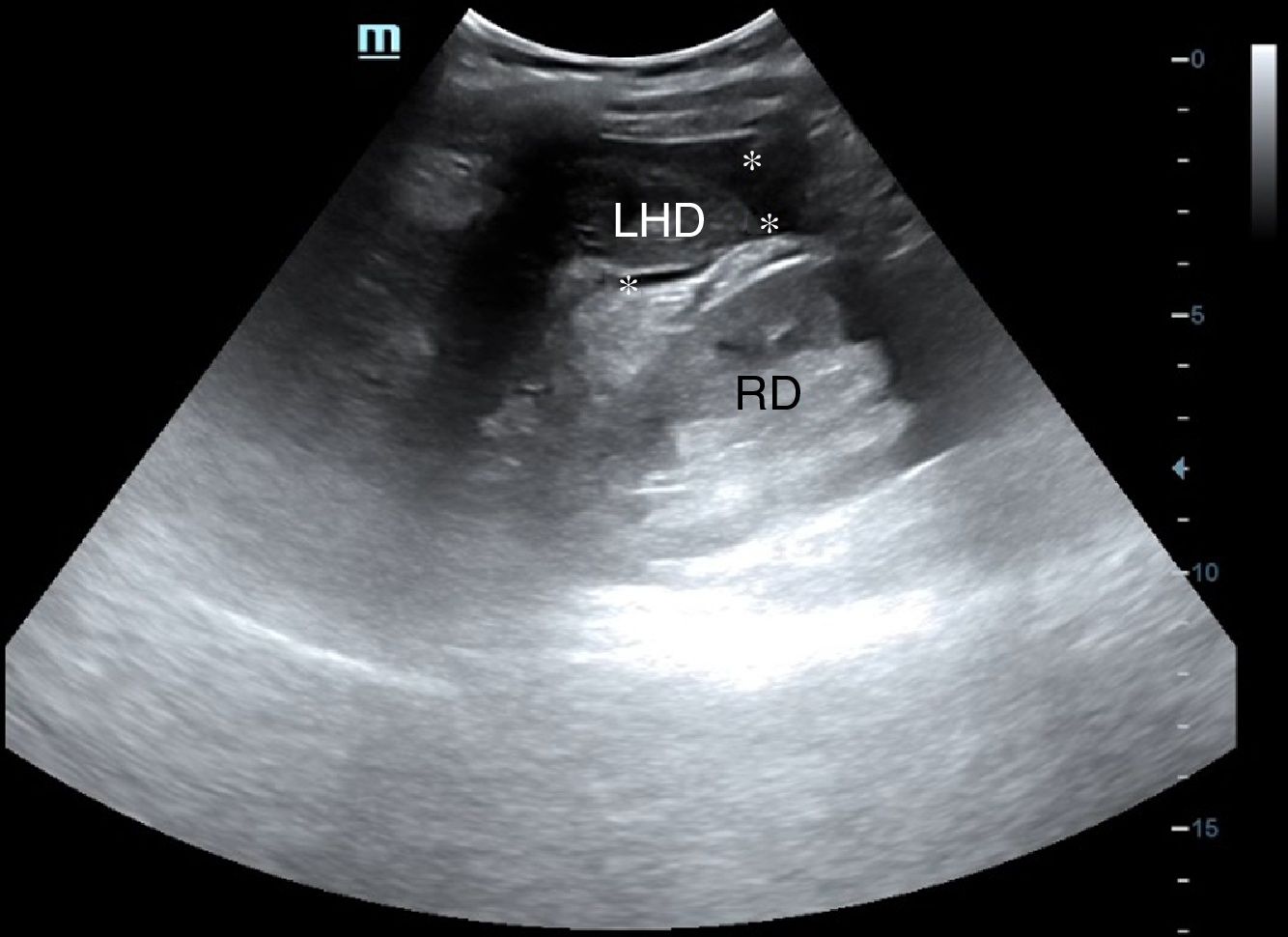
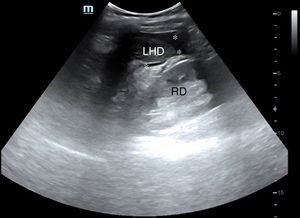
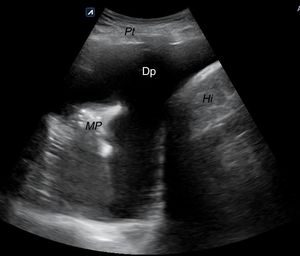
Línea medio-axilar derecha, para descartar hemoperitoneo (líquido en Morrison) (fig. 13) y/o derrame pleural derecho por encima del diafragma (fig. 14).
- 3.
Línea medio-axilar izquierda para descartar líquido en el espacio esplenorrenal (hemoperitoneo) y/o derrame pleural izquierdo por encima del diafragma.
- 4.
Espacio paracólico derecho (vacío derecho), oblicuo, para descartar hemoperitoneo.
- 5.
Espacio paracólico izquierdo, con el mismo fin.
- 6.
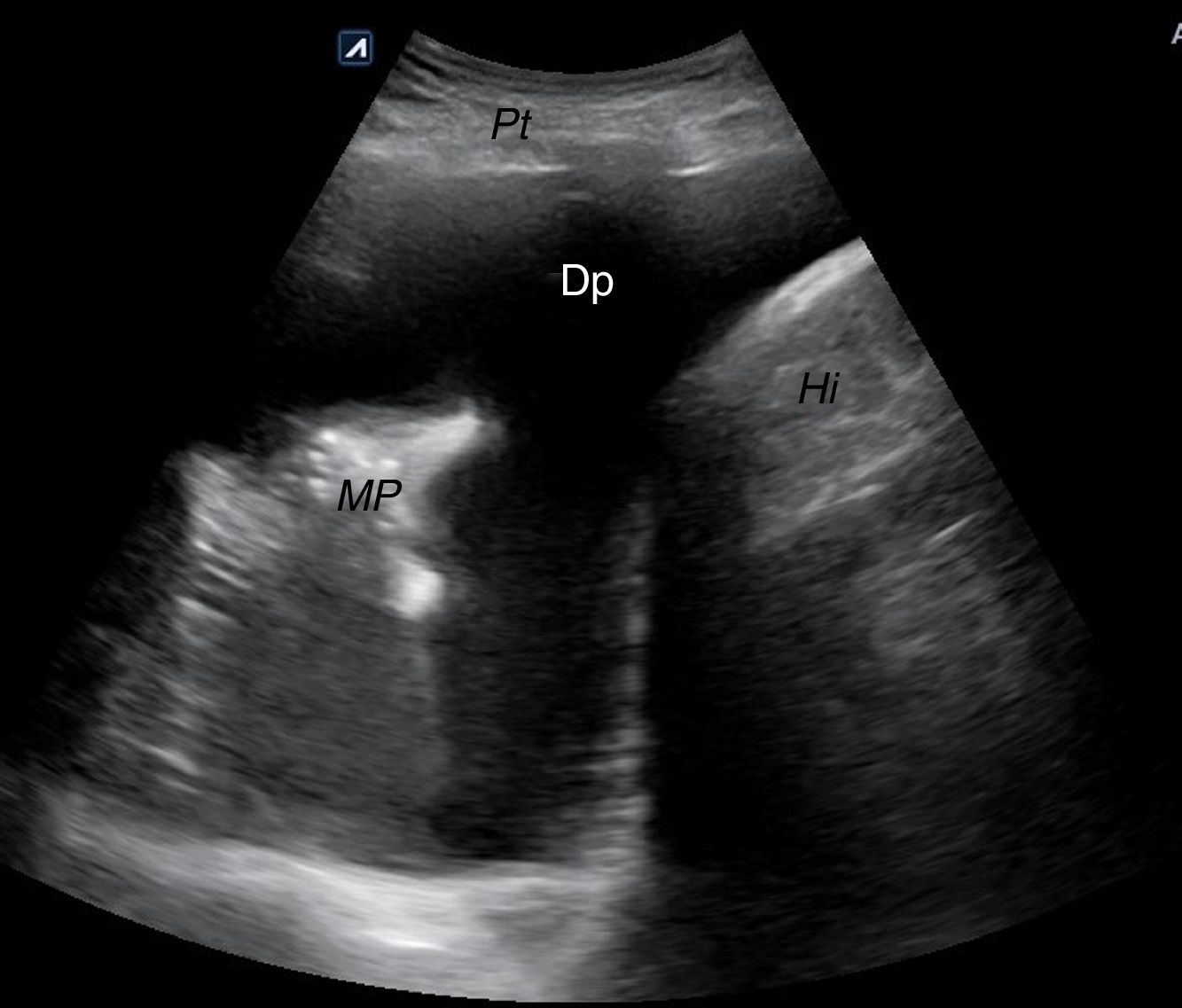
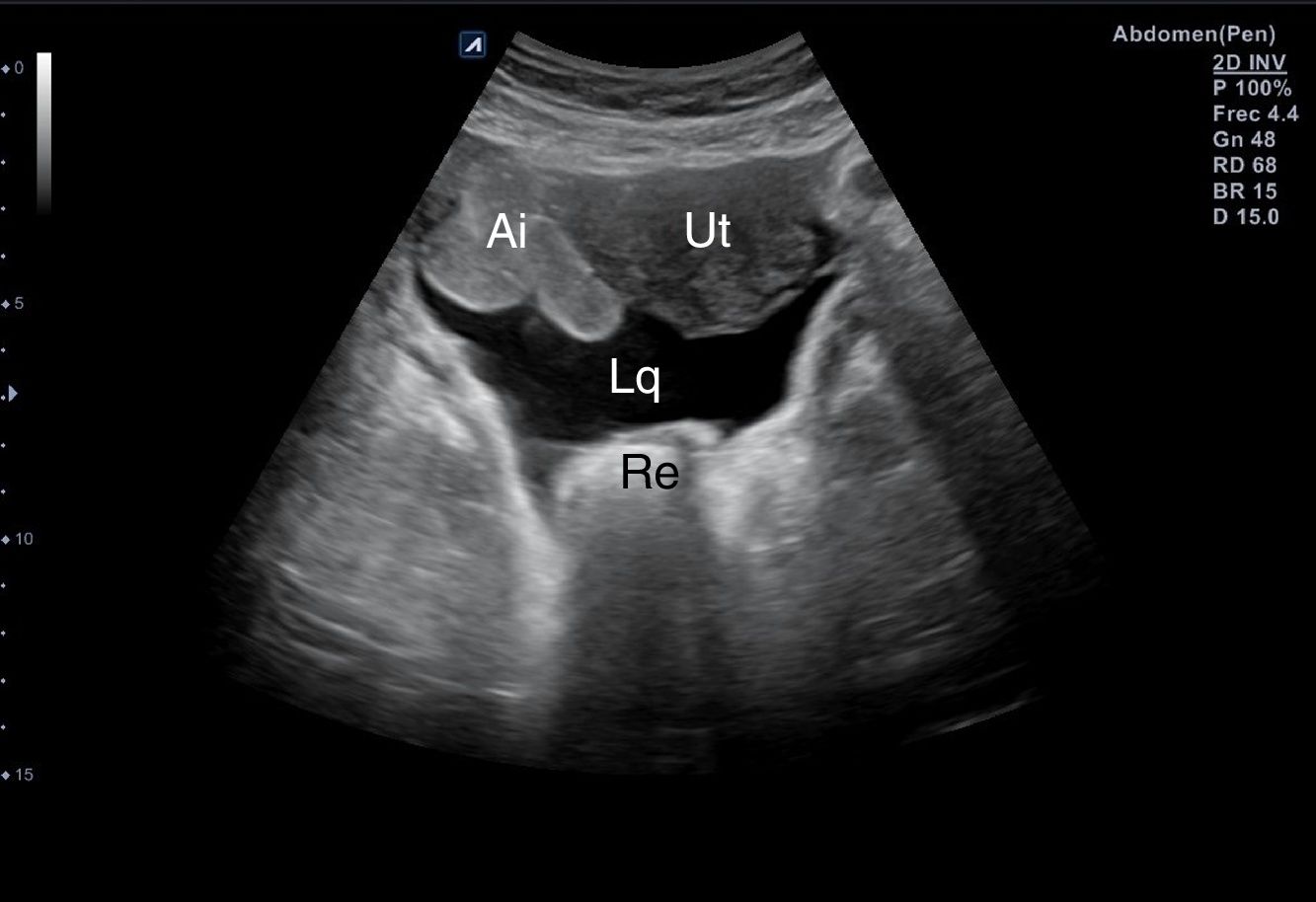
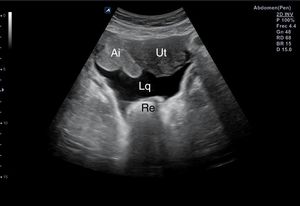
Hipogastrio, transversal/longitudinal, para descartar líquido en el espacio de Douglas (fig. 15) o recto-vesical en el varón.
- 7.
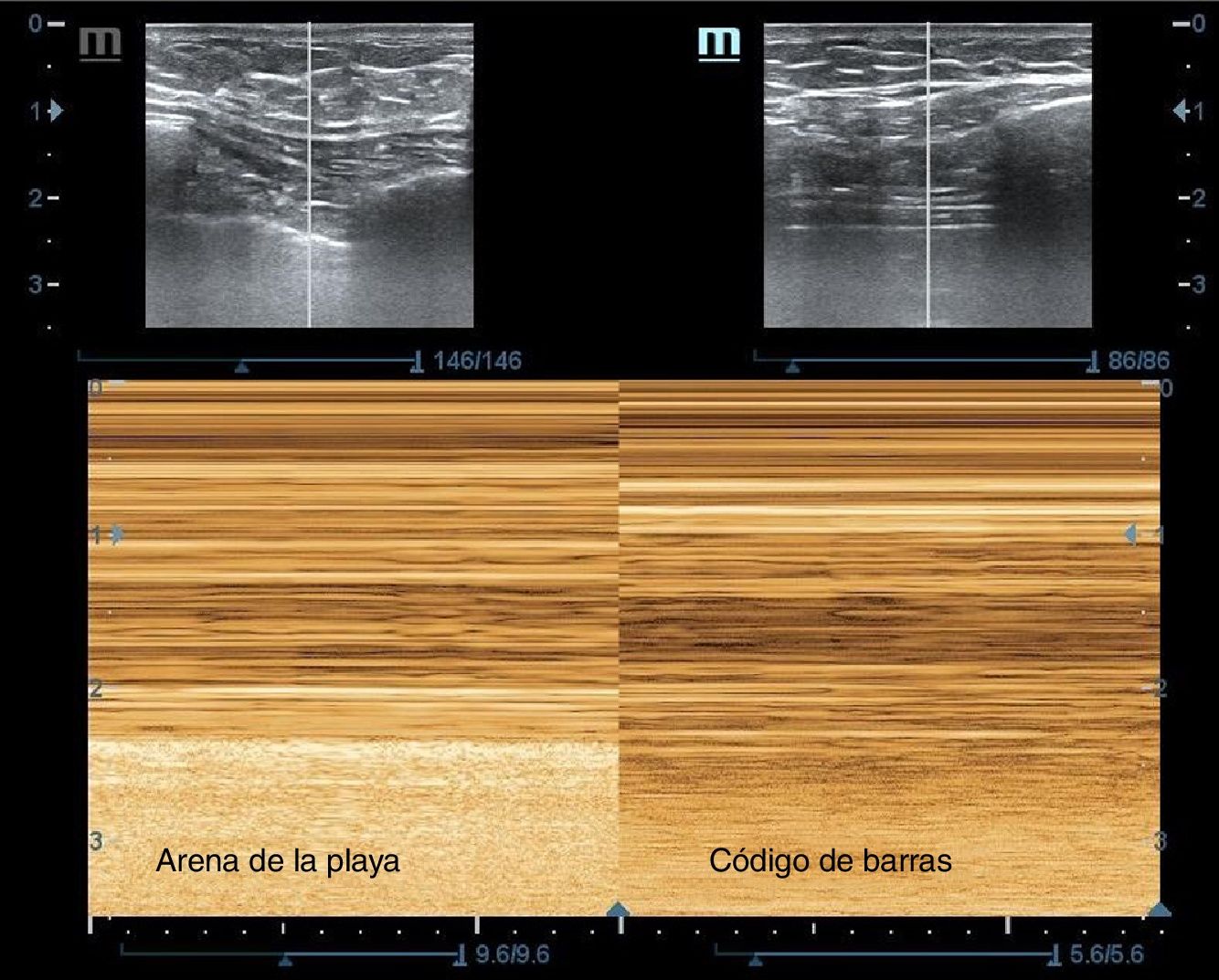
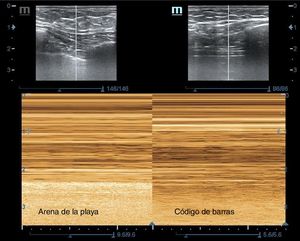
7 y 8. Ambos hemitórax, longitudinales, entre el 2.°-3.er espacios intercostales anteriores, para descartar neumotórax masivo (desaparición del deslizamiento pleural o signo del código de barras) (fig. 16).
Hallazgos esperables y utilidad clínica del protocolo e-FAST
| 1. Ventana subcostal (subxifoidea) | Descartar derrame pericárdico o hemoperitoneo |
| 2. Línea medioaxilar o axilar anterior derecha | Descartar hemoperitoneo (líquido libre en espacio de Morrison por debajo del diafragma) o derrame pleural/hemotórax derecho (por encima del diafragma) |
| 3. Línea medioaxilar o axilar posterior izquierda | Descartar hemoperitoneo (líquido libre en espacio esplenorrenal por debajo del diafragma) o derrame pleural/hemotórax izquierdo (por encima del diafragma) |
| 4. Espacio paracólico derecho | Descartar hemoperitoneo en vacío derecho |
| 5. Espacio paracólico izquierdo | Descartar hemoperitoneo en vacío izquierdo |
| 6. Ventana hipogástrica | Descartar hemoperitoneo (líquido libre) en fondo de saco de Douglas (mujer) o espacio rectovesical (varón) |
| 7. Hemitórax anterior derecho, 2.°-3.er espacio intercostal | Descartar neumotórax masivo derecho (ausencia de deslizamiento pleural, signo del código de barras) |
| 8. Hemitórax anterior izquierdo, 2.°-3.er espacio intercostal | Descartar neumotórax masivo izquierdo (ausencia de deslizamiento pleural, signo del código de barras) |
Todo el protocolo se puede realizar con una única sonda convex o sectorial, pero para la evaluación del deslizamiento pleural es preferible el empleo de una sonda lineal si está disponible.
Se deben evitar las pérdidas de tiempo por cambio de transductor o maniobras de mejora de calidad ecográfica. No debemos olvidar que no buscamos saber si es sangre u otro fluido, ni su procedencia, ni tampoco que, en esta fase de la atención, el tiempo es el factor más importante para tratar de salvar la vida del paciente y que un hallazgo dudoso no nos debe entretener, sino continuar la exploración, pues la siguiente maniobra podría resolver la duda que previamente se nos había generado.
El e-FAST se realizará en el lugar donde sea atendido el paciente con trauma toracoabdominal, ya sea en la calle (por los servicios de emergencias), en el punto de atención continuada (PAC) o en los servicios de urgencias hospitalarios (médicos de urgencias hospitalarios). El especialista en medicina familiar y comunitaria que ejerce en todos estos ámbitos debe conocer y dominar la ecografía en este campo25 para mejorar su capacidad diagnóstica y de manejo, lo que redundará en mayor eficacia de sus actuaciones en este arriesgado entorno.
Paciente con compromiso hemodinámicoEn 2013 la American Society of Echocardiography elaboró una guía para la realización de ecocardiografía enfocada que presta soporte a los no cardiólogos para evaluar la presencia de derrame pericárdico, crecimiento ventricular izquierdo o derecho, función cardiaca sistólica global y estado de la volemia intravascular26. Existen estudios que demuestran que la competencia para realizar estas valoraciones se puede adquirir con una curva de aprendizaje muy breve27-30, y que la realización de estudios protocolizados para obtener la información pertinente ocupa menos de 5min31,32.
Los protocolos ecográficos aplicables al paciente con compromiso hemodinámico o shock emplean solo unas pocas y predefinidas ventanas, así como limitados cortes ecográficos, ocupando poco tiempo, proporcionando, junto con la exploración física a la cabecera del paciente, información fiable sobre la presencia o ausencia de signos predecibles que orientan a la etiología y dirigen las actuaciones del clínico, lo que los convierte en muy rentables en condiciones de elevada exigencia para el profesional.
Un buen ejemplo de ellos es el Rapid Ultrasound in Shock (RUSH), que integra la ecocardiografía, el eco doppler venoso de las extremidades y el e-FAST33 y que ha mostrado niveles elevados de sensibilidad, especificidad y valor predictivo en pacientes con shock obstructivo, cardiogénico e hipovolémico, menor sensibilidad en el distributivo, y elevada concordancia entre la impresión inicial ecográfica y el diagnóstico definitivo34. Se basa en la evaluación sistematizada de los componentes de bomba (función sistólica), tanque (presión intravascular) y circuito (estado de los grandes vasos).
Técnica de estudio y utilidad clínica (tabla 5)Usando las sondas sectorial y lineal se evalúa consecutivamente el corazón (Heart), la vena cava inferior (VCI), la cavidad abdominal (espacio de Morrison y el resto de ventanas), la aorta y la presencia o ausencia del neumotórax (Pneumothorax), según la regla nemotécnica «HIMAP», complementada con el estudio del sistema venoso proximal de la extremidad inferior. En cada uno de los pasos del RUSH se pueden identificar los siguientes signos ecográficos:
- 1.
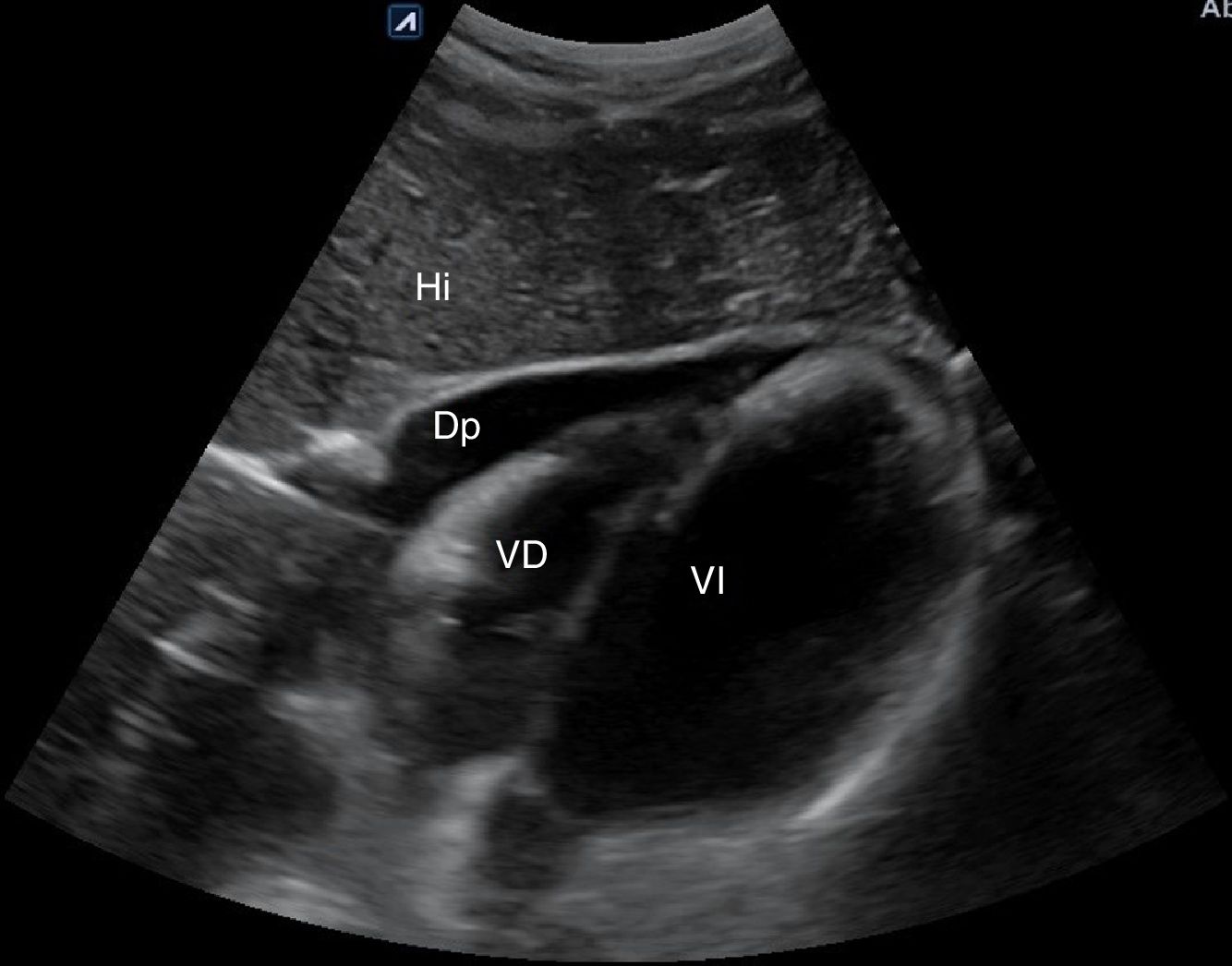
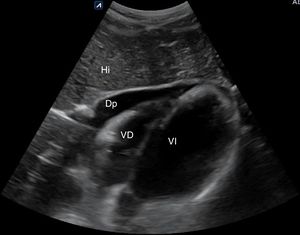
Bomba. El hallazgo de un corazón hipercontráctil, con colapso sistólico del ventrículo izquierdo (VI) y un ventrículo derecho (VD) pequeño, orienta hacia un shock hipovolémico. La disminución de la función sistólica global (acortamiento sistólico del diámetro del VI<30%) y el corazón dilatado hipocontráctil orientan hacia el shock cardiogénico. La presencia de derrame pericárdico (fig. 12) con signos de taponamiento (colapso diastólico de cavidades derechas) o signos de tensión del VD en caso de embolismo pulmonar (tamaño relativo del VD/VI>0,9) (fig. 17) identificarían el shock obstructivo. En el shock distributivo el corazón puede aparecer hipercontráctil (shock caliente) o hipocontráctil (shock frío).
- 2.
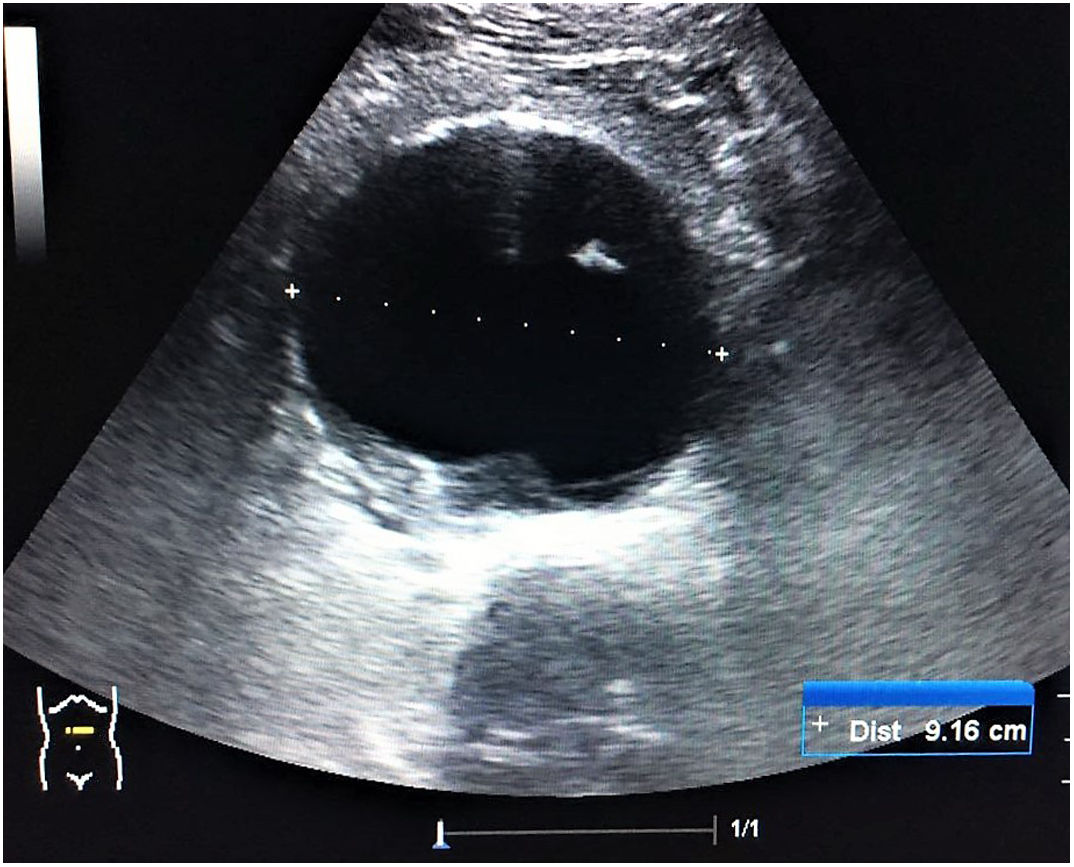
Tanque. Las alteraciones del calibre y la colapsabilidad de la VCI (fig. 18) definen el estado de volemia. Una VCI delgada y colapsable >50% orienta hacia la hipovolemia, lo que puede correlacionarse con la presencia de líquido libre en la cavidad abdominal (hemorragia interna) o líquido en el espacio pleural (hemotórax). Por otra parte, una VCI pletórica no colapsable asociada a múltiples líneas B pulmonares bilaterales e identificación de ascitis o derrame pleural bilateral son propios del shock cardiogénico, mientras que si se acompaña de ausencia de deslizamiento pleural, no líneas B y punto pulmón, es identificativo de neumotórax a tensión. Finalmente, en el shock séptico podemos encontrar una VCI pequeña colapsable y líquido libre en la cavidad abdominal (peritonitis) o neumonía con o sin derrame como origen de la sepsis.
- 3.
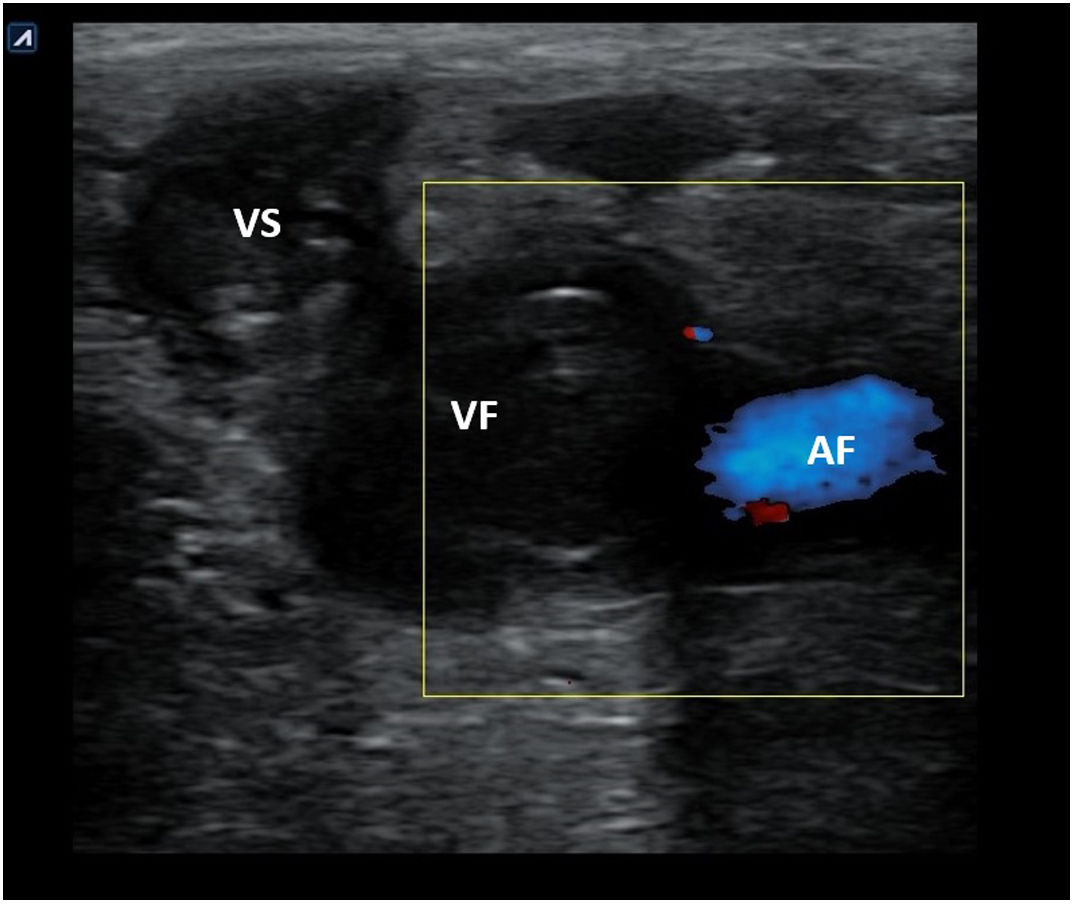
Circuito. La identificación de un aneurisma (fig. 19) o disección de aorta y la presencia de signos de trombosis venosa femoropoplítea (fig. 20) son los 2 objetivos principales de la evaluación vascular en pacientes con shock hipovolémico y obstructivo, respectivamente.
Utilidad del protocolo RUSH. Hallazgos que definen los distintos tipos de shock
| Elemento de valoración y ventanas ecográficas | Shock cardiogénico | Shock hipovolémico | Shock obstructivo | Shock distributivo |
|---|---|---|---|---|
| BombaParaesternal eje largoApical 4 cámarasSubxifoidea | Corazón dilatado hipocontráctil | Corazón hipercontráctilColapso sistólico del VIVD pequeño | Corazón hipercontráctilDerrame pericárdico ± taponamientoDilatación del VD con tensiónTrombos intracardiacos | Corazón hipercontráctil (shock caliente)Corazón hipocontráctil (shock frío) |
| TanqueSubxifoidea de VCIVentanas e-FAST | VCI dilatada no colapsableEdema pulmonar (líneas B)AscitisDerrame pleural bilateral anecoico | VCI pequeñaColapso>50%Vena yugular pequeñaLiquido peritonealLíquido pleural (e-FAST) | VCI dilatada no colapsableNeumotórax (no deslizamiento, no líneas B, punto pulmón) | VCI colapsada, pequeñaNeumonía (causa de sepsis)Líquido libre peritoneal (causa de sepsis) |
| CircuitoSupraesternalEpigástrica/abdominalCribado TVP | Ningún hallazgo | Aneurisma de aorta abdominalDisección aórtica | TVP (VF no compresible, VP no compresible) | Ningún hallazgo |
e-FAST: extended Focused Assessment with Sonography in Trauma; RUSH: Rapid Ultrasound in Shock; TVP: trombosis venosa profunda; VCI: vena cava inferior; VD: ventrículo derecho; VF: vena femoral; VI: ventrículo izquierdo; VP: vena poplítea.
Fuente: adaptada de Perera et al.33.
En la tabla 5 resumimos los hallazgos que definen cada uno de estos patrones ecográficos del RUSH que definen su utilidad en el paciente con inestabilidad hemodinámica.
Parada cardiacaEl uso de la ecografía en la parada cardiaca (PC) se ha mostrado más eficaz que el electrocardiograma para la detección de la actividad cardiaca mecánica, con independencia de la actividad eléctrica, modificando radicalmente su manejo. Además, ofrece pistas sobre las causas potencialmente reversibles de la misma, permite valorar la función cardiaca mejor que la exploración física y predice los resultados de las maniobras de RCP35. Tiene, por tanto, valor diagnóstico y pronóstico.
La condición necesaria para su aplicación es la posibilidad de poder ser realizada simultánea o concomitantemente con las propias maniobras de RCP, durante las pausas evaluativas de la presencia de pulso, sin necesidad de prolongarlas, lo que se ha observado que disminuye la supervivencia.
Se han desarrollado numerosos protocolos a lo largo del tiempo (Focused Echocardiographyc Evaluation in Life suport [FEEL]36, Eco-Guided Life Support [EGLS]37 o Concentrated Overview of Resuscitative Efforts [CORE]38, por citar algunos) que tienen en común la valoración subjetiva de signos ecográficos que resumen de forma rápida (en segundos) y eficaz la función cardiaca e identifican las causas tratables de PC.
Describimos someramente en este artículo el examen Cardiac Arrest Sonographyc Assessment (CASA)39 por su extremada sencillez. Se realiza con sonda sectorial, y se recomienda usar la ventana subxifoidea porque no interfiere con otras maniobras de la RCP. Se realiza en 3 sencillos pasos, coincidiendo con las pausas de RCP para valorar la presencia de pulso:
- •
Paso 1. En la primera pausa durante 10s se evalúa la presencia o ausencia de derrame pericárdico y de signos de taponamiento cardiaco como origen de la PC.
- •
Paso 2. En la segunda pausa se evalúa la presencia o ausencia de signos de sobrecarga aguda a tensión del VD para descartar el embolismo pulmonar como causa de la PC.
- •
Paso 3. En la tercera pausa se evalúa la presencia de actividad cardiaca mecánica, lo que indica el uso de vasopresores y el mantenimiento de las maniobras, o su ausencia, lo que, junto con la determinación de CO2 y el tiempo prolongado o indeterminado de parada por ausencia de testigos, puede aconsejar el cese de la atención médica.
Los autores declaran no tener ningún conflicto de intereses.







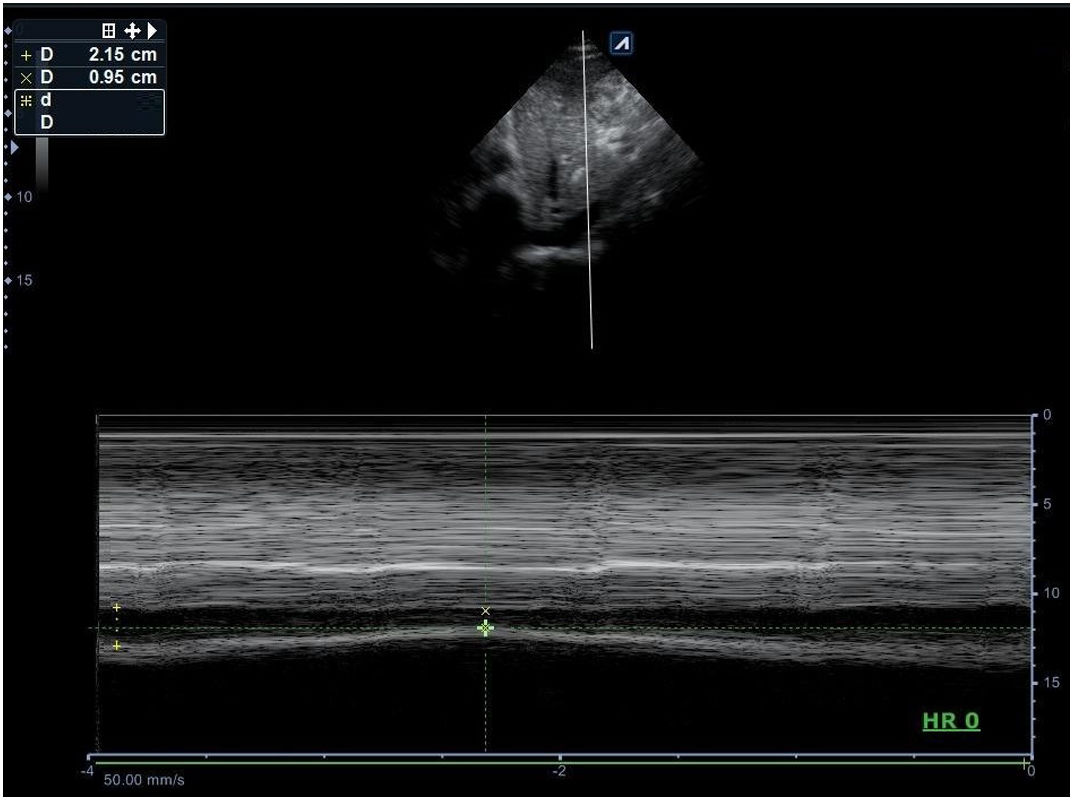


![Imagen en modo M sobre la vena cava inferior en ventana subxifoidea, donde se aprecia un calibre espiratorio de 2,15 cm e inspiratorio de 0,95 cm, que corresponde a una colapsabilidad del 55,8% ([2,15-0,95/2,15]*100). DE: diámetro en espiración; DI: diámetro en inspiración. Imagen en modo M sobre la vena cava inferior en ventana subxifoidea, donde se aprecia un calibre espiratorio de 2,15 cm e inspiratorio de 0,95 cm, que corresponde a una colapsabilidad del 55,8% ([2,15-0,95/2,15]*100). DE: diámetro en espiración; DI: diámetro en inspiración.](https://static.elsevier.es/multimedia/02126567/0000005100000006/v1_201906070610/S0212656719301167/v1_201906070610/es/main.assets/thumbnail/gr18.jpeg?xkr=ue/ImdikoIMrsJoerZ+w96p5LBcBpyJTqfwgorxm+Ow=)