En España, según datos del estudio Di@bet.es, un 13,8% de la población adulta padece diabetes y un 14,8% algún tipo de prediabetes (intolerancia a la glucosa, glucemia basal alterada o ambas). Puesto que la detección precoz de la prediabetes puede facilitar la puesta en marcha de medidas terapéuticas que eviten su progresión a diabetes, consideramos que las estrategias de prevención en las consultas de atención primaria y especializada deberían consensuarse. La detección de diabetes y prediabetes mediante un cuestionario específico (test de FINDRISC) y/o la determinación de la glucemia basal en pacientes de riesgo permiten detectar los pacientes con riesgo de desarrollar la enfermedad y es necesario considerar cómo debe ser su manejo clínico. La intervención sobre los estilos de vida puede reducir la progresión a diabetes o hacer retroceder un estado prediabético a la normalidad y es una intervención coste-efectiva. Algunos fármacos, como la metformina, también se han mostrado eficaces en reducir la progresión a diabetes aunque no son superiores a las intervenciones no farmacológicas. Finalmente, aunque no hay pruebas sólidas que apoyen la eficacia del cribado en términos de morbimortalidad, sí que se ha observado una mejora de los factores de riesgo cardiovascular.
El Grupo de Trabajo de Consensos y Guías Clínicas de la Sociedad Española de Diabetes, ha elaborado unas recomendaciones que han sido consensuadas con la Sociedad Española de Endocrinología y Nutrición, la Sociedad Española de Endocrinología Pediátrica, la Sociedad Española de Farmacia Comunitaria, la Sociedad Española de Medicina Familiar y Comunitaria, la Sociedad Española de Médicos Generales, la Sociedad Española de Médicos de Atención Primaria, la Sociedad Española de Medicina Interna y la Asociación de Enfermería Comunitaria y la Red de Grupos de Estudio de la Diabetes en Atención Primaria.
In Spain, according to the Di@bet.es study, 13.8% of the adult population suffers from diabetes and 14.8% from some form of prediabetes (impaired glucose tolerance, impaired fasting glucose or both). Since early detection of prediabetes can facilitate the implementation of therapeutic measures to prevent its progression to diabetes, we believe that preventive strategies in primary care and specialized clinical settings should be agreed. Screening for diabetes and prediabetes using a specific questionnaire (FINDRISC) and/or the measurement of fasting plasma glucose in high risk patients leads to detecting patients at risk of developing diabetes and it is necessary to consider how they should be managed. The intervention in lifestyle can reduce the progression to diabetes and reverse a prediabetic state to normal and is a cost-effective intervention. Some drugs, such as metformin, have also been shown effective in reducing the progression to diabetes but are not superior to non-pharmacological interventions. Finally, an improvement in some cardiovascular risk factors has been observed although there is no strong evidence supporting the effectiveness of screening in terms of morbility and mortality.
The Consensus and Clinical Guidelines Working Group of the Spanish Diabetes Society has issued some recommendations that have been agreed by the Sociedad Española de Endocrinología y Nutrición, Sociedad Española de Endocrinología Pediátrica, Sociedad Española de Farmacia Comunitaria, Sociedad Española de Medicina Familiar y Comunitaria, Sociedad Española de Médicos Generales, Sociedad Española de Médicos de Atención Primaria, Sociedad Española de Medicina Interna, Asociación de Enfermería Comunitaria and Red de Grupos de Estudio de la Diabetes en Atención Primaria.
El término de «prediabetes», también llamado «hiperglucemia intermedia» o «disglicemia», incluye la presencia de una glucemia basal alterada (GBA), de una intolerancia a la glucosa (ITG) o de ambas condiciones a la vez (GBA+ITG), situaciones todas ellas que implican un riesgo elevado de desarrollar diabetes tipo 2 (DM2) y de sufrir complicaciones cardiovasculares1. La GBA, definida entre los márgenes de 110-125mg/dl, según la Organización Mundial de la Salud –OMS– y de 100-125mg/dl según la American Diabetes Association –ADA–1 es una situación intermedia entre la glucemia basal (GB) normal y la diabetes. La ITG se define como una glucemia plasmática en sangre venosa entre 140mg/dl y 199mg/dl a las dos horas del test de tolerancia oral a la glucosa (TTOG) de 75g. Actualmente no existe una denominación de consenso para la prediabetes en función de la hemoglobina glucosilada (HbA1c): la ADA considera como prediabetes un valor de HbA1c entre 5,7 y 6,4%, mientras que el National Institute for Health and Care Excellence (NICE)2 propone el intervalo de 6 a 6,4%.
La prediabetes se asocia a un mayor riesgo de desarrollar DM2 pero la progresión es evitable. Más de la mitad de los europeos mantiene una situación de GBA o ITG hasta el final de su vida2. El riesgo promedio de desarrollar DM2 aumenta un 0,7% por año en las personas con niveles normales de glucosa, y entre el 5-10% por año, en las que tienen GBA o ITG. Aquellos con GBA e ITG simultáneamente presentan el doble de probabilidades de desarrollar DM2, que quienes tienen solo una de las dos situaciones2. Sin embargo, es posible retroceder de un estado prediabético a la normalidad. Se ha demostrado que durante un período de 3-5 años, alrededor del 25% de los individuos progresan a DM2, el 25% retornan a un estado normal de tolerancia a la glucosa y el 50% permanece en el estado prediabético3.
En España, según datos del estudio Di@bet.es, un 14,8% de la población adulta estudiada padece algún tipo de prediabetes: GBA (110-125mg/dl) 3,4%; ITG 9,2% y ambas 2,2%, después de ajustarlas por edad y sexo4.
El grupo de trabajo ha realizado una revisión narrativa de las guías de práctica clínica y publicaciones relacionadas con la detección de prediabetes y su tratamiento para prevenir la diabetes, con los siguientes criterios de estrategia de búsqueda bibliográfica: prediabetes (MESH) y texto libre; clinical query: diagnóstico y reglas de predicción clínica en las bases MEDLINE (Ovid), Embase (Ovid) y Cochrane (Willey) de 2008 a marzo 2014.
En la tabla 1 se muestra el resumen de las recomendaciones y de los niveles y calidad de la evidencia aplicando el sistema GRADE (Grading of Recommendations, Assesment, Developement and Evaluation) (http://www.gradeworkinggroup.org/). En el Anexo 1 (disponible en la web) se puede ver la clasificación del sistema GRADE.
Resumen de las recomendaciones y de los niveles y calidad de la evidencia aplicando el sistema GRADE (Grading of Recommendations, Assesment, Development and Evaluation)
| Recomendación | Grado/fuerza | Calidadde la evidencia | Observaciones |
|---|---|---|---|
| Se sugiere utilizar como puntos de corte para definir prediabetes: 110mg/dl como glucemia basal plasmática y 6% como HbA1c (según método DCCT/NGSP) | A favor/débil | Baja(1)Baja(2) | (1)Incidencia/prevalencia de retinopatía diabética para Hba1c(2)Incidencia/prevalencia de retinopatía diabética para GB |
| Se sugiere utilizar la estrategia actual de cribado oportunista con GB cada cuatro años en mayores de 45 años, dentro del contexto de detección de otros factores de riesgo cardiovascular | A favor/débil | Baja(1) | (1) Eficacia morbimortalidad cribado vs. no cribado |
| Se sugiere el cribado en dos etapas mediante el test de FINDRISC cada 4 años a partir de los 40 años y la GB cuando la puntuación obtenida sea mayor o igual a 15 | A favor/débil | Baja(1)Moderada(2)Moderada(3) | (1)Eficacia morbimortalidad cribado vs. no cribado(2) Validez de FINDRISC para cribado(3) Cribado mediante FINDRISC para retrasar/disminuir incidencia de DM2 |
| Se recomienda la modificación de estilos de vida (dieta y/o ejercicio) a las personas con prediabetes | A favor/fuerte | Moderada(1)Moderada(2)Alta(3) | (1)Dieta vs. nada(2)Ejercicio vs. nada(3)Dieta+ ejercicio vs. varios |
| Se sugiere no prescribir fármacos de forma rutinaria en las personas con prediabetes | A favor/débil | Baja(1) | (1)Fármacos vs. placebo |
| Se sugiere utilizar metformina en personas con prediabetes, que han fracasado con dieta y ejercicio y que presentan obesidad grado 2 (IMC ≥ 35kg/m2) o historia de diabetes gestacional y edad menor de 60 años | A favor/débil | Moderada(1) | (1)Metformina vs. placeboLa metformina no tiene indicación en prediabetesLos fármacos tienen efectos adversos. La prevención primaria con fármacos promueve la medicalización |
FINDRISC: Finnish Diabetes Risk Score; GB: glucemia basal.
Existen varias estrategias para el cribado de la diabetes3 que permiten detectar situaciones de prediabetes:
- a)
El «cribado oportunista», mediante la realización de glucemia sobre poblaciones que presentan un mayor riesgo de padecer prediabetes o DM2 (por ejemplo a partir de una edad o de un índice de masa corporal [IMC]). Esta estrategia permite conocer una situación de prediabetes prevalente, así como una diabetes no diagnosticada.
- b)
La utilización de «reglas de predicción clínica» para la detección de personas con riesgo de DM2 y prediabetes, a través de registros de bases de datos o historia clínica informatizada (alertas).
- c)
El uso de «escalas de riesgo o cuestionarios» para la detección de prediabetes y DM2 como sistemas de detección primaria para identificar subgrupos de la población en los que, en una segunda etapa, la prueba de glucemia puede ser realizada de manera más eficiente.
Hasta ahora, la supuesta eficacia del cribado se ha basado en modelos matemáticos que estimaban la disminución de mortalidad y de complicaciones relacionada con la DM25. Sin embargo, la mejor evidencia la proporcionan los ensayos clínicos aleatorizados (ECA), en los que se evalúa el cribado como intervención y las variables de resultado son la disminución de la morbimortalidad atribuida a la condición que se quiere cribar. Recientemente se han publicado 2 estudios de cohortes6,7 y un ECA8 que evalúan la eficacia del cribado y en los que no se han mostrado reducciones significativas en la morbimortalidad. Además, la evidencia disponible no permite confirmar ni descartar posibles efectos perjudiciales del cribado9,10.
En nuestro medio la estrategia de cribado habitual (oportunista, con determinación de la GB en función de la edad y de otros factores de riesgo) no ha sido evaluada mediante ECA. Un estudio observacional11 sobre los indicadores de calidad asistencial en las personas con DM2 en atención primaria entre 1996 y 2007, con datos de 335 centros de salud, de los que se eligieron aleatoriamente las historias de 33.506 pacientes, muestra que el control de los factores de riesgo cardiovascular ha mejorado mucho, incluyendo la media de hemoglobina glucosilada (HbA1c); asimismo, se ha reducido de forma significativa la prevalencia de complicaciones, sobre todo microvasculares pero también macrovasculares. Estos datos, junto con la existencia de intervenciones efectivas tanto en prediabetes como en DM2, pueden constituir una evidencia indirecta que justifique la necesidad de seguir haciendo el cribado oportunístico, especialmente en personas con factores de riesgo.
En conclusión, no hay pruebas sólidas que apoyen la eficacia del cribado de DM2 en términos de morbimortalidad, al menos en poblaciones con bajo riesgo de desarrollar DM28,12, pero no puede descartarse su eficacia en poblaciones de mayor riesgo o con diferentes prevalencias de DM2, por lo que en un reciente documento del National Screening Committee Norteamericano se recomienda mantener el cribado oportunístico dentro del contexto de la valoración del riesgo cardiovascular12.
Validez de reglas de predicción clínica (RPC) y test de FINDRISCCon el fin de mejorar la identificación de individuos con riesgo de padecer diabetes sin necesidad de someterlos sistemáticamente a pruebas de laboratorio (TTOG, HbA1c o GB), se han publicado multitud de estudios de validación de RPC. Hemos encontrado varias revisiones sistemáticas de diferentes RPC y de distintas estrategias de cribado, algunas de ellas en 2 etapas. Resulta imposible hacer una valoración comparativa entre ellas y dar un estimador común, por su variabilidad en numerosos aspectos13-15. Todas coinciden en afirmar que las RPC han de validarse en el contexto en que se vayan a aplicar, pero parece que la balanza se inclina a considerar el test de FINDRISC (Finnish Diabetes Risk Score) (Anexo 2, disponible en la web) como el de mejor rendimiento diagnóstico. El cuestionario FINDRISC, basado en los resultados en la incidencia de DM2 durante el seguimiento prospectivo de una cohorte de base poblacional durante 10 años fue desarrollado para identificar los sujetos con alto riesgo de desarrollar diabetes en el futuro. Se trata de un test de 8 ítems que puede ser autoadministrado y que permite detectar sujetos de alto riesgo en la población general y en la práctica clínica habitual con el fin de posteriormente identificar DM2 no detectada, intolerancia a la glucosa y síndrome metabólico. Se trata de una alternativa al TTOG que se considera un procedimiento de cribado invasivo, costoso y que consume mucho tiempo1,12,15.
En los estudios de validación del FINDRISC realizados en España existe cierta controversia acerca de cuál es el mejor punto de corte16,17. El punto de corte con mayor sensibilidad y especificidad del FINDRISC en el estudio Pizarra fue de 9 puntos, con un valor predictivo positivo de 22,2% y un valor predictivo negativo del 95,1%16. En cambio, en el ensayo clínico DE-PLAN de prevención de la diabetes, el punto de corte de riego elevado utilizado fue de 1517,18 que es el recomendado por las guías europeas3 a propuesta de los autores del test15 y por tanto el recomendado en este documento. En el estudio DE-PLAN el área bajo la curva ROC determinó el valor igual o superior a 14 como el mejor para detectar diabetes con una sensibilidad del 75,9% y una especificidad del 52,3% y para la prediabetes del 65,8 y 56,7%, respectivamente. El valor predictivo negativo para diabetes fue del 95,5 y del 78,4% para la prediabetes17.
Una gran limitación para el uso del FINDRISC es que el paciente no sabe calcular su propio IMC y que la medición del perímetro de cintura no se realiza habitualmente en nuestro medio. En nuestro medio el cribado de la diabetes se realiza habitualmente mediante la determinación de la GB en el contexto de la detección o seguimiento de otros factores de riesgo cardiovascular.
Recomendaciones de cribadoEl NICE2 recomienda realizar el cálculo de riesgo mediante el test de FINDRISC al menos cada 3-5 años en personas a partir de los 40 años, y también entre los 25-39 años, en caso de presencia de factores de riesgo de DM2 o raza china o negra. El Canadian Task Force on Preventive Health Care5 recomienda también cribado mediante una RPC validada como el FINDRISC cada 3-5 años, con una frecuencia anual en personas con alto riesgo de DM2 y recomienda la utilización de HbA1c como prueba diagnóstica tras el FINDRISC. En cambio la ADA, recomienda la GB cada cuatro años en pacientes mayores de 45 años y anual en los que tengan alguna glucemia previa alterada o riesgo elevado de diabetes1.
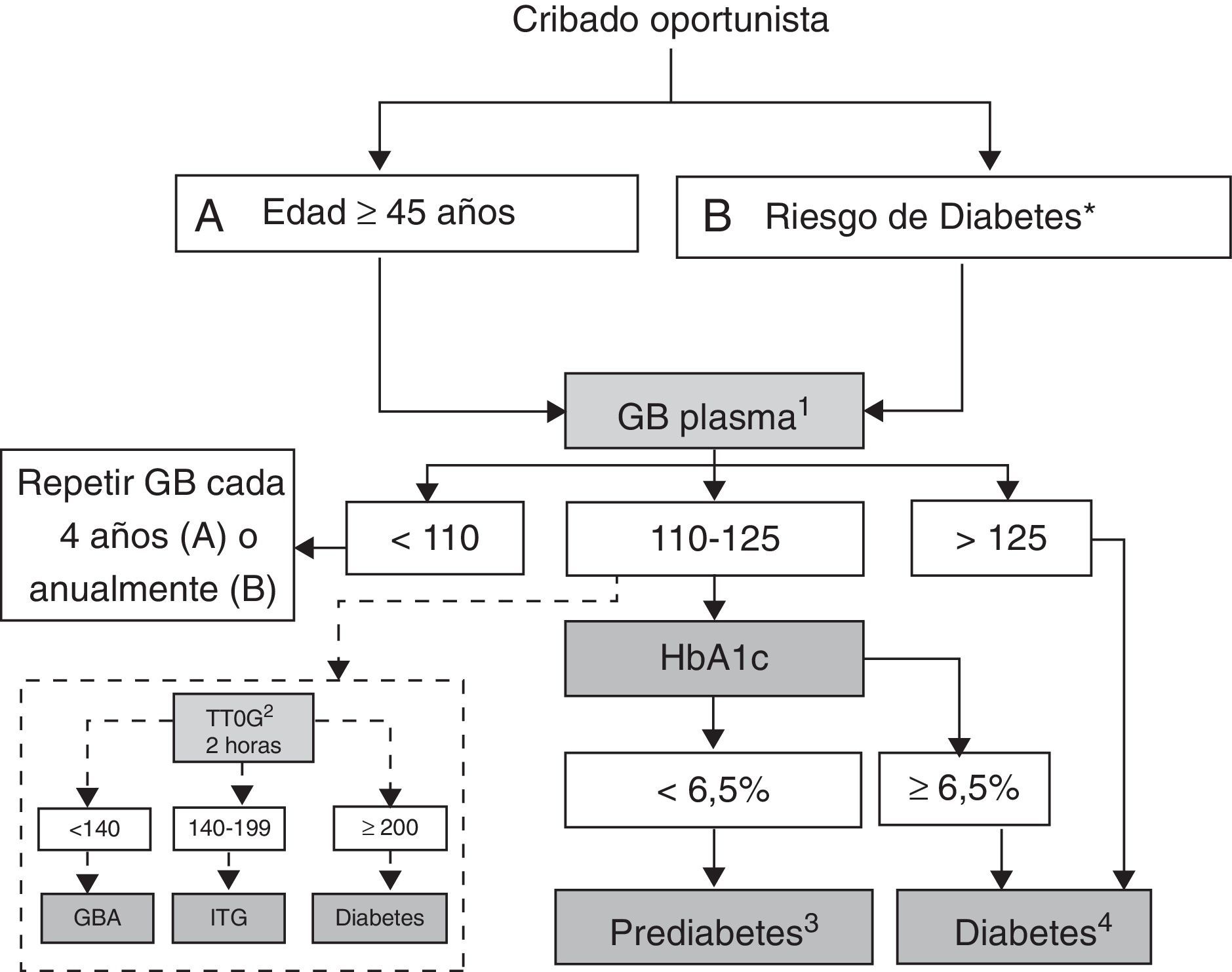
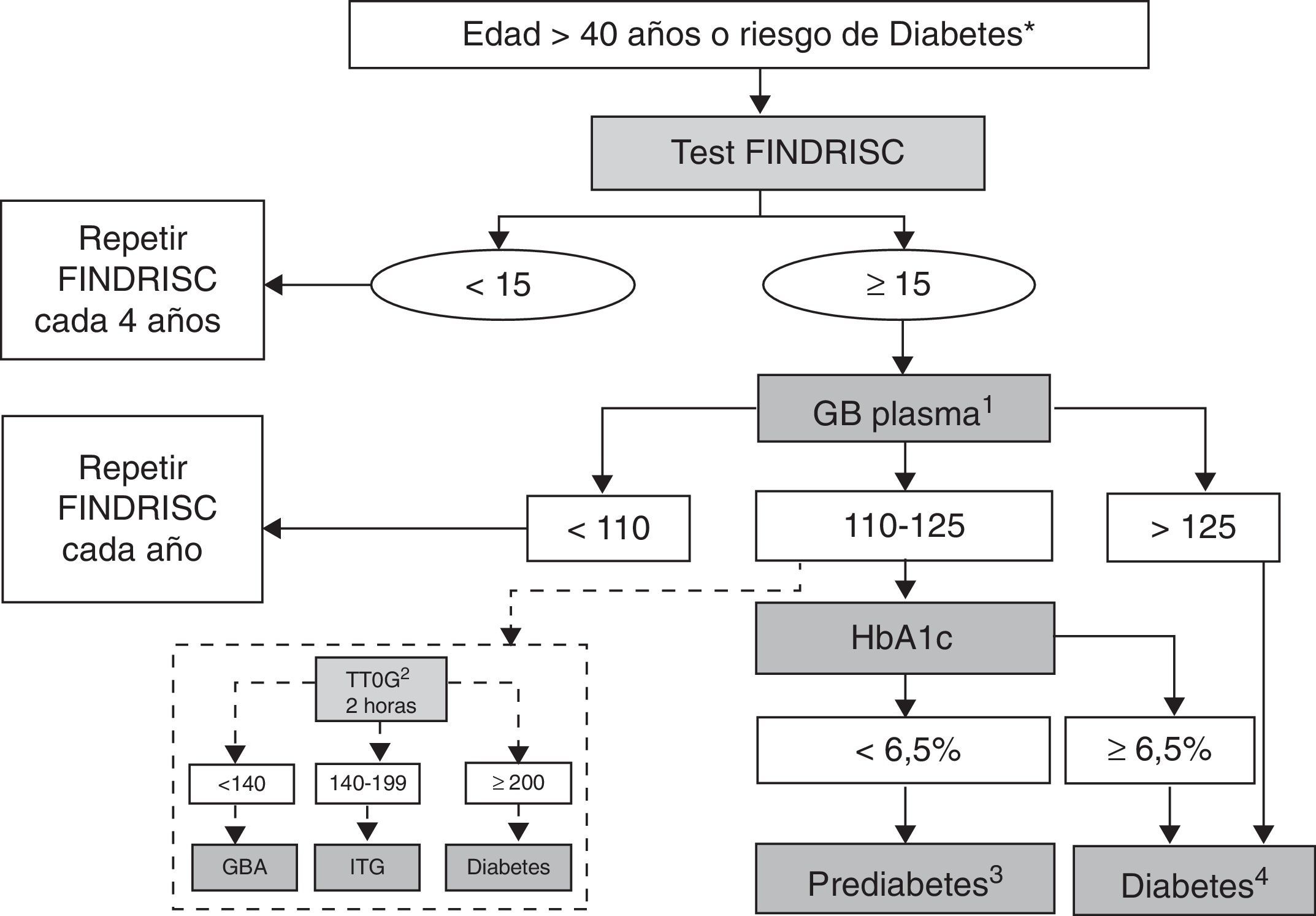
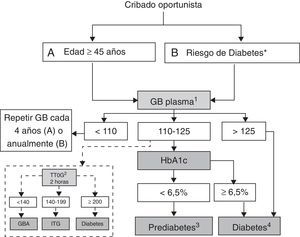
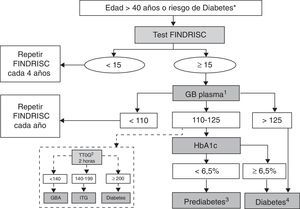
Tras sopesar las ventajas e inconvenientes de ambas opciones (tabla 2), el grupo de trabajo recomienda una periodicidad de cribado de DM2 cada 4 años en personas a partir de 40-45 años y una frecuencia anual en personas con alto riesgo de padecer DM2. Hasta que se disponga de los resultados de nuevos estudios que aporten evidencia de mayor calidad, se sugiere utilizar la estrategia actual de cribado oportunista con GB cada cuatro años en mayores de 45 años, dentro del contexto de detección de otros factores de riesgo cardiovascular (fig. 1) o bien el cribado en dos etapas mediante el test de FINDRISC cada 4 años a partir de los 40 años y la GB cuando la puntuación obtenida sea mayor o igual a 15 (fig. 2), en función de las características de los servicios asistenciales o el lugar en que se realiza el cribado. En el Anexo 2 se muestra el test de FINDRISC tal como aparece en la página web de la revista Diabetes, de la Sociedad Española de Diabetes (www.revistadiabetes.org/test.asp), lo que permite que la población general pueda acceder al test tanto a través de diferentes páginas web como de otros servicios, como por ejemplo en las farmacias comunitarias, y si este es positivo, recomendar al paciente que contacte con los servicios sanitarios.
Estrategias de cribado de prediabetes y diabetes
| Cribado oportunista actual dentro del contexto de cribado de otros factores de riesgo cardiovascular: |
| •Cribado de prediabetes y DM2 cada 4 años, mediante GB, a partir de los 45 años |
| •Cribado de DM2 anual mediante GB en personas de riesgo, definidas por antecedentes familiares de primer grado, hipertensión, hiperlipemia, obesidad, esteatosis hepática no alcohólica, tratamientos con fármacos hiperglucemiantes (antipsicóticos, corticoides, etc.), diabetes gestacional o patología obstétrica previas, GBA o ITG, hiperandrogenismo funcional ovárico o etnias de riesgo |
| •Si existe GB 110-125mg/dl, realizar una HbA1c (o TTOG) |
| •Si existe diabetes: tratamiento de DM2 y seguimiento clínico |
| Cribado en dos etapas mediante el test FINDRISC cada 4 años a partir de los 40 años, y entre los 25-39 años si existen factores de riesgo de DM2, y realizando la GB en segundo término |
| •< 15 puntos: repetir FINDRISC a los 4 años |
| •≥ 15 puntos: realizar GB: |
| a) Si no hay DM2 ni prediabetes: FINDRISC cada año y si es ≥ 15 realizar GB |
| b) Si hay prediabetes: HbA1c (o TTOG) y control anual con GB y HbA1c |
| c) Si existe diabetes: tratamiento de DM2 y seguimiento clínico |
GB: glucemia basal (mg/dl); GBA: glucemia basal alterada; ITG: intolerancia oral a la Glucosa; TTOG: test de tolerancia oral a la glucosa.
Algoritmo de detección de prediabetes y diabetes. Cribado basado en la glucemia basal (I). GB: glucemia basal (mg/dl); GBA: glucemia basal alterada; ITG: intolerancia oral a la glucosa; TTOG: test de tolerancia oral a la glucosa (mg/dl). 1. Repetir cada cuatro años si edad ≥ 45 años y GB <110 mg/dl y anualmente si riesgo de diabetes. 2. Considerar el TTOG especialmente en pacientes que han sufrido recientemente un evento coronario agudo. 3. Repetir GB y HbA1c cada año si prediabetes. 4. Confirmar en dos ocasiones. * Riesgo de diabetes: antecedente de hiperglucemia previa o factores de riesgo elevado para desarrollar diabetes (ver tabla 2).
Algoritmo de detección de prediabetes y diabetes. Cribado en dos etapas (II). GB: glucemia basal (mg/dl); GBA: glucemia basal alterada; ITG: intolerancia oral a la glucosa; TTOG: test de tolerancia oral a la glucosa (mg/dl). 1. Repetir GB cada año si prediabetes o FINDRISC ≥ 15 puntos. 2. Considerar el TTOG especialmente en pacientes que han sufrido recientemente un evento coronario agudo. 3. Repetir GB y HbA1c cada año si prediabetes. 4. Confirmar en dos ocasiones. *Riesgo de diabetes: antecedente de hiperglucemia previa o factores de riesgo elevado para desarrollar diabetes (ver tabla 2).
La hiperglucemia puede evaluarse mediante la glucemia basal (en ayunas), la glucemia a las dos horas de un TTOG con 75g de glucosa y/o mediante determinación de HbA1c. Cada prueba tiene sus ventajas y sus desventajas en términos de conveniencia, coste y reproducibilidad. La HbA1c fue incluida por la ADA1 en el 2009 para el diagnóstico de diabetes y prediabetes y ha mostrado algunas ventajas: no precisa de ayuno previo, tiene una mayor estabilidad preanalítica y ausencia de alteraciones día a día en periodos de enfermedad o estrés. La HbA1c además, es mejor predictor de eventos cardiovasculares que la glucemia basal19. Entre las desventajas se encuentran su coste, el difícil acceso a la prueba en determinadas áreas del mundo y la correlación inadecuada con la glucemia media en algunos individuos que presentan alteraciones en la vida media eritrocitaria o más discutido, en algunas etnias. Algunos autores recomiendan la realización del TTOG en sujetos con GBA porque un tercio de dichos individuos serán diagnosticados de diabetes18,20 y porque la glucemia posprandial determinada por TTOG se ha correlacionado también con la enfermedad cardiovascular21. Sin embargo su coste elevado, el tiempo consumido por profesionales y pacientes y su gran variabilidad, la han relegado en la práctica clínica habitual y ha sido desplazada por la GB y la HbA1c1,12. Finalmente, debemos señalar que la GBA, la ITG y la HbA1c identifican poblaciones diferentes18,20,21. También en pacientes tras un evento coronario agudo el TTOG permite detectar un mayor número de pacientes con diabetes que la GB o la HbA1c22, por lo que cuando los valores de GB y HbA1c no son concluyentes o normales sería recomendable realizar el TTOG en este grupo de pacientes23.
Los criterios diagnósticos de diabetes y prediabetes se muestran en la tabla 3. A pesar de que la ADA recomienda valores de HbA1c 5,7% y GB 100mg/dl1 para el diagnóstico de prediabetes, el grupo de trabajo ha optado por los valores de GB de 110mg/dl (criterio de la OMS 2006)24 y de HbA1c del 6% (límite superior de la normalidad según el método DCCT/NGSP) tal como propone el NICE2. La OMS en su informe de 2011 no ha aceptado un valor de diagnóstico de HbA1c para la prediabetes por no haber suficientes evidencias para recomendar uno u otro punto de corte25. Al igual que la OMS en su informe de 200624 un grupo de trabajo de la EASD26, también recomendó mantener el valor de 110mg/dl como límite superior de la normalidad.
Criterios diagnósticos de diabetes y prediabetes
| Diabetes tipo 2 |
| • HbA1c ≥ 6,5% |
| • Glucemia basal en ayunas ≥ 126mg/dl |
| • Glucemia a las 2 horas del TTOG ≥ 200mg/dl |
| Dos determinaciones en días distintos con cualquiera de los 3 criterios anteriores permiten establecer el diagnóstico |
| • Glucemia en plasma venoso al azar ≥ 200mg/dl con síntomas típicos |
| Prediabetes |
| • HbA1c 6-6,4%* |
| • Glucemia basal en ayunas 110- 125mg/dl** |
| • Glucemia a las 2 horas del TTOG 140-199mg/dl |
TTOG: test de tolerancia oral a la glucosa.
Los mismos factores de riesgo asociados a la diabetes están asociados a la prediabetes, la obesidad (especialmente visceral o abdominal), la dislipemia con triglicéridos elevados y/o colesterol-HDL reducido y la hipertensión arterial. Debemos controlar:
- -
Peso: debe determinarse en cada visita y calcular el IMC. También se recomienda medir el perímetro de la cintura, pues la obesidad central es un predictor de riesgo cardiovascular elevado y de riesgo de diabetes. En general se considera un valor de riesgo elevado 102cm en los varones y 88cm en las mujeres, excepto en personas de origen asiático que se reduce a 90 y 80cm, respectivamente (criterios de obesidad central del ATP-III, 2005). En nuestro país estos criterios han sido asumidos por la Estrategia NAOS (estrategia para la nutrición, actividad física y prevención de la obesidad, http://www.naos.aesan.msssi.gob.es/naos/estrategia/que_es/), que establece dos niveles de riesgo:
- -
Riesgo aumentado: hombres:>95cm y mujeres:>82cm.
- -
Riesgo muy aumentado: hombres:>102cm y mujeres:>88cm.
Además de la intervención dietética individualizada, en pacientes con un IMC>35kg/m2 debe considerarse la posibilidad de la cirugía bariátrica. La prescripción de fármacos antiobesidad como Orlistat, puede ser una ayuda para algunos pacientes, aunque su eficacia es limitada a largo plazo.
- -
Presión arterial: las recomendaciones no difieren de las de los pacientes con diabetes, con un objetivo de presión arterial<140/90mm Hg según el JNC 826, aunque las sociedades europeas de cardiología y diabetes mantienen el corte en 140/8523 y la ADA en 140/80mmHg27.
- -
Dislipemia: se recomienda un perfil lipídico anual. Las sociedades científicas proponen la utilización del colesterol LDL como objetivo principal para el tratamiento de la dislipemia, quedando el colesterol no-HDL como objetivo secundario y el límite dependerá de si se trata de prevención primaria o secundaria, sin que haya ninguna indicación específica para los pacientes con prediabetes, por lo que hemos asumido los criterios aplicados a los pacientes con DM2. Así, la ADA1 y las sociedades europeas de cardiología y diabetes23 proponen para la DM2 un objetivo general de colesterol LDL<100mg/dl y, opcionalmente, <70mg/dl en pacientes con enfermedad cardiovascular o bien una reducción del LDL del 30-40% (ADA)27 o incluso superior al 50%23 respecto del valor inicial si no se consigue el objetivo mencionado con el tratamiento con estatinas. Aunque las estatinas se han asociado a un aumento del riesgo de diabetes en población no diabética, los beneficios del tratamiento superan con creces este inconveniente en pacientes de riesgo cardiovascular elevado23,27.
Tabaquismo: debe registrarse en la historia clínica de todos los pacientes y ofrecer al paciente un programa activo para dejar de fumar.
- -
Riesgo cardiovascular: se recomienda realizar el cálculo de riesgo de enfermedad cardiovascular a los 10 años. En nuestro medio se utilizan las escalas de Framingham, Regicor (Framingham calibrada en la provincia de Girona) y SCORE calibrada para España. Estas últimas son las recomendadas por la SEH-LELHA y la Sociedad Europea de Hipertensión, mientras que las Regicor son las utilizadas por la historia informatizada en Cataluña y otras comunidades autónomas.
Hábitos nutricionales: debe incluir la ingesta calórica total diaria y la frecuencia de consumo de los distintos grupos de alimentos28.
- -
Actividad física: debe recogerse el nivel de actividad física en todos los individuos con prediabetes, utilizando cuestionarios sencillos o mediante podómetros.
El objetivo general es intentar revertir la condición de prediabetes y evitar que evolucione a diabetes. Los objetivos específicos son:
- •
Conseguir una reducción de un 5-10% de peso.
- •
Que el sujeto realice una actividad física de moderada intensidad (30min/día), al menos 5 días a la semana.
- •
Tener una glucemia basal<110mg/dl.
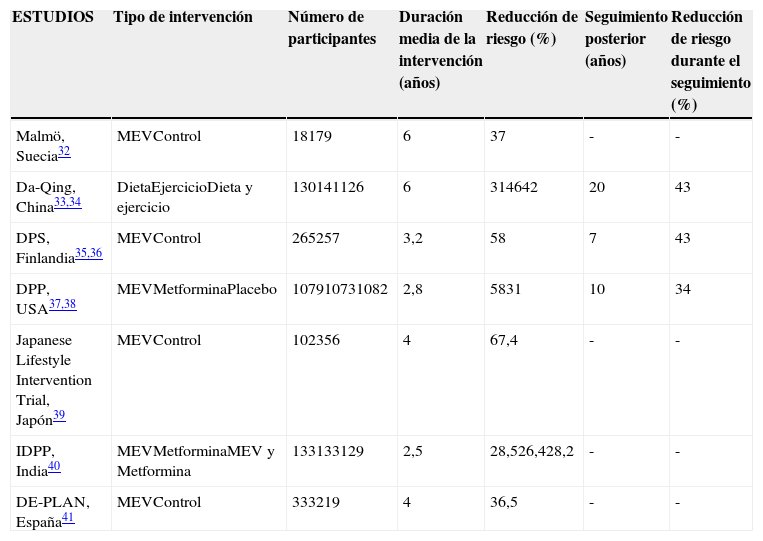
La pérdida de peso y el ejercicio mejoran la sensibilidad a la insulina y la tolerancia a la glucosa en sujetos diabéticos y no diabéticos29-31. Varios estudios prospectivos importantes32-42 y revisiones sistemáticas43-45 concluyen que la conversión de ITG a DM2 puede retrasarse o evitarse mediante un régimen de tratamiento basado en la dieta y el ejercicio32-42, obteniéndose reducciones del riesgo de diabetes que van desde el 28% en el «Indian Study»40 hasta el 67% en el «Japanese study»39. En la tabla 4 se detallan los resultados de ensayos clínicos en los que se evalúa la eficacia de la modificación de los estilos de vida en personas con prediabetes.
Ensayos clínicos aleatorizados sobre modificación de estilos de vida en pacientes con prediabetes
| ESTUDIOS | Tipo de intervención | Número de participantes | Duración media de la intervención (años) | Reducción de riesgo (%) | Seguimiento posterior (años) | Reducción de riesgo durante el seguimiento (%) |
|---|---|---|---|---|---|---|
| Malmö, Suecia32 | MEVControl | 18179 | 6 | 37 | - | - |
| Da-Qing, China33,34 | DietaEjercicioDieta y ejercicio | 130141126 | 6 | 314642 | 20 | 43 |
| DPS, Finlandia35,36 | MEVControl | 265257 | 3,2 | 58 | 7 | 43 |
| DPP, USA37,38 | MEVMetforminaPlacebo | 107910731082 | 2,8 | 5831 | 10 | 34 |
| Japanese Lifestyle Intervention Trial, Japón39 | MEVControl | 102356 | 4 | 67,4 | - | - |
| IDPP, India40 | MEVMetforminaMEV y Metformina | 133133129 | 2,5 | 28,526,428,2 | - | - |
| DE-PLAN, España41 | MEVControl | 333219 | 4 | 36,5 | - | - |
MEV: Modificación del estilo de vida basada en dieta y ejercicio; DPS: Diabetes Prevention Study; DPP: Diabetes Prevention Program; IDPP: Indian Diabetes Prevention Program; DE-PLAN: Diabetes in Europe-Prevention using Lifestyle, Physical Activity and nutritional intervention.
Tomado de Umpierrez GE y Pasquel FJ31
La pérdida de peso es el factor determinante en la prevención de la diabetes30, aunque en el estudio PREDIMED42 se concluye que la dieta mediterránea reduce la aparición de DM2 hasta un 40%, sin necesidad de reducción de peso (efecto cualitativo de la dieta).
Un metaanálisis publicado recientemente45 incluyó un total de 22 estudios con desenlaces evaluados al menos tras 12 meses de una intervención clasificada como prevención primaria no farmacológica y dio como resultado una pérdida de 2,71 kg de peso (IC:95% - 4,22 a 1,19) en el grupo de intervención respecto al grupo control. Traducido en términos de prevención, según los resultados del estudio DPP46, cada Kg de peso reducido se traslada a una reducción de un 16% en la incidencia de diabetes.
Una descripción pormenorizada de las intervenciones realizadas y las publicaciones resultantes está disponible en las páginas web oficiales de los estudios DPP http://diabetes.niddk.nih.gov/dm/pubs/preventionprogram/ y PREDIMED http://www.predimed.es/.
En cuanto a los costes económicos, las intervenciones sobre los estilos de vida (dieta y ejercicio) se han mostrado clínicamente efectivas y coste-efectivas en frenar la progresión a diabetes, tal como se determinó en la evaluación económica del Health Technology Assessment Programme británico43. Más recientemente, se ha publicado el análisis de coste-efectividad del estudio DE-PLAN-CAT_PREDICE en Cataluña que también lo corrobora41. En este estudio, con una reducción de la incidencia de diabetes del 36,5% la intervención intensiva fue coste-efectiva, siendo el incremento del coste por participante frente a la intervención estándar de 106 € en la intervención individual y de solo 10 € en la intervención grupal41. Finalmente, la intervención intensiva comportó un sobrecoste de 3.243 € por año de vida ganado ajustado por calidad41.
En relación a la reducción de complicaciones crónicas de la diabetes, en el estudio Da Qing, en población china, la intervención dietética durante 6 años en pacientes con ITG, y seguidos durante 20 años una vez finalizado el ensayo clínico, supuso una reducción del 47% de la retinopatía diabética47, del 29% en la mortalidad cardiovascular y del 41% en la mortalidad por todas las causas48. Se trata del primer estudio que ha reportado beneficios en términos de eventos mayores y, aunque al tratarse de población china sus resultados pueden ser difíciles de extrapolar a otras poblaciones, refuerzan la necesidad de promover los cambios de estilo de vida en los pacientes con prediabetes.
Modificación de los estilos de vidaLos bajos índices de cumplimiento terapéutico impulsan a plantear abordajes distintos, en los que se intenta transferir gradualmente la responsabilidad del cuidado de la diabetes a la persona afectada. Este proceso recibe el nombre de empoderamiento (empowerment) y básicamente consiste en darle la información y las habilidades necesarias al sujeto afecto para que se convierta en su propio gestor, involucrándole plenamente en el proceso terapéutico.
La educación terapéutica continuada y sistemática49,50 tiene por objetivo formar a los pacientes mediante programas educativos adecuados en la autogestión, en la adaptación del tratamiento a su propia enfermedad y a permitirle realizar su vida cotidiana. Asimismo, contribuye a reducir los costes de la atención sanitaria de larga duración para los pacientes y la sociedad.
Reducción de peso en personas con sobrepeso u obesidadPara perder peso son necesarias dietas con restricción calórica, ya sean bajas en hidratos de carbono, bajas en grasas con restricción de hidratos de carbono o la dieta mediterránea1,29,42. Esta última es más equilibrada, aporta ácidos grasos omega-3 y fibra y tiene numerosos beneficios metabólicos29.
La pérdida de peso efectiva y duradera es aquella que se produce lentamente y de forma progresiva. Es la que permite disminuir el porcentaje de grasa corporal, manteniendo la masa muscular y debe adaptarse al tipo de vida del individuo. Tras la consecución del peso adecuado es necesario su mantenimiento mediante un adecuado equilibrio ingesta/ejercicio, que constituye con toda seguridad la mayor dificultad. Es fundamental conseguir cambios en la conducta alimentaria y en la práctica de ejercicio y reforzarlos periódicamente49.
AlimentaciónLa recomendación general es realizar una alimentación equilibrada y cardiosaludable que aporte todos los nutrientes y la energía necesaria para evitar carencias. La dieta mediterránea es un buen modelo a seguir. La principal característica de la alimentación en el paciente con prediabetes es el control de la cantidad de hidratos de carbono de absorción rápida (azúcar, dulces, zumos, etc.) y la limitación de las grasas saturadas (carnes rojas, embutidos, bollería, etc.). Se debe estimular el consumo de frutas, vegetales, legumbres, cereales integrales y lácteos desnatados. El aceite de oliva, preferiblemente virgen extra, debería ser la principal fuente de grasa por su calidad nutricional, pero también son recomendables los frutos secos o las aceitunas.
Ejercicio físicoSe debe hacer una prescripción individualizada de ejercicio estableciendo las características generales del ejercicio aeróbico:a. Nivel de intensidad: debe estar entre el 60-75% de lo que se denomina el nivel de reserva cardiaca. Para calcular este nivel el Colegio Americano de Medicina del Deporte (American College of Sports Medicine)51 recomienda utilizar la fórmula de Karvonen. Esta fórmula tiene en cuenta el ritmo cardiaco en reposo, lo que permite ajustar la intensidad conforme mejora la forma física de la persona.
Así para un ejercicio a una intensidad del 60% sería: REE=RR+0,6 (FCmax - RR). Siendo REE: ritmo estimado en esfuerzo; FCmax: frecuencia cardiaca máxima (220-edad); RR: ritmo en reposo.
Otra forma más simple pero menos exacta para calcular la intensidad del ejercicio es usar el «Talking test». En este caso se trata de hacer ejercicio con una intensidad suficiente como para que la persona tenga dificultad para mantener una conversación.b. Frecuencia y progresión: el ejercicio debe realizarse de forma continuada.c. Duración: se recomienda un mínimo de 30 minutos al día de ejercicio aeróbico moderado, realizado al menos 5 días a la semana27,52 o bien, 90 minutos a la semana de ejercicio de alta intensidad52. También puede realizarse una combinación de ejercicio aeróbico y ejercicio de resistencia.
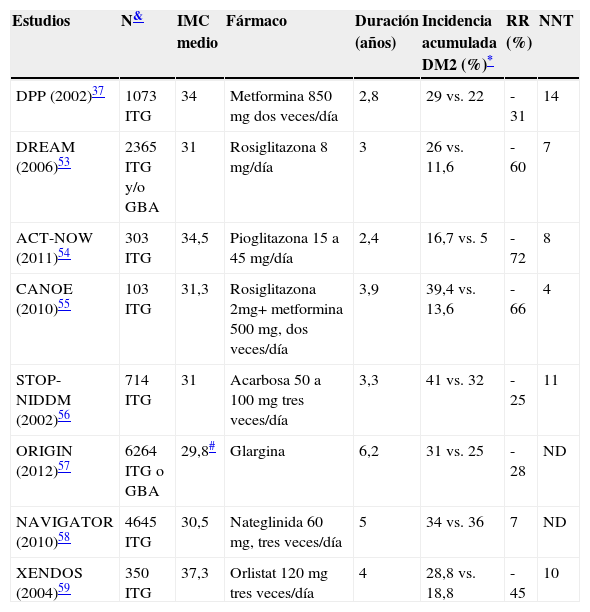
Tratamiento farmacológicoEn la tabla 5 se detallan los resultados de estudios en los que se evalúa la eficacia de medicamentos en el tratamiento de la prediabetes53-59. Actualmente en Europa, ningún fármaco incluye en su ficha técnica la indicación de prevención de la diabetes, a pesar de que en las recomendaciones de la ADA se justifica el uso de metformina en pacientes con prediabetes de riesgo muy elevado: obesidad grave (IMC ≥ 35kg/m2), historia de diabetes gestacional y edad menor de 60 años27. Para otros fármacos, la ADA considera que hasta la fecha no hay argumentos suficientes para recomendar su uso en pacientes con prediabetes, debido a sus costes, sus efectos secundarios o su efecto no persistente27.
Ensayos clínicos aleatorizados con fármacos en pacientes con prediabetes
| Estudios | N& | IMC medio | Fármaco | Duración (años) | Incidencia acumulada DM2 (%)* | RR (%) | NNT |
|---|---|---|---|---|---|---|---|
| DPP (2002)37 | 1073 ITG | 34 | Metformina 850mg dos veces/día | 2,8 | 29 vs. 22 | -31 | 14 |
| DREAM (2006)53 | 2365 ITG y/o GBA | 31 | Rosiglitazona 8mg/día | 3 | 26 vs. 11,6 | -60 | 7 |
| ACT-NOW (2011)54 | 303 ITG | 34,5 | Pioglitazona 15 a 45mg/día | 2,4 | 16,7 vs. 5 | -72 | 8 |
| CANOE (2010)55 | 103 ITG | 31,3 | Rosiglitazona 2mg+ metformina 500mg, dos veces/día | 3,9 | 39,4 vs. 13,6 | -66 | 4 |
| STOP-NIDDM (2002)56 | 714 ITG | 31 | Acarbosa 50 a 100mg tres veces/día | 3,3 | 41 vs. 32 | -25 | 11 |
| ORIGIN (2012)57 | 6264 ITG o GBA | 29,8# | Glargina | 6,2 | 31 vs. 25 | -28 | ND |
| NAVIGATOR (2010)58 | 4645 ITG | 30,5 | Nateglinida 60mg, tres veces/día | 5 | 34 vs. 36 | 7 | ND |
| XENDOS (2004)59 | 350 ITG | 37,3 | Orlistat 120mg tres veces/día | 4 | 28,8 vs. 18,8 | -45 | 10 |
ACT-NOW: Actos Now for the prevention of diabetes; CANOE: low-dose combination therapy with rosiglitazone and metformin to prevent type 2 diabetes mellitus; DPP: Diabetes Prevention Program; DREAM: Diabetes Reduction Assessment with ramipril and rosiglitazone Medication; NAVIGATOR: Long-term Study of Nateglinide+Valsartan to Prevent or Delay Type II Diabetes Mellitus and Cardiovascular Complications; ORIGIN: Outcome Reduction With Initial Glargine Intervention; STOP-NIDDM: STOP-Non insulin-Dependent Diabetes Mellitus; XENDOS:XENical in the prevention of Diabetes in Obese Subjects.
GBA: glucemia basal alterada; ITG: intolerancia a la glucosa; ND: no definido; NNT: número necesario para tratar; RR: Reducción del Riesgo.
En el metaanálisis de Phung et al.60 se analiza la eficacia de los antidiabéticos orales para revertir la hiperglucemia a normoglucemia. Incluye 13 estudios con 11.600 pacientes y muestra que el uso de fármacos antidiabéticos multiplica por dos la probabilidad de que los pacientes con prediabetes regresen a la normalidad en comparación con el placebo/control. En concreto las glitazonas y los inhibidores de alfa-glucosidasas aumentaron individualmente en 2 veces dicha probabilidad, mientras que biguanidas y sulfonilureas no alcanzan la significación estadística en la regresión a normoglucemia, pero se observó un efecto favorable sobre la glucemia para cada uno de estos antidiabéticos. Sin embargo, se debe ser cauto al comparar o extrapolar los resultados de estos ensayos clínicos, ya que muchas de las intervenciones se han hecho en pacientes con intolerancia a la glucosa y no se pueden aplicar estrictamente a otros tipos de pacientes con prediabetes definidos por la GB o la HbA1c. Finalmente se debe recordar que estaríamos tratando una entidad asintomática con fármacos que pueden producir efectos adversos graves (glitazonas) o molestos (acarbosa y meformina) y que, como se ha dicho previamente, ninguno de ellos está autorizado en esta indicación en Europa.
La prediabetes en el niño y adolescenteEn la década de los 90 se observó un incremento notable del diagnóstico de DM2 entre niños y adolescentes obesos en población americana, hasta el punto de etiquetar esta situación de epidemia61. Diversos estudios posteriores pusieron de manifiesto que la DM2 constituía entre un 20 y 30% de los nuevos diagnósticos de diabetes entre niños en edad escolar y adolescentes americanos. Los factores de riesgo que se relacionaron con esta enfermedad fueron: la presencia de una obesidad exógena, la edad puberal, una raza no caucásica, la existencia de antecedentes familiares de DM2 y la aparición de datos clínicos de insulinorresistencia (acantosis nigricans o síndrome de ovario poliquístico).
La ADA62 en el año 2000 estableció unas indicaciones para hacer una detección precoz de DM2 en población infanto-juvenil asintomática. Proponía descartarla mediante una determinación basal de glucosa o un TTOG, practicado cada dos años en aquellos niños y adolescentes obesos que asociara, además, 2 de los factores de riesgo anteriormente citados.
Los datos del estudio epidemiológico americano STOPP-TD263 fueron realmente alarmantes. Mostraron que en el año 2006 el 50% de los niños en edad escolar padecía sobrepeso u obesidad. Al realizar un TTOG, un 41% de los niños y adolescentes estaban en situación de prediabetes, hecho que tenía una mayor prevalencia a mayor proporción de obesidad y entre minorías raciales.
En la última década numerosos autores han estudiado la presencia de una DM2 mediante TTOG en niños y adolescentes europeos, obesos, de raza caucásica sin que asociaran otros factores de riesgo añadido. El resultado global de estos trabajos muestra una muy baja prevalencia de alteraciones del metabolismo hidrocarbonado en este grupo de pacientes que se sitúa globalmente en torno al 10% y, en general, se trata de una intolerancia hidrocarbonada o elevación de la glucemia basal, siendo el diagnóstico de DM2 anecdótico64,65. Aguayo et al.66, en 2013 mostraron que en un grupo de 150 niños y adolescentes obesos de raza caucásica solo un 3% tenía prediabetes y ninguno DM2. Sí, es un hecho reseñable y común en muchos de estos trabajos demostrar la presencia de una insulinoresistencia entre estos pacientes y su asociación a factores de riesgo cardiovascular, entre otros hipertensión y dislipemia65,66.
Existen pocos datos en relación con el desarrollo de DM2 en pacientes pediátricos obesos con prediabetes. Weiss et al. en 2003 mostraron que la cuarta parte de pacientes obesos con intolerancia a los hidratos de carbono en dos años desarrollaba una DM267, progresión similar a la objetivada en la población adulta. Los factores de riesgo asociados al desarrollo de diabetes fueron de nuevo, la raza no caucásica, el mayor IMC basal y el aumento de peso en el tiempo de estudio, a pesar del tratamiento instaurado.
La ADA en el 2014ha establecido las recomendaciones actuales para descartar una DM2 con un grado de recomendación E (basado en la opinión de expertos), en la población menor de 19 años27. Propone iniciar la detección a partir de los 10 años de edad o en el inicio de la pubertad, mediante la determinación de una HbA1C (glucemia basal o TTOG como alternativas en situaciones concretas de hemoglobinopatías o fibrosis quística) y repetir la determinación cada 3 años, si se cumplen los supuestos planteados en la tabla 6. Para la estimación del sobrepeso u obesidad se recomienda utilizar las tablas de peso y talla en población infantil española68.
Cribado de prediabetes y diabetes en niños y adolescentes menores de 19 años
| Pacientes con obesidad o sobrepeso(IMC>percentil 85 para edad y sexo, peso/talla>percentil 85 o peso>120% del ideal para su talla)* que asocien dos o más de los siguientes factores de riesgo: |
| Historia familiar de DM2 en familiares de 1.er o 2.° grado |
| Componente racial de riesgo: indios americanos, afroamericana, latina, americanos asiáticos y población de las islas del Pacífico |
| Existencia de signos derivados o relacionados con una insulinorresistencia: acantosis nigricans, hipertensión, dislipemia, ovario poliquístico o antecedente de haber nacido pequeño para la edad gestacional |
| Historia materna de diabetes o de diabetes gestacional en el embarazo del paciente |
*Utilizar las tablas de peso y talla en población infantil española68.
IMC: índice de masa corporal.
Dentro del planteamiento terapéutico en pacientes en edad pediátrica, obesos, con resistencia insulínica, prediabetes o DM2, el tratamiento inicial se basa en modificar los hábitos de vida para reducir la obesidad a través de incentivar una alimentación más saludable, con un contenido calórico adecuado para cada edad y un incremento de la práctica de ejercicio físico62. Este tipo de recomendaciones generales son similares a las descritas en el apartado 4 de este documento. No existen datos concluyentes en relación con la idoneidad de una terapia dietética concreta en población pediátrica. Es importante señalar algunos aspectos específicos para niños y adolescentes:
- -
Las modificaciones de vida se han de realizar en el conjunto del núcleo familiar.
- -
Un niño no debe recibir una alimentación con un contenido calórico inferior al adecuado para su edad, salvo en situaciones excepcionales y bajo un control médico estrecho.
- -
Durante la edad pediátrica y, dado que los niños están en crecimiento, mantener el peso corporal en muchas ocasiones significa disminuir el grado de obesidad y, por lo tanto mejorar.
- -
Como objetivo a medio plazo se pretende que el IMC de los pacientes se sitúe por debajo del rango de sobrepeso (IMC<percentil 85).
- -
El ejercicio físico en los niños ha de ser incorporado a su vida habitual y cuando se programe, elegir uno que le resulte atractivo y, a ser posible lo pueda realizar en grupo.
- -
Han de plantearse metas alcanzables a medio plazo y de forma consensuada, especialmente con los adolescentes.
La metformina es el único antidiabético oral aprobado para pacientes con DM2 de edad superior a 10 años. Sin embargo, no existen datos que hayan valorado la eficacia de dicho fármaco en la prevención del desarrollo de DM2 en pacientes pediátricos obesos con prediabetes y no está autorizada con esta indicación.
Para finalizar, Imperatore et al.69 estiman que la prevalencia de DM2 en población americana de edad inferior a 20 años se cuadriplicará en el año 2050 respecto a 2010 (22.820 casos en 2010 y 84.136 en 2050), según las cifras existentes y la evolución de la obesidad exógena en su población. La estimación más optimista augura un incremento notable de personas jóvenes afectas de DM2 y, por lo tanto, su prevención ha de seguir siendo una prioridad de salud pública. Para ello se han de establecer estrategias eficaces de prevención de la obesidad infantil y de intervención primaria en niños y adolescentes obesos con riesgo de desarrollar una DM2.
ConclusionesLa prediabetes afecta a un porcentaje elevado de la población y se asocia con un riesgo incrementado de desarrollar DM2. Sin embargo, es posible retroceder de un estado prediabético a los valores normales de glucosa en sangre.
El cribado oportunista en grupos de riesgo o bien en dos etapas, mediante el test FINDRISC, aunque no ha demostrado beneficios en términos de morbimortalidad, puede contribuir a detectar casos de prediabetes y a prevenir la DM2 y probablemente sus complicaciones crónicas. La detección y tratamiento precoz con cambios en los estilos de vida puede prevenir la aparición de DM2 y es una intervención coste-efectiva. En situaciones de riesgo muy elevado (IMC ≥ 35 Kg/m2 y edad<60 años) podría ser útil el tratamiento farmacológico coadyuvante con metformina, aunque ningún fármaco tiene aprobada esta indicación.
Conflicto de interesesLos autores declaran no tener ningún conflicto de intereses.
Componentes del Grupo de Trabajo de Consensos y Guías Clínicas de la Sociedad Española de Diabetes:
F. Álvarez Guisasola, S. Artola Menéndez, J. Escalada San Martín, F. Escobar Jiménez, P. Ezkurra Loyola, J.C. Ferrer García, J.A. Fornos Pérez, J. Girbés Borrás, J. Lafita Tejedor, J.L. Martín Manzano, M. Mata Cases, E. Menéndez Torre, C. Ortega Millán e I. Rica Echevarría.
Promovido por la Sociedad Española de Diabetes (SED) con la colaboración de la: Sociedad Española de Endocrinología y Nutrición (SEEN, Javier Escalada San Martín). Sociedad Española de Endocrinología Pediátrica (SEEP, Itxaso Rica Echevarría). Sociedad Española de Farmacia Comunitaria (SEFAC, José Antonio Fornos Pérez). Sociedad Española de Medicina Familiar y Comunitaria (SEMFYC. Fernando Álvarez Guisasola). Sociedad Española de Médicos Generales (SEMG, Carlos Miranda Fernández-Santos). Sociedad Española de Médicos de Atención Primaria (SEMERGEN, Javier Mediavilla Bravo). Sociedad Española de Medicina Interna (SEMI, Javier Ena Muñoz). Asociación de Enfermería Comunitaria (AEC, Grupo de atención a la cronicidad. Miguel Ángel Núñez).
Nota: Entre paréntesis los nombres de los profesionales que han revisado el documento.
Una lista de los componentes del Grupo de Trabajo de Consensos y Guías Clínicas de la Sociedad Española de Diabetes está disponible en el Apéndice.
Este Documento también se ha publicado en: Aten Primaria. 2014. http://dx.doi.org/10.1016/j.aprim.2014.12.002 Endocrinol Nutr. 2014. http://dx.doi.org/10.1016/j.endonu.2014.10.008 Semergen. 2014. http://10.1016/j.semerg.2014.12.001 Rev Clin Esp. 2015. http://dx.doi.org/10.1016/j.rce.2014.10.012.