La estenosis valvular aórtica severa en edad pediátrica supone un auténtico reto quirúrgico. Las opciones terapéuticas son altamente complejas, especialmente en niños menores de un año de edad. La cirugía de Ross está indicada en aquellos casos donde la reparación quirúrgica o la valvuloplastia con balón no han sido factibles. El objetivo del estudio es comparar los resultados postoperatorios y en el seguimiento de los pacientes menores de un año con la totalidad de pacientes intervenidos de Ross/Ross-Konno en nuestro centro.
MétodosSe recogieron de manera consecutiva todos los pacientes intervenidos en nuestro centro mediante estos dos procedimientos durante los últimos 10 años. Durante ese periodo, se intervinieron a 11 pacientes (cinco Ross y seis Ross-Konno) de los cuales tres corresponden a pacientes menores de un año.
ResultadosLa mortalidad hospitalaria es del 9,1% (un paciente) con una supervivencia a 10 años del 90,9%. El porcentaje de reoperaciones en el seguimiento es del 72,7% siendo mayor en los pacientes menores de un año (100 vs. 62,5%). Sólo un paciente requirió una reintervención sobre el autoinjerto en edad adulta. La necesidad de intervención sobre el tracto de salida derecho es del 64,6% a 10 años.
ConclusionesLa mortalidad postoperatoria y supervivencia a los 10 años de los pacientes intervenidos durante el primer año de vida no difiere del resto de pacientes de mayor edad, aunque la tasa de reintervenciones en el seguimiento es mayor en este subgrupo de pacientes.
Severe aortic valve stenosis in pediatric population represents a real surgical challenge. Therapeutic options are highly complex, especially in children under one year of age. Ross procedure is indicated in those cases where surgical repair or balloon valvuloplasty has not been feasible. The aim of the study is compare the postoperative outcomes and in the follow-up of patients under one year with all the patients who underwent Ross / Ross-Konno procedure in our centre.
MethodsConsecutive patients operated in our centre with these two procedures for the last ten years were collected. During this period, 11 patients were operated (5 Ross and 6 Ross-Konno) of which 3 corresponded to patients under one year of age.
ResultsHospital mortality is 9,1% (1 patient) with a 10-year survival of 90,9%. The reoperations percentage is 72,7%, higher in patients less than 1-year-old (100% vs. 62,5%). Only one patient required an autograft reoperation in the adulthood. The right ventricle outflow tract reoperation rate is 64,6% at 10 years.
ConclusionsPostoperative mortality and survival at 10 years of patients operated on during the first year of life does not differ from the rest of older patients, although the rate of reoperations in the follow-up is higher in this subgroup of patients.
La estenosis aórtica en edad pediátrica es una cardiopatía congénita poco frecuente, con una prevalencia de 0,20-0,24 de cada 1.000 nacidos vivos1, pero a menudo relacionada con otras afectaciones del tracto de salida del ventrículo izquierdo como son la hipoplasia del anillo aórtico, estenosis subaórtica por hipertrofia septal o fibroelastosis endomiocárdica.
Frecuentemente, estos pacientes son manejados mediante valvuloplastias aórticas percutáneas o valvulotomías quirúrgicas de forma repetida en la infancia2. En la mayoría de los casos, necesitarán de un reemplazo valvular aórtico a lo largo de su vida. Esta sustitución valvular viene limitada principalmente por el tamaño del paciente, siendo la sustitución valvular por prótesis mecánica con posibilidad de ampliación del anillo una técnica solamente útil en pacientes de mayor tamaño. Los problemas de este tipo de reemplazo valvular aparecen en el seguimiento, dada la necesidad de recambio protésico y anticoagulación permanente3.
La sustitución de la raíz aórtica usando un autoinjerto pulmonar fue descrita por primera vez por Donald Ross en el año 19674. Desde entonces, han surgido múltiples controversias derivadas principalmente de la durabilidad del autoinjerto en posición aórtica y la necesidad de recambios repetidos del conducto valvulado en posición pulmonar. En cambio, presenta un adecuado crecimiento y funcionalidad del autoinjerto a lo largo de los años5. Además, existen escasas series de pacientes por debajo del año de vida y su posible peor pronóstico a largo plazo respecto a los de mayor edad está todavía en duda.
Presentamos los resultados de esta técnica realizada en población pediátrica intervenidos en nuestro centro con especial hincapié en aquellos menores de un año de edad.
MétodosSe trata de un estudio observacional retrospectivo de los pacientes intervenidos en nuestro centro mediante la técnica de Ross/Ross Konno desde septiembre de 2010 hasta agosto de 2021. Durante ese periodo se intervinieron de manera consecutiva 11 casos, de los cuales cinco fueron intervenidos mediante la técnica de Ross y los otros seis mediante un Ross-Konno. De los 11, tres correspondieron a enfermos intervenidos con una edad igual o inferior a 12 meses (dos neonatos). Se muestran los resultados del total de la muestra y, además, se realiza una comparativa de dos grupos divididos en función de la edad: grupo 1 (lactantes), menores de 12 meses, grupo 2 (resto), mayores de 12 meses.
Los resultados se muestran para la recogida de datos y el análisis estadístico se utilizó el programa SPSS versión 24. Se realizó el test de Shapiro-Wilk para contrastar la normalidad de las muestras con resultado de distribución no normal, por lo que las variables cuantitativas continuas se muestran en medianas con rango intercuartil y las variables cualitativas en porcentajes. Se aplicó la prueba U de Mann-Whitney para comparar variables cuantitativas continuas y el test exacto de Fisher para las cualitativas dicotómicas con un nivel de significancia estadística < 0,05. El análisis de supervivencia se realizó mediante la estimación de Kaplan-Meier con test de log-rank.
Técnica quirúrgicaEn todos los pacientes se utilizó la vía de abordaje habitual mediante esternotomía media, canulación bicava y circulación extracorpórea con hipotermia entre 28 y 32 grados. La administración de cardioplegia fría (Custodiol) se realizó en la raíz aórtica excepto en los casos con insuficiencia aórtica moderada-severa donde también se suministró directamente en los ostia coronarios. Ningún paciente requirió de hipotermia profunda con parada circulatoria para llevar a cabo el procedimiento. El autoinjerto pulmonar se extrajo con una lengüeta de la pared libre del ventrículo derecho en los casos con hipoplasia del anillo aórtico y/u obstrucción subaórtica que requiriera de su ampliación mediante Ross-Konno. Dicha ampliación se realizó entre la coronaria derecha e izquierda. A su vez, se definió Ross-Konno como aquellos casos en que la apertura del anillo aórtico hacia el septo se realizó para liberar una obstrucción subaórtica. La lengüeta de pared libre del ventrículo derecho se utilizó para cerrar la apertura del septo interventricular por lo que ningún paciente requirió de un parche heterólogo para dicho fin.
En los casos donde se realizaron varios procedimientos durante la misma intervención, como la resección de la fibroelastosis miocárdica o la reparación de la válvula mitral, éstos se llevaron a cabo antes de implantar el autoinjerto pulmonar.
El autoinjerto pulmonar se implantó en el anillo aórtico mediante puntos sueltos dobles de prolene con pledget, manteniendo la simetría con las comisuras aórticas en dependencia de su número. No se utilizaron materiales protésicos como refuerzo de la sutura del anillo aórtico. Los ostia coronarios se implantaron mediante punch aórtico. Para la reconstrucción del tracto de salida del ventrículo derecho se utilizó en todos los casos un homoinjerto criopreservado, siendo pulmonar o aórtico en función de la disponibilidad del banco de tejidos. Dicho conducto se implantó directamente en el ventrículo derecho y en algunos casos sin isquemia miocárdica, durante la fase de recalentamiento. La desconexión de circulación extracorpórea se realizó de manera habitual, bajo control con ecocardiografía transesofágica.
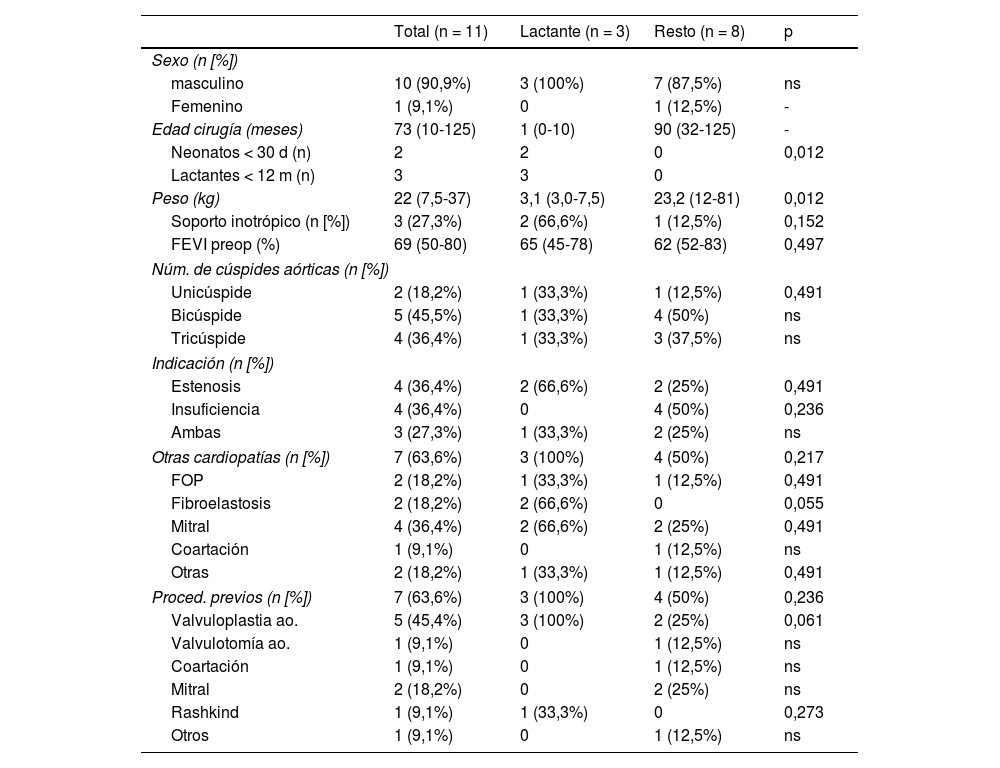
ResultadosCaracterísticas demográficasLos parámetros demográficos preoperatorios se muestran en la tabla 1. Comparando ambos grupos, lactantes vs. resto, la edad (un mes vs. 90) y el peso (3,1 kg vs. 23,2) alcanzaron una diferencia estadísticamente significativa entre grupos con una p de 0,012 en ambos casos. Este resultado es esperado debido a que hemos seleccionado previamente los pacientes de menor edad que conllevan, a su vez, un menor peso dentro del grupo de lactante. La indicación principal para la cirugía es la estenosis y la insuficiencia aórtica por igual (36,4%) en el total de la muestra, con una mayor tendencia a ser la estenosis la indicación predominante en el grupo lactante (66%).
Características preoperatorias
| Total (n = 11) | Lactante (n = 3) | Resto (n = 8) | p | |
|---|---|---|---|---|
| Sexo (n [%]) | ||||
| masculino | 10 (90,9%) | 3 (100%) | 7 (87,5%) | ns |
| Femenino | 1 (9,1%) | 0 | 1 (12,5%) | - |
| Edad cirugía (meses) | 73 (10-125) | 1 (0-10) | 90 (32-125) | - |
| Neonatos < 30 d (n) | 2 | 2 | 0 | 0,012 |
| Lactantes < 12 m (n) | 3 | 3 | 0 | |
| Peso (kg) | 22 (7,5-37) | 3,1 (3,0-7,5) | 23,2 (12-81) | 0,012 |
| Soporto inotrópico (n [%]) | 3 (27,3%) | 2 (66,6%) | 1 (12,5%) | 0,152 |
| FEVI preop (%) | 69 (50-80) | 65 (45-78) | 62 (52-83) | 0,497 |
| Núm. de cúspides aórticas (n [%]) | ||||
| Unicúspide | 2 (18,2%) | 1 (33,3%) | 1 (12,5%) | 0,491 |
| Bicúspide | 5 (45,5%) | 1 (33,3%) | 4 (50%) | ns |
| Tricúspide | 4 (36,4%) | 1 (33,3%) | 3 (37,5%) | ns |
| Indicación (n [%]) | ||||
| Estenosis | 4 (36,4%) | 2 (66,6%) | 2 (25%) | 0,491 |
| Insuficiencia | 4 (36,4%) | 0 | 4 (50%) | 0,236 |
| Ambas | 3 (27,3%) | 1 (33,3%) | 2 (25%) | ns |
| Otras cardiopatías (n [%]) | 7 (63,6%) | 3 (100%) | 4 (50%) | 0,217 |
| FOP | 2 (18,2%) | 1 (33,3%) | 1 (12,5%) | 0,491 |
| Fibroelastosis | 2 (18,2%) | 2 (66,6%) | 0 | 0,055 |
| Mitral | 4 (36,4%) | 2 (66,6%) | 2 (25%) | 0,491 |
| Coartación | 1 (9,1%) | 0 | 1 (12,5%) | ns |
| Otras | 2 (18,2%) | 1 (33,3%) | 1 (12,5%) | 0,491 |
| Proced. previos (n [%]) | 7 (63,6%) | 3 (100%) | 4 (50%) | 0,236 |
| Valvuloplastia ao. | 5 (45,4%) | 3 (100%) | 2 (25%) | 0,061 |
| Valvulotomía ao. | 1 (9,1%) | 0 | 1 (12,5%) | ns |
| Coartación | 1 (9,1%) | 0 | 1 (12,5%) | ns |
| Mitral | 2 (18,2%) | 0 | 2 (25%) | ns |
| Rashkind | 1 (9,1%) | 1 (33,3%) | 0 | 0,273 |
| Otros | 1 (9,1%) | 0 | 1 (12,5%) | ns |
ao: aórtica/aorta; FEVI: fracción de eyección del ventrículo izquierdo; FOP: foramen oval permeable; kg: kilogramos; núm: número; preop: preoperatorio; proced: procedimiento.
El resto de las características preoperatorias analizadas no muestran diferencias significativas, aunque sí destacaríamos en el grupo de lactantes, un mayor uso de soporte inotrópico preoperatorio y de procedimientos preoperatorios (en total se realizaron 11 procedimientos previos en siete pacientes: cuatro procedimientos en tres pacientes lactantes y siete en cuatro pacientes de otras edades), sobre todo de valvuloplastias aórticas, rozando la significancia estadística. Ambas observaciones se pueden justificar ya que se trata de un subgrupo de pacientes formado en su mayoría por pacientes neonatales ingresados en la Unidad de Cuidados Intensivos Neonatales con un estado crítico preoperatorio respecto al resto de pacientes. También es reseñable comentar que los dos pacientes neonatales presentan fibroelastosis endomiocárdica y afectación de la válvula mitral en distintos grados.
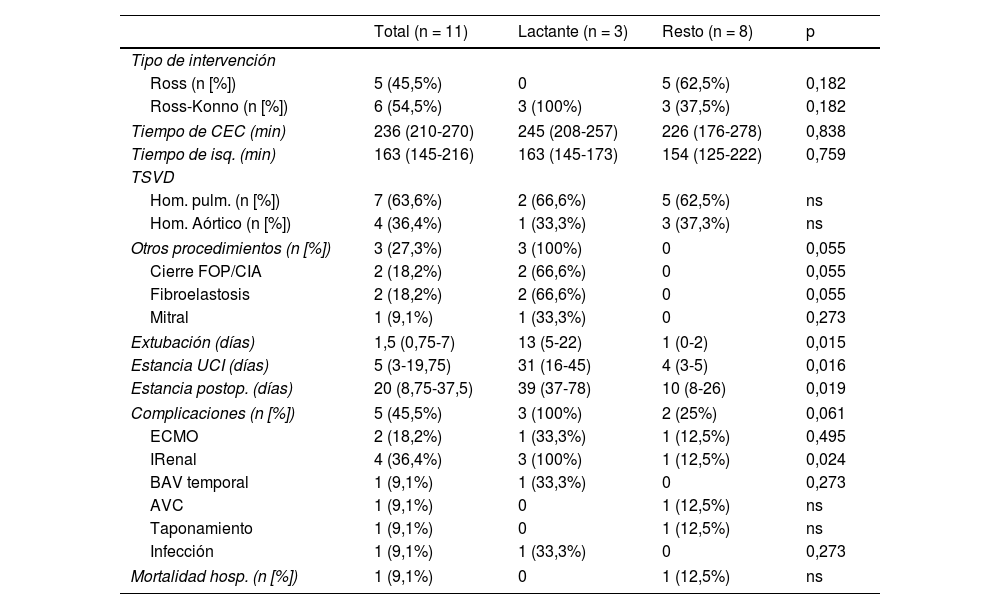
Datos intra y postoperatoriosLas características intra y postoperatorias están definidas en la tabla 2.
Características perioperatorias
| Total (n = 11) | Lactante (n = 3) | Resto (n = 8) | p | |
|---|---|---|---|---|
| Tipo de intervención | ||||
| Ross (n [%]) | 5 (45,5%) | 0 | 5 (62,5%) | 0,182 |
| Ross-Konno (n [%]) | 6 (54,5%) | 3 (100%) | 3 (37,5%) | 0,182 |
| Tiempo de CEC (min) | 236 (210-270) | 245 (208-257) | 226 (176-278) | 0,838 |
| Tiempo de isq. (min) | 163 (145-216) | 163 (145-173) | 154 (125-222) | 0,759 |
| TSVD | ||||
| Hom. pulm. (n [%]) | 7 (63,6%) | 2 (66,6%) | 5 (62,5%) | ns |
| Hom. Aórtico (n [%]) | 4 (36,4%) | 1 (33,3%) | 3 (37,3%) | ns |
| Otros procedimientos (n [%]) | 3 (27,3%) | 3 (100%) | 0 | 0,055 |
| Cierre FOP/CIA | 2 (18,2%) | 2 (66,6%) | 0 | 0,055 |
| Fibroelastosis | 2 (18,2%) | 2 (66,6%) | 0 | 0,055 |
| Mitral | 1 (9,1%) | 1 (33,3%) | 0 | 0,273 |
| Extubación (días) | 1,5 (0,75-7) | 13 (5-22) | 1 (0-2) | 0,015 |
| Estancia UCI (días) | 5 (3-19,75) | 31 (16-45) | 4 (3-5) | 0,016 |
| Estancia postop. (días) | 20 (8,75-37,5) | 39 (37-78) | 10 (8-26) | 0,019 |
| Complicaciones (n [%]) | 5 (45,5%) | 3 (100%) | 2 (25%) | 0,061 |
| ECMO | 2 (18,2%) | 1 (33,3%) | 1 (12,5%) | 0,495 |
| IRenal | 4 (36,4%) | 3 (100%) | 1 (12,5%) | 0,024 |
| BAV temporal | 1 (9,1%) | 1 (33,3%) | 0 | 0,273 |
| AVC | 1 (9,1%) | 0 | 1 (12,5%) | ns |
| Taponamiento | 1 (9,1%) | 0 | 1 (12,5%) | ns |
| Infección | 1 (9,1%) | 1 (33,3%) | 0 | 0,273 |
| Mortalidad hosp. (n [%]) | 1 (9,1%) | 0 | 1 (12,5%) | ns |
AVC: accidente vascular cerebral; BAV: bloqueo auriculoventricular; CEC: circulación extracorpórea; CIA: comunicación interauricular; ECMO: oxigenación por membrana extracorpórea; FOP: foramen oval permeable; Hom: homoinjerto; hosp: hospitalaria; isq: isquemia; IRenal: insuficiencia renal; postop: postoperatoria; pulm: pulmonar; TSVD: tracto de salida del ventrículo derecho; UCI: unidad de cuidados intensivos.
Se realizaron un total de 16 procedimientos en 11 pacientes sin diferencias significativas en cuanto a tiempos de circulación extracorpórea ni isquemia entre ambos grupos (245 vs. 226, p = 0,838 y 163 vs. 154, p = 0,759, respectivamente). El uso de un tipo u otro de homoinjerto criopreservado atiende a razones de disponibilidad, sin haber hallado diferencias entre los grupos.
En el grupo de lactantes, destaca la realización de un mayor número de procedimientos concomitantes en la misma intervención quirúrgica, realizando en todos los neonatos una resección de fibrosis endomiocárdica y una reparación mitral en un lactante. Los tiempos de intubación (13 vs. 1, p = 0,015), estancia en cuidados intensivos (31 vs. 4, p = 0,016) y la estancia hospitalaria (39 vs. 10, p = 0,019) fueron significativamente más largos en el grupo de lactantes que en el resto de los pacientes.
Respecto a las complicaciones postoperatorias, cinco pacientes (45,5%) tuvieron algún evento destacable en el postoperatorio, siendo esta frecuencia clínicamente mayor en el grupo de lactantes (100 vs. 25%, p = 0,061), pero sin alcanzar la significancia estadística. Dos pacientes necesitaron oxigenación por membrana extracorpórea (ECMO) postoperatoria (18,2%) con una recuperación completa en uno de los casos. La tasa de insuficiencia renal definida como la necesidad de terapia sustitutiva transitoria fue elevada en el grupo de lactantes, siendo utilizada la diálisis peritoneal en todos los casos. El resto de las complicaciones analizadas (accidente vascular cerebral, bloqueo aurículoventricular transitorio, infección definida como sepsis y taponamiento cardiaco) se repartieron de manera aleatorio entre ambos grupos sin haber más de un evento en cada una de ellas. La mortalidad postoperatoria fue de un caso (9,1%), un paciente en ECMO por disfunción cardíaca e hipertensión pulmonar severa que sufrió un accidente vascular cerebral hemorrágico al tercer día de soporte. Este paciente pertenecía al grupo de mayores de 12 meses.
SeguimientoEl tiempo medio de seguimiento fue de 104 meses (62-124) siendo en el grupo de lactantes inferior (62 vs. 113 meses, p = 0,153), sin alcanzar la significancia estadística. El seguimiento fue completo en todos los pacientes con supervivencia postoperatoria (n = 10). La supervivencia en el seguimiento fue del 91,9%, sin mortalidad añadida tras el alta hospitalaria.
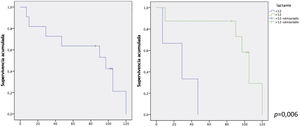
Se realizaron un total de 11 procedimientos en ocho pacientes después de la primera intervención. Solo tres pacientes siguen libres de reintervención tras el seguimiento. Estos tres pacientes corresponden a los mayores de 12 meses, ya que la totalidad de los lactantes ha requerido algún procedimiento durante su seguimiento (fig. 1). Ocho de estos procedimientos se realizaron sobre el conducto valvulado: cinco cateterismos mediante el implante de cuatro válvulas percutáneas, una angioplastia con balón y un stent, y tres recambios de conducto mediante cirugía (fig. 2). No se hallaron diferencias en función del homoinjerto usado, pulmonar o aórtico. Además, se realizaron dos procedimientos añadidos sobre la válvula mitral por estenosis (una sustitución y una reparación/plastia mitral). No se han identificado lesiones coronarias durante el seguimiento.
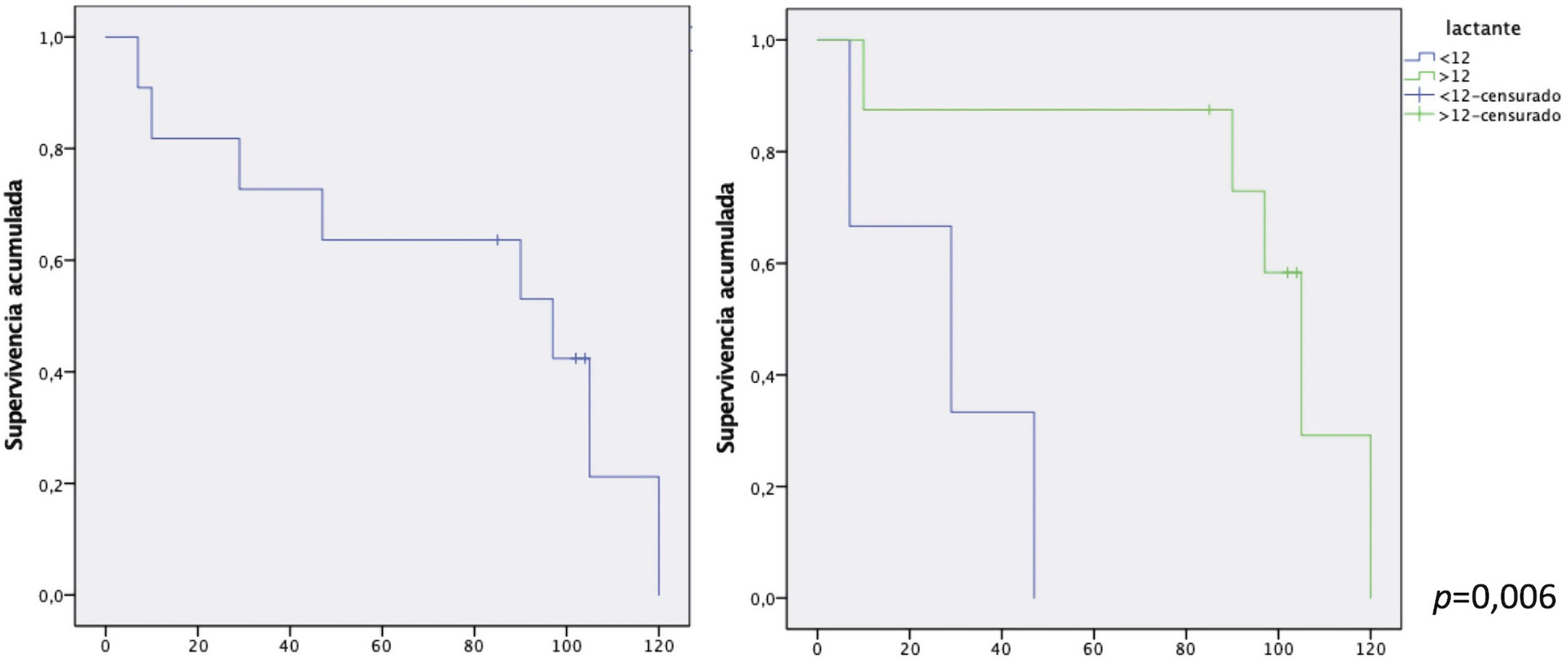
Gráficos de supervivencia Kaplan-Meier sobre supervivencia libre de eventos del total de la muestra y comparativa en función de la edad. A) Total de pacientes. El tiempo medio de supervivencia libre de evento de la muestra es de 80,1 meses (56,2-100,4) con un porcentaje libre de eventos del 63,6% y del 21,2% a cinco y 10 años, respectivamente. B) Comparativo en función de la edad. Los pacientes menores de 12 años tienen un tiempo medio de supervivencia de 27,6 meses (4,9-50,3) y una libertad de eventos del 33,3% a cinco años. En cambio, los mayores de 12 años tienen una libertad de eventos del 87,5% a cinco años con un tiempo medio de supervivencia de 99,7 meses (83,3-116,1).
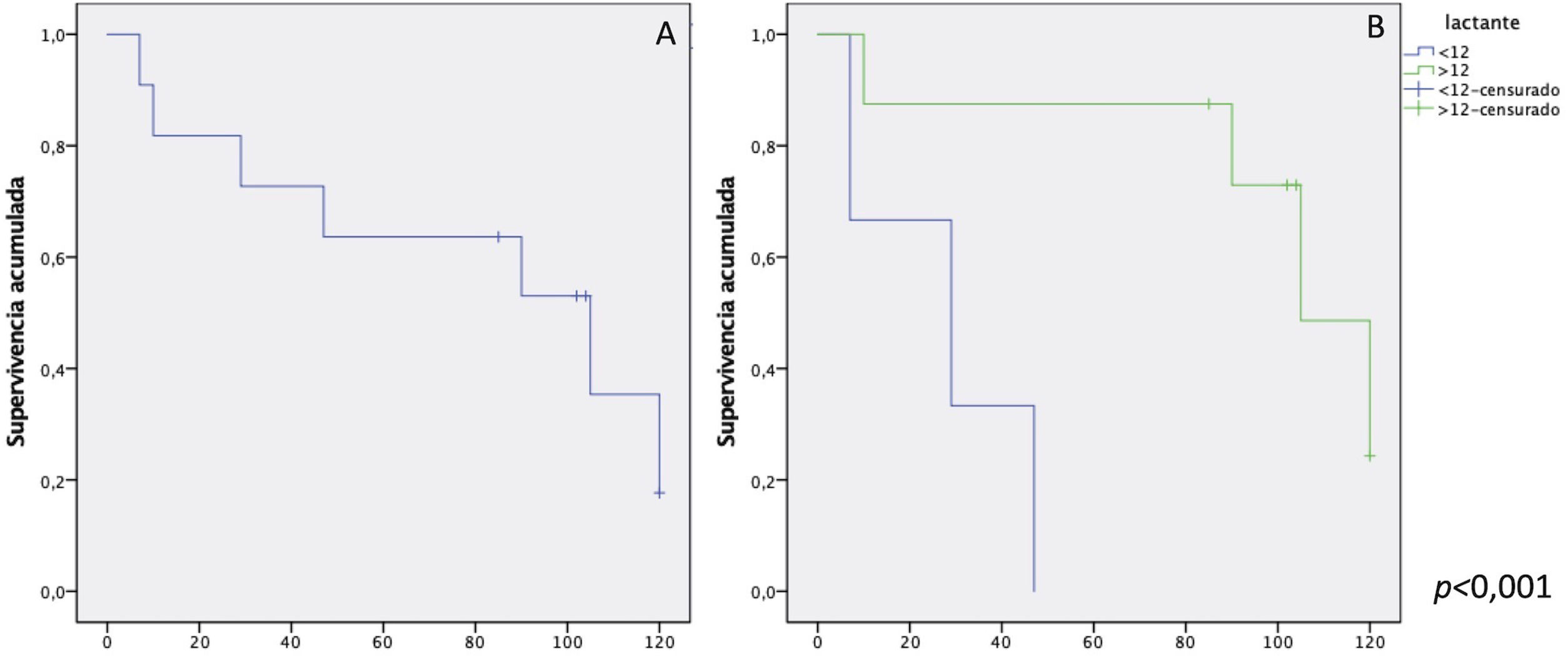
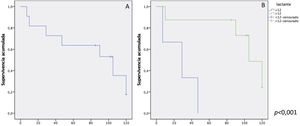
Gráficos de supervivencia Kaplan-Meier sobre supervivencia libre de reintervención sobre el tracto de salida del ventrículo derecho. A) Total de pacientes. El tiempo medio de supervivencia libre de evento de la muestra es de 78,9 meses (50,5-107,4) con un porcentaje libre de eventos del 63,6% y del 35,4% a cinco y 10 años respectivamente. B) Comparativo en función de la edad. Los pacientes menores de 12 años tienen un tiempo medio de supervivencia de 27,6 meses (4,9-50,3) y una libertad de eventos del 33,3% a cinco años. En cambio, los mayores de 12 años tienen una libertad de eventos del 72,9% a cinco años con un tiempo medio de supervivencia de 98,2 meses (69,6-126,7).
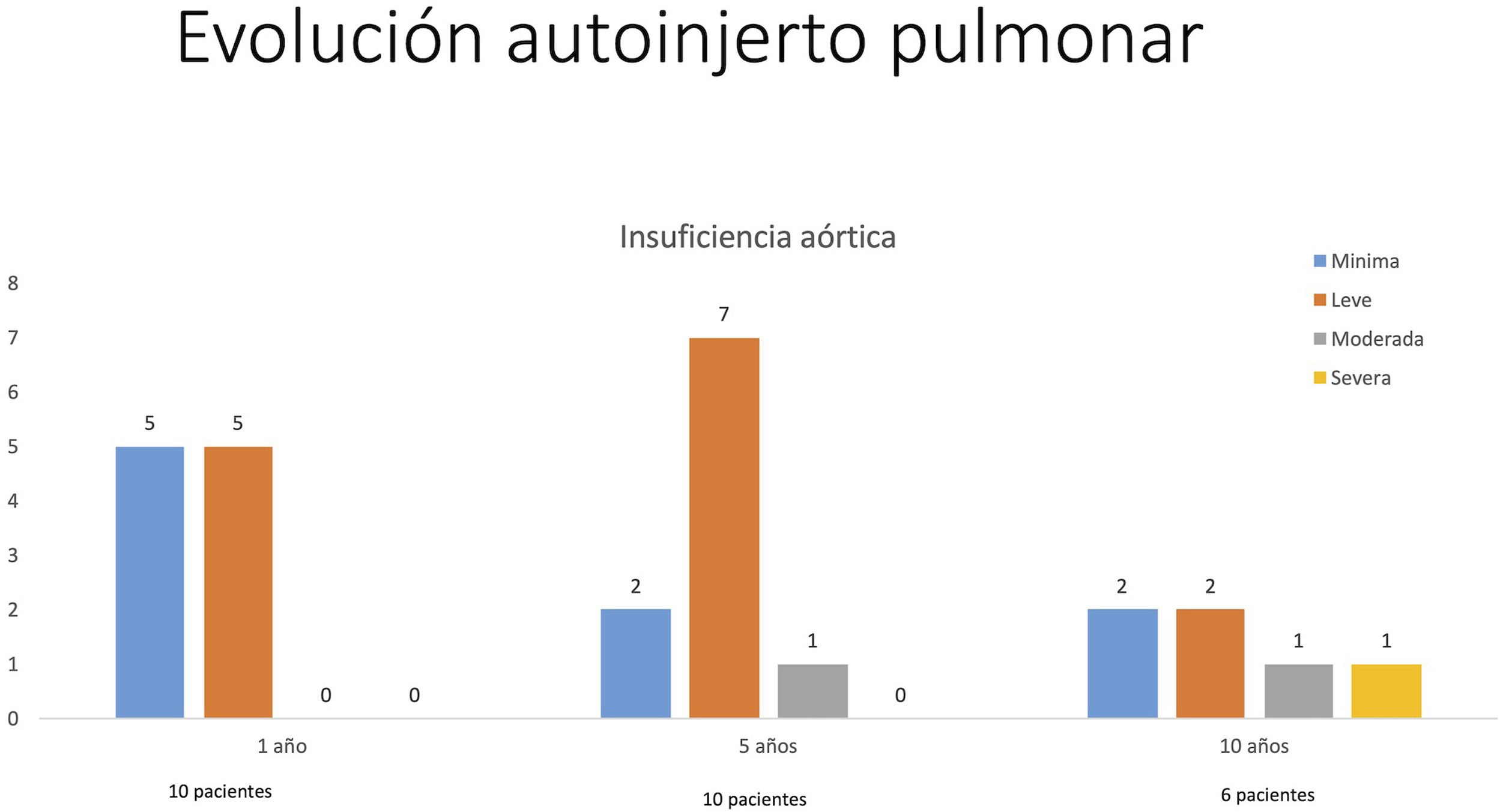
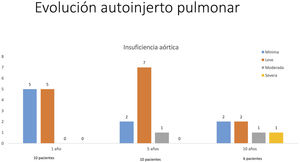
Respecto a la evolución de la función del autoinjerto pulmonar, sólo se llevó a cabo un procedimiento, realizado a los 97 meses de seguimiento, por insuficiencia aórtica severa que conllevó un reemplazo valvular por una prótesis mecánica en la edad adulta. La evolución de la insuficiencia aórtica se muestra en la figura 3. Solo en dos casos la regurgitación valvular fue superior e igual a moderada con un tiempo de seguimiento medio de 111 meses (90,1-132). No aparecieron gradientes medios superiores a 10 mmHg y solo dos pacientes presentaron una dilatación de la raíz aórtica con z-score superior a 2.
Evolución de la insuficiencia aórtica durante el seguimiento. El 80% de los pacientes presentan una insuficiencia aórtica leve o menor en el seguimiento, sin un incremento llamativo durante su evolución. La libertad de insuficiencia aórtica igual o mayor que moderada es del 90% a cinco años de seguimiento.
El reemplazo de la raíz aórtica con un autoinjerto pulmonar es una de las técnicas utilizadas para el tratamiento de la estenosis aórtica crítica en edad pediátrica.
La cirugía de Ross fue acogida con especial entusiasmo en la década de los 90, con una gran proyección en la mayoría de los centros europeos y americanos, pero en ciertos grupos quirúrgicos continúa creando controversia por una elevada tasa de reintervenciones y sus resultados a largo plazo6.
Elucidar qué paciente se puede beneficiar de una cirugía de Ross o Ross-Konno puede llegar a ser complejo, especialmente en pacientes con ventrículos izquierdos borderline con fibroelastosis endomiocárdica. Pero, considerando la disponibilidad limitada de los tamaños de las válvulas protésicas y la escasa durabilidad de los homoinjertos en posición aórtica, creemos que esta técnica puede ser una alternativa para los pacientes de menor edad.
Como es bien sabido, las ventajas de este procedimiento son un mejor perfil hemodinámico, potencial de crecimiento sin necesidad de anticoagulación o aparición de hemólisis, pero como en la mayoría de los procedimientos quirúrgicos sobre las cardiopatías congénitas, una edad inferior a 12 meses o la presencia de un menor peso suelen ser factores de peor pronóstico postoperatorio. El objetivo de este artículo era demostrar, basándonos en nuestra experiencia, si existe una mayor mortalidad en la cirugía de la raíz aórtica mediante el uso de autoinjerto pulmonar en lactantes. Según nuestros resultados, la mortalidad postoperatoria no difiere entre ambos grupos siendo nula en los pacientes lactantes. Nuestros resultados no son concordantes con otras de series publicadas en población infantil, oscilando entre el 8-11%, > 25% en series reportadas en edad neonatal7,8, posiblemente debido a nuestro bajo tamaño muestral, pero si con series recientemente publicada de 35 pacientes lactantes, de los cuales 13 son neonatos, sin mortalidad9.
Lo que sí hemos detectado en este grupo de pacientes, es un mayor soporte inotrópico preoperatorio, un mayor número de procedimientos pre e intraoperatorios y unos mayores tiempos de intubación, estancia en la unidad de críticos y en planta de hospitalización. Todos estos factores van en relación probablemente con una situación más crítica de estos pacientes, con ventrículos izquierdos en el límite, presencia de fibroelastosis endomiocárdica que condicionan ingresos más prolongados. Estos factores se han relacionado con una mayor mortalidad y complicaciones postoperatorias8, destacando en nuestra serie la tasa de insuficiencia renal, que también puede estar relacionada con varios factores como una mayor inmadurez del sistema renal, sobre todo en edad neonatal, un estado crítico preoperatorio con probable afectación renal y el uso de catéteres de diálisis peritoneal de forma sistemática en este tipo de población, para disminuir la presión intraabdominal, lograr un balance hídrico negativo y un menor tiempo de extubación10–12. No ha habido diferencias en cuanto a los tiempos de CEC e isquemia a pesar de que en pacientes de mayor peso (> 40 kg), se realizó la disección y extracción del autoinjerto sin pinzamiento aórtico, pero suponen un número pequeño dentro de la muestra. No lo efectuamos en pacientes de menor tamaño, para garantizar una correcta visualización del trayecto de las coronarias mediante la apertura previa de la aorta ascendente bajo isquemia miocárdica.
Un aspecto preocupante de esta técnica es saber cuál sería la durabilidad de una válvula pulmonar implantada en posición aórtica, donde tiene que soportar presiones sistémicas. Está demostrado que, a nivel histológico, el autoinjerto de válvula pulmonar mantiene una completa viabilidad de las tres capas con el desarrollo de un depósito inicial de colágeno en la cara ventricular y la aparición de células intersticiales, que se convertirán en miofibroblastos, en el interior de los velos. En efecto, la válvula pulmonar se transforma completamente en una válvula fenotípicamente aórtica13,14.
Este hecho podría justificar la buena respuesta hemodinámica que presentan estos pacientes a medio y largo plazo, con ausencia de estenosis aórtica en el seguimiento y una aparente adaptación del autoinjerto al incremento de las demandas de la circulación sistémica. También, estos cambios adaptativos podrían apoyar el crecimiento observado acorde con el somático, característica siempre deseada en cualquier tipo de prótesis en edad pediátrica.
En cambio, un aspecto preocupante es la posible dilatación del autoinjerto debido a la menor capacidad de la pared pulmonar a tolerar presiones elevadas, con el consiguiente riesgo de insuficiencia aórtica y disección espontánea. Es sabido que la debilidad de la pared pulmonar conlleva a una dilatación durante el seguimiento, hecho observado en dos de nuestros pacientes. Pero esta dilatación no ocasiona una mayor disfunción valvular en la mayoría de los casos15,16 ni mayor riesgo de disección aórtica, que queda limitada por la sutura de la aorta ascendente y en los botones coronarios. Para evitar esta excesiva dilatación, varios autores abogan por el uso de materiales externos o anillos protésicos con la intención de reforzar y dar soporte a la pared del autoinjerto17, aunque nosotros no somos partidarios del uso de estos materiales ya que, en nuestra opinión, puede limitar perjudicialmente su crecimiento y crear futuras estenosis. En cuanto a la anastomosis proximal del autoinjerto pulmonar, creemos que su implante con sutura a puntos sueltos ayuda a distribuir mejor la discrepancia de diámetro entre ambos anillos evitando asimetrías en la coaptación de las comisuras, situación que pudiera darse en el caso de realizar dicho implante a sutura continua.
Por otro lado, describimos distintas desventajas como la elevada tasa de reintervenciones asociadas al conducto valvulado implantado en el ventrículo derecho o la presencia de regurgitación valvular en el autoinjerto. El 80% de nuestra serie requiere durante el seguimiento de algún tipo de procedimiento, sea intervención quirúrgica o cateterismo cardiaco sobre el conducto del ventrículo derecho y, este porcentaje se eleva al 100% cuando analizamos el grupo de lactantes. En general, estos resultados no difieren de lo publicado en series de pacientes de similar edad, con una libertad de reintervención sobre el conducto a los cinco años del 43% respecto al 60% de nuestra serie18. No hemos encontrado diferencias entre el tipo de homoinjerto utilizado, aunque nuestra preferencia es hacia el uso de homoinjertos pulmonares, que en otras series sí que ha demostrado mayor durabilidad19,20, con una mayor calcificación y estenosis en los homoinjertos aórticos. En cambio, solo un paciente ha necesitado un recambio valvular del autoinjerto pulmonar dando una gran solidez a la técnica respecto la durabilidad a un seguimiento de 10 años. Recientemente, algunos autores se han reafirmado sobre la buena funcionalidad de los autoinjertos a 10 años, pero que ésta decae de forma evidente en la segunda década21,22.
Las limitaciones del estudio son evidentes, el tamaño de nuestra serie es pequeño para poder sacar conclusiones de estos resultados, aunque sean coherentes con lo publicado hasta la actualidad. Por ello, haría falta una mayor muestra para corroborar dicha tendencia.
ConclusionesLas cirugías de Ross y Ross-Konno son dos procedimientos con baja mortalidad fuera del periodo neonatal que demuestran una adecuada funcionalidad a largo plazo, pero con una elevada tasa de reintervenciones sobre el conducto valvulado del ventrículo derecho. Dada nuestra experiencia, reservamos este tipo de procedimientos en pacientes con obstrucción añadida del tracto de salida del ventrículo izquierdo, presencia de fibroelastosis endomiocárdica o regurgitación valvular severa no reparable.
Consideraciones éticasNo se ha solicitado aprobación por el comité ético ni consentimiento informado a los pacientes. Se trata de un estudio retrospectivo y no incluye datos de los pacientes.
FinanciaciónEste trabajo no ha recibido ningún tipo de financiación.
Conflicto de interesesLos autores declaran no tener ningún conflicto de intereses.