El cierre quirúrgico del ductus arterioso persistente (DAP) en prematuros provoca un cambio en el sistema circulatorio que afecta al miocardio inmaduro de estos pacientes. El objetivo del estudio fue analizar la respuesta del ventrículo izquierdo al cierre del DAP, basándonos en parametros ecocardiográficos pre- y postoperatorios.
MétodoAnálisis retrospectivo de los pacientes intervenidos de DAP menores de 1.500g en nuestro hospital durante un periodo de 5 años. Se recogieron datos de características clínicas, de manejo médico preoperatorio, ecocardiográficos y quirúrgicos, así como de estancia en UCI neonatal y hospitalización. La valoración del riesgo operatorio fue calculada según la escala completa Aristóteles de complejidad (ACCS). Los datos ecocardiográficos preoperatorios fueron obtenidos 24 horas antes de la intervención y los postoperatorios 24 horas después. Se recogieron características del DAP, fracción de eyección de ventrículo izquierdo (FEVI) y diámetro telediastólico de ventriculo izquierdo (DdVI).
ResultadosLa media de edad gestacional fue de 26,1±1,8 semanas y el peso medio al nacimiento de 823,5±191,9g, mientras que la mediana de edad en el momento de la cirugía fue de 15,5 días (IQR, 11-21). El ACCS medio fue de 14,02±2,48 (rango 9-20). Diecinueve pacientes (19%) fallecieron intrahospitalariamente. La correlación pre-posquirúrgica para los valores ecocardiográficos presentó una disminución significativa de los valores postintervención para la FEVI (p=0,0001) y el DdVI (p=0,001). El análisis por subgrupos según peso en el momento de la intervención mostró diferencias significativas para DdVI en los pacientes con más de 820g (p=0,002) pero no en los de peso igual o menor de 820g (p=0,311).
ConclusionesLos recién nacidos prematuros tienen un peor manejo de la sobrecarga de volumen producida por el DAP a causa de la inmadurez miocárdica. El cierre quirúrgico del DAP provoca un descenso en la precarga, que en estos pacientes se refleja en una peor adaptación a los cambios de volumen tras la cirugía en relación directa con el peso en el momento de la intervención.
Patent ductus arteriosus (PDA) ligation in premature infants causes changes in the circulatory system that affects the immature myocardium of the patients. The objective of the study was to analyse the response of left ventricle to PDA ligation, according to pre-operative and post-operative echocardiograph parameters.
MethodA retrospective analysis was performed on all patients (n=100) with less than 1500g birth weight undergoing PDA surgical ligation in this hospital during a five year period.
Data were collected on the clinical characteristics, pre-operative medical management, echocardiography, surgical intervention, and in-hospital stay and Neonatal Intensive Care Unit (NICU) stay. The assessment of operative risk was made by calculating the Aristotle comprehensive complexity score (ACCS). The preoperative echocardiography data were obtained 24hours before the intervention and 24hours after surgery. Characteristics of the patent ductus arteriosus, left ventricular ejection fraction (LVEF), and left ventricular end-diastolic dimension (LVEDD) were assessed.
ResultsThe mean gestational age and birth weight was 26.1±1.8 weeks and 823.5±191.9g, respectively. The mean ACCS was 14.02±2.48 (range, 9 to 20). The median age at surgery was 15.5 days (IQR, 11 to 21). Nineteen patients (19%) died during admission. No echocardiography variable was significant in the univariate analysis for mortality.
The pre-postoperative correlation for echocardiography values showed a significant decrease in post-intervention values for LVEF (P=.0001) and LVEDD (P=.001). The analysis by subgroups according to weight at the time of the intervention showed significant differences for LVEDD in patients with more than 820g (P=.002), but not in those of equal or less than 820g (P=.311).
ConclusionsPreterm infants have a worse management of the volume overload produced by the DAP because of myocardial immaturity. The surgical closure of the DAP causes a decrease in the preload that in these patients is reflected in a worse adaptation to volume changes after surgery in direct relation with the weight at the time of the intervention. Patients with less weight at PDA surgical ligation were more likely to have a worse management to load changes after operation.
La presencia de un ductus arterioso permeable (DAP) en prematuros es la afección cardiaca más frecuente en niños de menos de 1.500g de peso al nacimiento, con una incidencia del 33%1. Este se asocia frecuentemente con inestabilidad hemodinámica por la sobrecarga en la circulación pulmonar y en cavidades izquierdas. Los recién nacidos con muy bajo peso al nacimiento tienen menor capacidad de compensar esta sobrecarga, siendo más propensos a desarrollar fallo del ventrículo izquierdo2,3, debido a que el miocardio inmaduro posee menos fibras contráctiles por unidad de peso, lo que le resta adaptabilidad4.
El cierre quirúrgico de DAP en prematuros está indicado en caso de fallo del tratamiento médico o contraindicación del mismo5. El riesgo de estos pacientes no está tan relacionado con la cirugía como con el estado de maduración del prematuro6. Recientemente se ha demostrado en neonatos el empeoramiento de la función miocárdica tras el cierre quirúrgico de DAP, asociado a una modificación en la precarga7. Para ampliar esta información sobre la repercusión de la cirugía sobre el ventrículo izquierdo hemos planteado nuestro estudio.
El objetivo principal de este estudio ha sido ver la respuesta del miocardio inmaduro al cierre quirúrgico del DAP, y para ello hemos analizado los parámetros ecocardiográficos asociados a la función ventricular en nuestra población de neonatos de menos de 1.500g de peso al nacimiento intervenidos de cierre quirúrgico de DAP, buscando relación entre estos y la morbimortalidad, y hemos comparado estos parámetros pre- y postoperatoriamente en diferentes subgrupos para valorar el diferente impacto de la cirugía sobre estos.
MétodosSe ha realizado un estudio retrospectivo en el cual se han recogido todos los recién nacidos prematuros de menos de 1.500g de peso intervenidos de cierre de DAP en la Unidad de Cuidados Intensivos Neonatal (UCIN) de un hospital de referencia regional desde enero de 2008 hasta diciembre de 2013. El estudio fue aprobado por el Comité Ético de Investigación Clínica del hospital. Los padres de todos los niños incluidos en el estudio firmaron el consentimiento informado.
Se han recogido datos administrativos y poblacionales, características clínicas, antropométricas, datos de manejo médico preoperatorio, datos hematológicos y ecocardiográficos, datos de la intervención quirúrgica y de la estancia intrahospitalaria en la UCIN y en hospitalización, así como datos al alta hospitalaria y de seguimiento en las diferentes secciones del centro hospitalario. La valoración del riesgo operatorio se realizó calculando la puntuación en la escala Aristóteles de complejidad completa (ACCS)8. Los datos ecocardiográficos preoperatorios se obtuvieron 24horas antes de la intervención y los postoperatorios 24horas tras la cirugía.
Protocolo de manejoEl diagnóstico de DAP fue confirmado por ecocardiografía bidimensional y doppler color, en aquellos niños prematuros con sospecha clínica de DAP. La indicación de cierre quirúrgico se realizó en aquellos recién nacidos con ductus arterioso persistente hemodinámicamente significativo (DAPHS) sin respuesta al tratamiento médico (uno o 2 ciclos de ibuprofeno intravenoso) o con contraindicación para dicho tratamiento. Los criterios ecocardiográficos de DAPHS incluyen diámetro ductal mayor de 1,5mm con flujo continuo izquierda-derecha; sobrecarga de volumen y/o presión al menos ligera en cavidades izquierdas y disminución de flujo en arterias mesentérica superior, renal o cerebral media, y clínica de sobrecirculación pulmonar, hipoperfusión periférica o ambas9.
El protocolo de actuación aplicado es el Consenso Clínico de la Sociedad Iberoamericana de Neonatología (SIBEN) sobre el DAP en recién nacidos pretérmino el cual se inicia con restricción hídrica asociada a nutrición enteral trófica precoz con administración de 3 dosis de ibuprofeno intravenoso, una cada 24horas, siendo la primera de 10mg/kg y las otras 2 de 5mg/kg5.
Técnica quirúrgicaTodos los pacientes incluidos en el estudio fueron intervenidos en la UCIN del Hospital Materno-Infantil del HCUVA, en la incubadora, sin movilización del neonato, trasladándose el equipo quirúrgico, compuesto este por 2 cirujanos cardiovasculares pediátricos, enfermería quirúrgica y anestesiólogo, con el apoyo del personal de la UCIN. El procedimiento fue realizado bajo anestesia general inducida con etomidato y cisatracurio y mantenido con remifentanilo. El acceso quirúrgico fue a través de toracotomía posterolateral izquierda sin sección muscular, con el paciente en posición de decúbito lateral derecho. El cierre se realizó en todos los casos mediante un clip de titanio de 6mm (Ligaclip® MCA titanium clip 6.0mm. Ethicon endo-surgery, LLC. Puerto Rico, EE.UU.). Solo se dejó drenaje pleural cuando se observó lesión parenquimatosa pulmonar o sangrado mayor de lo esperado.
Análisis estadísticoEl programa estadístico SPSS versión 20.0 (IBM/SPSS Inc., Chicago, IL, EE.UU.) fue utilizado para el análisis. Las variables continuas con distribución normal fueron expresadas como media±desviación típica y analizadas mediante el test t de Student. Las variables continuas con distribución no normal fueron expresadas como mediana y el rango intercuartílico y analizadas mediante pruebas no paramétricas (U de Mann-Whitney). Las variables categóricas fueron expresadas como proporciones y analizadas usando el test de χ2. Se realizó el análisis univariante para determinar los posibles factores de riesgo de mortalidad y morbilidad. Las variables con significación estadística o cercanas a esta en el análisis univariante (p<0,10) fueron sometidas a un análisis de regresión logística para determinar los factores de riesgo independientes. La comparación entre sí de 2 variables continuas se realizó mediante las correlaciones bivariadas de Pearson. La conversión de variables continuas en categóricas dicotómicas se realizó aplicando las curvas ROC, y el cálculo del mejor punto de corte mediante el índice de Youden.
ResultadosUn total de 100 recién nacidos de menos de 1.500g fueron intervenidos de cierre quirúrgico de DAP en el periodo a estudio en nuestro hospital. Entre las características demográficas, clínicas, y de manejo perioperatorio cabe destacar que la edad gestacional media de los recién nacidos fue de 26,1±1,8 semanas, con predominio del sexo masculino (59%). La puntuación media en la ACCS modificada fue de 14,02±2,48. El peso medio al nacimiento fue de 823,5±191,9g, mientras que en el momento de la cirugía fue de 935,8±219,7g. La mediana de edad en el momento de la intervención fue de 15,5 (11-21) días. Más de la mitad de los niños necesitó administración de fármacos vasoactivos (54,2%) preoperatoriamente y un 48,4% en el postoperatorio inmediato. La mediana de días de intubación orotraqueal fue de 25 días (17,2-37,2), la de estancia en cuidados intensivos fue de 60 días (40-81,5), y en el hospital fue de 97 (65,5-127).
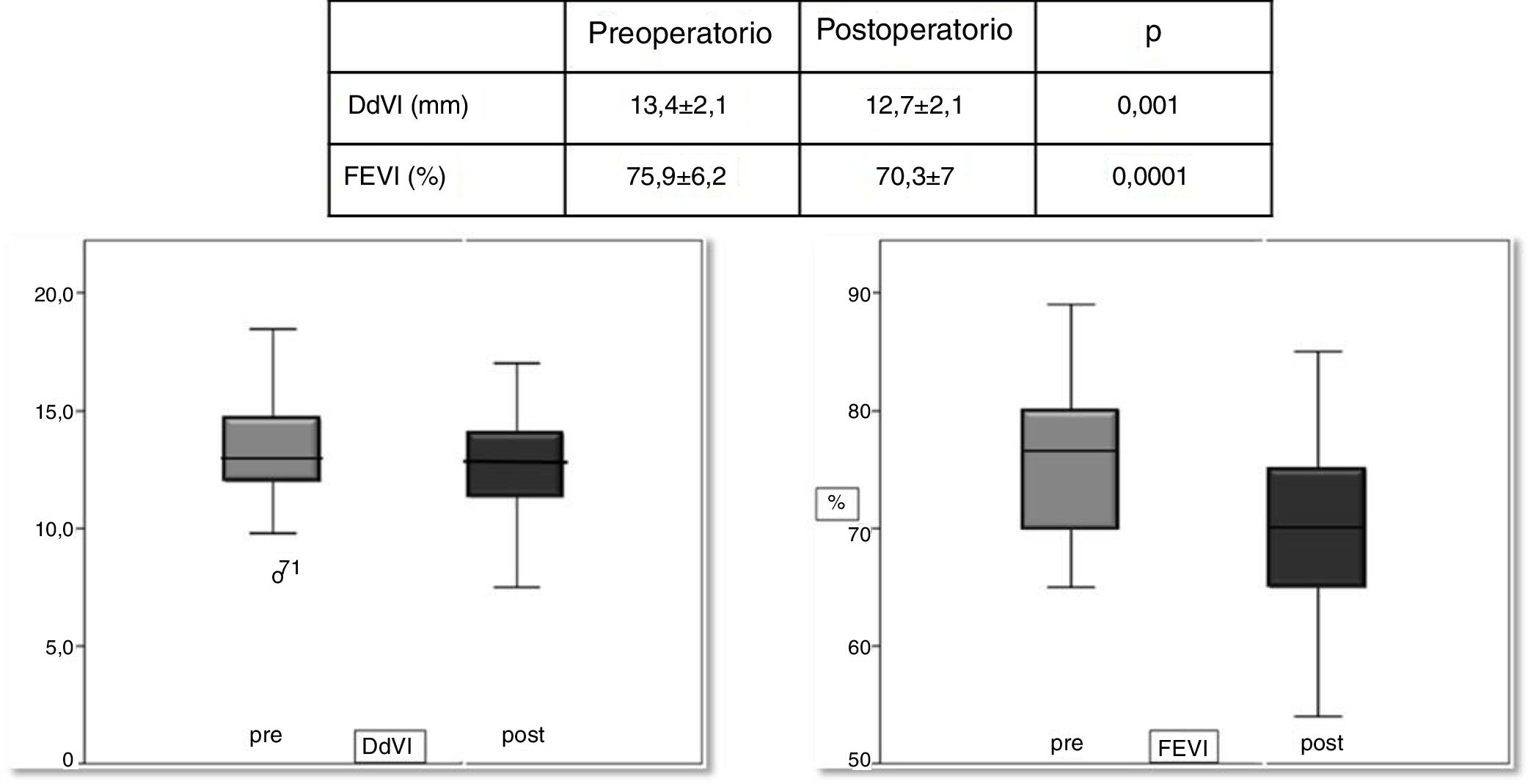
Los datos ecocardiográficos preoperatorios se tomaron 24horas antes de la intervención, siendo el tamaño medio del ductus 3,1±0,7mm con un rango de entre 2 y 5mm. La media de la relación entre aurícula izquierda y aorta para determinar la sobrecarga de volumen (Ai/Ao) fue de 1,5±0,25. El diámetro diastólico del ventrículo izquierdo (DdVI) medio fue de 13,4±2,1mm y la fracción de eyección de ventrículo izquierdo (FEVI) media fue de 75,9±6,2%.
Dentro del control ecocardiográfico a las 24horas, la media del DdVI fue de 12,7±2,13mm, mientras que la media de la FEVI fue de 70,3±7%.
La mortalidad hospitalaria fue del 19% (n=19), con una tasa de complicaciones precoces del 55,7%. Las causas de mortalidad no se asociaron a cirugía, no existiendo mortalidad intraoperatoria.
Ninguna variable ecocardiográfica fue significativa en el análisis univariado para la mortalidad. Sin embargo, al realizar este mismo análisis para morbilidad, encontramos que el DdVI (p=0,006) fue un factor predictor de complicaciones posquirúrgicas. Esta variable también resultó significativa en el análisis multivariado para la morbilidad (p=0,05; RR 1,59; IC: 0,99-2,53).
El análisis de mortalidad mediante curvas ROC mostró, entre los parámetros ecocardiográficos, que el peso en el momento de la cirugía tenía la mayor área bajo la curva (0,7) con un punto de corte óptimo de igual o menos de 820g, aunque de todos los factores de riesgo, el de mayor área bajo la curva fue el ACCS (0,91; con punto de corte óptimo para menos de 15).
Correlación pre-postoperatoria de datos ecocardiográficosAl analizar las diferencias para los valores de función y adaptabilidad (compliance) ventricular (FEVI y DdVI) antes y después de la intervención mediante correlaciones bivariadas, los resultados obtenidos muestran una disminución significativa de los valores postintervención respecto a los previos a la misma para la FEVI (p=0,0001) y para el DdVI (p=0,001) (fig. 1).
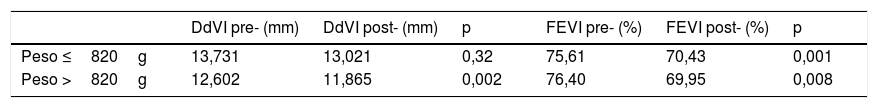
Se han aplicado las pruebas de correlación estadística pre-postoperatoria por subgrupos (divididos según punto de corte de curva ROC). En el análisis de estos subgrupos según peso en el momento de la intervención, obtuvimos diferencias estadísticamente significativas para DdVI en los pacientes con más de 820g (p=0,002), pero no en los de peso igual o menor de 820g (p=0,311). En cuanto a la FEVI, tanto en menos de 820g (p=0,001) como en más de 820g (p=0,008) se obtuvo una disminución significativa (tabla 1). Al comparar entre sí estos 2 subgrupos según el valor de cada parámetro ecocardiográfico se han encontrado diferencias significativas entre los 2 subgrupos respecto al DdVI prequirúrgico (p=0,037), mientras que el DdVI postoperatorio tiene tendencia hacia la significación (p=0,061), sin diferencias en la FEVI.
Correlación de medidas ecocardiográficas pre- y postoperatorias respecto a subgrupos de peso en el momento de la cirugía
| DdVI pre- (mm) | DdVI post- (mm) | p | FEVI pre- (%) | FEVI post- (%) | p | |
|---|---|---|---|---|---|---|
| Peso ≤820g | 13,731 | 13,021 | 0,32 | 75,61 | 70,43 | 0,001 |
| Peso >820g | 12,602 | 11,865 | 0,002 | 76,40 | 69,95 | 0,008 |
DdVI: diámetro telediastólico de ventrículo izquierdo; FEVI: fracción de eyección de ventrículo izquierdo; post: postoperatorio; pre: preoperatorio.
El análisis de los subgrupos según peso en el momento del nacimiento (valor de corte ≤900g) y según la puntuación en ACCS (valor de corte ≥15) no ha mostrado significación estadística para ninguna de las 2 variables analizadas.
DiscusiónEl cierre de DAP en prematuros afecta al corazón de estos al producir un cambio en la fisiología cardiovascular del recién nacido, incrementando la poscarga del ventrículo izquierdo y disminuyendo la precarga, resultando en una caída en el gasto del ventrículo izquierdo10. La adaptación de este a la nueva situación dependerá de la maduración del miocardio2,3. El miocardio inmaduro contiene menos fibras contráctiles por unidad de peso y el ventrículo izquierdo tiene menor adaptabilidad (compliance) en niños pretérmino que en niños a término4,11.
En nuestro estudio, en el análisis global de morbimortalidad, de todos los parámetros ecocardiográficos, únicamente el DdVI postoperatorio demostró ser factor predictor de morbilidad precoz. No se halló ninguna relación estadística respecto a la morbimortalidad ni con el tamaño, ni con la relación Ai/Ao, ni con la FEVI.
Las mediciones ecocardiográficas antes y después del cierre quirúrgico de DAP pueden darnos una idea de cómo se comporta el corazón del recién nacido. El-Khuffash et al.12 encuentran disminución significativa del DdVI en la primera hora y a las 18horas tras el cierre de ductus en su serie de prematuros, al igual que diferencias en la fracción de acortamiento en las medidas postoperatorias. Resultados similares hemos obtenido en nuestra población, obteniendo diferencias significativas en las mediciones pre-postoperatorias para los valoras de DdVI y de FEVI. Si usamos la DdVI como parámetro para valorar la precarga, nuestro estudio muestra un descenso significativo en la precarga tras la cirugía valorado a las 24horas (fig. 1) pasando de una media preoperatoria de 13,38 a 12,67mm en la medida postoperatoria (p=0,001). Tomando la FEVI como parámetro de valoración de la función ventricular izquierda también observamos una disminución significativa (75,87% vs. 70,28%, p=0,0001) 24horas después de la intervención (fig. 1). McNamara et al.9 describen también una reducción significativa en la precarga del ventrículo izquierdo (disminución en DdVI y Ai/Ao tras la intervención) y un descenso en la contractilidad del ventrículo izquierdo (reducción en fracción de acortamiento y en gasto del ventrículo izquierdo) con un descenso máximo a las 8horas tras la intervención.
Comparación de neonatos de menos de 820g frente a más de 820gLos recién nacidos de muy bajo peso al nacimiento son menos capaces de compensar los cambios hemodinámicos y son más propensos a desarrollar fallo ventricular izquierdo13. El miocardio inmaduro muestra un estado contráctil basal mayor y una mayor sensibilidad a los cambios en la pre- y poscarga14-16. La intolerancia de este miocardio a estas variaciones puede deberse a diferencias en la arquitectura de las miofibras o inmadurez de los receptores de desarrollo o de regulación17. Existen estudios que reflejan una repuesta limitada del ventrículo izquierdo a los cambios de volumen en el periodo neonatal18.
McNamara et al.9, al comparar neonatos de menos de 1.000g frente a otros con más de 1.000g de peso, encuentran que la frecuencia de pacientes con fracción de acortamiento de menos del 25% y con gasto cardiaco de ventrículo izquierdo de menos de 170ml·kg−1·min−1 fue mayor en el grupo de menos de 1.000g, lo que sugiere que la maduración del miocardio es un elemento importante en la respuesta al cierre del DAP. Nuestros datos muestran que los pacientes con menos de 820g en el momento de la intervención manejan peor los cambios de volumen asociados al cierre quirúrgico del DAP, de forma que se produce una caída significativa en la FEVI (p=0,001) sin disminución del DdVI (p=0,3), lo que indicaría una dilatación del ventrículo izquierdo mantenida tras la intervención, mientras que en los de más de 820g también se produce una disminución significativa tanto en la FEVI (p=0,008) como en el DdVI (p=0,02), lo que reflejaría una mejor adaptación a los cambios de volumen tras la cirugía en este grupo de neonatos de mayor madurez.
ConclusiónPor lo tanto, podemos concluir que los recién nacidos prematuros tienen un peor manejo de la sobrecarga de volumen producida por el DAP a causa de la inmadurez miocárdica y que el cierre quirúrgico del DAP provoca un descenso en la precarga, que en estos pacientes se refleja en una peor adaptación a los cambios de volumen tras la cirugía en relación directa con el peso en el momento de la intervención; esto es, a menor peso, peor capacidad de adaptación, valorado desde el punto de vista ecocardiográfico.
Conflicto de interesesLos autores declaran no tener ningún conflicto de intereses.