El implante valvular aórtico transcatéter (TAVI) ha mostrado resultados excelentes, constituyendo una alternativa terapéutica a la sustitución valvular aórtica para pacientes de riesgo quirúrgico alto o excesivo. Sin embargo, no existe un claro consenso sobre los beneficios del TAVI en pacientes con riesgo quirúrgico intermedio. Realizamos una revisión sistemática de la literatura y el consiguiente metaanálisis considerando resultados periprocedimiento y en el seguimiento máximo disponible.
MétodosSe realizó una búsqueda bibliográfica combinando 3 grupos de palabras clave: «TAVR/TAVI/transcatheter aortic valve implantation/transcatheter aortic valve replacement» AND «intermediate risk» AND «aortic valve replacement/AVR/surgery». Fueron considerados los trabajos publicados en los últimos 6 años.
ResultadosFueron seleccionados 21 trabajos: 4 estudios prospectivos aleatorizados y 17 estudios observacionales, 13 de ellos ajustados por análisis de propensiones. No existieron diferencias significativas en la mortalidad (RR=1; IC95%: 0,99-1,02) o incidencia de accidente cerebrovascular (RR=0,96; IC95%: 0,77-1,20) en el seguimiento máximo (1-3 años). La lesión vascular (accidente cerebrovascular) grave fue significativamente mayor en el grupo TAVI (RR=4,39; IC95%: 2,17-8,91), así como la necesidad de implante de marcapasos permanente (RR=2,96; IC95%: 2-4,36) y la incidencia de fuga paravalvular significativa (≥2+; RR=6,83; IC95%: 4,64-10,05). Tanto la incidencia de fibrilación auricular (RR=0,39; IC95%: 0,25-0,61) como de fallo renal (RR=0,45; IC95%: 0,28-0,72) fueron superiores en el grupo quirúrgico.
ConclusionesTras comparar TAVI frente a la sustitución valvular aórtica en pacientes con riesgo quirúrgico intermedio mediante metaanálisis, no se han identificado diferencias significativas en términos de mortalidad o accidente cerebrovascular a lo largo del seguimiento. Sin embargo, el diferente perfil de complicaciones de cada una de las técnicas debería guiar la selección de pacientes realizada por el Heart-Team para reducir la morbilidad posprocedimiento.
Transcatheter aortic valve implantation (TAVI) has shown excellent results, and is a therapeutic alternative to aortic valve replacement for high or excessive surgical risk patients. However, there is no clear consensus about the benefits of TAVI for patients with intermediate surgical risk. A systematic review of literature and subsequent meta-analysis was carried out considering outcomes after the procedure and during the maximum available follow-up.
MethodsA systematic review of literature was performed, combining three clusters of Keywords: “TAVR/TAVI/transcatheter aortic valve implantation/transcatheter aortic valve replacement “AND “intermediate risk” AND “aortic valve replacement/AVR/surgery”. Studies published in the last 6 years were considered for analysis.
ResultsA total of 21 studies were included in the analysis, of which 4 were randomised controlled trials and 17 were observation studies, with 13 of them being propensity-score adjusted. No differences were found in terms of mortality (RR=1.00, 95% CI: 0.99-1.02) or incidence of cerebrovascular accident (RR=0.96, 95% CI: 0.77-1.20) during the maximum follow-up (1-3 years). A major vascular lesion (cerebrovascular accident) (RR=4.39, 95% CI: 2.17-8.91), need of permanent pacemaker implantation (RR=2.96, 95% CI: 2.00-4.36), and residual significant paravalvular leak (≥2+; RR=6.83, 95% CI: 4.64-10.05) were significantly higher in TAVI group. The incidence of atrial fibrillation (RR=0.39, 95% CI: 0.25-0.61) and kidney failure (RR=0,45, 95% CI: 0.28-0.72) were higher in the surgical group.
ConclusionsAfter comparing TAVI and aortic valve replacement in patients with intermediate surgical risk using meta-analysis, no significatant differences were identified in terms of mortality or cerebrovascular accident during follow-up. However, the different profile of complications of each technique should guide patient selection by the Heart-Team in order to reduce post-procedural morbidity.
El implante valvular aórtico transcatéter (TAVI) ha mostrado buenos resultados en sus 3 lustros de existencia, planteándose como una alternativa terapéutica al tratamiento quirúrgico convencional. Sin embargo, la evidencia de resultados a largo plazo es todavía limitada en comparación con los de la sustitución valvular aórtica quirúrgica por bioprótesis. Además, la presentación de la enfermedad valvular aórtica abarca un amplio espectro de perfiles clínicos de pacientes lo cual exige la individualización de las indicaciones.
Múltiples estudios han demostrado los beneficios del TAVI1 en pacientes de alto riesgo quirúrgico (STS-PROM>10% y/o EuroSCORE I logístico>20%) y aquellos considerados inoperables por un equipo multidisciplinar o Heart-Team, por encima del tratamiento quirúrgico o la abstinencia terapéutica. Sin embargo, la extensión de indicaciones del TAVI hacia pacientes con riesgo quirúrgico intermedio o bajo debe considerar la experiencia limitada del comportamiento del TAVI en el seguimiento a largo plazo y la necesidad de presentar resultados equiparables a los de la técnica quirúrgica en pacientes de similar perfil de riesgo.
La reciente publicación del seguimiento a 2 años de los estudio PARTNER22 y US-PIVOTAL3 han revelado mejores resultados del grupo TAVI para eventos de mortalidad y accidente cerebrovascular (ACV) tanto periprocedimiento como en el seguimiento mantenido. Sin embargo, aspectos como la necesidad de implante de marcapasos posprocedimiento, la tasa de complicaciones vasculares o las fugas paravalvulares en grado ligero o superior continúan penalizando la técnica percutánea frente a la alternativa quirúrgica. En particular, la implicación clínica en un seguimiento más prolongado de las fugas paravalvulares no está bien establecida, consideradas con impacto clínicamente significativo aquellas con grado moderado o superior4 pero existiendo ya evidencia sobre el impacto de las fugas en grado ligero3 y la progresión o aparición de novo de estas hasta en un 25% de los casos5.
Por su lado, la alternativa quirúrgica ha experimentado una notable evolución en los últimos tiempos con la difusión de estrategias mínimamente invasivas tanto en las técnicas quirúrgicas como de perfusión con circulación extracorpórea así como la extensión del uso de prótesis de implante rápido y sin sutura con datos que indican una significativa mejoría de los resultados perioperatorios6.
En este estudio tratamos de actualizar y sintetizar la evidencia disponible de los resultados del TAVI frente al tratamiento quirúrgico convencional en pacientes con riesgo quirúrgico intermedio en el seguimiento máximo disponible mediante estudio de metaanálisis.
MétodosRevisión bibliográficaSe realizó una búsqueda bibliográfica sistemática en MedLine® utilizando diferentes combinaciones de palabras clave distribuidas en 3 grupos: «TAVR/TAVI/transcatheter aortic valve implantation/transcatheter aortic valve replacement» AND «intermediate risk» AND «aortic valve replacement/AVR/surgery». Fueron considerados los trabajos publicados en los últimos 6 años y hasta el 28 de febrero de 2018.
Selección de estudiosLa selección de trabajos fue realizada por 2 investigadores independientes. Un cribado preliminar por títulos y resúmenes fue llevado a cabo por cada uno de los investigadores de forma independiente. Las diferencias surgidas entre ambos fueron solucionadas por discusión entre ellos. Solo en aquellos trabajos considerados como válidos por ambos fue valorada su elegibilidad por medio del análisis del manuscrito completo. Fueron incluidos en el estudio los trabajos con los siguientes criterios:
- •
Escritos en lengua inglesa y/o castellano.
- •
Estudios comparativos de TAVI y cirugía en pacientes con estenosis aórtica severa.
- •
Grupos comparables en características preintervención, dándose preferencia a aquellas estrategias de aleatorización en la asignación de los grupos de estudio o remuestreo por técnica de análisis de propensiones en el caso de los trabajos no aleatorizados.
- •
Expresión de riesgo quirúrgico estimado por scores de riesgo siendo este para ambos grupos de estudio<20% para EuroSCORE I logístico y/o<10% para STS-PROM.
- •
Expresión de resultados de mortalidad y/o incidencia de ACV a lo largo del seguimiento.
- •
Al menos 20 pacientes en cada uno de los grupos de estudio.
Ambos investigadores obtuvieron los datos de los trabajos de forma independiente, realizando un análisis y discusión de los mismos conjuntamente. Las características y variables consideradas en el estudio extraídas de los trabajos fueron las siguientes: diseño del estudio; año de publicación; número de pacientes incluidos y asignados a cada uno de los grupos de estudio; periodo de inclusión/aleatorización; máximo seguimiento; riesgo quirúrgico medio de los pacientes incluidos en cada uno de los grupos de estudio; tipo de prótesis implantadas; vía de abordaje para el implante en el caso del grupo TAVI; tasa de mortalidad y de ACV en el seguimiento máximo; tasa de lesión vascular grave periprocedimiento (o en su defecto sangrado grave atribuible a lesión vascular según criterios VARC), necesidad de implante de marcapasos permanente posprocedimiento, tasa de fuga paravalvular posprocedimiento grado≥2+, incidencia de fibrilación auricular (FA) de nueva aparición posprocedimiento y tasa de fallo renal posprocedimiento con o sin necesidad de terapia renal sustitutiva.
Los resultados de mortalidad y ACV de los pacientes fueron considerados según el grupo al que fueron preliminarmente asignados/aleatorizados si bien se consideraron los resultados según el tratamiento recibido (TAVI o cirugía) en aquellos trabajos donde los datos no fueron expresados por intención de tratar.
Los resultados de mortalidad fueron considerados como mortalidad por todas las causas a lo largo del seguimiento. Asimismo, el ACV fue considerado en cualquiera de sus formas de presentación clínica. Estos resultados fueron analizados para los pacientes asignados al grupo TAVI de forma conjunta, independientemente de la vía de abordaje. En el caso de los pacientes asignados al grupo quirúrgico, no se hizo distinción según variantes en la estrategia llevada a cabo como implante de prótesis convencional o sin sutura/de implante rápido, así como tampoco se consideró de forma independiente la utilización de abordajes mínimamente invasivos. Los datos de lesión vascular grave, necesidad de implante de marcapasos permanente o fuga paravalvular grado≥2+fueron valorados preferentemente en las fases precoces posprocedimiento (previo al alta hospitalaria o en los primeros 30 días), si bien en aquellos trabajos en los que solo fue comunicado el resultado al final del seguimiento también fueron incluidos ya que la tasa de desarrollo de estas complicaciones presenta ligeros cambios. Además, los pacientes con fuga paravalvular significativa presentan un peor pronóstico de supervivencia en el seguimiento, pudiendo quedar esta complicación infraestimada de no considerar los datos más precoces.
Análisis estadístico y síntesis de datosSe llevó a cabo un metaanálisis de acuerdo con las recomendaciones de la Cochrane Handbook for Systematic Reviews of Interventions, versión 5.0.2, utilizando el programa Review Manager, versión 5.3. Los resultados de las variables continuas fueron expresados como media±desviación estándar. Los resultados de las variables dicotómicas fueron expresados como número de eventos respecto del total de pacientes. Siempre que fue posible se utilizaron los valores absolutos de los eventos ocurridos para cada uno de los resultados de mortalidad y ACV, obtenidos al final del seguimiento máximo, permitiendo calcular el riesgo relativo (RR) combinado para cada uno de los eventos adversos. Se aplicó el método de estadístico de Mantel-Haenszel para variables no continuas para un modelo de efectos aleatorios en la síntesis de los datos. Para evaluar la presencia de sesgos de publicación utilizamos el test de correlación de Begg y funnel-plot. Se evaluó la heterogeneidad utilizando el estadístico I2, considerando como no aceptables los valores mayores del 85%.
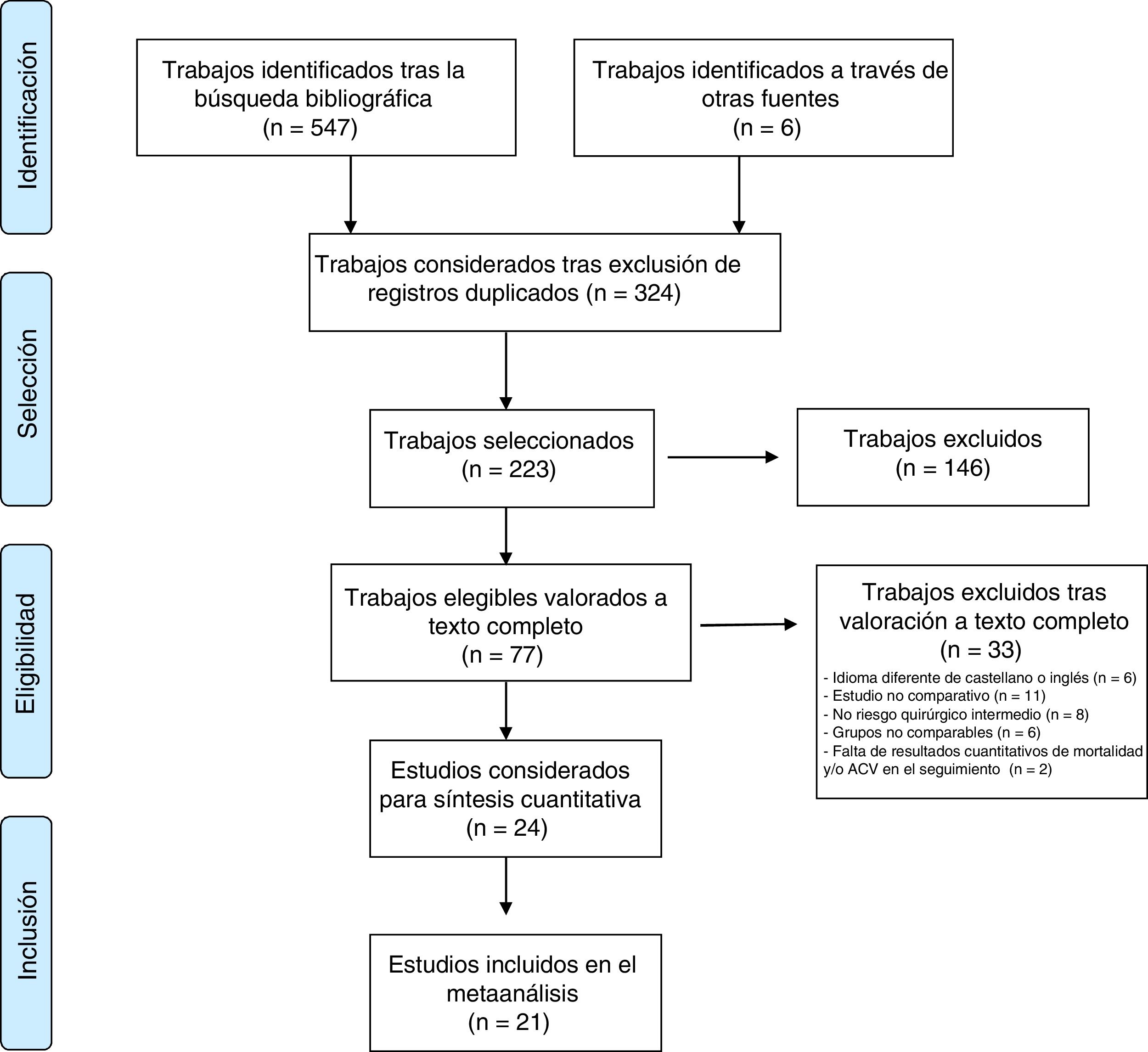
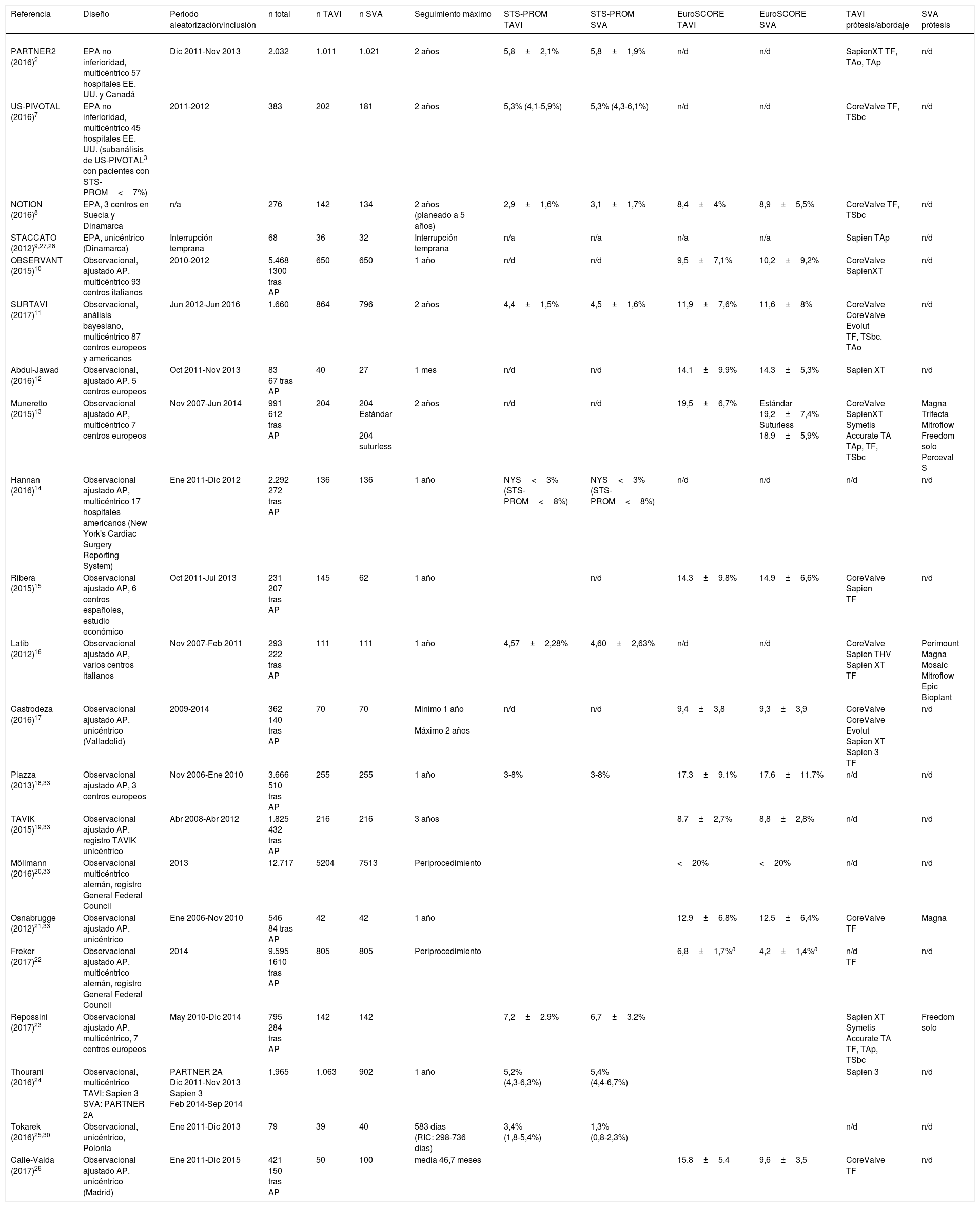
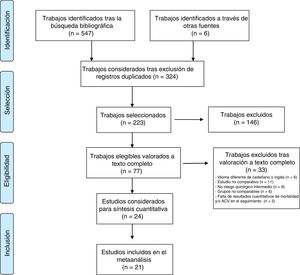
ResultadosSelección de estudios y datos de estudioEl proceso de selección de estudios queda resumido en el diagrama PRISMA de la figura 1. Finalmente, fueron seleccionados 21 trabajos: 4 estudios prospectivos aleatorizados (EPA)2,7–9 y 17 estudios observacionales10–26, 13 de los cuales ajustados por análisis de propensiones10,12–19,21–23,26, que se resumen en la tabla 1. Fueron seleccionados adicionalmente 9 metaanálisis preexistentes27–35 cuyos datos complementaron los obtenidos de los diferentes trabajos (ver resumen en tabla 2). En el caso del estudio US-PIVOTAL3, fue seleccionado un trabajo7 que incluye un subanálisis de pacientes con riesgo quirúrgico STS-PROM<7%, al tratarse la serie original de un estudio con población más heterogénea y predominio de riesgo quirúrgico alto. El estudio US-PIVOTAL original fue, por lo tanto, excluido a fin de evitar duplicidad/solapamiento de pacientes. Fue tolerado el solapamiento existente en el trabajo de Thourani24, que comparte el grupo quirúrgico con parte de los pacientes incluidos en el estudio PARTNER22, siendo diferente el grupo de pacientes incluidos en el grupo TAVI de ambos estudios.
Resumen de características de trabajos incluidos en el estudio
| Referencia | Diseño | Periodo aleatorización/inclusión | n total | n TAVI | n SVA | Seguimiento máximo | STS-PROM TAVI | STS-PROM SVA | EuroSCORE TAVI | EuroSCORE SVA | TAVI prótesis/abordaje | SVA prótesis |
|---|---|---|---|---|---|---|---|---|---|---|---|---|
| PARTNER2 (2016)2 | EPA no inferioridad, multicéntrico 57 hospitales EE. UU. y Canadá | Dic 2011-Nov 2013 | 2.032 | 1.011 | 1.021 | 2 años | 5,8±2,1% | 5,8±1,9% | n/d | n/d | SapienXT TF, TAo, TAp | n/d |
| US-PIVOTAL (2016)7 | EPA no inferioridad, multicéntrico 45 hospitales EE. UU. (subanálisis de US-PIVOTAL3 con pacientes con STS-PROM<7%) | 2011-2012 | 383 | 202 | 181 | 2 años | 5,3% (4,1-5,9%) | 5,3% (4,3-6,1%) | n/d | n/d | CoreValve TF, TSbc | n/d |
| NOTION (2016)8 | EPA, 3 centros en Suecia y Dinamarca | n/a | 276 | 142 | 134 | 2 años (planeado a 5 años) | 2,9±1,6% | 3,1±1,7% | 8,4±4% | 8,9±5,5% | CoreValve TF, TSbc | n/d |
| STACCATO (2012)9,27,28 | EPA, unicéntrico (Dinamarca) | Interrupción temprana | 68 | 36 | 32 | Interrupción temprana | n/a | n/a | n/a | n/a | Sapien TAp | n/d |
| OBSERVANT (2015)10 | Observacional, ajustado AP, multicéntrico 93 centros italianos | 2010-2012 | 5.468 1300 tras AP | 650 | 650 | 1 año | n/d | n/d | 9,5±7,1% | 10,2±9,2% | CoreValve SapienXT | n/d |
| SURTAVI (2017)11 | Observacional, análisis bayesiano, multicéntrico 87 centros europeos y americanos | Jun 2012-Jun 2016 | 1.660 | 864 | 796 | 2 años | 4,4±1,5% | 4,5±1,6% | 11,9±7,6% | 11,6±8% | CoreValve CoreValve Evolut TF, TSbc, TAo | n/d |
| Abdul-Jawad (2016)12 | Observacional, ajustado AP, 5 centros europeos | Oct 2011-Nov 2013 | 83 67 tras AP | 40 | 27 | 1 mes | n/d | n/d | 14,1±9,9% | 14,3±5,3% | Sapien XT | n/d |
| Muneretto (2015)13 | Observacional ajustado AP, multicéntrico 7 centros europeos | Nov 2007-Jun 2014 | 991 612 tras AP | 204 | 204 Estándar 204 suturless | 2 años | n/d | n/d | 19,5±6,7% | Estándar 19,2±7,4% Suturless 18,9±5,9% | CoreValve SapienXT Symetis Accurate TA TAp, TF, TSbc | Magna Trifecta Mitroflow Freedom solo Perceval S |
| Hannan (2016)14 | Observacional ajustado AP, multicéntrico 17 hospitales americanos (New York's Cardiac Surgery Reporting System) | Ene 2011-Dic 2012 | 2.292 272 tras AP | 136 | 136 | 1 año | NYS<3% (STS-PROM<8%) | NYS<3% (STS-PROM<8%) | n/d | n/d | n/d | n/d |
| Ribera (2015)15 | Observacional ajustado AP, 6 centros españoles, estudio económico | Oct 2011-Jul 2013 | 231 207 tras AP | 145 | 62 | 1 año | n/d | 14,3±9,8% | 14,9±6,6% | CoreValve Sapien TF | n/d | |
| Latib (2012)16 | Observacional ajustado AP, varios centros italianos | Nov 2007-Feb 2011 | 293 222 tras AP | 111 | 111 | 1 año | 4,57±2,28% | 4,60±2,63% | n/d | n/d | CoreValve Sapien THV Sapien XT TF | Perimount Magna Mosaic Mitroflow Epic Bioplant |
| Castrodeza (2016)17 | Observacional ajustado AP, unicéntrico (Valladolid) | 2009-2014 | 362 140 tras AP | 70 | 70 | Minimo 1 año Máximo 2 años | n/d | n/d | 9,4±3,8 | 9,3±3,9 | CoreValve CoreValve Evolut Sapien XT Sapien 3 TF | n/d |
| Piazza (2013)18,33 | Observacional ajustado AP, 3 centros europeos | Nov 2006-Ene 2010 | 3.666 510 tras AP | 255 | 255 | 1 año | 3-8% | 3-8% | 17,3±9,1% | 17,6±11,7% | n/d | n/d |
| TAVIK (2015)19,33 | Observacional ajustado AP, registro TAVIK unicéntrico | Abr 2008-Abr 2012 | 1.825 432 tras AP | 216 | 216 | 3 años | 8,7±2,7% | 8,8±2,8% | n/d | n/d | ||
| Möllmann (2016)20,33 | Observacional multicéntrico alemán, registro General Federal Council | 2013 | 12.717 | 5204 | 7513 | Periprocedimiento | <20% | <20% | n/d | n/d | ||
| Osnabrugge (2012)21,33 | Observacional ajustado AP, unicéntrico | Ene 2006-Nov 2010 | 546 84 tras AP | 42 | 42 | 1 año | 12,9±6,8% | 12,5±6,4% | CoreValve TF | Magna | ||
| Freker (2017)22 | Observacional ajustado AP, multicéntrico alemán, registro General Federal Council | 2014 | 9.595 1610 tras AP | 805 | 805 | Periprocedimiento | 6,8±1,7%a | 4,2±1,4%a | n/d TF | n/d | ||
| Repossini (2017)23 | Observacional ajustado AP, multicéntrico, 7 centros europeos | May 2010-Dic 2014 | 795 284 tras AP | 142 | 142 | 7,2±2,9% | 6,7±3,2% | Sapien XT Symetis Accurate TA TF, TAp, TSbc | Freedom solo | |||
| Thourani (2016)24 | Observacional, multicéntrico TAVI: Sapien 3 SVA: PARTNER 2A | PARTNER 2A Dic 2011-Nov 2013 Sapien 3 Feb 2014-Sep 2014 | 1.965 | 1.063 | 902 | 1 año | 5,2% (4,3-6,3%) | 5,4% (4,4-6,7%) | Sapien 3 | n/d | ||
| Tokarek (2016)25,30 | Observacional, unicéntrico, Polonia | Ene 2011-Dic 2013 | 79 | 39 | 40 | 583 días (RIC: 298-736 días) | 3,4% (1,8-5,4%) | 1,3% (0,8-2,3%) | n/d | n/d | ||
| Calle-Valda (2017)26 | Observacional ajustado AP, unicéntrico (Madrid) | Ene 2011-Dic 2015 | 421 150 tras AP | 50 | 100 | media 46,7 meses | 15,8±5,4 | 9,6±3,5 | CoreValve TF | n/d |
AP: análisis de prospecciones; EPA: estudio prospectivo aleatorizado; n/a: no aplicable; n/d: no disponible; RIC: rango intercuartílico; SVA: sustitución valvular aórtica; TAo: transaórtico; TAp: transapical; TAVI: implante de válvula aórtica transcatéter; TF: transfemoral; TSbc: transubclavio.
a EuroSCORE II.
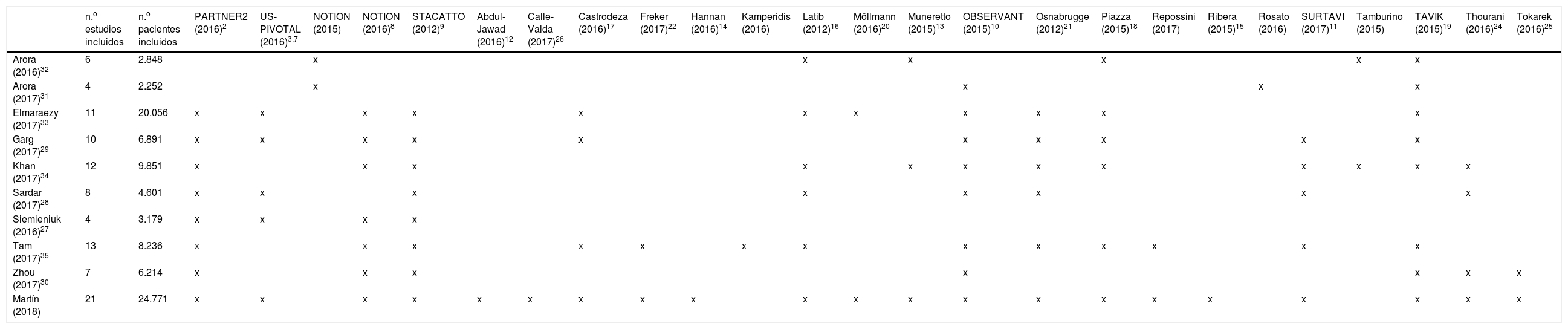
Resumen de metaanálisis publicados en los últimos 3 años y de los estudios incluidos en los mismos
| n.o estudios incluidos | n.o pacientes incluidos | PARTNER2 (2016)2 | US-PIVOTAL (2016)3,7 | NOTION (2015) | NOTION (2016)8 | STACATTO (2012)9 | Abdul-Jawad (2016)12 | Calle-Valda (2017)26 | Castrodeza (2016)17 | Freker (2017)22 | Hannan (2016)14 | Kamperidis (2016) | Latib (2012)16 | Möllmann (2016)20 | Muneretto (2015)13 | OBSERVANT (2015)10 | Osnabrugge (2012)21 | Piazza (2015)18 | Repossini (2017) | Ribera (2015)15 | Rosato (2016) | SURTAVI (2017)11 | Tamburino (2015) | TAVIK (2015)19 | Thourani (2016)24 | Tokarek (2016)25 | |
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| Arora (2016)32 | 6 | 2.848 | x | x | x | x | x | x | |||||||||||||||||||
| Arora (2017)31 | 4 | 2.252 | x | x | x | x | |||||||||||||||||||||
| Elmaraezy (2017)33 | 11 | 20.056 | x | x | x | x | x | x | x | x | x | x | x | ||||||||||||||
| Garg (2017)29 | 10 | 6.891 | x | x | x | x | x | x | x | x | x | x | |||||||||||||||
| Khan (2017)34 | 12 | 9.851 | x | x | x | x | x | x | x | x | x | x | x | x | |||||||||||||
| Sardar (2017)28 | 8 | 4.601 | x | x | x | x | x | x | x | x | |||||||||||||||||
| Siemieniuk (2016)27 | 4 | 3.179 | x | x | x | x | |||||||||||||||||||||
| Tam (2017)35 | 13 | 8.236 | x | x | x | x | x | x | x | x | x | x | x | x | x | ||||||||||||
| Zhou (2017)30 | 7 | 6.214 | x | x | x | x | x | x | x | ||||||||||||||||||
| Martín (2018) | 21 | 24.771 | x | x | x | x | x | x | x | x | x | x | x | x | x | x | x | x | x | x | x | x | x |
La mayoría de los trabajos han sido publicados en los últimos 3 años. Destaca el carácter multicéntrico de los estudios, siendo 3 de los 4 trabajos aleatorizados2,7,8 y 11 de los 16 observacionales10–16,18,20,22–24. La mayor parte de la evidencia considerada procede de centros americanos (EE. UU. y Canadá) y europeos, destacando la contribución en estos últimos de centros italianos y escandinavos. En 3 trabajos, la evidencia tiene una procedencia íntegra de centros de nuestro país15,17,26. Los periodos de inclusión/aleatorización no superan los 2 años en la mayoría de los trabajos, si bien en 4 de ellos este tiempo es más prolongado y se remonta hasta 2006-7 en 4 estudios13,16,18,21. El número de pacientes incluidos es limitado, incluso en los EPA, donde se concentra el principal volumen de pacientes en el estudio PARTNER22. El tamaño de los estudios observacionales es más homogéneo si bien la mayor parte sufre una gran reducción del tamaño efectivo de pacientes incluidos en el estudio al aplicar el remuestreo por análisis de propensiones. La excepción la establece el trabajo de Möllman et al.20 con un número de pacientes muy superior al del resto de trabajos observacionales, exigiendo la realización de reanálisis para comprobar su influencia sobre la magnitud de efecto y el análisis de heterogeneidad en cada uno de los subanálisis realizados. El seguimiento máximo fue mayoritariamente de un año, superándolo en 8 trabajos, 7 de ellos con seguimiento igual o superior a 2 años2,7,8,11,19,25,26. Los riesgos quirúrgicos medios de los pacientes fueron comparables entre los pacientes asignados a cada uno de los grupos de estudio y se encontraron dentro del rango considerado como riesgo quirúrgico intermedio (STS-PROM 3-8% y EuroSCORE I logístico 10-20%). El tipo de prótesis implantada fue irregular, particularmente en el caso de las prótesis del grupo quirúrgico donde solo se comunican en 2 trabajos. La mayoría de los implantes de TAVI se concentra en las diferentes generaciones de Edwards Sapien (Edwards Lifesciences, Irvine, CA, EE. UU.) y de Medtronic Corevalve (Medtronic, Minneapolis, MN, EE. UU.), predominando el abordaje vía transfemoral siendo incluso exclusivo en el diseño de algunos trabajos6,12,15–17,21,22.
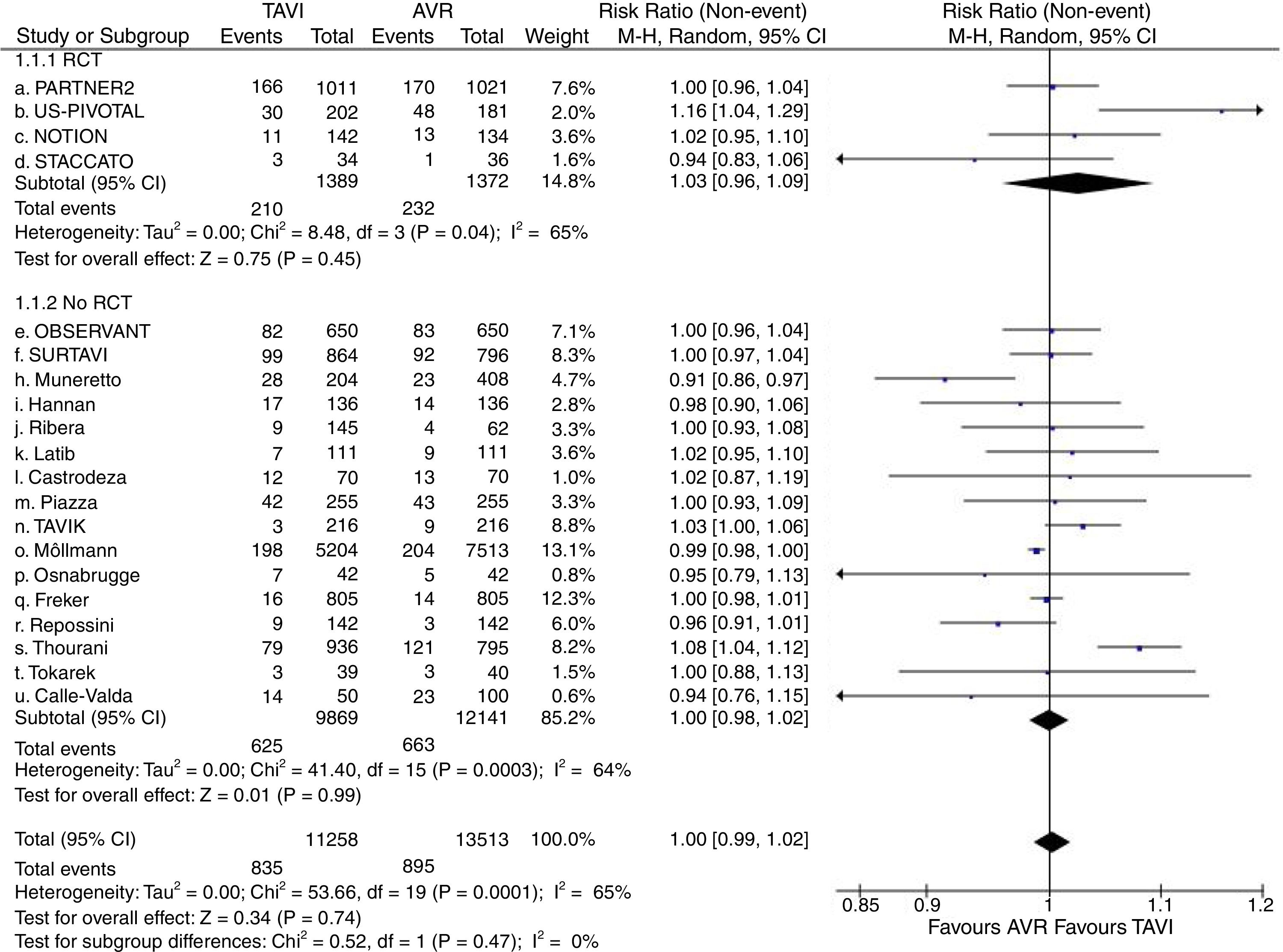
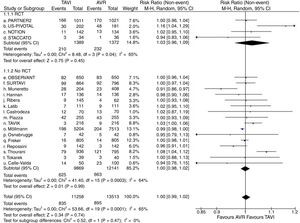
Resultado de mortalidadVeinte estudios (4 EPA2,7–9 y 16 observacionales10,11,13–26) contenían datos de mortalidad en el seguimiento. El análisis incluyó un total de 24.771 pacientes (11.258 en grupo TAVI y 13.513 en grupo quirúrgico), presentando 835 (7,42%) fallecidos entre los asignados al grupo TAVI y 895 (6,6%) entre los intervenidos quirúrgicamente. El modelo no mostró diferencias significativas en términos de supervivencia entre ambas alternativas de tratamiento (RR=1; IC95%: 0,99-1,02; I2=65%) (fig. 2). No existieron diferencias significativas en el subanálisis de EPA y observacionales así como tampoco se produjo modificación significativa de la magnitud de efecto ni del análisis de heterogeneidad al excluir del metaanálisis al trabajo de Möllman et al.20. El test de Begg (p=0,586) no mostró sesgo de publicación y fue aplicado funnel-plot para la selección de trabajos incluidos en el análisis a efectos de minimizar este sesgo.
Diagrama de árbol de mortalidad en el seguimiento máximo de TAVI versus sustitución valvular aórtica en pacientes con riesgo quirúrgico intermedio. AVR: sustitución valvular aórtica; M-H: Mantel-Haenszel; RCT: estudio prospectivo aleatorizado; TAVI: implante valvular aórtico transcatéter; 95% IC: intervalo de confianza al 95%.
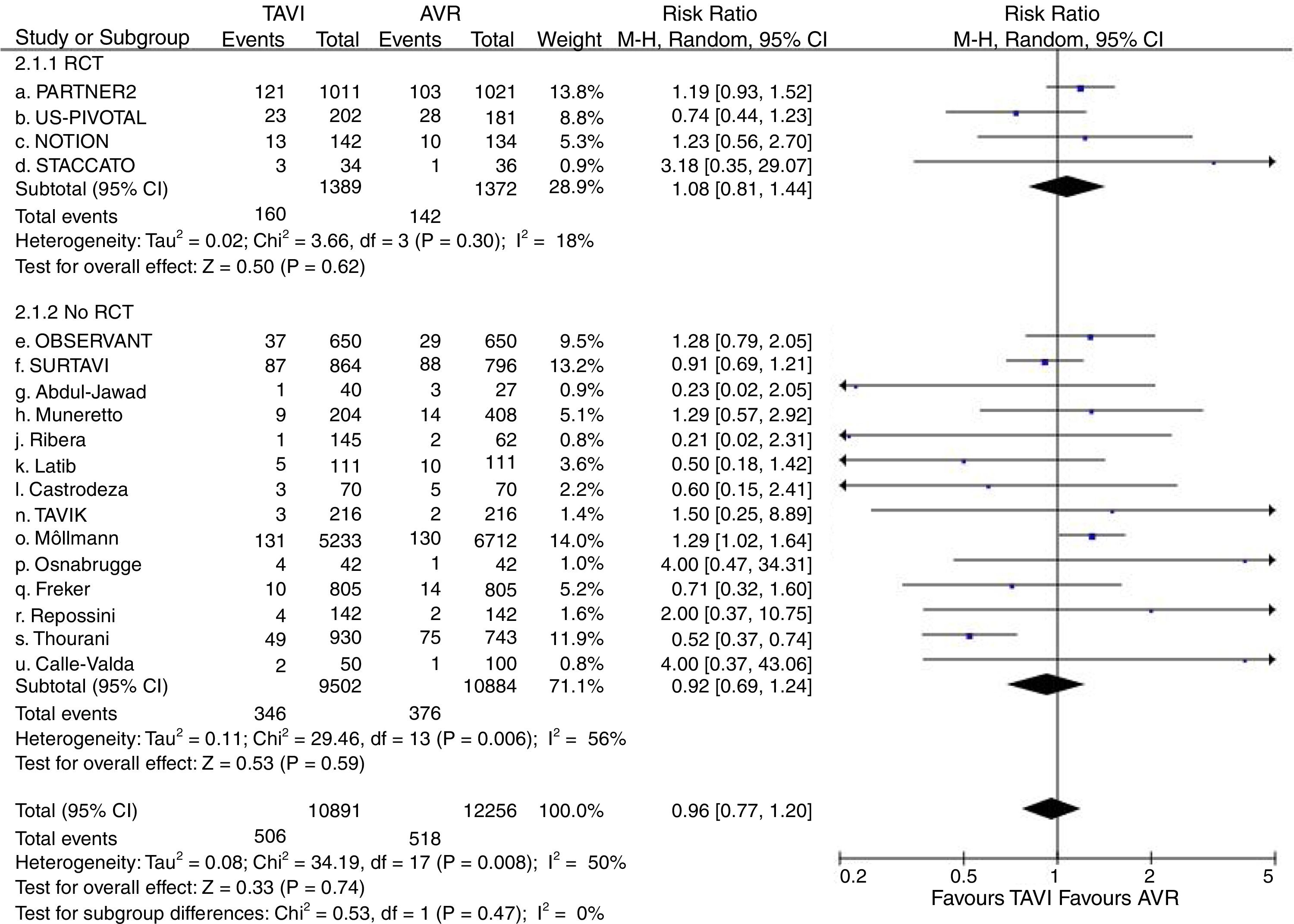
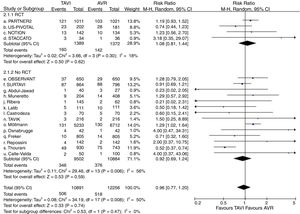
Dieciocho estudios (4 EPA2,7–9 y 14 observacionales10–13,15–24,26) contenían datos válidos de incidencia de ACV en el seguimiento. Fueron considerados 23.147 pacientes (10.891 en grupo TAVI y 12.256 en grupo quirúrgico), presentando ACV 506 (4,64%) de los asignados al grupo TAVI y 518 (4,23%) de los intervenidos quirúrgicamente. En el análisis no se evidenciaron diferencias significativas en la incidencia de ACV entre ambas alternativas de tratamiento (RR=0,96; IC95%: 0,77-1,20; I2=50%) (fig. 3). No existieron diferencias significativas en el subanálisis de EPA y observacionales así como tampoco se produjo modificación significativa de la magnitud de efecto ni del análisis de heterogeneidad al excluir del metaanálisis al trabajo de Möllman et al.20. El test de Begg (p=0,312) no mostró sesgo de publicación y fue aplicado funnel-plot para la selección de trabajos incluidos en el análisis a efectos de minimizar este sesgo.
Diagrama de árbol de incidencia de accidente cerebrovascular en el seguimiento máximo de TAVI versus sustitución valvular aórtica en pacientes con riesgo quirúrgico intermedio. AVR: sustitución valvular aórtica; M-H: Mantel-Haenszel; RCT: estudio prospectivo aleatorizado; TAVI: implante valvular aórtico transcatéter; 95% IC: intervalo de confianza al 95%.
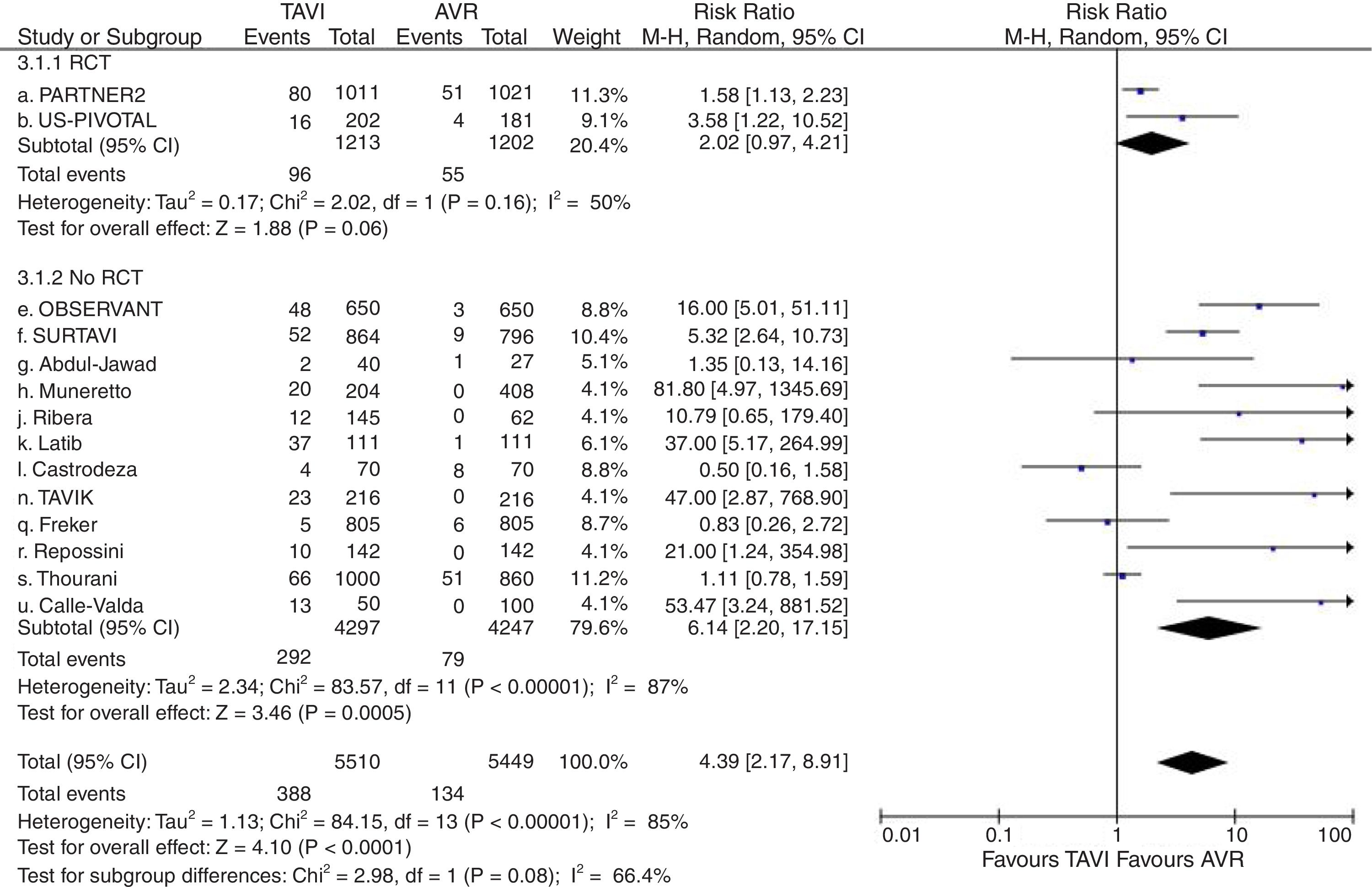
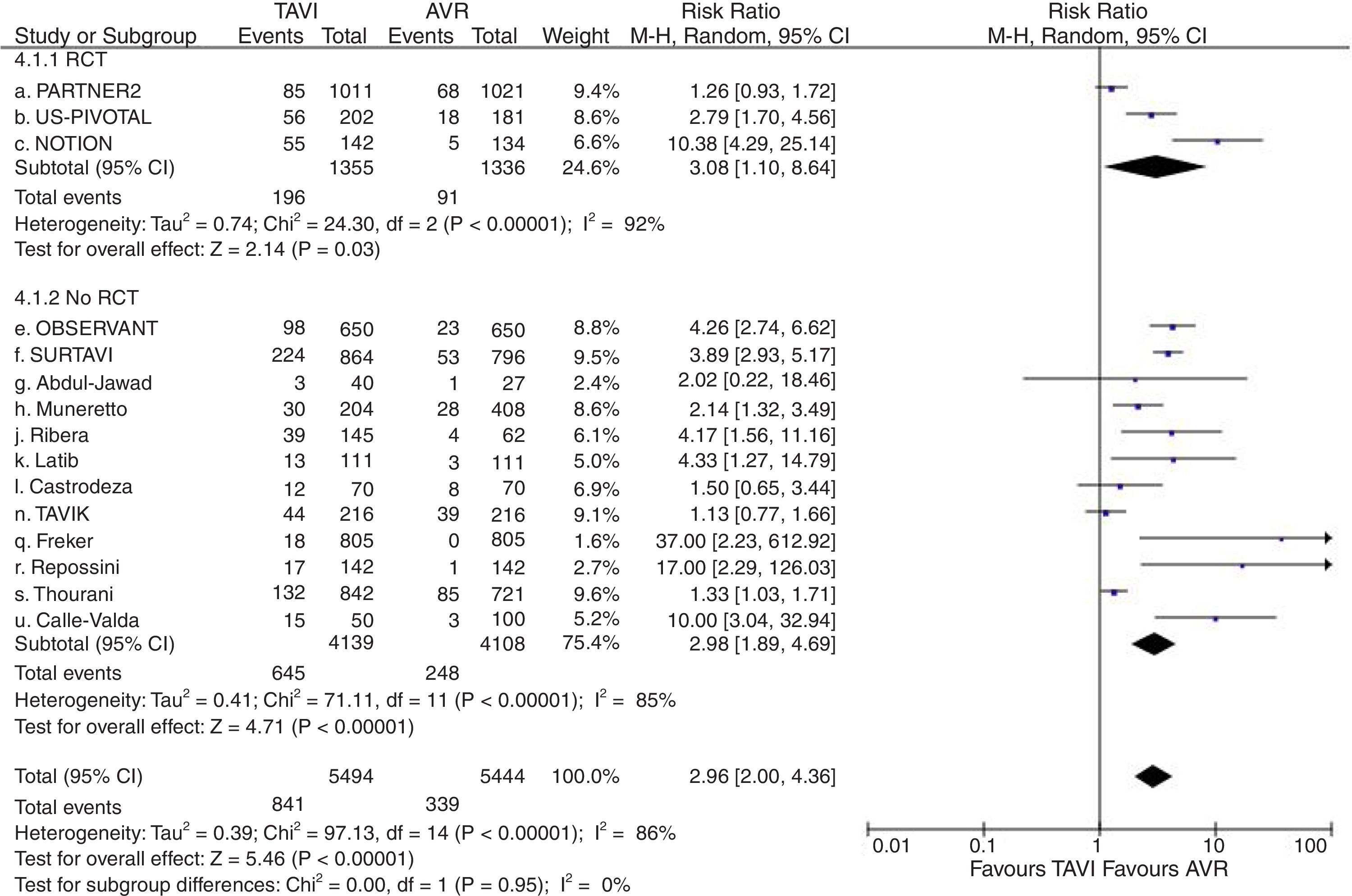
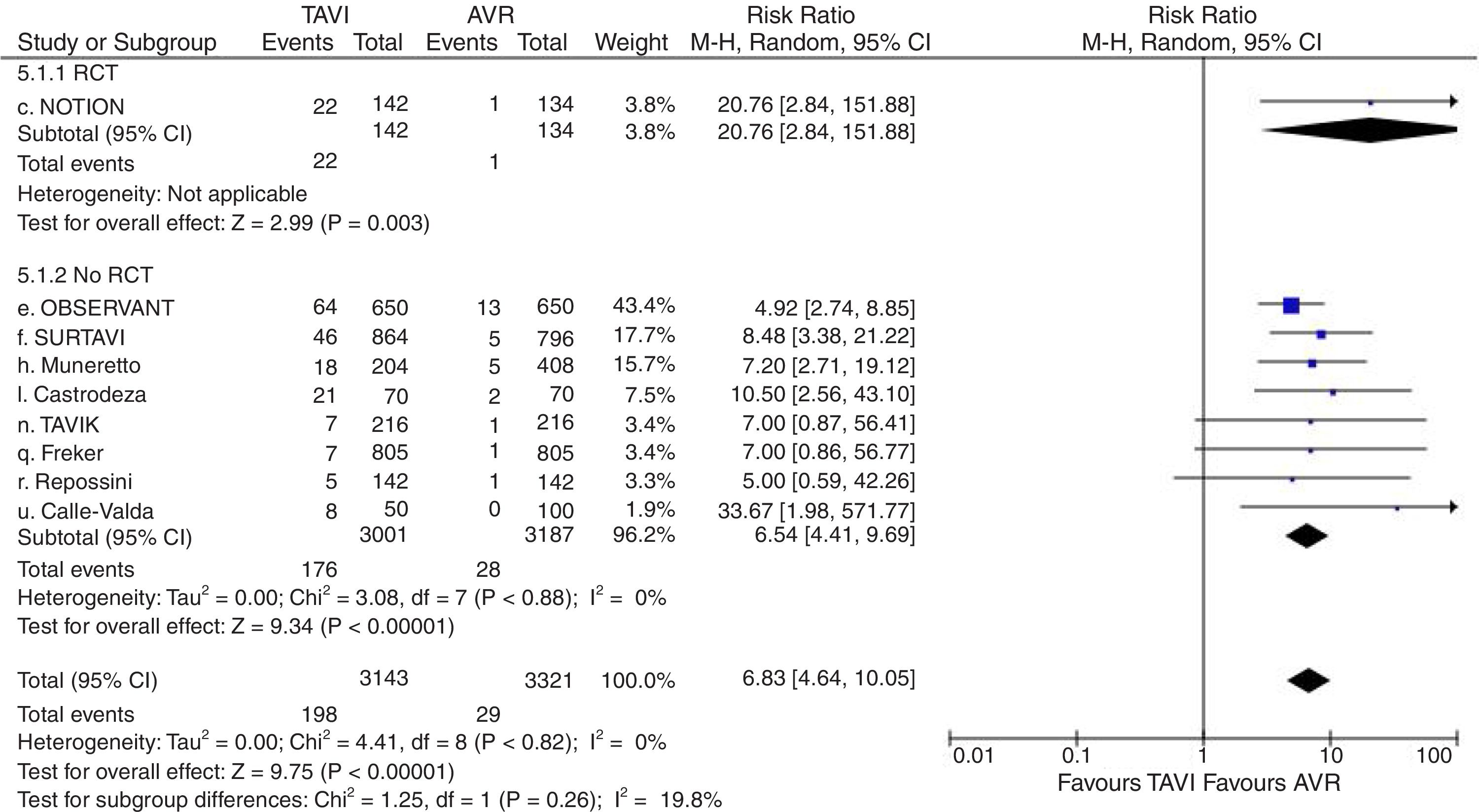
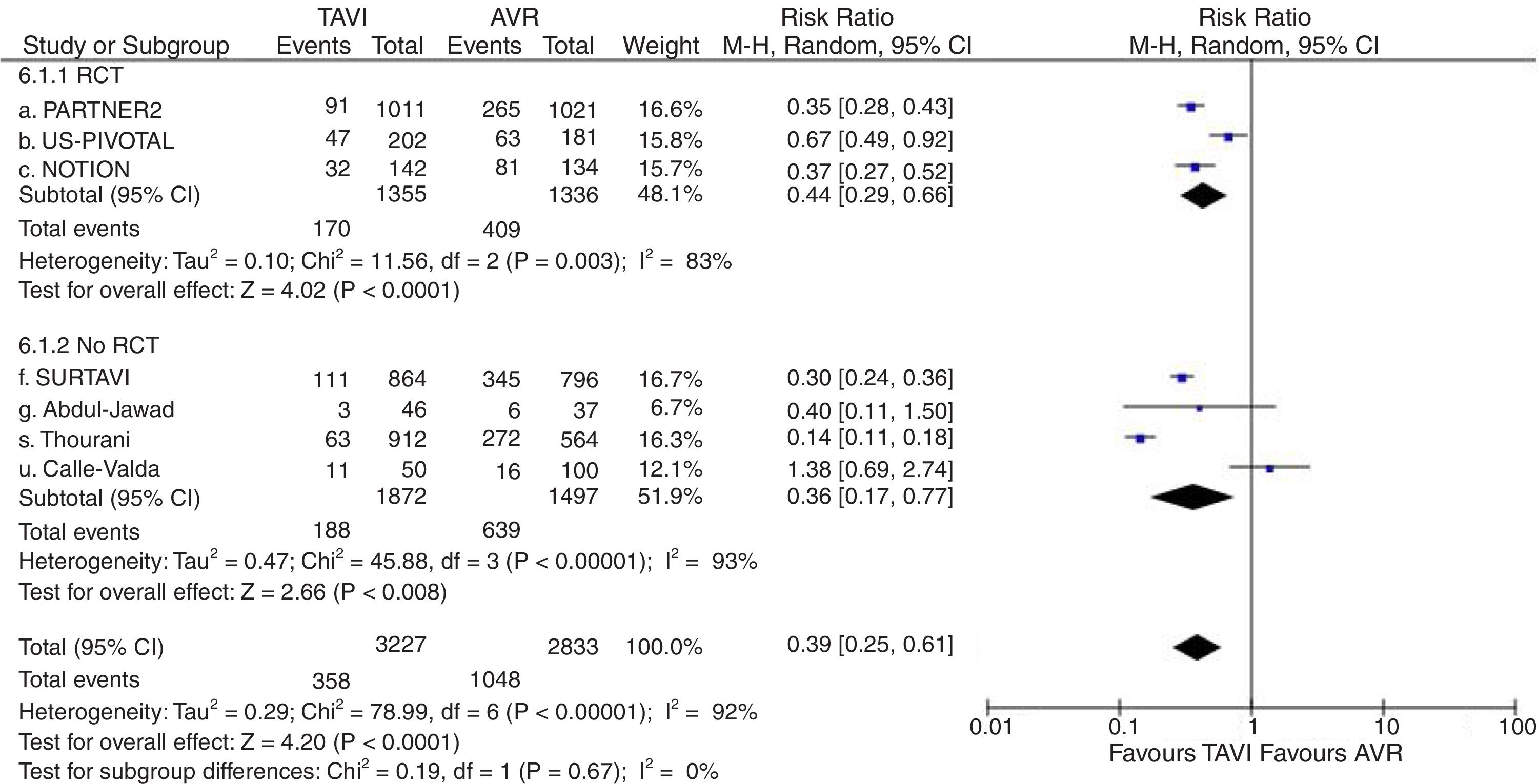
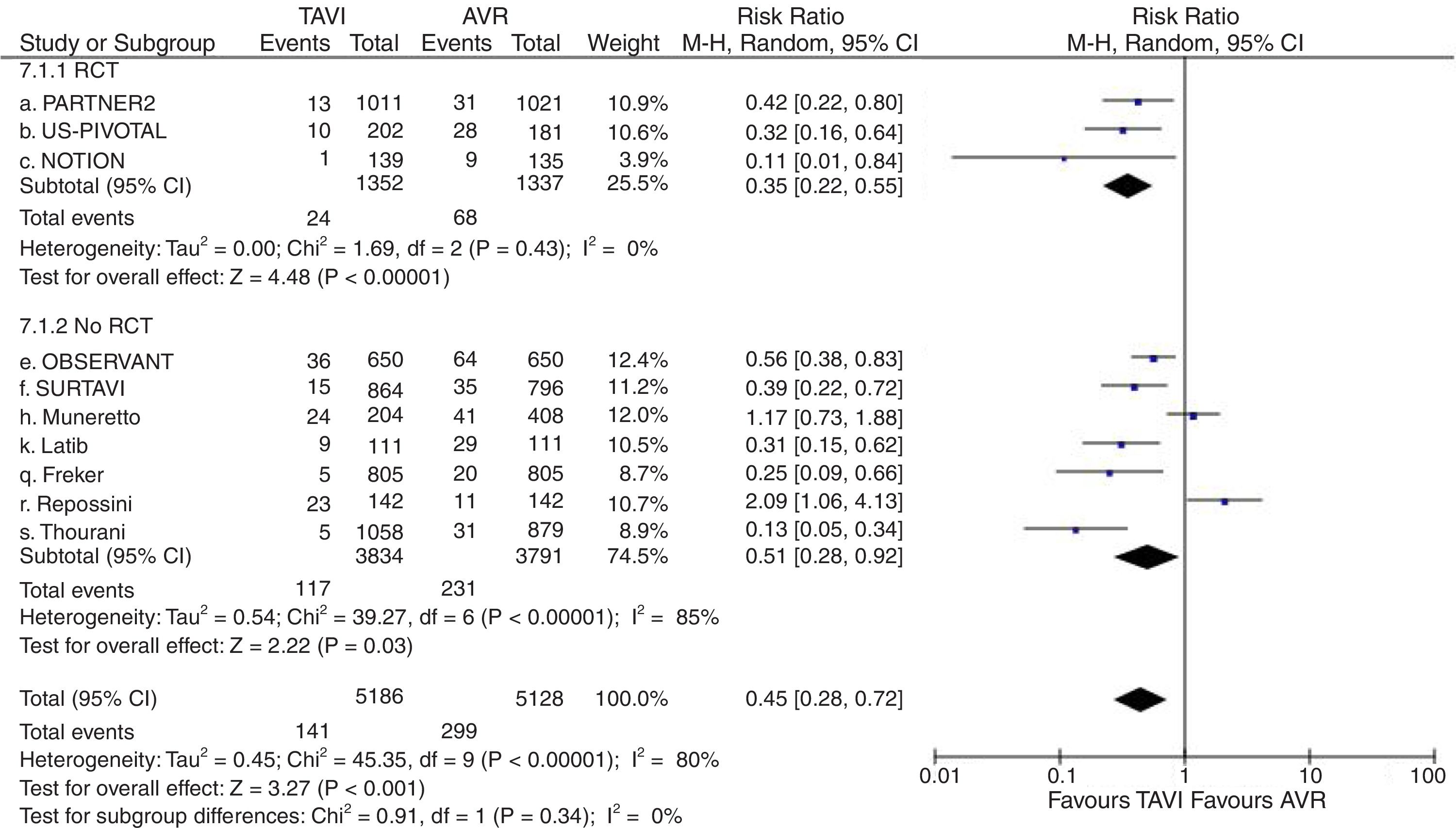
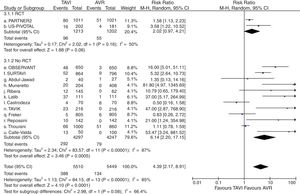
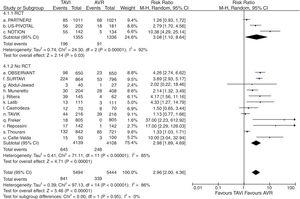
Catorce estudios2,7,10–13,15–17,19,22–24,26 proporcionaron datos válidos sobre la tasa complicaciones vasculares graves, 15 sobre necesidad de implante de marcapasos posprocedimiento2,7,8,10–13,15–17,19,22–24,26, 9 sobre fuga paravalvular significativa (grado≥2+)8,10,11,13,17,19,22,23,26, 7 sobre FA2,7,8,11,12,24,26 y 10 sobre fallo renal2,7,8,10,11,13,16,22–24. Globalmente considerados, la lesión vascular grave fue significativamente mayor en el grupo TAVI (RR=4,39; IC95%: 2,17-8,91) (fig. 4), así como la necesidad de implante de marcapasos permanente (RR=2,96; IC95%: 2-4,36) (fig. 5) y la incidencia de fuga paravalvular significativa (RR=6,83; IC95%: 4,64-10,05) (fig. 6). Tanto la incidencia de FA (fig. 7) como de fallo renal (fig. 8) mostraron resultados favorables al grupo TAVI (FA: RR=0,39; IC95%: 0,25-0,61; fallo renal: RR=0,45; IC95%: 0,28-0,72). Los únicos análisis de complicaciones posprocedimiento con heterogeneidad aceptable fueron los de la incidencia de fuga paravalvular significativa (I2=19,8%) y el de fallo renal (I2=80%). Fue aplicado funnel-plot para la selección de trabajos incluidos en cada uno de los análisis a efectos de minimizar el sesgo de publicación.
Diagrama de árbol de incidencia de lesión vascular grave periprocedimiento de TAVI versus sustitución valvular aórtica en pacientes con riesgo quirúrgico intermedio. AVR: sustitución valvular aórtica; M-H: Mantel-Haenszel; RCT: estudio prospectivo aleatorizado; TAVI: implante valvular aórtico transcatéter; 95% IC: intervalo de confianza al 95%.
Diagrama de árbol de necesidad de implante de marcapasos posprocedimiento de TAVI versus sustitución valvular aórtica en pacientes con riesgo quirúrgico intermedio. AVR: sustitución valvular aórtica; M-H: Mantel-Haenszel; RCT: estudio prospectivo aleatorizado; TAVI: implante valvular aórtico transcatéter; 95% IC: intervalo de confianza al 95%.
Diagrama de árbol de incidencia de fuga paravalvular significativa residual (grado≥2+) de TAVI versus sustitución valvular aórtica en pacientes con riesgo quirúrgico intermedio. AVR: sustitución valvular aórtica; M-H: Mantel-Haenszel; RCT: estudio prospectivo aleatorizado; TAVI: implante valvular aórtico transcatéter; 95% IC: intervalo de confianza al 95%.
Diagrama de árbol de incidencia de fibrilación auricular posprocedimiento de TAVI versus sustitución valvular aórtica en pacientes con riesgo quirúrgico intermedio. AVR: sustitución valvular aórtica; M-H: Mantel-Haenszel; RCT: estudio prospectivo aleatorizado; TAVI: implante valvular aórtico transcatéter; 95% IC: intervalo de confianza al 95%.
Diagrama de árbol de incidencia de fallo renal posprocedimiento de TAVI versus sustitución valvular aórtica en pacientes con riesgo quirúrgico intermedio. AVR: sustitución valvular aórtica; M-H: Mantel-Haenszel; RCT: estudio prospectivo aleatorizado; TAVI: implante valvular aórtico transcatéter; 95% IC: intervalo de confianza al 95%.
A fecha actual, este metaanálisis entre TAVI y tratamiento quirúrgico sobre mortalidad y ACV en el seguimiento en pacientes con estenosis aórtica significativa y riesgo quirúrgico intermedio es el más extenso tanto en número de estudios como de pacientes incluidos presente en la literatura, incluyendo 21 trabajos y más de 24.000 pacientes. Complementariamente a los metaanálisis ya publicados, incluye los 4 EPA en seguimiento en la actualidad conjuntamente así como estudios observacionales considerados desigualmente entre los mismos (ver tabla 2). Es destacable la inclusión en los metaanálisis ya publicados de los datos del EPA STACCATO9, interrumpido prematuramente por la acumulación de eventos adversos en la rama de tratamiento TAVI-transapical, que también ha sido incluido en nuestro trabajo a pesar de su limitada trascendencia y el impacto sobre la heterogeneidad que comporta un estudio con un tamaño muestral tan reducido. En lo que respecta a los trabajos observacionales, 13 de incorporan estrategias de muestreo por medio de análisis de propensiones10,12–19,21–23,26 que reducen la introducción de sesgos así como el estudio SURTAVI11, que incorpora un análisis bayesiano que aporta robustez suficiente para permitir incorporar 4480 pacientes más sobre los proporcionados por los EPA.
El análisis realizado no muestra diferencias significativas en la mortalidad o incidencia de ACV a lo largo del seguimiento máximo mostrado por los estudios. Tanto el PARTNER22 como el US-PIVOTAL3 tienen un diseño de no inferioridad, a diferencia del estudio NOTION8 o de los trabajos observacionales. Paradójicamente, es en estos EPA de no inferioridad donde se muestran resultados estadísticamente significativos a favor del TAVI en el seguimiento a 2 años, con mejores resultados para el evento compuesto particularmente para la alternativa de abordaje transfemoral y en el subgrupo de población de mujeres. Al estar diseñados con objetivo de no inferioridad, las asunciones de superioridad de subgrupos deben considerarse con extrema cautela. Por otra parte, el estudio NOTION fue diseñado con una inclusión «all comers», incluyendo por tanto a pacientes de riesgo intermedio pero también bajo (STS-PROM medio<4%, EuroSCORE I logístico medio<9%, edad media 79 años), pudiendo infraestimar la tasa de eventos adversos en ambos grupos de tratamiento. La contrapartida la ofrece el estudio de Muneretto et al.13, con resultados superiores para la opción quirúrgica en cuanto a mortalidad, eventos cardio- y cerebrovasculares mayores. El resto de estudios no muestran, individualmente, diferencias entre ambas alternativas de tratamiento.
Con ello, el TAVI en pacientes de riesgo intermedio constituye una alternativa terapéutica equivalente en términos de supervivencia e incidencia de eventos cerebrovasculares graves a corto-medio plazo, respecto de la opción de tratamiento quirúrgico convencional. Asimismo, constituye una alternativa de tratamiento menos invasiva y que puede conseguir una recuperación media más rápida del enfermo.
Sin embargo, el procedimiento TAVI todavía comporta morbilidades significativamente mayores a la cirugía convencional en términos de lesión vascular grave (RR=4,39; p<0,00001), necesidad de implante de marcapasos permanente (RR=2,96; p<0,00001) o fuga paravalvular (RR=6.83, p<0,00001), con el correspondiente impacto en la calidad de vida y pronóstico en el seguimiento. Este impacto, evidentemente, debe ser de mayor importancia según se van implantando este tipo de prótesis en pacientes más jóvenes, con más esperanza de vida y, por tanto, mayor probabilidad de presentar eventos desfavorables durante un seguimiento más largo.
No existe evidencia de que la estimulación con marcapasos afecte a la mortalidad a largo plazo, aunque sí existen datos que indican una peor recuperación funcional de los pacientes y una ausencia de mejoría de la función ventricular izquierda en caso con disfunción sistólica36. Sin embargo, este aspecto no está profundamente estudiado en estos subgrupos de pacientes con moderado riesgo quirúrgico y, por ende, mayor esperanza de vida que los pacientes con riesgo elevado o contraindicación para cirugía convencional. Adicionalmente, estos pacientes tienen sistemáticamente hipertrofia ventricular izquierda y, con mucha frecuencia, disfunción ventricular diastólica a la que la pérdida de la sincronía auriculoventricular por estimulación monocameral o intra/interventricular puede resultar en peor tolerancia al ejercicio o menor recuperación de la disfunción ventricular preexistente.
En cuanto a las fugas paravalvulares residuales, está ampliamente demostrado que las de grado moderado o severo reducen la supervivencia a corto-medio plazo en estos pacientes2. Como se ha comentado previamente, además existen trabajos en los que se sugiere que las fugas leves también podrían tener un impacto desfavorable en la supervivencia4. Ello se achaca a la dificultad para cuantificar correctamente la severidad de este tipo de regurgitaciones aórticas en este contexto, por lo que en muchas ocasiones podrían estar infraestimadas37,38. Además algunos estudios que sugieren que la regurgitación aórtica «aguda», es decir, en pacientes en los que previamente no existía insuficiencia aórtica, presenta una tolerancia significativamente peor que en pacientes en los que la insuficiencia acompañaba a la estenosis previamente al procedimiento19. Ello podría explicar que grados poco relevantes de regurgitación sean mal tolerados postoperatoriamente.
Es por todo ello que la estratificación de riesgos individuales tanto de mortalidad como de las diferentes morbilidades derivadas del procedimiento resulta clave a través del Heart-Team para la toma de decisiones sobre el mejor manejo de los pacientes con estenosis aórtica significativa y riesgo quirúrgico intermedio, pacientes con esperanzas de vida mayores y en los que cualquiera de estas complicaciones mantenidas en el tiempo puede afectar a su supervivencia. Por ello creemos imprescindible que debe incluirse en el establecimiento de la indicación factores tales como:
- -
Aspectos de índole técnica (abordajes disponibles, riesgo de embolización de material cálcico, oclusión coronaria, sangrado periprocedimiento, reducción de la invasividad del procedimiento quirúrgico, etc.)
- -
Aspectos relacionados con la morbilidad posprocedimiento (mayores tasas de fallo renal agudo y FA postoperatoria en la opción quirúrgica, mayores tasas de implante de marcapasos permanente, lesión vascular grave o fuga paravalvular en el TAVI, entre otros)
- -
Aspectos referentes a la durabilidad de las prótesis implantadas39,40 (tanto prótesis quirúrgicas sin suturas como del TAVI)
- -
Aspectos relativos al coste-eficiencia (siendo, desde un punto de vista de la responsabilidad ética, preferente la opción terapéutica más eficiente). A este respecto, el estudio de Ribera et al.15 ofrece un completo análisis económico de centros de nuestro país, mostrando como alternativa de tratamiento más eficiente a la opción quirúrgica. El elevado coste del material intraprocedimiento y del propio dispositivo TAVI no consiguen compensar la reducción que suponen en la estancia hospitalaria, pudiendo ser el TAVI una alternativa más eficiente en sistemas sanitarios diferentes al nuestro con más elevados costes de hospitalización.
Indudablemente, el tratamiento de pacientes con estenosis aórtica significativa y riesgo quirúrgico intermedio por TAVI deja de poder considerarse un procedimiento «compasivo», por lo que decisiones como la «operabilidad» del enfermo en caso de complicación de procedimiento percutáneo y la necesidad de realizar conjuntamente los procedimientos entre cardiólogos y cirujanos cardiovasculares, constituyen un hecho necesario para garantizar los resultados y calidad asistencial ofrecida a los enfermos, debiendo ser considerado desaconsejable el tratamiento de este perfil de pacientes en unidades sin servicio de cirugía cardiovascular o hemodinámica en la misma institución en los que esta colaboración no sea posible, máxime en pacientes de riesgo de oclusión coronaria ostial que puedan requerir un procedimiento intervencionista coronario emergente por manos expertas o pacientes que sean candidatos a cirugía abierta de rescate inmediata en caso de complicaciones susceptibles de cirugía (es decir, pacientes de alto riesgo pero operables y, sobre todo, pacientes de riesgo moderado o bajo). Además, la integración de los registros de resultados tanto de mortalidad como de las complicaciones descritas en cada una de las alternativas de tratamiento en la experiencia concreta de cada institución debe ser considerada por el Heart-Team a la hora de guiar la toma de decisiones.
Limitaciones del trabajoEl estudio atiende a diferentes limitaciones. Primero: el número de pacientes en los diferentes estudios individuales es limitado; sin embargo, la valoración conjunta en un modelo de metaanálisis permite una mejor potencia estadística. Segundo: la variedad de dispositivos TAVI disponibles así como la de vías de abordaje es muy amplia, pudiendo incrementar la heterogeneidad de procedimientos y resultados. No obstante, casi la totalidad de prótesis implantadas corresponde a diferentes generaciones de Edwards Sapien® (Edwards Lifesciences, Irvine, CA, EE. UU.) y Medtronic Corevalve® (Medtronic, Minneapolis, MN, EE. UU.), siendo el abordaje transfemoral preferencial en todos los estudios e incluso, en algunos de ellos, exclusivo. Si bien este hecho permite que los resultados se ajusten mejor a la práctica en nuestro medio, deja una elevada incertidumbre sobre los resultados de otros dispositivos a corto y largo plazo. Tercero: algunos trabajos incluyen centros con la disponibilidad de uno solo de los procedimientos (TAVI o cirugía) y han recibido financiación privada para su realización. Aunque este hecho puede condicionar la asignación de pacientes a una de las alternativas de tratamiento en los estudios observacionales, la mayoría de los estudios han sido realizados en centros con ambas alternativas de tratamiento y habiéndose realizado la inclusión de pacientes recientemente, con la curva de aprendizaje superada para ambas técnicas. Tampoco se evidenciaron sesgos de publicación significativos. Cuarto: los seguimientos disponibles son todavía muy limitados para poder valorar el comportamiento a largo plazo de ambas alternativas de tratamiento, en términos de mortalidad e incidencia de eventos cardiovasculares mayores, evolución de fugas paravalvulares y durabilidad de TAVI y prótesis sin suturas. Quinto: el estudio NOTION8 incluye a pacientes con perfil de riesgo quirúrgico bajo, no siendo estrictamente objeto del análisis realizado. Sin embargo, se trata de un EPA de excelente calidad, siendo ambos grupos de tratamiento comparables, con pacientes de similar perfil de riesgo, lo cual no introduce sesgos en el análisis comparativo. Sexto: en el análisis secundario de complicaciones posprocedimiento, el fracaso renal y la FA permitieron un análisis más limitado que el de otros resultados, al estar representados de forma limitada en los estudios analizados. No obstante, estas complicaciones junto a otras como la hemorragia periprocedimiento, grado de trasfusión de hemoderivados, etc. presentan un impacto significativo sobre la supervivencia y resultados a corto y medio plazo, siendo aparentemente más frecuentes en los pacientes sometidos a tratamiento quirúrgico. Séptimo: aunque la asignación de pacientes a TAVI y tratamiento quirúrgico en los estudios observacionales se ha apoyado en una decisión multidisciplinar (Heart-Team), existe cierto componente subjetivo en cada uno de los equipos que puede variar entre los diferentes grupos de trabajo sobre la preferencia de remisión de los pacientes a una u otra alternativa de tratamiento. Esta heterogeneidad queda compensada con el gran volumen de trabajos incluidos, 14 de ellos multicéntricos.
ConclusionesEl metaanálisis realizado entre TAVI y tratamiento quirúrgico sobre mortalidad y ACV en el seguimiento a medio plazo en pacientes con estenosis aórtica significativa y riesgo quirúrgico intermedio no muestra diferencias significativas entre ambos procedimientos. Sin embargo, el TAVI presenta una tasa superior de lesión vascular grave, necesidad de implante de marcapasos y fuga paravalvular significativa posprocedimiento, e inferior para la FA y fallo renal respecto del tratamiento quirúrgico (aunque resaltando una heterogeneidad aceptable solo para la necesidad de implante de marcapasos y el fallo renal posprocedimiento). La toma de decisiones sobre el manejo de estos pacientes deberá ponderar desde un punto de vista multidisciplinar aspectos técnicos, clínicos y de eficiencia económica a fin de optimizar las indicaciones y utilización de recursos sanitarios. Son necesarios nuevos estudios así como el mantenimiento del seguimiento a largo plazo de los actualmente en curso para poder determinar la mejor alternativa terapéutica para los diferentes perfiles de pacientes dentro del estrato de riesgo quirúrgico intermedio.
Conflicto de interesesLos autores declaran no tener ningún conflicto de intereses.