El modelo clásico de función cardíaca ha sido asumido durante décadas. Este modelo está basado en la ley de Frank-starling, enunciado con corazones extirpados. La hipótesis de Torrent-Guasp ha conseguido que el estudio de la acción mecánica cardíaca recupere la importancia que le corresponde. Esta hipótesis ha llevado a revisar conceptos clásicos tales como que la banda mio-cárdica sería generadora de la reducción tridimensional, que la unidad morfológica de las aurículas y ventrículos contrasta con la unidad funcional vertical auriculoventricular y que el nuevo concepto del ventrículo y del corazón implicaría considerarlo una bomba de succión.
En este concepto, la energía almacenada en sístole se libera en favor de una dilatación rápida durante la relajación, originando la succión diastólica como un fenómeno secundario al retroceso elástico pasivo del helicoide ventricular. Hay argumentos en contra: el rápido incremento de la tensión de la pared ventricular tras la apertura mitral, ¿no está suficientemente explicado en el modelo clásico? Por otra parte, ¿las aurículas tienen una función de bomba y su contracción contribuye en un 20% al llenado ventricular? Hay resultados que apoyan los gradientes de presión para explicar el llenado y apoyar el modelo clásico.
Los cambios geométricos han generado un interés creciente para la aplicación de la cirugía de restauración ventricular. Basándose en la geometría elipsoidal del ventrículo izquierdo, se presenta una técnica de restauración sin parches sintéticos con buenas perspectivas de supervivencia y cambios geométricos favorables. la hipótesis de To1rrent-Guasp exige una confirmación prioritaria, integrando a equipos multidisciplinarios.
The classic model of cardiac function has been assumed for decades. This model that not reflects the interaction between systole and diastole, is based in Frank-starling law, statement with hearts removed. The hypothesis of Torrent Guasp has achieved that the study of cardiac mechanical action to regain the importance it deserves. This hypothesis has led to revise classic concepts: ventricular myocardial band without fixed support points generating a three dimensional reduction; the morphological unit of the atria and ventricles is opposited to functional unit vertical atrium-ventricle; the new concept is that the heart is one suction pump.
In this concept the energy stored in systole is released for a rapid expansion during relaxation, resulting in diastolic suction as a secondary phenomenon to the passive elastic recoil of the helical ventricular. Their arguments against it: the rapid increase in ventricular wall stress following mitral opening, according to Laplace law, is not sufficiently explained in the classic model? On the other hand, the atria are pumping function and its contraction contributes 20% to ventricular filling? There are results of the study of the cardiac cycle that support pressure gradients to explain and support the classic model.
Changes of ventricular geometry have created a growing interest for the application of ventricular restoration techniques. Their correlation with the anatomic and pathophysiological fundaments of the ventricle contributes to knowledge of news procedures without patches with good results. The hypothesis of Torrent Guasp requires a confirmation of priority, integrating cardiologists, anatomists, physiologists, researches and surgeons.
«La mecánica cardíaca es homologable a la de las fibras circulares de los vasos sanguíneos, que llevan a cabo su función sin puntos de apoyo fijos».
Francisco Torrent Guasp1
IntroducctiónFrancisco Torrent Guasp nunca creyó que la sangre pudiera entrar en el ventrículo izquierdo si no era por un mecanismo de succión. Consideraba que la diferencia de presión periférica con el corazón es pequeña y no lo puede hacer por vis a tergo. El desnivel que la retorna es la aspiración ventricular. El corazón es una estructura conformada por una banda muscular que comienza en la inserción de la arteria pulmonar y termina a nivel de la aorta, formando una doble hélice que limita los ventrículos. Las dos cámaras que envuelven la banda muscular son la izquierda, de conformación elipsoide, y la derecha, de estructura semilunar. Pues bien, la contracción de esta banda explica no solo la sístole del corazón sino también la succión de la sangre2.
La pregunta inevitable que surge es que para que puedan retorcerse las bandeletas que rodean los ventrículos, deberían hacerlo sobre un punto de apoyo rígido, al igual que un tendón lo hace teniendo de palanca una inserción ósea; ¿los hay en el corazón? El corazón no necesita esa apoyatura. Cuando el corazón se llena de sangre, esta se comporta como una inserción ósea. La banda muscular es una doble helicoide suspendida de la aorta y de la pulmonar que utiliza de apoyo al hemoes-queleto, o sea, al llenado cardíaco. Sobre este punto, al rotar la base y la punta del ventrículo izquierdo en sentidos opuestos se genera una torsión muscular. Este movimiento antihorario del ápex permite generar presiones elevadas reduciendo la deformación, como si se exprimiese una toalla3,4.
Bomba de succiónLa acción mecánica del corazón es compleja porque es el resultado de integrar las propiedades intrínsecas del miocardio bajo numerosas influencias extrínsecas: resistencia a la expulsión de la sangre, sistema nervioso vegetativo y catecolaminas, frecuencia cardíaca y ejercicio, retorno venoso y volumen sanguíneo. Los textos de anatomía describen el corazón, pero dedican escasa atención a la disposición adoptada por las fibras miocárdicas. Los fisiólogos ni siquiera suelen mencionar el problema, como si la mecánica cardíaca no guardara relación con el diseño del andamiaje desarrollado por las fibras musculares en la pared de los ventrículos. Es imposible interpretar las mediciones de la función cardíaca con fines diagnósticos si no se tiene en cuenta la estructura morfológica. Los cardiólogos e investigadores clínicos centran su atención en los aspectos moleculares y pretenden explicar la insuficiencia cardíaca siguiendo modelos neurohor-monales. Sin embargo, los tratamientos farmacológicos que actúan sobre la activación neurohormonal enlentecen, pero no detienen, la insuficiencia cardíaca o bien son ineficaces. El tamaño y los cambios de la geometría son responsables de las anomalías estructurales de los miocitos y del miocardio, que empeoran la función cardíaca, aumentan la actividad neurohormonal y reducen la respuesta del sistema cardiovascular. El pronóstico de los pacientes con insuficiencia cardíaca, la morbimortalidad, está directamente relacionado con la dilatación ventricular.
La capacidad miocárdica se halla condicionada por la orientación de las fibras cardíacas. En ese aspecto, el corazón cónico tiene fibras miocárdicas helicoidales y circulares circunferenciales. Las vías de orientación de las fibras determinan la función, y así, la fracción de eyección (FE) es del 60% cuando las fibras helicoidales normales se contraen y cae al 30% si se acortan las fibras transversas5. El desarrollo de una configuración esférica modifica la orientación de las fibras helicoidales hacia una dilatación transversal y disminuye la fuerza contráctil.
En los modelos clásicos, después de cada sístole, el corazón permanece pasivo llenándose de sangre por efecto de la presión venosa6. En cambio, en el desarrollo actual, un quantum de la energía de cada sístole se almacena en el corazón y activa la siguiente fase de relajación7. La vigencia fisiológica del antiguo modelo se refrenda a través de la ley de Frank-Starling, pero no refleja la interacción sístole-diástole, y esta ley se enunció con corazones extirpados.
En el modelo actual, la interrelación entre ambas fases cardíacas resulta crítica para el correcto funcionamiento del corazón. Ahora bien, la energía acumulada en la sístole ¿cómo se gasta en la diástole?:
- –
Por el movimiento que adquiere en la sístole, el corazón se impulsa hacia abajo y la sangre en dirección inversa (principio de acción y reacción de Newton). En la diástole, en cambio, el corazón se proyecta hacia arriba a contracorriente de la sangre que entra. Esto último aumenta la velocidad de la sangre y ayuda a impulsar el llenado.
- –
La sístole comprime tanto los elementos elásticos del corazón como sus fibras musculares a tal punto que, incluso la tendencia natural de los ventrículos es hacia la expansión sin que haya llenado externo. De esta manera se genera una presión negativa intraventricular o succión. Tyberg8, ocluyendo la válvula mitral en el perro con un balón, ha demostrado que en diástole el ventrículo izquierdo produce un descenso de la presión por debajo del cero. Esto hace que el corazón sea una bomba de succión dinámica, pero para que esta bomba tenga efectividad, la dinámica del retroceso elástico debe poseer una limitante que permita una efectiva sístole posterior2.
Debemos recordar que en el modelo tradicional, el gasto está determinado únicamente por la presión de llenado venoso del lado derecho. La presión auricular es demasiado baja para explicar el llenado del corazón. Sobre esta «duda clave» en relación a la explicación clásica, F. Torrent Guasp desarrolló el concepto de bomba de succión activa apoyado por la estructura fisiomuscular que describió. Las últimas zonas contraídas del segmento ascendente de la lazada apexiana miocárdica producen la succión de la sangre desde la aurícula hacia el ventrículo izquierdo9. Esta situación traería aparejado situaciones inexplicadas en electrofisiología, ya que la onda T coincidiría con la contracción del septum, lo cual hace imprescindible investigaciones futuras al respecto2.
Los movimientos cardíacos durante la sístole y la diástole responden a fenómenos de inercia y retrocesos elásticos, no a presiones estáticas de llenado. Los corazones de mamíferos persisten en su vaciado y llenado, después de extirpados y colocados en solución tamponada. La longitud que alcanzan las fibras musculares cardíacas no viene determinada solo por la posición de llenado cardíaco, interviene el mecanismo de succión. Por el contrario, si hay fallo en la contracción sistólica, tal como sucede en la insuficiencia cardíaca, es factible razonar que no habrá liberación suficiente de energía en la fase de relajación. El papel de la presión de llenado venoso, en estos corazones, es aquí más relevante de acuerdo a la ley de Frank-Starling.
¿Cómo se produce la succión diastólica?Las evidencias están presentes desde la anatomía funcional actual hasta en la histología. La descripción anatómica en doble hélice de la gran banda miocárdica de Torrent-Guasp remeda en su torsión la estructura microscópica conjuntiva de sostén del corazón, situación que refuerza dicha investigación. Los alargamientos residen tanto en la propia estructura del sarcómero como en los componentes de la célula muscular que conforman el citoesqueleto7. El sarcómero se expande lateralmente y aumenta su diámetro. Esta expansión lateral extiende los discos Z. De esta forma, se constituye en el mecanismo de almacenamiento de parte de la energía de contracción, que podría utilizarse como energía de expansión.
En esto participa el tejido conjuntivo. La superficie externa de las células musculares está cubierta de fibras conectivas de colágeno y elastina con propiedades de tensión y deformación dispuestas helicoidalmente en red. Esta estructura en red devuelve a las células musculares su configuración original, evitando que se produzca un estiramiento excesivo de los sarcómeros para lograr una buena succión durante la fase de relajación.
El citoesqueleto fibroso debe entenderse como la sumatoria de los componentes fibrosos entrelazados, indispensables para la conservación de la geometría ventricular. El andamiaje constituido por colágeno coordina las fibras musculares al reunirlas en paquetes de estructuras crecientes, teniendo como fin mantener un estiramiento óptimo para lograr una efectiva contracción posterior. Este citoesqueleto se halla constituido por una malla de forma cuadricular que envuelve individualmente a los sarcómeros, los cuales se hallan reunidos en manojos por estructuras conectivas denominadas tirantes o amarras giradas en forma helicoidal sobre su mismo eje7.
Los sarcómeros miocárdicos en condiciones normales sufren un alargamiento que va desde 1,85 μm en el periodo de contracción hasta los 2,05 μm en el estado de reposo. En sístole, el acortamiento del sarcómero es solo del 12%, pero con esta escasa cifra el ventrículo izquierdo se vacía en un 70%. Esta eficacia logra que la eyección se realice a una velocidad de 300 cm/seg y a una presión de 120/80 mmHg, permitiendo una reducción tridimensional del ventrículo izquierdo del 15% en sus ejes longitudinal, anteroposterior y transversal10,11.
La disposición helicoidal de las fibras musculares (macro y microscópica) permite esta eficiencia al lograr una contracción que se inicia en el tracto de salida del ventrículo derecho y termina en el ápex izquierdo, según Torrent Guasp es un pistón cardíaco en el lugar de izquierdo. En esta reducción tridimensional hay tres componentes:
- –
Un componente anular de las lazadas basal y apexiana que da lugar a un movimiento de constricción miocárdica en el plano transversal.
- –
Un movimiento longitudinal de acortamiento secundario al que realiza el acortamiento del elemento helicoidal que actúa como si fuera un muelle.
- –
Un movimiento de expresión del componente helicoidal, antihorario en el ventrículo izquierdo y horario en el ventrículo derecho.
Estos tirantes de tejido conectivo, con una disposición similar a los cables tensores de los puentes colgantes con trenzado helicoidal, ha sugerido la idea de un almacenamiento de energía sistólica, que, liberada en el proceso diastólico, permite el efecto de bomba de succión. El movimiento de retorcimiento de las fibras originaría fuerzas de recuperación que inician la diástole contribuyendo a la succión diastólica.
Los corazones de mamíferos en una solución tamponada se autoimpulsan por contar con la estructura de tirantes. En cambio, en el corazón de la rana no existe tal impulsión por carecer de estas amarras como elementos de sujeción interfibrilar. Paradójicamente, un invertebrado como el calamar succiona agua por medio de la cámara hueca envuelta de una estructura muscular, logrando con la expulsión el efecto de propulsión a chorro. Esto puede efectuarlo por contar dicha musculatura con tirantes.
El retroceso del ventrículo izquierdo produce el levantamiento del ventrículo derecho, favoreciendo su llenado rápido y acelerado. El movimiento del corazón entero contribuye al llenado. Por efecto de este mecanismo, el aumento de contractilidad del lado izquierdo incrementa el rendimiento del lado derecho.
En síntesis, el mecanismo de succión por retroceso elástico del helicoide ventricular es un proceso ventricular activo. Durante el periodo de relajación isovolu-métrica del ventrículo izquierdo hay una contracción del segmento ascendente de la lazada apexiana. La succión inicial estaría explicada por este mecanismo9,10. La situación planteada podríamos asemejarla a un «mecanismo de sopapa». A medida que las paredes que ejercen la succión ventricular se venzan y dilaten, el «mecanismo de sopapa» se precarizaría, pudiéndose establecer a través de este concepto una visión diferente de la insuficiencia cardíaca y de su gravedad.
Asimismo, al abrirse la válvula mitral e incrementarse el estrés de la pared con caída del grosor de la pared, se alargan las fibras permitiendo al ventrículo llenarse rápidamente. La gran velocidad de llenado con presiones bajas estaría demostrada por el fenómeno de succión. Este mecanismo activo de la gran banda miocárdica de Torrent-Guasp sobre el efecto diastólico abre un amplio panorama sobre las técnicas quirúrgicas de restauración, tanto en la forma como en el volumen, y consecuente función del ventrículo iz-quierdo11–15.
Argumentos a favorEl mecanismo de llenado ventricular ha generado varias hipótesis, que pueden resumirse en dos:
- –
El ventrículo es una bomba de succión durante la diástole. Esta hipótesis fue propuesta por Era-sístrato en el siglo IV a. C. y posteriormente por Galeno y Vesalio6.
- –
El llenado ventricular se realiza por el latido de las aurículas, según Harvey, o por el gradiente de presión. Esta hipótesis fue propuesta en la década de 1920 por Wiggers16.
El llenado diastólico por un mecanismo de succión está apoyado por la hipótesis de Torrent Guasp1 y por estudios experimentales y clínicos. Los tres componentes de la reducción tridimensional del corazón in-teraccionan sinérgicamente a través de la banda muscular, que se pliega sobre sí misma y se retuerce; al estar colgados los ventrículos de la arteria pulmonar y la aorta, las desplaza caudal y ventralmente. En la sístole hay una reorientación tridimensional de la arquitectura cardíaca con el helicoide, que se acorta en sentido longitudinal, transversal y de torsión. Se contrae el anillo auriculo-ventricular, se expande ligeramente el anillo aórtico, descienden los planos mitral y aórtico y se mantiene abierto el tracto de salida del ventrículo izquierdo. El descenso de la base actúa como un émbolo aspirante que aumenta el retorno venoso.
La succión sobreviene en la diástole precoz, desde el final de la fase de relajación isovolumétrica- apertura de la válvula mitral hasta el punto F, simultáneo con el tercer ruido. Durante este periodo, se ha documentado la presencia de una presión intraventricular negativa, tanto en clínica humana2,17 como en animales con oclusión de la válvula mitral con un balón8,18. Durante la sístole se almacena una energía mecánica que se libera en favor de una dilatación rápida durante la relajación cardíaca, originando el fenómeno de succión, que explica la gran velocidad de llenado con gradientes de presión muy bajos. Esta succión se ve favorecida por varios mecanismos19.
- –
La hipótesis de Torrent Guasp. La succión diastólica es secundaria al retroceso elástico pasivo del helicoide ventricular, como si se tratase de un resorte con propiedades elásticas. La relajación se hace casi explosiva y el sarcómero salta como un resorte para recuperar su longitud original. Si el volumen sistólico final se reduce, las fuerzas expansivas restauradoras son mayores; mientras que en las sobrecargas de presión o de volumen (miocardiopatía hipertrófica, insuficiencia cardíaca) se produce enlentecimiento de la relajación y reducción de la succión.
- –
La tensión de la pared ventricular después de la apertura de la válvula mitral se incrementa rápidamente por el aumento del radio intracavitario y la reducción del grosor de la pared, de acuerdo con la ley de Laplace. Esta fuerza expansiva actúa al final de la fase de relajación alargando las fibras y permitiendo llenarse rápidamente al ventrículo a pesar de una presión baja de llenado. Los cambios del grosor de la pared son previos a los cambios en el radio de la cavidad, es decir, el adelgazamiento de la pared precede y condiciona el llenado ventricular.
- –
El llenado diastólico de las arterias coronarias puede participar en la expansión activa miocárdica. El llenado del reservorio coronario durante la diástole puede distender la masa miocárdica como si el ventrículo fuera un cuerpo cavernoso y se generase un mecanismo eréctil que prolonga la cavidad ventricular. La circulación coronaria se convierte en una protección del músculo ventricular isquémico durante la sístole y se expande en diástole con el llenado del lecho coronario. Basándose en este principio, se ha desarrollado un modelo cardíaco compuesto por un doble saco elástico, cuyo aumento hidráulico de la presión intramural genera una expansión diastólica ventricular y que ha sido aplicado en dispositivos de asistencia circulatoria paracorpórea.
- –
El ventrículo derecho está diseñado para expulsar grandes volúmenes de sangre contra resistencias bajas, gracias a su forma semilunar de gran superficie. A diferencia del ventrículo izquierdo, donde la sangre es transferida desde el orificio mitral hasta el ápex antes de ser dirigido a la aorta, en el ventrículo derecho la sangre es enviada directamente desde el orificio tricúspide a la arteria pulmonar siguiendo una línea central de lavado que forma 90º.
En el modelo clásico de función cardíaca, las aurículas tienen dos funciones principales: una función de transporte o de bomba y una función de reservorio para realizar el llenado ventricular rápido. Como los ventrículos, las aurículas responden a un aumento de la longitud de la fibra con un aumento de la fuerza de contracción, y en reposo la contracción auricular contribuye en un 20% al llenado ventricular. El aumento de la contractilidad auricular y una desviación hacia la izquierda de las curvas de función de la aurícula o una desviación hacia la derecha de las curvas de fuerza-velocidad puede ser producida por estimulación simpática, inhibición vagal o por agentes inotrópicos. En la fibrilación auricular, los mecanismos de reserva circulatorios pueden mantener el gasto cardíaco en reposo o bien la pérdida de la contracción auricular puede producir graves consecuencias sobre el llenado ventricular y la función del corazón.
Hay resultados contrastados del estudio de las fases del ciclo cardíaco con suficiente peso para apoyar las curvas-gradiente de presión en la explicación del llenado ventricular:
- –
Durante el comienzo de la fase de relajación isovolumétrica, la presión del ventrículo izquierdo desciende por debajo de la presión de la aurícula izquierda poco después del vértice de la onda V auricular izquierda.
- –
La fase de llenado rápido ventricular al final de la fase de relajación isovolumétrica coincide con una continuación del descenso de la presión auricular que comenzó durante la relajación isovolumétrica. El final de la fase de llenado rápido ventricular y el comienzo de la fase de llenado ventricular lento se caracterizan por un cambio de inclinación en la curva de volumen ventricular.
- –
Durante la fase de llenado ventricular lento, las presiones de la aurícula y del ventrículo izquierdo aumentan lentamente hasta la siguiente sístole auricular. La contracción auricular y el aumento de llenado ventricular que produce se manifiestan por un aumento de la presión y del volumen ventricular.
Estas cuestiones no pueden resolverse si el fisiólogo permite que el anatómico realice su análisis estructural en solitario y si el clínico no admite que es preciso realizar un esfuerzo especial para aplicar los métodos diagnósticos. Nuestro grupo está centrando sus esfuerzos en los estudios de modelización cardiovascular del ventrículo izquierdo a través de una tecnología original desarrollada por Next Limit, la Universidad Paul Sabatier-Toulouse III, la E.T.S. Ingenieros Navales de la Universidad Politécnica de Madrid y el Canal de Experiencias Hidrodinámicas de El Pardo, para analizar la biomecánica computacional del ventrículo izquierdo20. Estas herramientas nos ofrecen información relevante sobre la fisiología cardiovascular y nos permitirán confirmar la hipótesis de Torrent Guasp y la validez del modelo de succión en el llenado ventricular.
Remodelado reverso del ventrículo izquierdoLa dilatación ventricular es un estado de adaptación a diferentes enfermedades cardiovasculares. Como resultado de esta situación se produce un remodelado cardíaco que conlleva un aumento de la tensión parietal y la dilatación progresiva. En el miocito, el proceso conduce a un deslizamiento irreversible, y consecuente desviación de la curva de presión/volumen hacia la derecha, aumento de los volúmenes ventriculares e insuficiencia mitral agregada. Este proceso de dilatación continuo determina el mayor riesgo de mortalidad en estos pacientes21.
Esta situación ha motivado que el estudio de la geometría ventricular alterada en la insuficiencia cardíaca sea de primordial interés para la aplicación de nuevas terapéuticas quirúrgicas que intentan restaurar esta situación, con el fin de mejorar su pronóstico.
Ya el genial Leonardo da Vinci (1452-1519), al estudiar el ventrículo izquierdo y la raíz aórtica, efectuó para sus análisis trazados geométricos22. Por su parte, W. Harvey realizó en su obra Exercitatio anatomica de motu cordis et sanguinis in animalibus (1628) la descripción del ventrículo izquierdo con forma estrecha y alargada durante la fase de eyección, tendiendo hacia una esfera durante la diástole2. El interés por estos estudios se remonta a Woods23 en 1892, pero es a mediados del siglo XX cuando Burton halla que el incremento de los volúmenes cardíacos aunado a un mayor radio interno del ventrículo produce una mayor tensión o estrés sobre su pared24.
Distintas técnicas quirúrgicas se han puesto en consideración clínica para solucionar tanto el tema de la dilatación ventricular como de las zonas postinfarto no contráctil. El análisis de ellas nos indica la necesidad de concurrir a una estrategia que retorne al ventrículo izquierdo a su configuración nativa para lograr la reconstrucción elipsoide.
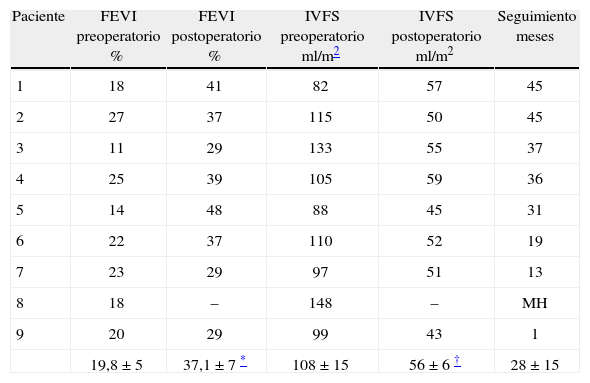
Material y métodosFueron intervenidos nueve pacientes, siete hombres, de 65±8 años , con insuficiencia cardíaca en clase funcional de la New York Heart Association (NYHA) III/IV (3,25) y una FE < 27%. La experiencia fue realizada en el Hospital Presidente Perón (Argentina). Los datos preoperatorios pueden observarse en la Tabla I.
Reconstrucción ventricular elipsoidal
| Paciente | FEVI preoperatorio % | FEVI postoperatorio % | IVFS preoperatorio ml/m2 | IVFS postoperatorio ml/m2 | Seguimiento meses |
| 1 | 18 | 41 | 82 | 57 | 45 |
| 2 | 27 | 37 | 115 | 50 | 45 |
| 3 | 11 | 29 | 133 | 55 | 37 |
| 4 | 25 | 39 | 105 | 59 | 36 |
| 5 | 14 | 48 | 88 | 45 | 31 |
| 6 | 22 | 37 | 110 | 52 | 19 |
| 7 | 23 | 29 | 97 | 51 | 13 |
| 8 | 18 | – | 148 | – | MH |
| 9 | 20 | 29 | 99 | 43 | 1 |
| 19,8±5 | 37,1±7 * | 108±15 | 56±6 † | 28±15 |
MH: mortalidad hospitalaria.
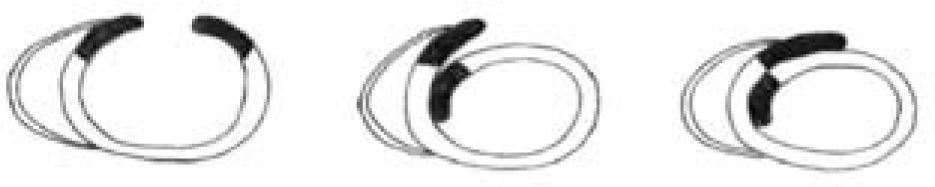
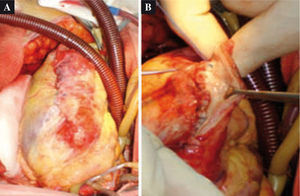
Como tratamiento concomitante a un paciente se le realizó cardiomioimplante con células madre de médula ósea; a siete pacientes, revascularización coronaria (tres asociados a terapia celular); en un paciente se remplazó la válvula mitral y cardiomioimplante celular. A todos se les efectuó reducción ventricular elipsoidal (Fig. 1).
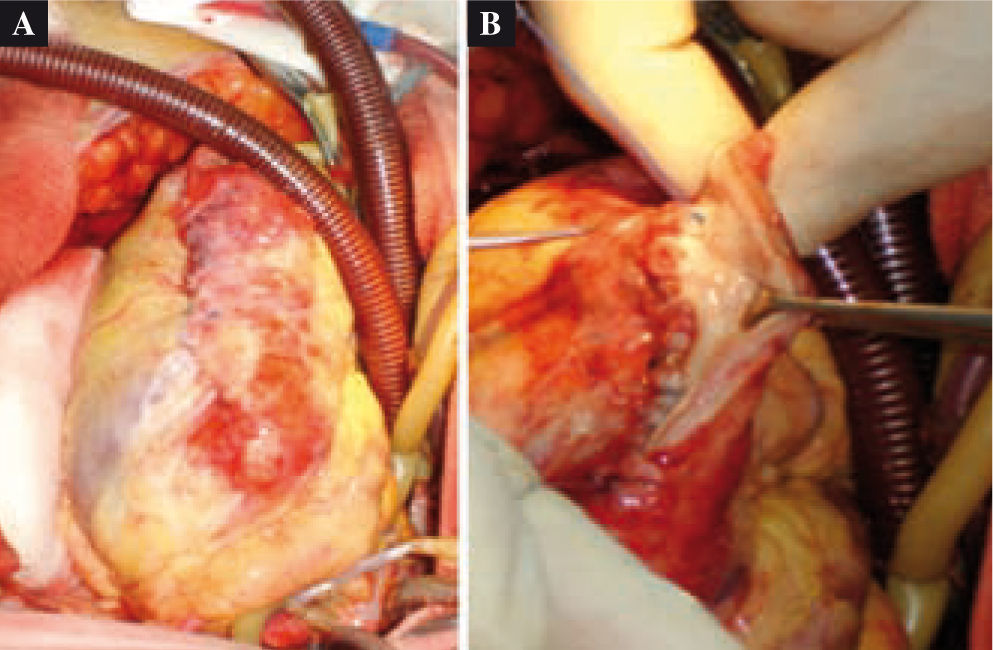
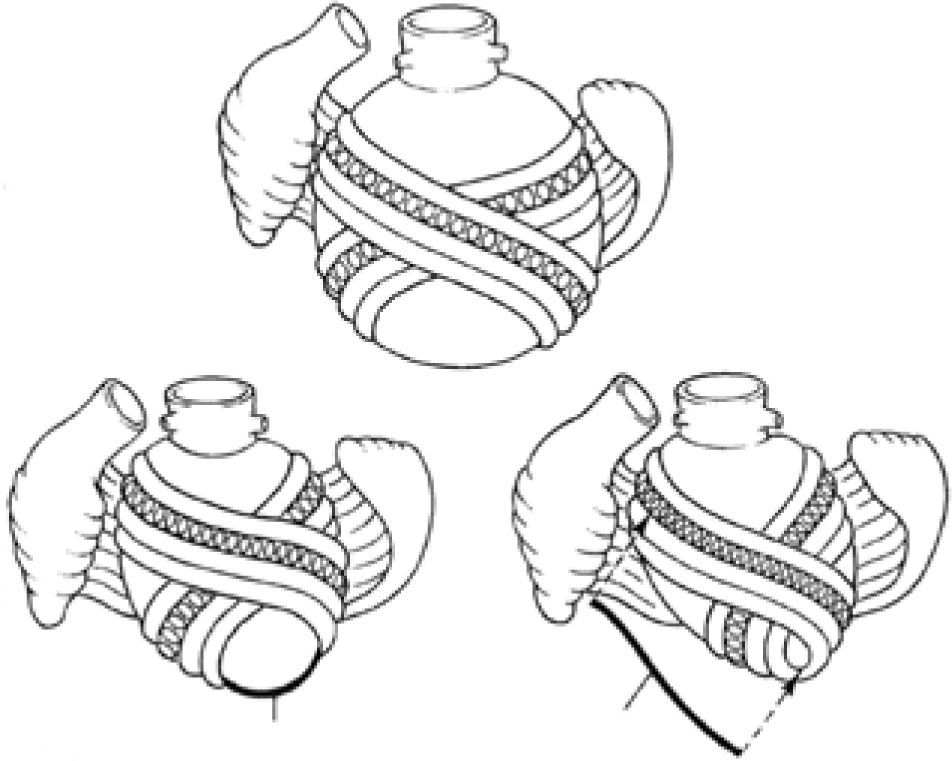
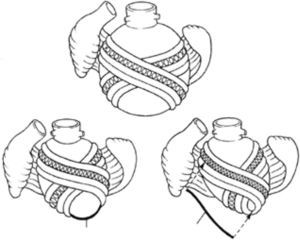
Técnica de reconstrucción elipsoidalLa técnica de reconstrucción elipsoidal del ventrículo izquierdo asume la posibilidad de restaurar su geometría dentro de la forma que necesita su función mecánica. Consta de los siguientes pasos (Figs. 2A y B):
- –
Una incisión longitudinal a lo largo de la arteria descendente anterior en la pared avascular del ventrículo izquierdo.
- –
El borde izquierdo de la incisión mediante una sutura continua es llevado al septum interventricular.
- –
El borde marginal remanente, o sea, del derecho, es suturado a la pared libre del ventrículo izquierdo.
- –
Tanto la incisión original como el tamaño de las solapas deben obedecer a la dilatación que presenta el ventrículo, o mejor dicho, a la cavidad que se desea conservar, con el fin de reducir el volumen ventricular.
Falleció un paciente en el postoperatorio inmediato a causa de infección mediastinal. Dos pacientes requirieron apoyo con inotrópicos durante 48horas. Los pacientes restantes cursaron sin complicaciones en el postoperatorio. Ocho pacientes completaron un promedio de seguimiento de 28±15 meses sin registrarse necesidad de reingresos ni mortalidad tardía (Tabla I).
La clase funcional (NYHA) pasó de 3,25±4 a 1,37±0,2 (p<0,0001 ); la fracción de eyección del ventrículo izquierdo (FEVI) aumentó de 19,8±5 a 37,1±7% (p<0,05 ) y el índice de volumen sistólico del ventrículo izquierdo (IFSVI) se redujo de 108,6±16 a 55,6±6ml/m2 (p<0,005) (Fig. 3).
DiscusiónFundamentos de la restauración elipsoidalLos fundamentos que implican restaurar la geometría del ventrículo izquierdo hacia una forma elipsoidal son: geométricos, anatómicos, funcionales y volumétricos.
GeométricosLa reconstrucción elipsoidal, forma geométrica que asume el ventrículo izquierdo, tiene que ver con la eficiencia en su función. Estructura y función están indisolublemente unidas para obtener el mayor rendimiento mecánico. La forma elipsoidal que presenta el ventrículo izquierdo se caracteriza por poseer la presencia de un diámetro mayor y dos diámetros menores de iguales dimensiones.
AnatómicosLos estudios llevados a cabo por Torrent Guasp1 han sido fundamentales para acoplar la relación anatómica que presenta el corazón a la mecánica cardíaca. Las cavidades ventriculares están definidas en su descripción por una banda miocárdica que describe dos vueltas en espiral extendiéndose desde la raíz de la arteria pulmonar hasta la raíz de la aorta. En esta configuración helicoidal se distingue un segmento ascendente y un segmento descendente. La banda miocárdica ventricular de esta forma describe dos espirales, lo cual implica que los ventrículos actúen como una musculatura circular. Esta contracción se ejerce sobre un punto de apoyo móvil, el cual está representado por el contenido delimitado por la propia musculatura circular, es decir, no hay puntos de apoyo extrínsecos (p. ej. musculatura esquelética), sino que, al contrario, es apoyado por el volumen residual intraventricular, lo cual le permite llevar a cabo tanto la función de expulsión como la de almacenamiento sanguíneo.
FuncionalesFísicamente, la presión intraventricular ejerce sobre la pared que la contiene una tensión que se resuelve con la ley del marqués Pierre de Laplace (1749–1827). Esta ecuación resuelve que la tensión por cm2 es igual al diámetro, por la presión, por pi. En este fundamento se explica como valioso el concepto desarrollado por la cirugía de reducción ventricular de Batista25, la cual se halla en consonancia con los postulados físicos mencionados.
VolumétricosSe vuelve imprescindible manejar no solo la forma (elipsoide) sino también el volumen cardíaco. El hecho mencionado que el efecto de torsión se realiza sobre el mismo contenido volumétrico determina un proceso autoexpansivo (autoorganizativo). A mayor volumen, mayor esfericidad, y viceversa. Cuando existe un 20% de masa ventricular complicada se inicia la remodelación, y esta pone en marcha la sobrecarga volumétrica.
Es definitivo saber que la esfericidad ventricular lleva como consecuencia un mayor estrés de pared. El estrés parietal actúa en tres direcciones: meridional o longitudinal, circunferencial y radial26. Cuando existe disfunción ventricular, el estrés de mayor incremento es el longitudinal. Estos hallazgos no solamente corresponden a pacientes con miocardiopatía dilatada idiopática, sino también a aquellos con cardiopatía isquémica con función ventricular deprimida, insuficiencia aórtica, insuficiencia mitral, comunicaciones interventriculares y estenosis aórtica con función ventricular deprimida. Incluso esta alteración en la geometría ventricular izquierda es el determinante principal de la aparición de regurgitación mitral funcional tanto en cardiopatías isquémicas como en idiopáticas27.
Antecedentes quirúrgicosSe vuelve imprescindible manejar no solo la forma (elipsoide) sino también el volumen cardíaco. El hecho mencionado que el efecto de torsión se realiza sobre el mismo contenido volumétrico determina un proceso autoexpansivo (autoorganizativo). A mayor volumen, mayor esfericidad, y viceversa. Cuando existe un 20% de masa ventricular complicada se inicia la remodelación, y esta pone en marcha la sobrecarga volumétrica.
La técnica de reducción ventricular de Batista25 consiste en resecar un segmento de la masa ventricular izquierda y consecuente sutura de los bordes remanentes, con el fin de reducir la cámara cardíaca. Puede acompañarse de reparación de la insuficiencia mitral. Ciertos autores consideran a este agregado táctico como el aspecto de mayor beneficio fisiopatológico en el contexto de la reducción de la masa ventricular. Con esta cirugía se busca reducir el diámetro del ventrículo izquierdo y eliminar la insuficiencia mitral. Los efectos hemodinámicos que se persiguen son el incremento de la FE y el índice cardíaco, mejorando la clase funcional. Además, se produce disminución del estrés parietal y de la presión intraventricular izquierda.
Los estudios a largo plazo no han determinado la viabilidad clínica de este procedimiento. La mortalidad operatoria es superior al 15%, y permanece alta durante los primeros meses del postoperatorio. La insuficiencia cardíaca y las arritmias han sido las principales causas de muerte en el seguimiento. La sobrevida actual a los seis meses del 56%28 hace que la faz técnica de esta cirugía deba revisarse, no así los principios físicos ya explicados.
La ventriculectomía parcial con esta técnica se hace sobre la pared anterolateral del ventrículo izquierdo, respetando la inserción de los músculos papilares. El área de distribución coronaria es el de la circunfleja. Se considera que por cada 3,14 cm (pi) de músculo resecado en su circunferencia, se produce la disminución de 1 cm en el diámetro de fin de diástole. La resección origina modificaciones estructurales en la geometría de los músculos papilares con el consiguiente alargamiento de las cuerdas tendinosas. Para evitar este prolapso de la válvula, se propuso aproximar ambas valvas en su sector medio a nivel del borde libre29.
Por su parte, también es posible el remodelado geometricoquirúrgico de la pared ventricular anterior después del infarto, incluyendo la resección de segmentos no contráctiles (técnica de Dor)30. Su eficiencia fue evaluada en 439 pacientes por Athanasuleas31. Estos pacientes fueron seguidos hasta 18 meses. Los procedimientos que se acompañaron incluyeron cirugía de revascularización coronaria en el 89%, plastia mitral en el 22% y sustitución mitral en el 4%. La mortalidad operatoria fue del 6,6%. La FE en el postoperatorio aumentó desde 29±10,4% a 39±12,4%, mientras que el volumen de fin de sístole disminuyó desde 109±71 a 69±42ml/m2. La supervivencia a los 18 meses fue del 84%.
Las presentaciones versátiles y los resultados logrados con la cirugía de reducción ventricular de Batista hacen que por el momento no tenga indicación clara. No existe documentación bibliográfica de beneficios a largo plazo. Este procedimiento, por el momento, no debe ser considerado dentro de las estrategias primarias en el tratamiento quirúrgico de la insuficiencia cardíaca grave. La resección ventricular realizada por Batista se llevó a cabo en una zona del elipsoidal ventricular inadecuado. No ha tenido en cuenta esta técnica la viabilidad en esos segmentos, la cual se agrega la resección de la arteria circunfleja o ramas de la misma, con la consiguiente isquemia y arritmias postoperatorias. Con este procedimiento se encontraron infartos de ambos músculos papilares, el cual puede ser asociado con el desarrollo de arritmia, infarto de miocardio y hemorragia pericárdica, contribuyentes indudables a la persistencia de la insuficiencia cardíaca. Nosotros creemos que esta situación se debe no al fallo conceptual del uso de la ecuación de Laplace, sino a vulnerar los fundamentos anatómicos y fisiológicos que nos ofrece el estudio pormenorizado de la función cardíaca.
La reconstrucción elipsoidal realizada de acuerdo a los fundamentos geométricos anatómicos y funcionales aquí presentados suman una serie de méritos cuando la comparamos con las técnicas tradicionales (Jatene, Dor, Batista)32 (Fig. 3). Ellos son:
- –
Preservación del músculo cardíaco al actuar sobre el área limitada por los segmentos descendente y ascendente de la banda miocárdica ventricular de acuerdo a los trabajos de Torrent Guasp1.
- –
Esta zona topográfica del corazón es avascular, lo cual impide arrastrar durante la resección el sistema arterial.
- –
En esta punta geográfica del corazón denominada ápex, el conducto que limitan las bandas ascendente y descendente origina un conducto virtual en el cual el endocardio se adosa al epicardio constituyendo una zona débil favorable a discinesias33.
- –
Preserva la arteria circunfleja.
- –
El efecto geométrico de solapa realizado con esta técnica conlleva un efecto de ciña en el periodo tardío del seguimiento.
- –
La porción excluida (anterior y punta del septum) no ejerce una presión directa desde dentro del corazón, poseyendo una indudable vitalidad para soportar la función cardíaca.
- –
Dada la distorsión del septum apical que sufre el remodelado, que está adelgazada, esta técnica elimina la discinesia en esta región aportando rigidez al tabique.
- –
Esta técnica no implica colocación de parches sintéticos, evitando dejar zonas no contráctiles en la superficie de contracción ventricular izquierda.
- –
La táctica mencionada acerca a los segmentos ascendente y descendente de la banda muscular, los cuales se encuentran separados en la insuficiencia cardíaca, contribuyendo a una mejora de la función.
- –
Consideramos tratar con esta técnica tanto la distorsión del septum como mejorar la función diastólica.
- –
La recuperación de la forma elipsoidal del corazón podría actuar sobre la alteración estructural del aparato mitral. Nosotros hemos observado que, después de la reducción del ventrículo, la válvula no necesitó reparación34.
La restauración hacia la geometría ventricular ha estimulado tanto el uso de técnicas para su evaluación como, asimismo, anular la distorsión espacial en la insuficiencia cardíaca. Indudablemente, la esfericidad a la cual acude el ventrículo izquierdo durante la insuficiencia cardíaca tiene un valor pronóstico ominoso. La geometría ventricular es un marcador sensible de la función y del pronóstico. Sea causa o consecuencia, su aparición determina en el paciente un aumento del consumo de oxígeno a través de un aumento del estrés de pared34,35. Seguramente es la consecuencia, pero también conlleva la culpabilidad de perpetuar la alteración.
La reconstrucción elipsoidal del ventrículo izquierdo pudo realizarse con baja morbimortalidad en pacientes con dilatación grave, disfunción sistólica e insuficiencia cardíaca avanzada grado D. La reducción del volumen ventricular se mantuvo en el seguimiento a largo plazo.
La mejoría de la clase funcional y de la FE del ventrículo izquierdo también pueden atribuirse a los procedimientos asociados, aunque la reducción del volumen del ventrículo tiene un papel importante. Esta técnica ayuda a reconstruir el ventrículo con una geometría elipsoidal alineando la salida del flujo hacia la aorta.