La trombosis es una de las causas de muerte más importante en los países industrializados. La trombosis arterial es responsable del infarto de miocardio y de los accidentes cerebrovasculares y se genera en zonas de daño arterial. Los antiplaquetarios y anticoagulantes desempeñan un papel fundamental en la prevención y tratamiento. La enfermedad tromboembólica venosa, a través de la trombosis venosa profunda y la embolia pulmonar, es la tercera causa de muerte después de los eventos arteriales. Ésta suele tratarse con anticoagulantes. En este trabajo se revisan los nuevos fármacos antiplaquetarios y anticoagulantes y su impacto en la cirugía cardiovascular.
Thrombosis is the main cause of mortality in the industrialized countries. Arterial thrombosis, responsible of acute myocardial infarction and cerebrovascular accidents are characterized by the presence of rich clots in platelets and with scanty fibrin (called “white thrombus”) that are generated in places of vascular injury. Under these circumstances antiplatelet agents are required for prevention and treatment. Nevertheless, as thrombin is the main enzyme of the coagulation system and is also a powerful platelet activator, anticoagulants are used to prevent arterial thrombosis. Venous tromboembolism, which includes deep venous thrombosis (DVT) and pulmonary embolism (PE), constitutes the third reason of cardiovascular mortality after myocardial infarction and stroke. Venous thrombi result from an activation of the coagulation and are constituted principally by fibrin, in which the red blood cells remain trapped together with scanty platelets (called “red thrombus”); they are generally treated with anticoagulant agents. In this paper we will discuss the new antiplatelet and anticoagulant agents and their impact in cardiovascular surgery.
La trombosis es la principal causa de mortalidad en los países industrializados y en vías de desarrollo. La trombosis arterial, responsable del infarto agudo de miocardio (IAM) e ictus isquémico, se caracteriza por la presencia de coágulos ricos en plaquetas y con escasa fibrina (denominados «trombos blancos»), que se generan en lugares de lesión vascular y se previenen y tratan con agentes antiplaquetarios. Sin embargo, como la trombina, principal enzima del sistema de coagulación, es un potente activador plaquetar, también se emplean anticoagulantes para prevenir la trombosis arterial. La enfermedad tromboembólica venosa (ETV), que incluye la trombosis venosa profunda (TVP) y la embolia pulmonar (EP), constituye la tercera causa de mortalidad cardiovascular tras el IAM e ictus. Los trombos venosos resultan de una activación de la coagulación y están constituidos principalmente por fibrina, en la que quedan atrapados los glóbulos rojos, y escasas plaquetas (denominados «trombos rojos»); se previenen y tratan generalmente con agentes anticoagulantes.
Agentes antiplaquetariosLas plaquetas desempeñan un papel esencial en la aterotrombosis. Estudios patológicos han demostrado que la ruptura de una placa aterosclerótica, responsable de la oclusión coronaria en dos tercios de los pacientes con síndromes coronarios agudos (SCA), expone colágeno subendotelial y otros componentes de la matriz extracelular que interaccionan con las plaquetas a través de receptores específicos. Dicha interacción promueve la adhesión y activación plaquetar, la liberación de mediadores (tromboxano A2 y adenosín difosfato [ADP]) y la expresión de glucoproteínas IIb/IIIa que promueven la agregación y formación del tapón hemostático. Por ello, la administración de fármacos antiplaquetarios que interfieren las diferentes fases de este proceso es fundamental en el manejo de pacientes con trombosis arterial (Tabla I).
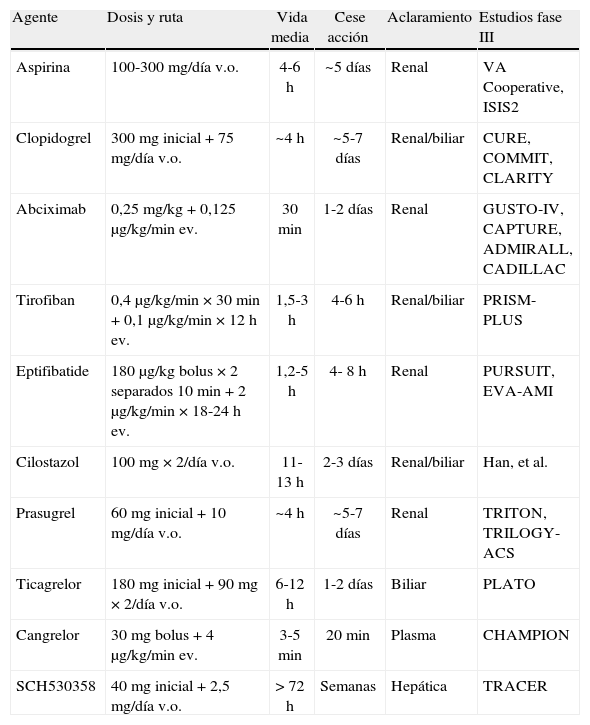
Características y desarrollo clínico de agentes antiplaquetarios clásicos y nuevos
| Agente | Dosis y ruta | Vida media | Cese acción | Aclaramiento | Estudios fase III |
| Aspirina | 100-300mg/día v.o. | 4-6h | ~5días | Renal | VA Cooperative, ISIS2 |
| Clopidogrel | 300mg inicial+75mg/día v.o. | ~4h | ~5-7días | Renal/biliar | CURE, COMMIT, CLARITY |
| Abciximab | 0,25mg/kg+0,125µg/kg/min ev. | 30min | 1-2días | Renal | GUSTO-IV, CAPTURE, ADMIRALL, CADILLAC |
| Tirofiban | 0,4µg/kg/min×30min+0,1µg/kg/min×12h ev. | 1,5-3h | 4-6h | Renal/biliar | PRISM-PLUS |
| Eptifibatide | 180µg/kg bolus×2separados 10min+2µg/kg/min×18-24h ev. | 1,2-5h | 4- 8h | Renal | PURSUIT, EVA-AMI |
| Cilostazol | 100mg×2/día v.o. | 11-13h | 2-3días | Renal/biliar | Han, et al. |
| Prasugrel | 60mg inicial+10mg/día v.o. | ~4h | ~5-7días | Renal | TRITON, TRILOGY-ACS |
| Ticagrelor | 180mg inicial+90mg×2/día v.o. | 6-12h | 1-2días | Biliar | PLATO |
| Cangrelor | 30mg bolus+4µg/kg/min ev. | 3-5min | 20min | Plasma | CHAMPION |
| SCH530358 | 40mg inicial+2,5mg/día v.o. | > 72h | Semanas | Hepática | TRACER |
La aspirina inhibe de forma irreversible la ciclooxigenasa y ha demostrado eficacia en la reducción de la mortalidad cardiovascular y eventos isquémicos en pacientes con SCA. Sin embargo, no inhibe completamente la agregación, posee efectos secundarios, fundamentalmente gastrointestinales, y su efecto permanece a lo largo de la vida media de la plaqueta (5-9días).
Las tienopiridinas, fundamentalmente clopidogrel, son antagonistas selectivos del receptor P2Y12 del ADP. En combinación con aspirina (terapia antiplaquetaria dual) se ha consolidado como el tratamiento estándar de pacientes con SCA y, particularmente, en aquellos que reciben un dispositivo intracoronario (stent). Su administración en forma de monoterapia estaría asimismo recomendada en pacientes con intolerancia a la aspirina. Sin embargo la inhibición plaquetaria es del 50%, existe una alta variabilidad individual y su metabolismo depende del citocromo CYP450, por lo que puede verse influenciado por la administración de diversos fármacos. Por sus características farmacocinéticas, su empleo debe posponerse en caso de cirugía de revascularización al menos 5-7días, estando contraindicado en el perioperatorio inmediato1,2.
Guías sobre el uso de antiplaquetarios en cirugía cardíacaLa guía clínica europea recomienda suspender aspirina 2-10días antes de la cirugía cardíaca electiva para reducir la hemorragia perioperatoria3. Los pacientes con SCA que requieren cirugía cardíaca con carácter urgente deberían continuar con aspirina hasta el día de la cirugía (grado B de recomendación).
En pacientes que necesitan cirugía cardíaca con carácter urgente, debería suspenderse el clopidogrel 5-7días antes de la cirugía. El beneficio sobre la reducción de hemorragia perioperatoria sería a expensas de un incremento del 1% del riesgo de cardiopatía isquémica mientras se espera la cirugía (grado B).
Nuevos antiplaquetariosEl prasugrel es una tienopiridina de tercera generación que se convierte en metabolito activo muy rápidamente, inhibiendo de forma más eficiente que el clopidogrel la agregación plaquetaria. Su rápida absorción oral y metabolismo permite obtener concentraciones máximas al cabo de 30min. Su uso se ha aprobado por la Food and Drug Administration (FDA) para pacientes con SCA en los que se planifica una intervención coronaria percutánea (angioplastia ± stent), en particular en pacientes con IAM. Sin embargo, su beneficio clínico conlleva mayor riesgo hemorrágico en relación con clopidogrel (2,4 vs 1,8%; hazard ratio [HR]: 1,32), no estando indicado en pacientes con historia previa de ictus, edad inferior a 75años y peso inferior a 60kg. En el 40% de pacientes del estudio TRITON que fueron sometidos a cirugía de revascularización miocárdica, prasugrel aumentó la incidencia de hemorragias mayores (18,8 vs 2,7%; HR: 9,19), por lo que no debería administrarse 1 semana antes de la realización de la cirugía.
Ticagrelor (AZD61409) es una nueva clase de inhibidor del receptor P2Y12 del ADP que actúa de forma reversible y no requiere metabolización hepática, siendo un potente inhibidor de la agregación plaquetaria. Se absorbe rápidamente, alcanzando un pico plasmático a las 2h, con una vida media de 7-12h. Recientemente se ha publicado el estudio PLATO en pacientes con SCA, observándose una reducción de 16% de eventos vasculares en relación con clopidogrel, sin incremento de las complicaciones hemorrágicas (11,6 vs 11,2%; p=0,43), si bien hubo una mayor incidencia de hemorragia intracraneal y episodios de bradicardia, por lo que se precisan estudios adicionales que confirmen su eficacia y seguridad.
Cangrelor es otro inhibidor irreversible del ADP por vía endovenosa. El inicio y cese de acción son rápidos con inhibición del 100% de la función plaquetaria. Se han realizado estudios en pacientes con SCA con y sin intervención coronaria percutánea que no han demostrado superioridad sobre clopidogrel, pero podría ser un antiplaquetario de interés como terapia puente perioperatoriamente en pacientes en los que podría discontinuarse el clopidogrel y que van a ser sometidos a cirugía de revascularización miocárdica.
SCH530348 es un potente inhibidor de la trombina que inhibe un 80% la agregación plaquetaria a la dosis inicial de 40mg vía oral (v.o.) sin aumentar significativamente la incidencia de hemorragia. Su uso se está evaluando en pacientes con SCA con resultados preliminares prometedores (TRA-PCI).
Las principales características e indicaciones para los nuevos antiplaquetarios se recogen en las tablas II y III4–6.
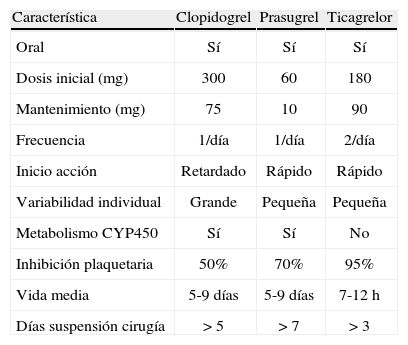
Características de los nuevos antipla-quetarios
| Característica | Clopidogrel | Prasugrel | Ticagrelor |
| Oral | Sí | Sí | Sí |
| Dosis inicial (mg) | 300 | 60 | 180 |
| Mantenimiento (mg) | 75 | 10 | 90 |
| Frecuencia | 1/día | 1/día | 2/día |
| Inicio acción | Retardado | Rápido | Rápido |
| Variabilidad individual | Grande | Pequeña | Pequeña |
| Metabolismo CYP450 | Sí | Sí | No |
| Inhibición plaquetaria | 50% | 70% | 95% |
| Vida media | 5-9días | 5-9días | 7-12h |
| Días suspensión cirugía | > 5 | > 7 | > 3 |
Recomendaciones nuevos antiplaquetarios en la práctica clínica
| Clopidogrel |
| – Tratamiento SCA (con y sin elevación ST) |
| – Pacientes con SCA susceptibles de intervencionismo coronario y con elevado riesgo hemorrágico |
| – Suspender al menos 5días antes de circulación extracorpórea (CEC) o cirugía mayor |
| Prasugrel |
| – SCA con elevación ST e intervencionismo coronario |
| – Eventos isquémicos con clopidogrel |
| – Contraindicado en: |
| • Paciente con antecedentes de ictus o accidente isquémico transitorio (AIT) |
| • Edad > 75años |
| • Peso < 60kg |
| – Suspender al menos 7días antes de CEC o cirugía mayor |
| Ticagrelor |
| – Tratamiento médico o intervencionista de SCA con anatomía coronaria no definida |
| – Pacientes en los que no se puede diferir cirugía de revascularización urgente |
| – Terapia puente en pacientes que reciben clopidogrel o plasugrel y requieren terapia antiplaquetaria previa cirugía |
| – Evitar en pacientes con EPOC y arritmias |
| – Suspender al menos 3días antes de CEC o cirugía mayor |
Durante los últimos 65años los únicos anticoagulantes orales disponibles han sido los antivitamina K (AVK) (Sintrom o warfarina). A pesar de su eficacia antitrombótica presentan numerosas limitaciones; las dosis de AVK difieren entre pacientes a causa de polimorfismos genéticos que afectan a su metabolismo; asimismo, múltiples interacciones con fármacos y alimentos afectan a la respuesta anticoagulante a AVK. Por ello, los pacientes requieren controles analíticos frecuentes y ajuste de dosis para asegurar el rango terapéutico requerido en cuanto al índice internacional normalizado (INR) (generalmente establecido en INR 2-3), con el consiguiente inconveniente para el paciente y elevados costes sanitarios. Además, sólo se consiguen niveles terapéuticos en la mitad de los pacientes. Todo ello hace que sean necesarios nuevos anticoagulantes orales administrados en dosis fijas y que presenten una respuesta anticoagulante predecible, de forma que no requieran monitorización y que puedan reemplazar a las AVK en el tratamiento antitrombótico.
¿Cuáles son las ventajas potenciales de los nuevos anticoagulantes orales?Los nuevos fármacos han sido diseñados para ser administrados en dosis fijas, sin necesidad de monitorización de laboratorio. Su efecto no se ve interferido por los alimentos, mientras que la interacción con otros fármacos es escasa. Por ello, los nuevos anticoagulantes tienen el potencial de simplificar el tratamiento a largo plazo de pacientes con trombosis7. Los prometedores resultados de estudios clínicos recientes en el ámbito de la trombosis venosa y arterial sugieren que, a corto plazo, pueden reemplazar a las AVK (Tabla IV).
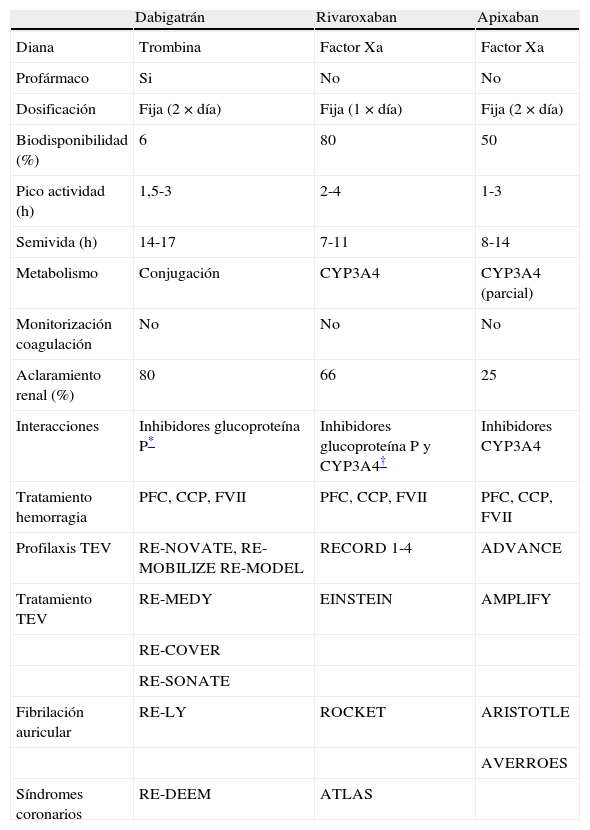
Características farmacológicas de los nuevos anticoagulantes orales y desarrollo clínico
| Dabigatrán | Rivaroxaban | Apixaban | |
| Diana | Trombina | Factor Xa | Factor Xa |
| Profármaco | Si | No | No |
| Dosificación | Fija (2×día) | Fija (1×día) | Fija (2×día) |
| Biodisponibilidad (%) | 6 | 80 | 50 |
| Pico actividad (h) | 1,5-3 | 2-4 | 1-3 |
| Semivida (h) | 14-17 | 7-11 | 8-14 |
| Metabolismo | Conjugación | CYP3A4 | CYP3A4 (parcial) |
| Monitorización coagulación | No | No | No |
| Aclaramiento renal (%) | 80 | 66 | 25 |
| Interacciones | Inhibidores glucoproteína P* | Inhibidores glucoproteína P y CYP3A4† | Inhibidores CYP3A4 |
| Tratamiento hemorragia | PFC, CCP, FVII | PFC, CCP, FVII | PFC, CCP, FVII |
| Profilaxis TEV | RE-NOVATE, RE-MOBILIZE RE-MODEL | RECORD 1-4 | ADVANCE |
| Tratamiento TEV | RE-MEDY | EINSTEIN | AMPLIFY |
| RE-COVER | |||
| RE-SONATE | |||
| Fibrilación auricular | RE-LY | ROCKET | ARISTOTLE |
| AVERROES | |||
| Síndromes coronarios | RE-DEEM | ATLAS |
PFC: plasma fresco congelado; CCP: concentrado de complejo protrombínico; CYP: citocromo.
Dabigatrán etexilato (Pradaxa®, Boehringer-Ingelheim) es un inhibidor oral directo de la trombina en avanzadas fases de desarrollo, con el que se han completado importantes estudios clínicos en trombosis venosa y arterial.
Se trata de un profármaco con una biodisponibilidad del 6% tras la ingesta. Tras su administración es rápidamente convertido por esterasas a dabigatrán. Alcanza un pico plasmático a las 2h de su administración, siendo eliminado por vía renal, con una vida media de 14-17h, lo que permite una o dos dosis diarias. Las principales interacciones farmacológicas son con inhibidores de glucoproteína P, como quinidina (contraindicado el dabigatrán) y verapamilo, así como con amiodarona, que potencian el efecto (Tabla IV).
Además de su eficacia en la prevención del tromboembolismo venoso (TEV) en pacientes sometidos a artroplastia de cadera y rodilla (estudios RE-MODEL, REMOBILIZE y RE-NOVATE) se han completado estudios con series amplias, tanto en el tratamiento de la ETV (estudio RE-COVER) como en la prevención del ictus recurrente en pacientes con fibrilación auricular (FA, estudio RE-LY)7–10 (Tabla IV).
Inhibidores del factor xaLos inhibidores orales del factor Xa son pequeñas moléculas que se unen de forma reversible al centro activo del factor Xa. Presentan una elevada disponibilidad, inicio rápido de acción, semivida de 7-12h y aclaramiento renal y extrarrenal. Rivaroxaban (Xarelto®, Bayer Shering Pharma AG) y apixaban (Pfizer, Bristol-Myers Squibb) son los fármacos en fases más avanzadas de investigación clínica (Tabla IV). Estudios fase III con rivaroxaban en la profilaxis de ETV en cirugía ortopédica mayor (programas RECORD) demuestran que es más efectivo que enoxaparina sin aumentar el riesgo hemorrágico. Sobre la base de estos estudios, rivaroxaban ha obtenido la aprobación de la Agencia Reguladora Europea para esta indicación. Otros estudios clínicos en curso evalúan su efecto en el tratamiento de la ETV (estudio EINSTEIN), prevención del ictus isquémico en pacientes con fibrilación auricular y en la prevención de recurrencia isquémica en pacientes con síndromes coronarios agudos (estudio ATLAS-TIMI 51)7,8,11 (Tabla IV).
Apixaban también parece un agente prometedor en la profilaxis y tratamiento de la trombosis venosa y arterial. Se absorbe rápidamente por vía oral, con un pico de actividad a las 3h y semivida de 12h. Estudios recientes indican que puede ser un fármaco prometedor en pacientes con SCA y FA9–12.
ConclusionesLos nuevos agentes antiplaquetarios se suman al armamentario terapéutico de pacientes con trombosis arterial, fundamentalmente SCA, donde pueden sustituir la terapia estándar de aspirina y/o clopidogrel. Conocer sus características farmacológicas será de crucial importancia para reducir las complicaciones hemorrágicas en caso de cirugía de revascularización o cualquier otro procedimiento de cirugía mayor.
En los últimos años se han diseñado nuevos anticoagulantes dirigidos contra dianas específicas de la coagulación. Entre ellos los inhibidores orales de la trombina y del factor Xa se encuentran en fases avanzadas de desarrollo clínico, en pacientes con FA, SCA y ETV. Administrados en dosis fijas, producen una respuesta anticoagulante más predecible que las AVK, eliminando la necesidad de monitorización de laboratorio y el frecuente ajuste de dosis. Ambos grupos de fármacos presentan un perfil farmacocinético y farmacodinámico más ventajoso que los existentes, por lo que se aproximan a las características del anticoagulante ideal (Tabla V). Sin embargo, existen aún cuestiones por resolver, como la falta de antídoto y su papel en el tratamiento en poblaciones especiales, como embarazo, insuficiencia renal y ancianos. No obstante, de los prometedores resultados clínicos obtenidos con dabigatrán en el tratamiento de la ETV y en la prevención del ictus isquémico en pacientes con fibrilación auricular, se infiere que éste y otros nuevos anticoagulantes orales reemplazarán a corto plazo a las AVK en el tratamiento de la trombosis.
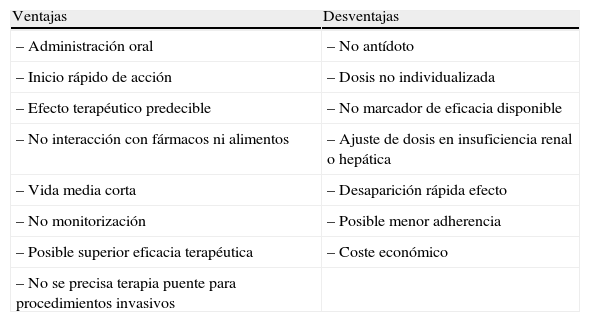
Ventajas y desventajas de los nuevos anticoagulantes orales
| Ventajas | Desventajas |
| – Administración oral | – No antídoto |
| – Inicio rápido de acción | – Dosis no individualizada |
| – Efecto terapéutico predecible | – No marcador de eficacia disponible |
| – No interacción con fármacos ni alimentos | – Ajuste de dosis en insuficiencia renal o hepática |
| – Vida media corta | – Desaparición rápida efecto |
| – No monitorización | – Posible menor adherencia |
| – Posible superior eficacia terapéutica | – Coste económico |
| – No se precisa terapia puente para procedimientos invasivos |