La fibrilación auricular postoperatoria complica con frecuencia la cirugía de revascularización coronaria. Nuestra hipótesis es que el aislamiento quirúrgico de las venas pulmonares podría reducir el riesgo de fibrilación auricular postoperatoria en los pacientes con perfil de alto riesgo.
Métodos y resultadosEstudio aleatorizado simple ciego, en pacientes de al menos 65 años, con antecedentes de hipertensión arterial o diabetes, pero sin fibrilación auricular previa, asignados a cirugía de revascularización (grupo control) o a cirugía más aislamiento epicárdico de las venas pulmonares (Cardioablate® BP2, Medtronic) y el aislamiento del apéndice auricular (grupo intervención). Todos los pacientes recibieron un Reveal® XT subcutáneo (Medtronic) para monitorizar a largo plazo la fibrilación auricular. Se consideró fibrilación auricular postoperatoria todo episodio de 2 min o más producido antes del alta. Se incluyó a 50 pacientes (edad promedio 71,6 años, 84% hombres), sin diferencias en las tasas de diabetes, hipertensión arterial o uso de betabloqueantes. No se presentaron complicaciones perioperatorias y no hubo aumento del tiempo operatorio promedio a causa del aislamiento de las venas pulmonares (200,6±54,8 min controles versus 201,2±30,3 min grupo intervención; p=0,47). Los pacientes con aislamiento de las venas pulmonares presentaron un 24% de fibrilación auricular postoperatoria versus un 60% en el grupo control, p=0,01. Se necesitó amiodarona en el 44% de los controles que presentaron fibrilación auricular versus el 16% en el grupo de intervención (p=0,06).
ConclusiónUna técnica quirúrgica simple como el aislamiento epicárdico de las venas pulmonares permite una disminución significativa de la fibrilación auricular postoperatoria.
Post operative atrial fibrillation is highly prevalent after CABG surgery; we hypothesized that pulmonary vein isolation, would reduce the risk of post operative atrial fibrillation in patients with high risk profile.
Methods and resultsPatients at least of 65 years old with history of either hypertension or diabetes, but not previous atrial fibrillation were randomized (1:1 singe blind) to a CABG surgery only (controls) or CABG plus pericardial isolation of both right and left pulmonary veins (Cardioablate® BP2, Medtronic), plus left atrial appendage exclusion. In all cases a Reveal® XT (Medtronic) was implanted for long term monitoring. Any atrial fibrillation lasting 2min or longer were considered as post operative atrial fibrillation. We included 50 patients (84% men; mean age 71.6 y.o.). There were no acute complications and no significant changes in surgical times due to the addition of PV isolation (200.6±54.8minutes, controls; versus 201.2±30.3minutes, intervention group; P=.47). There were no differences in basal characteristics, beta –blockers or ACE/Ang II inhibitors use, but a marked reduction of new atrial fibrillation in patients with pulmonary vein isolation (24% intervention group, versus 60% controls, P=.01). More patients with post op atrial fibrillation needed amiodarone for at least 30 days: 44% group control vs 16% intervention group; P=.06).
ConclusionA simple and time efficient surgical technique could significantly decrease the incidence of post operative atrial fibrillation, in pts with no history of atrial fibrillation, but high risk profile.
La fibrilación auricular (FA) es una verdadera pandemia del siglo xxi; su presentación aumenta con la edad, la presencia de diabetes y de hipertensión arterial, inclusive en pacientes sin valvulopatías y con aurículas de tamaño normal.
Los pacientes en el postoperatorio de diversas cirugías son proclives a desarrollar episodios de FA, y en el caso de la cirugía de revascularización coronaria, entre el 20 y el 50% de los pacientes presentarán episodios, los cuales retardan el alta hospitalaria, requieren el uso de antiarrítmicos y se asocian a peor pronóstico a corto y mediano plazo, aumentando la morbilidad y la mortalidad1.
La cirugía de MAZE es altamente eficaz para recuperar el ritmo sinusal a largo plazo (en el orden del 90%), incluso en pacientes valvulares con FA persistente y con aurículas dilatadas; sin embargo, la compleja técnica quirúrgica requerida ha evitado que esta opción sea muy difundida2.
De modo más reciente, técnicas denominadas mini-MAZE, con lesiones parciales en la aurícula izquierda, han logrado tasas de éxito mucho menores (en el orden del 30%) en los mismos pacientes, quizás debido a que una vez que la aurícula se dilata y se remodela, se necesitan lesiones más extensas para lograr restablecer el ritmo sinusal. No obstante, se acepta que los pacientes que deban ser intervenidos de todos modos por cirugía valvular o coronaria, y que presenten antecedentes de FA, son candidatos para diversas técnicas de tratamiento quirúrgico concomitante de la FA3.
En pacientes seleccionados, el aislamiento por catéter de las venas pulmonares obtiene una tasa de éxito de entre el 60 y el 90%, lo cual confirma que mientras menos enfermas estén las aurículas, menos lesiones son necesarias para mantener el paciente libre de FA4,5.
Los mismos pacientes con riesgo de presentar FA en el postoperatorio son los pacientes que presentarán más FA espontánea a largo plazo. Estos pacientes son así susceptibles de necesitar procedimientos costosos a largo plazo, como el aislamiento por catéter de las venas pulmonares6-9.
Nuestra hipótesis de trabajo parte del hecho que no siempre se puede tener el tórax ampliamente expuesto, como en el caso de la cirugía de revascularización coronaria, y que si de modo preventivo se aíslan las venas pulmonares con una técnica simple, a corto plazo se puede disminuir la incidencia de FA postoperatoria y a largo plazo se podría disminuir la aparición de FA en pacientes de alto riesgo.
Materiales y métodosNuestro estudio piloto se realizó en el Centre Hospitalier Universitaire de Sherbrooke (CHUS), Quebec, entre diciembre del 2009 y septiembre del 2013. Se incluyó a pacientes en espera de cirugía de revascularización coronaria, de al menos 65 años, con antecedentes de hipertensión arterial o diabetes, sin cirugía torácica previa y sin antecedentes de FA. El estudio fue aprobado por el Comité de Ética del Centro de Investigación Clínica del CHUS. Los pacientes fueron aleatorizados a simple ciego a recibir la cirugía de revascularización (grupo control) o a la cirugía más el aislamiento epicárdico de las venas pulmonares mediante el uso del sistema de radiofrecuencia Cardioablate® BP2 (Medtronic) y la exclusión del apéndice auricular (grupo intervención). En todos los pacientes, se implantó un sistema de monitorización subcutáneo (Reveal® XT, Medtronic) al final de la cirugía, y previo marcaje del mejor lugar de detección de las señales cardiacas, para el registro a corto y a largo plazo de la aparición de FA. Los pacientes fueron monitorizados durante su estancia hospitalaria con los sistemas habituales de la unidad de recuperación cardiovascular o mediante telemetría, luego de su transferencia al piso.
Todos los pacientes recibían antiagregantes plaquetarios y fueron operados con circulación extracorpórea, hipotermia a 34°C, exploración de la aorta con una sonda de ecoepiaórtico seguida de pinzamiento aórtico, parada cardiaca con cardioplejía sanguínea a 10°C, repetida de manera intermitente entre cada anastomosis distal, despinzamiento total y pinzamiento parcial de la aorta para realizar las anastomosis proximales. Se utilizó un control ecocardiográfico peroperatorio en todos los pacientes.
En los enfermos en que se realizó un aislamiento de las venas pulmonares, las derechas se aislaron con circulación extracorpórea a corazón latiendo y las izquierdas después del pinzamiento aórtico, seguido de la exclusión de la orejuela izquierda, con una bolsa de tabaco en su base, utilizando un Prolene 3/0 y añadiendo una ligadura de seda 2.
Se consideró FA postoperatoria a todo episodio de al menos 2 min de duración (límite impuesto por la tecnología del sistema Reveal® XT) y se revisaron los trazados de telemetría de todos los pacientes para confirmar el diagnóstico de FA. Los resultados se expresan como presencia o ausencia de FA, y como carga relativa de FA (porcentaje de tiempo en FA según el tiempo de monitorización).
El manejo postoperatorio inmediato se realizó en una unidad de recuperación, y si bien el equipo médico estaba al tanto del procedimiento realizado, no se dictó ninguna línea especial de conducta para estos pacientes, que fueron tratados de acuerdo con su evolución clínica y sin acceso a los registros del monitor subcutáneo.
El monitor Reveal® XT fue interrogado de modo diario durante la estancia hospitalaria (para evitar la pérdida de datos a causa de posible registro de ruido); luego del alta, se instruyó a los pacientes a interrogar su monitor una vez al día (con llamadas telefónicas de recordatorio cada semana) y a comunicarse con la enfermera responsable en caso de arritmia o memoria plena del monitor; se realizó luego una lectura a la visita concomitante de seguimiento quirúrgico a los 30 días, y se instruyó seguir interrogando el monitor una vez por semana, con lecturas y visitas al hospital 2 veces al año, luego de la visita del mes. El seguimiento total planificado fue de 3 años o hasta el fin de la vida útil del monitor Reveal® XT. Este reporte se ha preparado luego de completar el seguimiento de 24 meses en todos los pacientes.
El análisis estadístico se realizó a posteriori, con la asistencia del equipo de estadística del Centro de Investigación Clínica, mediante el uso del sistema SPSS 14.
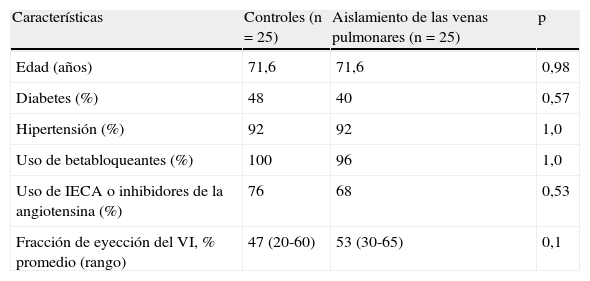
ResultadosSe incluyó a 50 pacientes, con un solo operador en todas las cirugías, para lograr homogeneidad en el aislamiento de las venas pulmonares. Las características basales fueron similares en los 2 grupos (tabla 1). La edad promedio±desviación estándar en ambos grupos fue de 71,6±4,6 años (rango de 65 a 81 años) y el 84% de los pacientes fueron varones. La diabetes y la hipertensión arterial tuvieron una distribución similar, y tampoco hubo diferencias significativas en cuanto al uso de betabloqueantes y de inhibidores de la enzima de conversión en ambos grupos.
Características basales de la población
| Características | Controles (n = 25) | Aislamiento de las venas pulmonares (n = 25) | p |
| Edad (años) | 71,6 | 71,6 | 0,98 |
| Diabetes (%) | 48 | 40 | 0,57 |
| Hipertensión (%) | 92 | 92 | 1,0 |
| Uso de betabloqueantes (%) | 100 | 96 | 1,0 |
| Uso de IECA o inhibidores de la angiotensina (%) | 76 | 68 | 0,53 |
| Fracción de eyección del VI, % promedio (rango) | 47 (20-60) | 53 (30-65) | 0,1 |
Durante el estudio, no se produjeron infartos de miocardio, ni accidentes vasculares cerebrales, ni decesos asociados a la cirugía durante el período postoperatorio inmediato. Un paciente del grupo control, transferido a su hospital de referencia, murió antes de los 30 días a causa de una probable hipoxia nocturna con secuelas, y con deseo posterior de la familia de suspender todo tratamiento. No hubo complicaciones asociadas al aislamiento de las venas pulmonares; los tiempos necesarios para aislar las venas fueron de 23±3,9 s para las venas derechas y de 22,2±3,2 s para las venas izquierdas; recordamos que el sistema utilizado aplica radiofrecuencia hasta que la impedancia cambia para asegurar que una lesión transmural ha sido lograda.
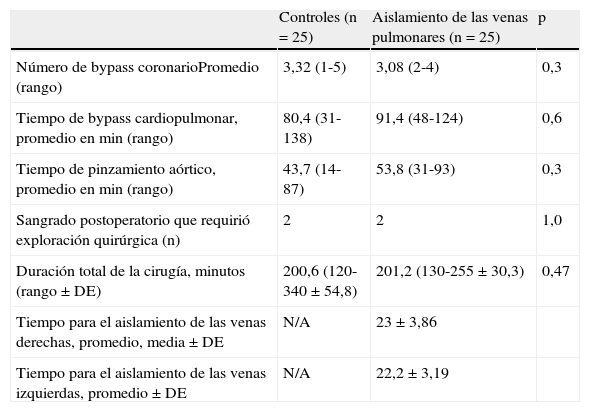
La duración de la cirugía fue similar en ambos grupos, 200,6±54,8 min (rango de 120 a 340 min) para el grupo control versus 201,2±30,3 min (rango de 130 a 255 minutos) para el grupo de intervención (p=0,47), y tampoco hubo diferencias significativas en los tiempos de circulación extracorpórea y pinzamiento aórtico, o en el número de puentes (entre 1 a 5) entre los grupos control y de intervención (tabla 2).
Resultados quirúrgicos
| Controles (n = 25) | Aislamiento de las venas pulmonares (n = 25) | p | |
| Número de bypass coronarioPromedio (rango) | 3,32 (1-5) | 3,08 (2-4) | 0,3 |
| Tiempo de bypass cardiopulmonar, promedio en min (rango) | 80,4 (31-138) | 91,4 (48-124) | 0,6 |
| Tiempo de pinzamiento aórtico, promedio en min (rango) | 43,7 (14-87) | 53,8 (31-93) | 0,3 |
| Sangrado postoperatorio que requirió exploración quirúrgica (n) | 2 | 2 | 1,0 |
| Duración total de la cirugía, minutos (rango±DE) | 200,6 (120-340±54,8) | 201,2 (130-255±30,3) | 0,47 |
| Tiempo para el aislamiento de las venas derechas, promedio, media±DE | N/A | 23±3,86 | |
| Tiempo para el aislamiento de las venas izquierdas, promedio±DE | N/A | 22,2±3,19 |
DE: desviación estándar.
Se registraron 4 casos de sangrado postoperatorio, que requirió reintervención, 2 en cada grupo; en ninguno de los casos el sangrado provino de las lesiones realizadas para aislar las venas pulmonares.
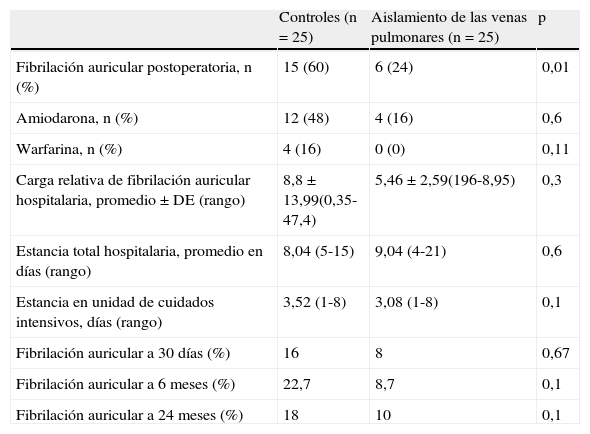
El objetivo principal de este estudio, la incidencia de FA postoperatoria, fue disminuido de modo significativo en el grupo de aislamiento preventivo de las venas pulmonares; 15 pacientes (60%) del grupo control presentaron FA versus 6 pacientes (24%) del grupo en el que se realizó el aislamiento de las venas pulmonares (p=0,01). Del mismo modo, el uso de amiodarona fue más elevado en el grupo control (44% de los pacientes del grupo control que presentaron FA requirieron amiodarona versus 16% del grupo intervención, p=0,06), si bien la diferencia no fue significativa debido al número escaso de pacientes. Ningún paciente del grupo de intervención requirió anticoagulación, mientras que 4 pacientes del grupo control fueron dados de alta con warfarina (tabla 3). La carga relativa de FA fue superior en el grupo control, pero sin alcanzar diferencia estadística: la carga fue de 7,4±13,4 (rango de 0,4 a 47,4) para el grupo control versus 5,4±2,6 (rango de 2,2 a 8,9) para el grupo de intervención, p=0,08. Tampoco se observó diferencias en cuanto a la duración total de estancia (7,9±2,9 días en el grupo control versus 8,9±4,4 días en el grupo intervención; p=0,8), ni en cuanto a la estancia en la unidad de cuidados intensivos entre ambos grupos. No hubo diferencias significativas en la tasa de FA a 30 días (16% para el grupo control versus 8% para el grupo intervención, p=0,67).
Resultados postoperatorios
| Controles (n = 25) | Aislamiento de las venas pulmonares (n = 25) | p | |
| Fibrilación auricular postoperatoria, n (%) | 15 (60) | 6 (24) | 0,01 |
| Amiodarona, n (%) | 12 (48) | 4 (16) | 0,6 |
| Warfarina, n (%) | 4 (16) | 0 (0) | 0,11 |
| Carga relativa de fibrilación auricular hospitalaria, promedio±DE (rango) | 8,8±13,99(0,35-47,4) | 5,46±2,59(196-8,95) | 0,3 |
| Estancia total hospitalaria, promedio en días (rango) | 8,04 (5-15) | 9,04 (4-21) | 0,6 |
| Estancia en unidad de cuidados intensivos, días (rango) | 3,52 (1-8) | 3,08 (1-8) | 0,1 |
| Fibrilación auricular a 30 días (%) | 16 | 8 | 0,67 |
| Fibrilación auricular a 6 meses (%) | 22,7 | 8,7 | 0,1 |
| Fibrilación auricular a 24 meses (%) | 18 | 10 | 0,1 |
Un paciente de cada grupo retiró el consentimiento, declinando las visitas de seguimiento; un paciente de cada grupo murió antes del seguimiento a 6 meses (uno del grupo control mencionado previamente y un segundo del grupo de intervención, con causa desconocida). Un total de 6 pacientes pidieron retirar el monitor subcutáneo a causa de dolor en el sitio de implante antes del final del seguimiento (el mapeo de las mejores señales requirió un implante bajo, entre el tercero y el cuarto espacio intercostal y de modo oblicuo al eje mayor, razón probable del aumento del dolor); en 3 pacientes más se tuvo que implantar un desfibrilador (2 en prevención primaria de la muerte súbita, por fracción de eyección inferior al 30%, y un tercer paciente a causa de taquicardia ventricular); así, se cuenta con datos sobre la FA a 6 meses en 23 pacientes del grupo intervención y en 22 pacientes del grupo control; con estas limitaciones, se registró FA paroxística asintomática en la visita a los 6 meses en el 22,7% de los pacientes del grupo control versus el 8,7% de los pacientes del grupo intervención, p=NS. Un total de 20 pacientes del grupo intervención y de 22 pacientes del grupo control completaron el seguimiento de 24 meses, con presencia de FA en el 18% de los pacientes del grupo control (siempre asintomática, excepto un paciente con aleteo auricular permanente) y en el 10% de los pacientes del grupo intervención (p=NS).
No se presentó, hasta el momento, ningún aleteo auricular izquierdo, complicación posible luego del aislamiento de las venas pulmonares. Los pacientes que requirieron la extracción del monitor subcutáneo han sido seguidos en visita anual con ECG, según protocolo habitual de seguimiento quirúrgico, sin evidencia de FA sintomática y con ritmo sinusal en el ECG.
Al final del seguimiento disponible, los pacientes que presentaron FA fueron todos pacientes que la presentaron también en el postoperatorio, tanto en el grupo control como en el de intervención.
DiscusiónDiversas intervenciones farmacológicas y no farmacológicas han sido empleadas para disminuir la aparición de FA en el postoperatorio de la cirugía de revascularización coronaria1,10. Los mecanismos son diversos, pero se estima que la FA comienza en la aurícula izquierda cuando se acumulan elementos (sustrato anormal, aumento de las extrasístoles que actúan como gatillo, desbalance entre el tono simpático y parasimpático) que, sumados al estrés quirúrgico, desencadenan la arritmia11-13, y de allí nuestra hipótesis de intervención: el aislamiento preventivo de las venas pulmonares, como tratamiento concomitante durante una cirugía de revascularización coronaria, podría disminuir los focos arritmogénicos (confinando las extrasístoles a las venas) y, al realizar el aislamiento a partir del epicardio, efectuaría una denervación local (pues muchos de los plexos autonómicos terminan cerca del ostium de las venas pulmonares); en ambos casos, se altera la iniciación de la arritmia y se altera su mantenimiento por eliminación de los rotores periantrales.
El apéndice auricular puede ser considerado como una quinta vena pulmonar y su aislamiento contribuye también a eliminar esta estructura arritmogénica, así como disminuir el riesgo embólico al eliminar la fuente más frecuente de trombosis, en caso de que la fibrilación se presente de todos modos. El objetivo principal de nuestra técnica fue disminuir a corto plazo la incidencia de FA postoperatoria, pero con un objetivo mayor en la mira a largo plazo: disminuir la incidencia de FA en pacientes sin antecedentes de FA pero de alto riesgo de desarrollar esta arritmia.
La población estudiada es representativa de los pacientes actuales que son sometidos a cirugía de revascularización coronaria: pacientes cada vez más añosos y con múltiples comorbilidades, como hipertensión arterial, diabetes y disfunción ventricular izquierda, lo cual puede explicar en parte la incidencia superior de FA postoperatoria en el grupo control.
La técnica quirúrgica, si bien de una cierta complejidad, en manos experimentadas, no aumenta de modo significativo la duración de la cirugía ni la tasa de complicaciones.
Si bien el objetivo a corto plazo es claro (presencia o ausencia de FA en el postoperatorio), nuestro estudio es el primero que investiga esta técnica con el adyuvante de una monitorización intensiva de las arritmias, mediante el implante de un monitor subcutáneo. Eso puede además explicar que la tasa de arritmia en el grupo control es superior a la de los controles históricos, pues es aceptado que la monitorización más intensiva incrementa la probabilidad de diagnosticar episodios asintomáticos de arritmia; así nuestro estudio es el primero que puede, sin duda alguna, obtener la verdadera incidencia de FA postoperatoria14.
El aislamiento quirúrgico de las venas pulmonares es parte de las recomendaciones actuales como cirugía concomitante en caso de cirugía cardiaca, cuando existen antecedentes de FA, pero el aislamiento preventivo no ha sido ampliamente estudiado. Los resultados en nuestros pacientes en quienes se aíslan las venas pulmonares son concluyentes: una disminución significativa en la aparición de FA postoperatoria. Es cierto que el uso de un monitor subcutáneo podría diagnosticar episodios tan breves que no tendrían impacto clínico, pero en nuestro estudio, el equipo a cargo de los cuidados postoperatorios no estaba al tanto de las lecturas del monitor subcutáneo y todas las conductas fueron basadas en la monitorización convencional y el estado clínico de los pacientes, que necesitaron —aunque sin diferencias estadísticas— de más amiodarona en el grupo control que en el grupo intervención, tendencia que, de modo indirecto, muestra que la FA, luego del aislamiento de las venas pulmonares, podría ser de menor duración y, por lo tanto, tener menor impacto clínico. Si bien la carga relativa promedio de FA no mostró diferencias significativas, la tendencia es clara: ningún paciente del grupo intervención presentó una carga relativa superior al 9%, mientras que en el grupo control la carga relativa máxima fue del 47%, todo lo cual nos indica que el aislamiento de las venas pulmonares logra no solo disminuir el porcentaje de FA postoperatoria, sino que además, cuando la FA se presenta, es de menor duración y con menor impacto clínico; esto está apoyado por el hecho de que ningún paciente del grupo intervención requirió anticoagulación al alta.
Es reconocido el hecho de que la FA postoperatoria aumenta no solo la morbilidad, sino también la mortalidad a largo plazo15, de ahí el interés de desarrollar técnicas simples que disminuyan la incidencia de FA postoperatoria; en nuestro estudio, los criterios de inclusión buscaron a pacientes sin antecedentes clínicos de FA (imposible, sin embargo, saber si habían ya presentado episodios de fibrilación asintomática) pero de alto riesgo; esto puede haber ayudado a que la intervención se muestre eficaz de modo significativo, al aumentar las probabilidades de que los pacientes del grupo control presenten FA postoperatoria, como efectivamente ocurrió (a pesar del uso cuasi universal de betabloqueantes y la alta penetrancia del uso de bloqueadores del sistema renina angiotensina).
Nuestras estimaciones iniciales mostraban que para demostrar una disminución del 50% de la FA postoperatoria (p<0,05 y 80% de poder estadístico), en el orden del 30 al 15%, se necesitaban 134 pacientes en cada grupo y, del mismo modo, que para poder disminuir a largo plazo la aparición de FA en el orden del 50% (tasa acumulativa a 3s años del 10 al 5%), se necesitaban de 474 pacientes en cada grupo. Nuestro estudio piloto podría mostrar resultados sesgados por una simple falta de poder estadístico; la tendencia clara y el hecho de que varios parámetros van en la misma dirección muestran un claro potencial de esta técnica, sin aumento de duración de la cirugía y sin aumento del riesgo quirúrgico.
Según nuestra mejor información, por el momento, un solo grupo canadiense, posteriormente al inicio de nuestro proyecto, ha aplicado la técnica de aislamiento de venas pulmonares, estudio aún no publicado, pero sin el uso del monitor subcutáneo; este grupo no observó diferencias en cuanto a la incidencia de FA clínica, definida como aquella que necesitaba prolongar la estancia hospitalaria o el uso de medicamentos para el control de la arritmia. No contamos con mayor información para explicar las diferencias con respecto a nuestro estudio.
De modo accesorio, y si bien el número limitado de pacientes y la pérdida de sujetos en el seguimiento complican las conclusiones (inclusive si los pacientes retirados tuviesen todos FA, aun así no hay diferencia estadística a 24 meses), podemos decir que, a mediano plazo, quienes de modo espontáneo, o gracias a la intervención fueron «resistentes» a la aparición de FA en el postoperatorio, tienen también más probabilidad de seguir libres de arritmia a mediano plazo, mientras quienes presentan un sustrato más enfermo, y FA a pesar de la intervención, seguirán presentando episodios en el seguimiento.
El impacto clínico, para una técnica que se puede realizar sin prolongar la cirugía, puede ser enorme, no solo a corto plazo, lo que demostramos en este estudio, sino, y sobre todo, a largo plazo, pues las técnicas de aislamiento de venas pulmonares por catéter son costosas, complejas y efectivas solo para la mitad a los 2 tercios de los pacientes tratados, dado que aislar las venas con catéteres desde el exterior difícilmente puede lograr la transmuralidad necesaria y fácilmente obtenible cuando el tórax está abierto.
Finalmente, si bien nuestros resultados son muy alentadores, los únicos resultados positivos están circunscritos al período postoperatorio; un estudio con el número suficiente de pacientes debería ser realizado para confirmar que esta simple técnica consolida el impacto clínico que hemos observado en nuestro estudio piloto.
ConclusiónEl aislamiento preventivo de las venas pulmonares, realizado como procedimiento concomitante a una cirugía de revascularización coronaria, es una técnica segura, que no aumenta de modo significativo el tiempo operatorio y que logra, en pacientes de alto riesgo, una disminución significativa de la FA postoperatoria. No se presentaron diferencias significativas al seguimiento de hasta 24 meses; sin embargo, el seguimiento a largo plazo con un dispositivo de monitorización subcutáneo permite obtener datos precisos sobre la presencia de arritmia asintomática. Un estudio con un número suficiente de pacientes podría confirmar si este simple gesto quirúrgico logra disminuir también la carga de FA a largo plazo.
FinanciaciónInvestigación realizada con una ayuda de Medtronic de Canadá.
Conflicto de interesesLos autores declaran no tener ningún conflicto de intereses.
La SECTCV, en su XXI Congreso Nacional de Sevilla, en junio del 2012, otorgó a este estudio primer premio como mejor trabajo de investigación.