La cardioplejia Custodiol® ofrece protección miocárdica durante tres horas mediante dosis única permitiendo realizar procedimientos complejos sin interrupción. Existe discusión respecto a la conveniencia de la protección miocárdica ofrecida mediante dosis única.
ObjetivoComparar resultados de morbimortalidad perioperatorios de cardioplejia cristaloide usada en nuestro centro (St. Thomas no. 2 [ST2]) respecto a Custodiol en cirugías complejas.
Material y métodoEstudio retrospectivo comparativo en pacientes intervenidos desde mayo 2016 a diciembre 2019 de cirugía cardíaca con tiempos de pinzamiento mayor de 80 minutos, clasificados según el tipo de cardioplejia: grupo ST2 vs. grupo Custodiol.
ResultadosSe incluyeron 712 pacientes: 548 en grupo ST2 y 164 en grupo Custodiol. Respecto a las variables preoperatorias, en el grupo Custodiol hubo más mujeres, más reintervenciones, mayor número de casos emergentes y un EuroSCORE Logístico y ii más elevados (4,90% vs. 7,19%, p = 0,000).
Además, el grupo Custodiol presentó mayores tiempos de circulación extracorpórea (CEC) (127 vs. 149 minutos, p = 0,000) y de pinzamiento (106 vs. 124 minutos, p = 0,0001) y un mayor porcentaje de pacientes requirió desfibrilación tras el despinzamiento (16,2% vs. 34,6%, p = 0,000).
La mortalidad operatoria fue similar (3,8% vs. 6,1%, p = 0,152). La estancia hospitalaria fue dos días mayor en el grupo Custodiol.
En el análisis multivariante, el tipo de cardioplejia no resultó factor de riesgo independiente para morbilidad postoperatoria ni mortalidad.
ConclusionesNuestro centro propone Custodiol® en casos complejos con tiempos de pinzamiento largos como alternativa comparable y segura a la cardioplejia cristaloide convencional, ya que ofrece una cómoda protección miocárdica con la misma incidencia de complicaciones postoperatorias.
Custodiol® cold crystalloid cardioplegia offers myocardial protection for up to three hours with one single dose, allowing to perform complex procedures without interruption. There is concern about the adequacy of single dose cardioplegia in terms of myocardial protection.
ObjectiveTo compare results of perioperative morbidity and mortality of conventional crystalloid cardioplegia used in our hospital (St.Thomas 2 [ST2]) versus Custodiol in complex cardiac surgery.
MethodsA retrospective comparative study was conducted between patients who underwent cardiac surgery with aortic cross-clamping times over 80 minutes, from May 2016 until December 2019. They were divided into two groups of cardioplegia: ST2 group versus Custodiol group.
ResultsThe study included 712 patients, of whom 548 were in ST2 group and 164 in Custodiol group. Preoperative variables showed a greater number of women, re-interventions, and emergent cases, with the highest EuroSCORE ii (4.90% vs. 7.19%, p = 0.000) in the Custodiol group.
The Custodiol group also had longer cardiopulmonary bypass times (127 vs. 149 minutes, p = 0.000) and aortic cross-clamping times (106 vs. 124 minutes, p = 0.0001), and a greater number of ventricular arrhythmias that needed defibrillation (16.2% vs. 34.6%, p = 0.000).
Surgical mortality did not show any differences (3.8% vs. 6.1%, p = 0.152). Hospital stay was two days longer in the Custodiol group.
In multivariate analysis, type of cardioplegia did not result in an independent risk factor for post-operative morbidity and mortality.
ConclusionsThis hospital centre proposes the use of Custodiol in complex cardiac surgery with prolonged aortic cross-clamping times as a safe alternative to conventional crystalloid cardioplegia, as it offers good myocardial protection for surgeons, with same incidence of post-operative complications.
El daño miocárdico tras una inadecuada protección miocárdica intraoperatoria se asocia a morbimortalidad perioperatoria1.
Los componentes ideales de las soluciones cardiopléjicas se encuentran en constante debate.
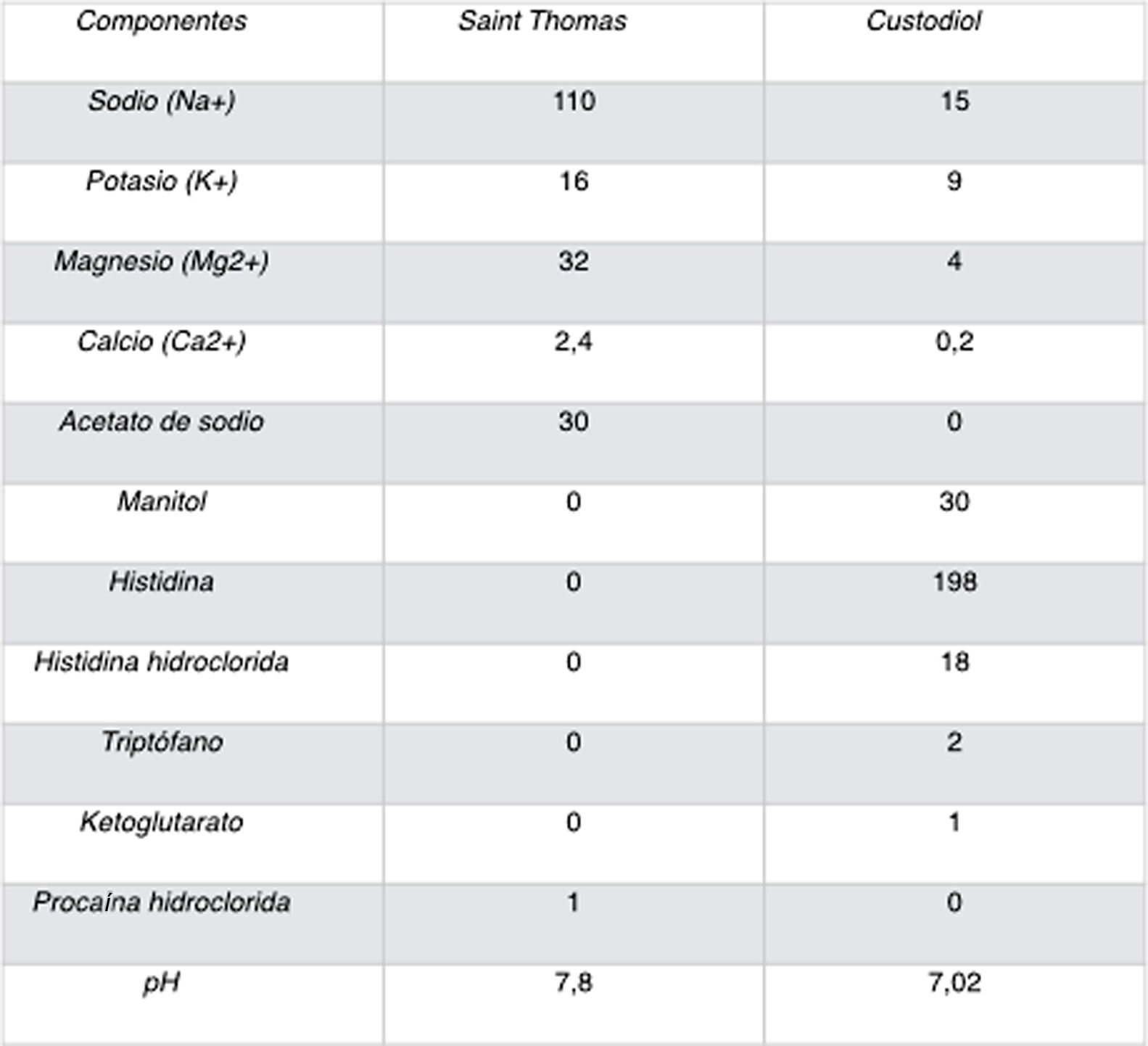
Las variantes históricas de cardioplejia principales han sido la solución Bretschneider, que consistía primariamente de sodio, magnesio y procaína; la solución Saint Thomas, consistente en potasio, magnesio y procaína añadida a Ringer, y las soluciones ricas en potasio que no contenían ni magnesio ni procaína.
Otra es la variante cardiopléjica hemática rica en potasio, que se basa en la sangre como vehículo de reparto por su capacidad de tampón y oxigenación2-6.
La cardioplejia cristaloide ofrece una protección miocárdica excelente, con tasas de infarto perioperatorio < 4% y de mortalidad perioperatoria < 2%7,8. Se trata de una cardioplejia extracelular e induce una parada cardíaca en diástole por despolarización de la membrana.
La solución cardiopléjica de Bretschneider, HTK (histidina-triptofano-ketoglutarato) o Custodiol® se considera atractiva en cirugía cardíaca y para preservación de órganos en trasplante, ya que se administra como única dosis ofreciendo una protección miocárdica durante un período de hasta tres horas, permitiendo la realización de procedimientos complejos sin interrupción9-13. Descrita por Bretschneider en 197012, fue clasificada como una cardioplejia cristaloide e intracelular debido a su bajo contenido en sodio y calcio. El mecanismo de actuación es diferente al de las cardioplejias extracelulares, ya que induce la parada cardíaca causando una hiperpolarización de la membrana del miocito.
En la figura 1 se observan los componentes de la cardioplejia cristaloide convencional Saint Thomas y Bretschneider. El alto contenido en histidina tampona la acidosis causada por el acúmulo de metabolitos anaerobios durante el largo período de isquemia, el ketoglutarato mejora la producción de ATP durante la reperfusión, el triptófano estabiliza la membrana celular y el manitol disminuye el edema celular y actúa como eliminador de radicales libres. La osmolaridad del HTK es fisiológica, por lo que no hay trasvase de agua del espacio extracelular al intracelular.
Hay controversia sobre la aparición de hiponatremia como consecuencia de la rápida administración del alto volumen requerido de esta solución cardiopléjica baja en sodio. Estas fluctuaciones en la concentración del sodio se han asociado a convulsiones postoperatorias en la población pediátrica14,15.
Las cardioplejias de dosis única tipo Custodiol han captado interés creciente, sobre todo en cirugía mínimamente invasiva, ya que permite al cirujano una cómoda protección miocárdica sin necesidad de ser readministrada cada cierto intervalo, con el consumo de tiempo y la interrupción de la intervención que ello conlleva.
Existe una comprensible preocupación sobre la conveniencia de la protección miocárdica ofrecida por una sola dosis de cardioplejia. A pesar de su uso extendido en Europa, hay pocos estudios comparando la eficacia del Custodiol con la cardioplejia cristaloide de uso convencional.
El objetivo del presente trabajo es comparar los resultados de morbimortalidad perioperatoria de la solución cardiopléjica cristaloide de uso convencional en nuestro centro (St. Thomas no. 2) respecto a la solución Custodiol en cirugías cardíacas complejas.
Material y métodosTipo de estudioEstudio retrospectivo comparativo elaborado a partir de una base de datos recogida de forma prospectiva en el servicio de Cirugía Cardíaca del Hospital Universitario de Son Espases.
El período del estudio fue de tres años y medio (mayo 2016-diciembre 2019).
Fueron consideradas cirugías cardíacas complejas aquellas con tiempo de pinzamiento mayor o igual a 80 minutos.
Un total de 712 pacientes fueron incluidos en el estudio. Se clasificaron según el tipo de cardioplejia empleada: grupo Saint Thomas no. 2 (ST2) versus grupo Custodiol. No se aplicaron criterios de exclusión de sujetos.
La elección del tipo de cardioplejia fue a criterio del cirujano responsable, basándose en la complejidad de la intervención y duración prevista del tiempo de isquemia.
Todos los pacientes firmaron el consentimiento informado para cirugía cardíaca. Dada la naturaleza retrospectiva del estudio, no se requirió consentimiento informado específico. La base de datos empleada para la realización del presente estudio se encuentra autorizada por el Comité Ético de nuestro hospital y en ella se encuentra codificada la identificación de los pacientes cumpliendo con los requisitos de la Ley Orgánica de Protección de Datos (15/1999).
No se modificó intencionadamente el curso postoperatorio del paciente dado que el uso de ambas cardioplejias entra dentro de la práctica clínica habitual en nuestro centro.
Modo de administración de la cardioplejiaEn nuestro centro se administra cardioplejia cristaloide ST2 a través de un sistema de presión independiente del circuito de la bomba de circulación extracorpórea desde la cabecera del paciente que va conectado a la cánula de cardioplejia de la raíz, infundiéndose la cardioplejia de forma anterógrada y continua a una presión de 300 mmHg. También se puede infundir a través de una cánula de retroplejia por el seno coronario a una presión de 200 mmHg o bien mediante las cánulas anterógradas selectivas de los ostium coronarios a una presión de 150-200 mmHg. El volumen de infusión inicial suele ser entre 700 y 1.000 mL. Posteriormente cada 20 o 30 minutos se debe administrar una nueva dosis de entre 300-700 mL.
Se monitoriza la temperatura septal en todo momento para comprobar la correcta distribución de la cardioplejia y enfriamiento del corazón.
La estrategia de infusión de la cardioplejia Custodiol consiste en administrar inicialmente dos bolsas de 1.000 mL cada una (en total 2.000 mL) a 5-8°C a través del mismo sistema descrito anteriormente, proporcionando hasta 180 minutos de isquemia de forma ininterrumpida. Alcanzado este tiempo y si se prevé un tiempo de pinzamiento más prolongado, se administra un recuerdo de 1.000 mL más.
Variables analizadasSe dividieron las variables en preoperatorias, intraoperatorias y postoperatorias.
En cuanto a las variables preoperatorias, se realizó un análisis comparativo respecto a características demográficas y comorbilidades, la clase funcional preoperatoria para disnea o angina (New York Heart Association [NYHA] o Canadian Cardiovascular Society [CCS], según correspondiera)16,17, la prioridad quirúrgica (carácter electivo, urgente o emergente) y si se trataba de una reintervención. Por último, los datos ecocardiográficos preoperatorios considerados como factores pronósticos también fueron recogidos: la fracción de eyección del ventrículo izquierdo (FEVI) preoperatoria, si existía disfunción severa del mismo (FEVI < 30%) y la presencia de hipertensión pulmonar severa (HTP > 55 mmHg).
Se calculó la mortalidad predicha mediante el EuroScore Logístico y el EuroScore ii18,19.
Las variables intraoperatorias estudiadas fueron el tiempo de circulación extracorpórea (CEC), el tiempo de pinzamiento, el volumen de cardioplejia infundida, la necesidad de transfusiones y número de las mismas y la presencia de arritmia ventricular con necesidad de desfibrilación tras despinzamiento.
Los tipos de cirugías realizadas (variable categoría operatoria) se clasificaron en valvulares aislados, polivalvulares, coronarios, combinados (valvular y coronario), cirugías de aorta y otros (corrección de cardiopatías congénitas, complicaciones mecánicas del infarto, etc).
Las variables postoperatorias evaluadas fueron: presencia de infarto (IAM) perioperatorio (definido por elevación de biomarcadores de necrosis miocárdica con la cifra de troponina i ultrasensible [hsTnI], nueva onda Q en el electrocardiograma o nuevos segmentarismos en la ecocardiografía)20-22, síndrome de bajo gasto (disminución del gasto cardíaco con índice cardíaco [IC] < 2,0 L/min/m2, tensión arterial sistólica < 90 mmHg con signos de hipoperfusión tisular en ausencia de hipovolemia con necesidad de inotropos a altas dosis o uso de asistencia mecánica circulatoria como balón de contrapulsación o uso de membrana de oxigenación extracorpórea [ECM])23,24, complicaciones neurológicas (ictus, coma o convulsiones), fracaso renal agudo (clasificación RIFLE 3)25,26, intubación prolongada mayor de 48 horas, y fibrilación auricular (FA) postoperatoria de novo.
Se compararon los días de estancia en Unidad de Cuidados Intensivos (UCI) y días de estancia total hospitalaria, así como la mortalidad operatoria (mortalidad hospitalaria o dentro de los 30 primeros días postoperatorios).
Método estadísticoLas variables continuas se expresaron mediante la media y desviación estándar. Las variables categóricas se expresaron mediante frecuencias y porcentajes. Para la comparación de las variables continuas se empleó el test de la U de Mann Whitney y para las variables categóricas se usó el test de χ2 o el test exacto de Fisher, según correspondiera.
Se expresaron algunos de los resultados mediante gráficos de tallo y hojas mostrando la mediana y rango intercuartílico.
Se realizó un análisis univariante para determinar factores de riesgo independientes para el desarrollo de las complicaciones y de la mortalidad, escogiendo las variables con una asociación p < 0,1, incluyendo la variable objeto de estudio «tipo de cardioplejia». En cuanto al desarrollo de complicaciones, se decidió utilizar un end-point combinado, denominado «morbilidad», que incluyó: infarto perioperatorio, intubación prolongada, necesidad de transfusiones, insuficiencia renal aguda (RIFLE 3), bajo gasto postoperatorio, complicaciones neurológicas y fibrilación auricular postoperatoria.
Posteriormente se realizó un análisis multivariante mediante regresión logística con las variables que demostraron asociación significativa en el análisis univariante para determinar la asociación real con las variables dependientes a estudio, expresándolo como odds ratio (OR) con su intervalo de confianza (CI 95%). Se realizaron tres modelos de análisis multivariante: uno para predictor de desfibrilación, otro para predictor de morbilidad y otro para predictor de mortalidad.
Se consideró estadísticamente significativo un valor de p < 0,05.
Para el análisis de los datos se empleó el software Statistical Package for the Social Sciences® versión 22.0 (IBM, SPSS, Chicago, IL, USA).
ResultadosA lo largo del período del estudio se incluyeron 712 pacientes: 548 pertenecían al grupo ST2 y 164 al grupo Custodiol.
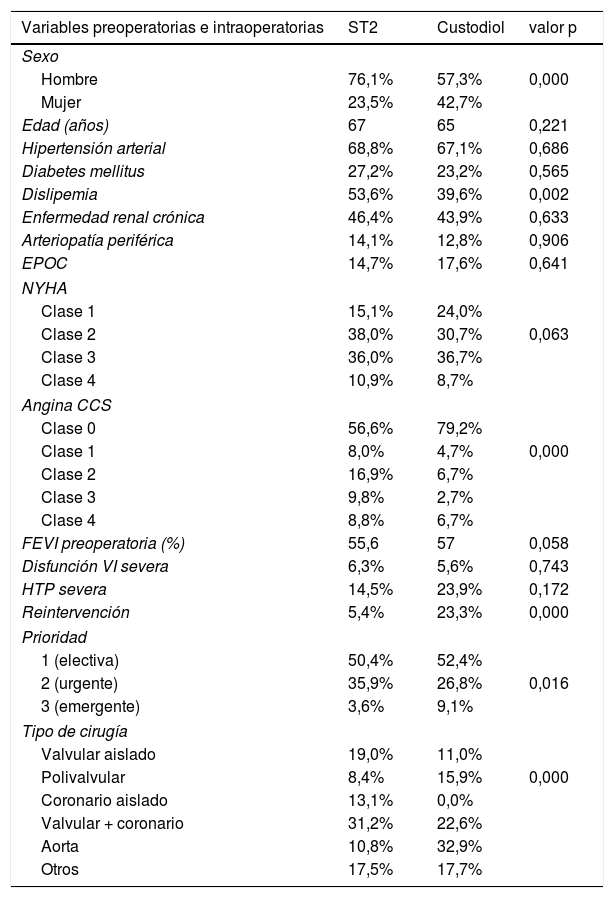
Las variables preoperatorias se muestran en la tabla 1. Se observó en el grupo Custodiol un mayor número de mujeres, menos dislipemia, menor número de pacientes con angina, mayor número de reintervenciones y mayor número de casos emergentes, de forma estadísticamente significativa.
Comparación entre los dos grupos: ST2 y Custodiol respecto a las variables preoperatorias y el tipo de cirugía realizada. Las variables categóricas se expresan como porcentajes, las variables cuantitativas con la media
| Variables preoperatorias e intraoperatorias | ST2 | Custodiol | valor p |
|---|---|---|---|
| Sexo | |||
| Hombre | 76,1% | 57,3% | 0,000 |
| Mujer | 23,5% | 42,7% | |
| Edad (años) | 67 | 65 | 0,221 |
| Hipertensión arterial | 68,8% | 67,1% | 0,686 |
| Diabetes mellitus | 27,2% | 23,2% | 0,565 |
| Dislipemia | 53,6% | 39,6% | 0,002 |
| Enfermedad renal crónica | 46,4% | 43,9% | 0,633 |
| Arteriopatía periférica | 14,1% | 12,8% | 0,906 |
| EPOC | 14,7% | 17,6% | 0,641 |
| NYHA | |||
| Clase 1 | 15,1% | 24,0% | |
| Clase 2 | 38,0% | 30,7% | 0,063 |
| Clase 3 | 36,0% | 36,7% | |
| Clase 4 | 10,9% | 8,7% | |
| Angina CCS | |||
| Clase 0 | 56,6% | 79,2% | |
| Clase 1 | 8,0% | 4,7% | 0,000 |
| Clase 2 | 16,9% | 6,7% | |
| Clase 3 | 9,8% | 2,7% | |
| Clase 4 | 8,8% | 6,7% | |
| FEVI preoperatoria (%) | 55,6 | 57 | 0,058 |
| Disfunción VI severa | 6,3% | 5,6% | 0,743 |
| HTP severa | 14,5% | 23,9% | 0,172 |
| Reintervención | 5,4% | 23,3% | 0,000 |
| Prioridad | |||
| 1 (electiva) | 50,4% | 52,4% | |
| 2 (urgente) | 35,9% | 26,8% | 0,016 |
| 3 (emergente) | 3,6% | 9,1% | |
| Tipo de cirugía | |||
| Valvular aislado | 19,0% | 11,0% | |
| Polivalvular | 8,4% | 15,9% | 0,000 |
| Coronario aislado | 13,1% | 0,0% | |
| Valvular + coronario | 31,2% | 22,6% | |
| Aorta | 10,8% | 32,9% | |
| Otros | 17,5% | 17,7% | |
CCS: Canadian Cardiovascular Society; EPOC: enfermedad pulmonar obstructiva crónica; FEVI: fracción de eyección del ventrículo izquierdo; HTP: hipertensión pulmonar; NYHA: New York Heart Association.
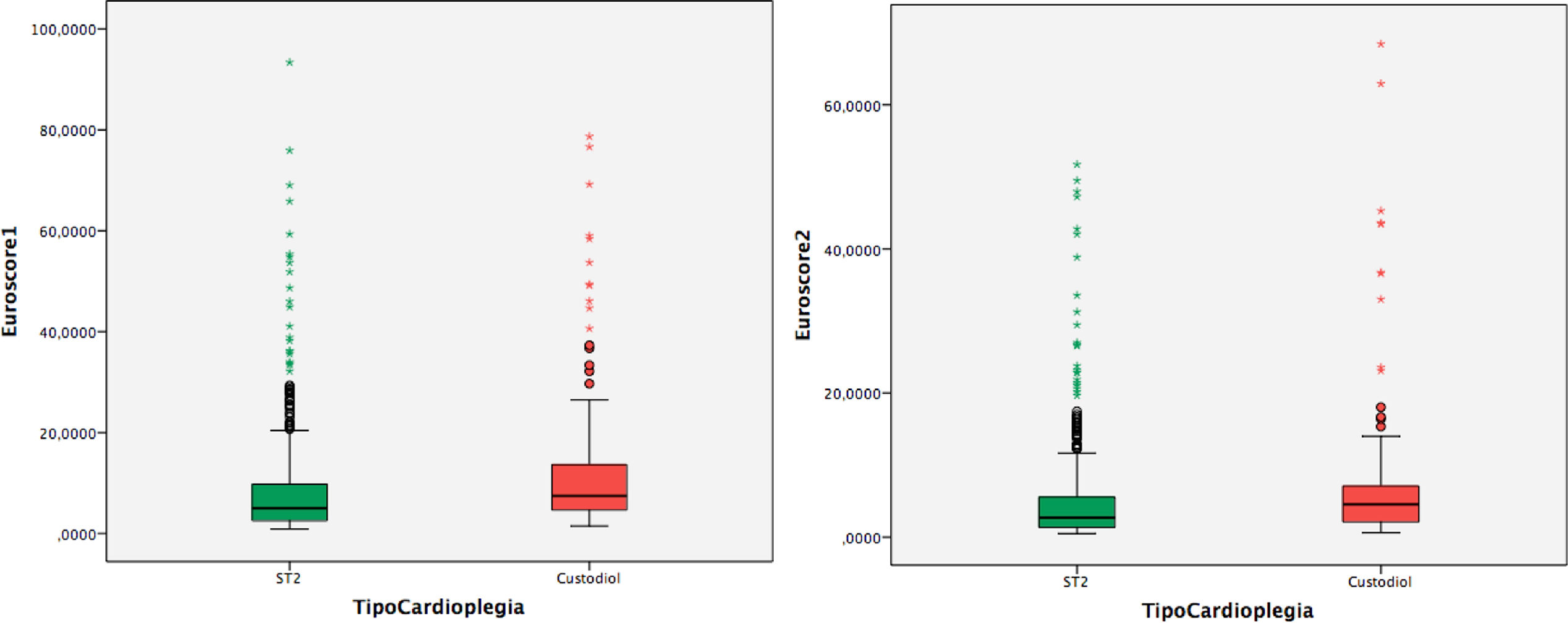
En cuanto a la mortalidad estimada preoperatoria (figs. 2a y 2b), se halló tanto un EuroScore Logístico (8,62 vs. 12,59%, p = 0,000) como un EuroScore ii (4,90 vs. 7,19%, p = 0,000) superiores en el grupo Custodiol.
A) Diagrama de tallo y hojas que muestra las diferencias en los valores del EuroSCORE Logístico entre el grupo ST2 y el grupo Custodiol, p = 0,000. B) Diagrama de tallo y hojas que muestra las diferencias en los valores del EuroSCORE ii entre el grupo ST2 y el grupo Custodiol, p = 0,000.
Respecto al tipo de intervención realizada (tabla 1) se encontraron mayor número de intervenciones de aorta y de polivalvulares en el grupo Custodiol, mientras que todos los coronarios aislados se realizaron usando ST2, p = 0,000.
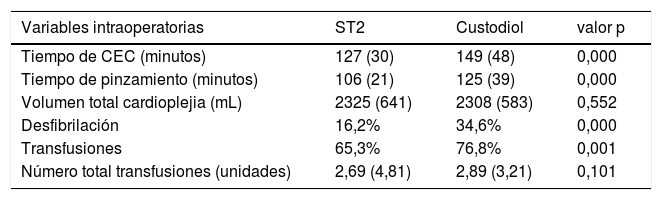
Al analizar las variables intraoperatorias (tabla 2), se observaron un tiempo de CEC y de pinzamiento más prolongados en el grupo Custodiol. Por otro lado, la presencia de arritmias con necesidad de desfibrilación tras el despinzamiento fue también superior en el grupo Custodiol, de forma estadísticamente significativa. Además, un mayor porcentaje de pacientes en el grupo Custodiol necesitó transfusiones intraoperatorias; sin diferencias en el número total de transfusiones ni en el volumen de cardioplejia infundida.
Variables intraoperatorias y su distribución entre grupos. Las variables categóricas se expresan como porcentajes, las variables cuantitativas con la media y la desviación estándar entre paréntesis
| Variables intraoperatorias | ST2 | Custodiol | valor p |
|---|---|---|---|
| Tiempo de CEC (minutos) | 127 (30) | 149 (48) | 0,000 |
| Tiempo de pinzamiento (minutos) | 106 (21) | 125 (39) | 0,000 |
| Volumen total cardioplejia (mL) | 2325 (641) | 2308 (583) | 0,552 |
| Desfibrilación | 16,2% | 34,6% | 0,000 |
| Transfusiones | 65,3% | 76,8% | 0,001 |
| Número total transfusiones (unidades) | 2,69 (4,81) | 2,89 (3,21) | 0,101 |
CEC: circulación extracorpórea.
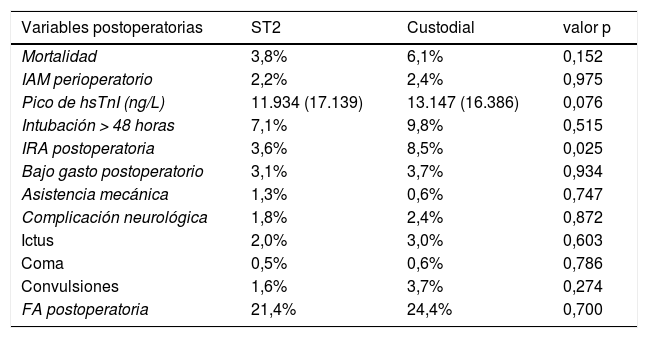
No se encontraron diferencias respecto a la mortalidad operatoria. En cuanto a las complicaciones postoperatorias: no se observaron diferencias significativas para infarto perioperatorio, pico máximo de troponina, síndrome de bajo gasto o necesidad de asistencia mecánica, complicaciones neurológicas, intubación prolongada y fibrilación auricular de novo. En cambio, sí que se halló una mayor tasa de fracaso renal RIFLE 3 postoperatorio en el grupo Custodiol (tabla 3).
Variables postoperatorias y su distribución entre grupos. Las variables categóricas se expresan como porcentajes, las variables cuantitativas con la media y la desviación estándar entre paréntesis
| Variables postoperatorias | ST2 | Custodial | valor p |
|---|---|---|---|
| Mortalidad | 3,8% | 6,1% | 0,152 |
| IAM perioperatorio | 2,2% | 2,4% | 0,975 |
| Pico de hsTnI (ng/L) | 11.934 (17.139) | 13.147 (16.386) | 0,076 |
| Intubación > 48 horas | 7,1% | 9,8% | 0,515 |
| IRA postoperatoria | 3,6% | 8,5% | 0,025 |
| Bajo gasto postoperatorio | 3,1% | 3,7% | 0,934 |
| Asistencia mecánica | 1,3% | 0,6% | 0,747 |
| Complicación neurológica | 1,8% | 2,4% | 0,872 |
| Ictus | 2,0% | 3,0% | 0,603 |
| Coma | 0,5% | 0,6% | 0,786 |
| Convulsiones | 1,6% | 3,7% | 0,274 |
| FA postoperatoria | 21,4% | 24,4% | 0,700 |
FA: fibrilación auricular; hsTnI: troponina i ultrasensible; IAM: infarto agudo de miocardio; IRA: insufiencia renal aguda.
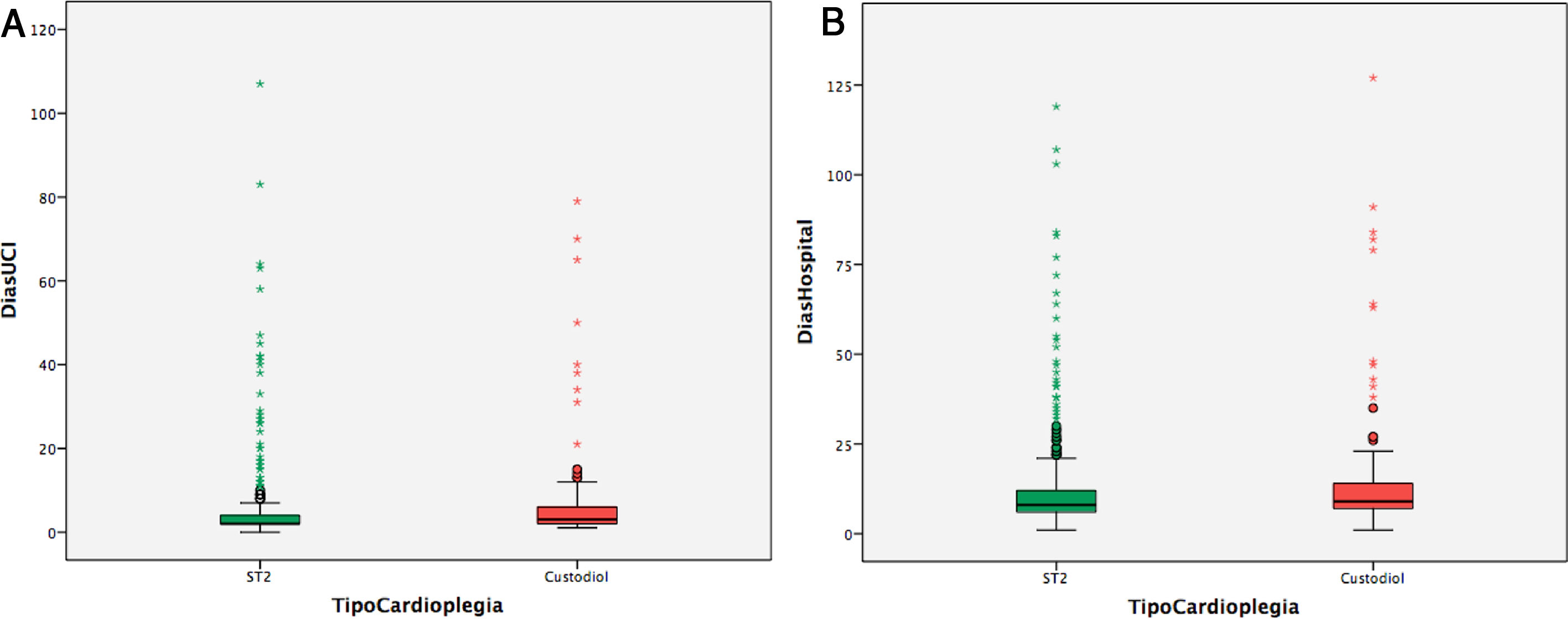
Por otra parte, las figuras 3a y 3b muestra diferencias significativas en cuanto a los días de estancia en UCI: 4,97 días (DS 9,44) vs. 6,70 días (DS 11,53) (p = 0,000) y en los días de estancia hospitalaria total: 12,08 días (DS 13,13) vs. 14,71 días (DS 17,61).
A) Diagrama de tallo y hojas que muestra las diferencias en los días de estancia en la Unidad de Cuidados Intensivos entre el grupo ST2 y el grupo Custodiol, p = 0,000. B) Diagrama de tallo y hojas que muestra las diferencias en los días de estancia hospitalaria total entre el grupo ST2 y el grupo Custodiol, p = 0,005.UCI: Unidad de Cuidados Intensivos.
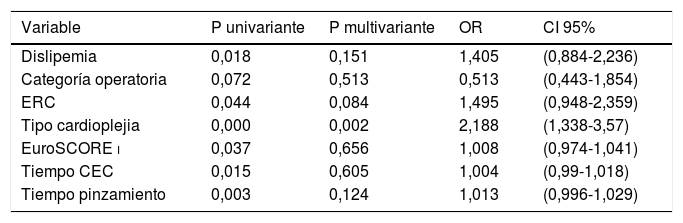
Respecto al análisis de predicción de arritmias ventriculares con necesidad de desfibrilación, en el análisis univariante las siguientes variables se asociaron con necesidad de desfibrilación de forma estadísticamente significativa: la dislipemia (p = 0,018), la categoría operatoria (p = 0,072), la enfermedad renal crónica (p = 0,044), el tipo de cardioplejia (p = 0,000), el EuroSCORE i (p = 0,037), el tiempo de CEC (p = 0,015) y el tiempo de pinzamiento (p = 0,003). Al realizar el análisis multivariante solo se identificó el tipo de cardioplejia como factor de riesgo independiente para la necesidad de desfibrilación, con dos veces más riesgo de arritmias ventriculares que requirieron desfibrilación en el grupo de Custodiol (tabla 4).
Análisis univariante y multivariante para la variable «necesidad de desfibrilación tras el despinzamiento» a partir de las posibles variables confusoras
| Variable | P univariante | P multivariante | OR | CI 95% |
|---|---|---|---|---|
| Dislipemia | 0,018 | 0,151 | 1,405 | (0,884-2,236) |
| Categoría operatoria | 0,072 | 0,513 | 0,513 | (0,443-1,854) |
| ERC | 0,044 | 0,084 | 1,495 | (0,948-2,359) |
| Tipo cardioplejia | 0,000 | 0,002 | 2,188 | (1,338-3,57) |
| EuroSCORE i | 0,037 | 0,656 | 1,008 | (0,974-1,041) |
| Tiempo CEC | 0,015 | 0,605 | 1,004 | (0,99-1,018) |
| Tiempo pinzamiento | 0,003 | 0,124 | 1,013 | (0,996-1,029) |
CEC: circulación extracorpórea; CI: intervalo de confianza; ERC: enfermedad renal crónica; OR: odds ratio.
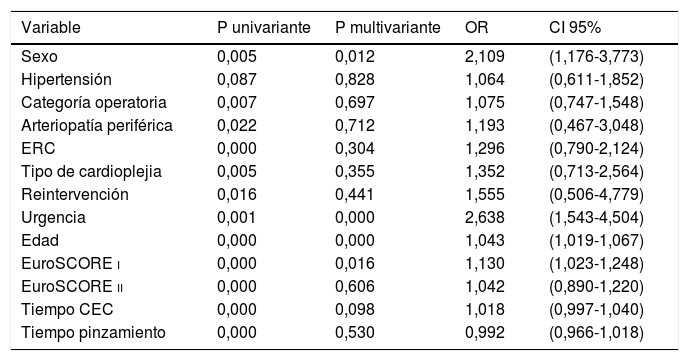
Al realizar el análisis univariante para valorar la morbilidad o complicaciones postoperatorias, las siguientes variables resultaron asociadas: el sexo (p = 0,005), la hipertensión (p = 0,087), la categoría operatoria (p = 0,007), la arteriopatía periférica (p = 0,022), la enfermedad renal crónica (p = 0,000), el tipo de cardioplejia (p = 0,005), la reintervención (p = 0,016), la urgencia (p = 0,000), la edad (p = 0,000), el EuroSCORE i (p = 0,000), el EuroSCORE ii (p = 0,000), el tiempo de CEC (p = 0,000) y el tiempo de pinzamiento (p = 0,000). Al realizar el análisis multivariante para morbilidad postoperatoria, se encontraron como factores de riesgo independientes para la aparición de complicaciones: el sexo (con el doble de riesgo para las mujeres), la urgencia (con el doble de riesgo para las cirugías urgentes), la edad (con un 4% más de riesgo por cada año) y el EuroSCORE i (con 13% más de riesgo para cada punto añadido). El tipo de cardioplejia no resultó un factor de riesgo independiente para el desarrollo de complicaciones (tabla 5).
Análisis univariante y multivariante para la variable dependiente «morbilidad o complicaciones postoperatorias» a partir de las diferentes variables independientes confusoras
| Variable | P univariante | P multivariante | OR | CI 95% |
|---|---|---|---|---|
| Sexo | 0,005 | 0,012 | 2,109 | (1,176-3,773) |
| Hipertensión | 0,087 | 0,828 | 1,064 | (0,611-1,852) |
| Categoría operatoria | 0,007 | 0,697 | 1,075 | (0,747-1,548) |
| Arteriopatía periférica | 0,022 | 0,712 | 1,193 | (0,467-3,048) |
| ERC | 0,000 | 0,304 | 1,296 | (0,790-2,124) |
| Tipo de cardioplejia | 0,005 | 0,355 | 1,352 | (0,713-2,564) |
| Reintervención | 0,016 | 0,441 | 1,555 | (0,506-4,779) |
| Urgencia | 0,001 | 0,000 | 2,638 | (1,543-4,504) |
| Edad | 0,000 | 0,000 | 1,043 | (1,019-1,067) |
| EuroSCORE i | 0,000 | 0,016 | 1,130 | (1,023-1,248) |
| EuroSCORE ii | 0,000 | 0,606 | 1,042 | (0,890-1,220) |
| Tiempo CEC | 0,000 | 0,098 | 1,018 | (0,997-1,040) |
| Tiempo pinzamiento | 0,000 | 0,530 | 0,992 | (0,966-1,018) |
CEC: circulación extracorpórea; CI: intervalo de confianza; ERC: enfermedad renal crónica; OR: odds ratio.
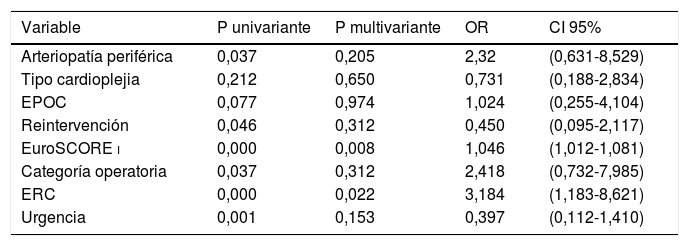
Por último, las siguientes variables independientes resultaron asociadas con la mortalidad en el análisis univariante: la urgencia (p = 0,001), la categoría operatoria (p = 0,037), la arteriopatía periférica (p = 0,037), la enfermedad renal crónica (p = 0,000), la EPOC (p = 0,077), la reintervención (p = 0,046) y el EuroSCORE i (p = 0,000). El tipo de cardioplejia no resultó asociado de forma significativa en este análisis (p = 0,212). Al realizar el análisis multivariante, los únicos factores de riesgo independientes que se encontraron para la mortalidad fueron la enfermedad renal crónica (multiplicando hasta por tres veces el riesgo de fallecer en caso de enfermedad renal crónica) y el EuroSCORE i (con 4% más por cada punto añadido) (tabla 6).
Análisis univariante y multivariante para la variable dependiente «mortalidad» a partir de las diferentes variables independientes confusoras
| Variable | P univariante | P multivariante | OR | CI 95% |
|---|---|---|---|---|
| Arteriopatía periférica | 0,037 | 0,205 | 2,32 | (0,631-8,529) |
| Tipo cardioplejia | 0,212 | 0,650 | 0,731 | (0,188-2,834) |
| EPOC | 0,077 | 0,974 | 1,024 | (0,255-4,104) |
| Reintervención | 0,046 | 0,312 | 0,450 | (0,095-2,117) |
| EuroSCORE i | 0,000 | 0,008 | 1,046 | (1,012-1,081) |
| Categoría operatoria | 0,037 | 0,312 | 2,418 | (0,732-7,985) |
| ERC | 0,000 | 0,022 | 3,184 | (1,183-8,621) |
| Urgencia | 0,001 | 0,153 | 0,397 | (0,112-1,410) |
CEC: circulación extracorpórea; CI: intervalo de confianza; EPOC: enfermedad pulmonar obstructiva crónica; ERC: enfermedad renal crónica; OR: odds ratio.
Nuestro centro propone el uso de Custodiol® como opción segura en cirugía cardíaca compleja y con previsión de tiempos de isquemia prolongados.
La mayoría de los estudios publicados hasta la fecha que comparan la cardioplejia tipo Custodiol frente a otros tipos son de naturaleza retrospectiva27-29. Además, la mayoría comparan Custodiol con cardioplejia hemática30 y existen pocos estudios comparativos con otros tipos de cristaloide31,32.
El estudio comparativo más grande hasta la fecha fue el publicado por Hoyer et al. en 201727: estudió de forma retrospectiva a 7.263 pacientes sometidos a sustitución valvular aórtica aislada, 5.998 mediante Custodiol y 1.007 mediante hemática Calafiore. Tras realizar un pareamiento por puntaje de propensión, seleccionaron 825 pares de pacientes. No hubo diferencias en la mortalidad operatoria pero sí que encontraron diferencias en la supervivencia a largo plazo para aquellos pacientes con disfunción ventricular severa a favor de la cardioplejia hemática.
El trabajo de Misfeld y Davierwala de Leipzig en 201233 es la serie más larga publicada con 2.731 pacientes sometidos a cirugía mitral por minitoractomía derecha. Se concluyó que la cardioplejia Custodiol administrada vía anterógrada parece ser la más eficaz y segura para cirugía mitral mini-invasiva, con supervivencia a cinco años del 87,3%.
En el metaanalisis de Edelman et al. publicado en 2013 a partir de 14 estudios comparativos entre Custodiol y cardioplejia convencional (hemática o cristaloide) en cirugía cardíaca adulta y ocho grandes series de casos10, se analizó como objetivo primario la mortalidad, y como objetivos secundarios la protección miocárdica y las arritmias. Se encontraron tasas similares de mortalidad, de infarto perioperatorio y de síndrome de bajo gasto postoperatorio. Sin embargo, se encontraron mayores tasas de arritmias ventriculares durante la reperfusión en el grupo de Custodiol.
A diferencia de los anteriores, en el presente estudio los pacientes comparados son sometidos a cirugías cardíacas complejas (tiempos de pinzamientos superiores a 80 minutos, entre los que se incluyen reintervenciones y cirugía de aorta) y muestran un perfil de riesgo intermedio-alto (EuroSCORE logístico y ii medios de un 12% y 7% en el grupo Custodiol). Es más, el grupo Custodiol presentó características preoperatorias de mayor riesgo: mayor número de mujeres, de reintervenciones y de casos emergentes.
Respecto al tipo de cirugía, se observaron más casos de polivalvulares y de cirugía de aorta en el grupo Custodiol, lo que indica la mayor complejidad de cirugías.
Hasta la fecha, no tenemos conocimiento de ningún estudio que solo haya incluido casos de estas complejas características para probar la eficacia del Custodiol en adultos. Liu et al., en 200834, compararon el Custodiol frente a cardioplejia convencional en tiempos de pinzamiento > 90 min en población pediátrica, mostrando la solución HTK como segura en estos procedimientos.
En algunos estudios publicados previamente9,32,35,36 los tiempos de pinzamiento fueron más cortos en el grupo de cardioplejia convencional. Así, nuestro estudio mostró en el grupo Custodiol que el tiempo de CEC y de isquemia fueron superiores al grupo ST2, lo cual probablemente indica que las cirugías en el grupo Custodiol fueron más complejas ya que el tipo de cardioplejia per se, con su administración mediante dosis única, no debería alargar el tiempo de isquemia de la cirugía.
Quizás la diferencia hallada más importante para los dos tipos de cardioplejia tras el análisis multivariante, fue la necesidad de desfibrilación tras el despinzamiento por arritmias ventriculares durante la reperfusión, con una OR de 2,2 para el grupo Custodiol. La mayoría de las publicaciones muestran también incidencias mayores en los grupos Custodiol9,29,35,37. Las arritmias ventriculares son una manifestación del daño por isquemia-reperfusión y pueden ser indicativo de mala protección miocárdica38,39; sin embargo, los resultados del presente estudio muestran que no tuvo repercusión en cuanto a infarto perioperatorio u otros eventos adversos postoperatorios.
En cambio, no se encontraron diferencias entre los grupos respecto a la tasa de fibrilación auricular de novo, al igual que en estudios previos9,10,29,32.
En cuanto a la mortalidad operatoria (6,1 en Custodiol vs. 3,8% en ST2) no se hallaron diferencias significativas. Hay que destacar que la mortalidad observada estuvo por debajo de la predicha por EuroScore ii en ambos grupos (7,2 para Custodiol y 4,9% para ST2). En el metaanálisis de Edelman et al.10 la mortalidad comparada entre ambos grupos fue también similar (aproximadamente un 2%). El hecho de que nuestras cifras de mortalidad sean más elevadas se atribuye al perfil de alto riesgo de los pacientes y la complejidad de cirugías incluidos en nuestro estudio.
En nuestro estudio, al realizar el análisis multivariante para «mortalidad», solo se hallaron como factores de riesgo independientes de mortalidad: el EuroSCORE i (con una OR de 1,046) y la enfermedad renal crónica (ERC) (con una OR de 3,1). El tipo de cardioplejia, sin embargo, no resultó asociado estadísticamente.
Respecto al infarto perioperatorio o la cifra pico de troponinas, tampoco se hallaron diferencias. Resultados acordes a aquellos publicados hasta la fecha3,4,9,28,32,35,36.
Tampoco se encontraron diferencias respecto al síndrome de bajo gasto postoperatorio ni en la necesidad de asistencia mecánica, hallazgos similares a los descritos en la bibliografía3,4,9,29,32; aunque las tasas de bajo gasto postoperatorio reportadas son mucho mayores (en torno a un 13-15%). Hay que mencionar la limitación de la interpretación de estos datos por la heterogeneidad de resultados, influido por la dificultad para unificar la definición de esta condición clínica intercentros.
Cabe destacar las diferencias significativas respecto a la presencia de insuficiencia renal aguda (IRA) postoperatoria, con un 8,5% en Custodiol frente a un 3,6% en ST2. Sin embargo, dado que podía existir un factor de confusión debido al perfil de mayor riesgo de los pacientes del grupo Custodiol, al realizar el análisis multivariante para el end-point combinado «morbilidad» en el que se incluía la IRA postoperatoria, se pudo comprobar que el tipo de cardioplejia no influía en la aparición de complicaciones postoperatorias. No se han encontrado trabajos en la literatura que evidencien diferencias respecto a la IRA postoperatoria28-30.
En el modelo de análisis multivariante para «morbilidad», los únicos factores de riesgo independientes que influían en el desarrollo de complicaciones postoperatorias fueron: el sexo femenino (con una OR de 2,1), el carácter urgente de las intervenciones (con una OR de 2,6), la edad (con una OR de 1,043) y el EuroSCORE i (con una OR de 1,13).
En cuanto a la hiponatremia desencadenada con la administración de Custodiol, algunos autores como Lueck et al.40 defienden administrar pequeños volúmenes (25-100 mL) de NaCl (5,85%) o NaHCO3 (8,4%) al circuito durante el reparto de cardioplejia para contrarrestarla. Otros autores aspiran por el seno coronario todo el contenido de cardioplejia que se infunde o colocan un hemofiltro en el circuito. Nuestro equipo de perfusión ceba la bomba con suero fisiológico, en lugar de Plasmalyte®, para intentar que la depleción de sodio no sea tan acusada, pero no se emplea ninguna estrategia de corrección de la misma posteriormente.
Según nuestra experiencia y la bibliografía28, la hiponatremia aislada tras la aplicación de Custodiol no tiene un impacto negativo en los resultados del paciente. El «sobretratamiento» del bajo contenido en sodio, especialmente en niños, se debe evitar, sobre todo si la osmolaridad está en un rango fisiológico, para prevenir complicaciones neurológicas severas14,15. Si analizamos las complicaciones neurológicas en nuestro estudio, no se observaron diferencias ni para ictus, coma o convulsiones.
Por último, sí que se observaron diferencias en la estancia postoperatoria en UCI y estancia hospitalaria global, siendo superiores para Custodiol. Sin embargo, creemos que el hecho de que esta diferencia sea inferior a dos días, teniendo en cuenta el perfil de mayor riesgo del grupo Custodiol, presenta escasa relevancia clínica.
La principal limitación del estudio es su naturaleza retrospectiva y todos los sesgos que esto puede conllevar. Además, aunque las intervenciones se realizaron por distintos cirujanos, se trata de un estudio unicéntrico lo cual limita su generalización. Serán necesarios estudios multicéntricos prospectivos aleatorizados entre la cardioplejia Custodiol y ST2 en grupos homogéneos para realmente poder determinar la superioridad de una u otra.
Como conclusión, destacamos que la cardioplejia Custodiol de administración única ofrece una cómoda protección miocárdica y segura en pacientes de alto riesgo y cirugías complejas, sin diferencias en la mortalidad y similares tasas de complicaciones postoperatorias, que la administración en dosis repetidas de cardioplejia cristaloide convencional ST2 usada en nuestro centro.
FinanciaciónNo se recibió patrocinio de ningún tipo para llevar a cabo este artículo.
Conflicto de interesesLos autores declaran no tener ningún conflicto de intereses.