En los pacientes con malformación congénita de la válvula mitral la cirugía reparadora es la mejor opción. Sin embargo, en pacientes con válvulas gravemente displásicas, el reemplazo de la válvula mitral es la única solución. El propósito de este estudio es evaluar los resultados a corto y a medio plazo del reemplazo de la válvula mitral con prótesis mecánicas en pacientes pediátricos de 5 o menos años.
MétodosEntre 2003 y 2012 se recogieron los datos de 15 pacientes menores de 5años de edad que fueron operados de recambio valvular mitral en nuestro hospital.
ResultadosLa media de edad fue de 21,5meses, y la de peso, de 8,2kg. El 53% de los pacientes tenían síntomas antes de los 6meses. La válvula mitral en paracaídas fue el tipo de malformación más frecuente (33%), seguido de la mitral en hamaca (26%). En el 80% de los casos se realizó plastia mitral sin éxito. La prótesis más utilizada fue la de St. Jude Medical® n.°23 La media de seguimiento fue de 47,9meses. Como complicaciones más relevantes, se tuvo que colocar marcapasos permanente en un paciente, otro tuvo hemorragia gastrointestinal debido a la anticoagulación y un paciente requirió, después de 3 años y 4 meses, re-recambio valvular mitral. La mortalidad operatoria fue del 6,6%.
ConclusionesEl reemplazo de la válvula mitral en niños menores de 5años conlleva un alto riesgo. En nuestra experiencia, los resultados a medio plazo son satisfactorios.
Reconstructive surgery is considered the main objective in patients with congenital malformations of the mitral valve. However, in patients with severely dysplastic valves, mitral valve replacement is considered the only option.
The purpose of this study is to evaluate results in the short and medium term of mitral valve replacement with mechanical prosthesis in the first 5 years of life.
MethodsData was collected on 15 patients less than 5 years of age, who underwent mitral valve replacement in our hospital between 2003 and 2012.
ResultsThe mean age was 21.5months and mean weight 8.2kg. A total of 53% of the patients presented with symptoms before 6months of age. Parachute mitral valve was the most frequent type of malformation (33%), followed by hammock mitral valve (26%). In 80% of the cases mitral valve repair was unsuccessful. The most frequent used prosthesis was St. Jude Medical® No.23. The mean follow-up time was 47.9 months. As for complications, a permanent pacemaker was implanted in one patient, another patient had gastrointestinal bleeding due to anticoagulation, and another patient required another mitral valve replacement after 3years and 4months. Hospital mortality was 6.6%.
ConclusionsMitral valve replacement in children less than 5years of age involves high risks. In our experience, the medium term results are satisfactory.
Si bien la plastia es el tratamiento de elección para la patología de la válvula mitral en niños, en ocasiones la válvula está gravemente displásica, lo que hace imposible su reconstrucción y obliga al recambio valvular mitral (RVM). La selección del sustituto valvular más apropiado no ha sido definida, aunque actualmente la mayoría de los cirujanos coinciden en que, a pesar de sus problemas inherentes, las válvulas mecánicas son la opción más adecuada1. El RVM en niños pequeños constituye un reto debido al pequeño tamaño del anillo de la válvula, la obstrucción del tracto de salida del ventrículo izquierdo, la compresión de la arteria circunfleja y la lesión del sistema de conducción. Estos problemas están relacionados por la falta de prótesis de tamaño adecuado. La colocación de una prótesis relativamente grande puede causar la compresión de las estructuras cardiacas, con la consecuente morbilidad y/o mortalidad. Además, es difícil llevar una anticoagulación adecuada en este grupo de pacientes.
En este trabajo presentamos un análisis de nuestra experiencia en 10años con el uso de prótesis mecánica en posición mitral en pacientes de 5 o menos años de vida.
MétodosPoblación de estudioSe realizó un estudio retrospectivo y descriptivo de pacientes menores de 5años con enfermedad valvular mitral que fueron sometidos a RVM por prótesis mecánica desde enero de 2003 a diciembre de 2012. Se incluyeron pacientes con lesión de la válvula mitral de forma exclusiva, ya sea de causa congénita o adquirida, y pacientes que presentaban lesión del aparato subvalvular mitral, como ocurre en el origen anómalo de la coronaria izquierda de la arteria pulmonar (ALCAPA, por sus siglas en inglés).
Las variables estudiadas se dividieron en 3 grupos: demográficas y clínicas, quirúrgicas y postoperatorias. Dentro de las demográficas y clínicas se incluyeron el sexo, el peso a la cirugía, la edad a la cirugía, la edad de inicio de síntomas, el tipo de malformación congénita, las lesiones más frecuentemente asociadas y la necesidad de ventilación mecánica preoperatoria. Como variables quirúrgicas se estudiaron el antecedente de cirugía cardiaca, el tipo y tamaño de la prótesis utilizada y la cirugía asociada al RVM. Entre las variables postoperatorias y de seguimiento se contemplaron el tiempo de ventilación mecánica, la estancia en la unidad de cuidados intensivos (UCI), la estancia hospitalaria y las complicaciones del tipo: fuga paravalvular, necesidad de marcapasos definitivo, recambio de la prótesis implantada, hemorragia por anticoagulantes, trombosis de la prótesis, accidente cerebrovascular y la clase funcional (NYHA modificada por Ross) en el seguimiento postoperatorio.
Análisis estadísticoLos datos recogidos se analizaron utilizando el programa estadístico SPSS 15.0 para Windows (SPSS Inc, Chicago, Illinois, EE.UU.). Las variables cualitativas se expresaron como porcentajes, y las cuantitativas, como media y desviación estándar. Las curvas de supervivencia, el periodo libre de eventos mayores y el periodo de reintervención se realizaron con el método de Kaplan-Meier.
ResultadosCaracterísticas clínicasEntre el año 2003 y 2012, 15 pacientes fueron intervenidos quirúrgicamente de RVM con prótesis mecánica; 9 de estos fueron varones (60%). La media de edad al momento de la cirugía fue de 21,8±14,08meses (rango 6 a 48) y la de peso, de 8,2±2,69kg (rango 4,6 a 12,5). Ocho pacientes (53%) presentaron disnea a la alimentación antes de los 6meses de edad. La malformación congénita más frecuente fue válvula mitral en paracaídas en 5 casos (33%), seguida por la válvula mitral en hamaca en un 26% (4 casos). Como lesión asociada, el conducto arterioso persistente (CAP) se encontró en el 47% de los pacientes, seguido de la comunicación interventricular, presente en 3 pacientes (20%). En 5 pacientes (33%) se requirió soporte ventilatorio mecánico preoperatorio para el manejo de la insuficiencia cardiaca (tabla 1).
Resumen de las características clínicas, anatómicas y quirúrgicas
| Variable | n (%) |
|---|---|
| 15 | |
| Sexo m/f | 9/6 (60/40) |
| Edad (meses) | 21,8±14,08 (6-48) |
| Peso (kg) | 8,2±2,69 (4,6-12,5) |
| Índice de masa corporal (kg/m2) | 0,42±0,1 (0,28-0,59) |
| Malformación congénita asociada | |
| CAP | 7 (47) |
| CoAo | 2 (13) |
| CIV | 3 (20) |
| Membrana subaórtica | 1 (7) |
| Estenosis aórtica (válvula bicúspide) | 1 (7) |
| Ventilación mecánica preoperatoria | 5 (33) |
| Procedimientos previos diferentes a plastia mitral | |
| Doble ligadura o sección y sutura de CAP | 4 (27) |
| Cierre de CAP con Amplatzer | 1 (7) |
| Reimplante de arteria coronaria izquierda | 1 (7) |
| Valvuloplastía tricuspídea | 1 (7) |
| Reemplazo valvular aórtico | 1 (7) |
| Cierre de CIV | 1 (7) |
| Resección de estenosis subaórtica | 1 (7) |
| Coartectomía extendida | 1 (7) |
| Aortoplastia con balón | 1 (7) |
| Valvulotomía aórtica con balón | 1 (7) |
CAP: conducto arterioso persistente; CIV: comunicación interventricular; CoAo: coartación de aorta.
Algunos pacientes, de manera inicial, fueron sometidos a corrección de otras cardiopatías diferentes a la de la válvula mitral. Se procedió al cierre del CAP en 5 casos (33%); en 4 de ellos se realizó sección y sutura como procedimiento simultáneo al cierre de defecto septal interventricular, resección de rodete subaórtico o coartectomía extendida, y en un paciente se ocluyó con un dispositivo por cateterismo intervencionista. En un paciente con estenosis aórtica valvular se realizó valvulotomía con balón en el periodo neonatal; en el seguimiento presentó endocarditis valvular aórtica infecciosa, por lo que fue necesario colocar una prótesis aórtica y posteriormente mitral por endocarditis mitral. Este fue el único paciente de nuestra serie cuyo RVM se debió a una cardiopatía adquirida. Otro paciente con ALCAPA se operó de reimplante de la coronaria izquierda pero en el seguimiento persistió con insuficiencia mitral importante, por lo que se procedió al RVM (tabla 1). En 12 pacientes (80% de la serie) se intentó en primera instancia realizar plastia mitral; en 4 casos esta se realizó como parte de una cirugía previa al RVM (5,7meses fue el tiempo promedio que transcurrió desde que se realizó la plastia hasta el RVM), y en 8 pacientes (67%) la plastia valvular se realizó en el mismo acto quirúrgico del RVM. En 3 casos (20%), por anatomía no favorable para cirugía reconstructiva, de inicio se procedió a la colocación de la prótesis mitral. Todas las prótesis fueron colocadas en posición supraanular con el fin de colocar una válvula de mayor tamaño y evitar las posibles complicaciones (obstrucción subvalvular aórtica, bloqueo auriculoventricular, compresión de la arteria circunfleja). La prótesis mecánica de St. Jude Medical® se utilizó en 14 (93%) de los casos.
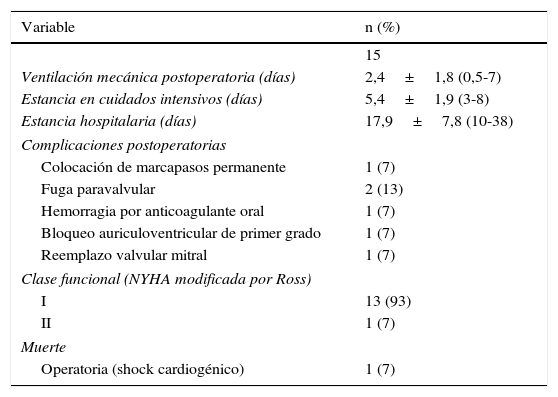
Evolución postoperatoriaUn paciente (6,6%) murió en el postoperatorio inmediato secundario a shock cardiogénico. El tiempo de ventilación mecánica durante la estancia en la UCI fue de 2,4±1,8días (rango 12h a 7días). El tiempo promedio de estancia en la UCI fue de 5,4±1,9días (rango 3 a 8días). El tiempo de hospitalización tomado en cuenta desde el momento de la cirugía hasta su alta hospitalaria fue de 17,9±7,8días (rango 10 a 38días). En el seguimiento tardío —una media de 47,9±28,37 meses— 2 pacientes presentaron fuga paravalvular ligera sin repercusión hemodinámica, un paciente presentó hemorragia gastrointestinal importante que requirió transfusión de hemoderivados; complicación que fue secundaria al inadecuado uso del anticoagulante oral (INR≥5). En otro paciente, un año después de la cirugía se requirió la colocación de un marcapasos definitivo DDDR (Boston Scientific®). Otro paciente necesitó re-RVM a los 3años y 4meses por disfunción protésica. En este último caso se debió a pannus en la prótesis. Ninguno de los pacientes presentó accidente cerebrovascular o trombosis de la válvula en el seguimiento. La clase funcional NYHA modificada por Ross es i en 13 pacientes (93%); solo uno de los pacientes está en clase funcional ii (tabla 2).
Curso postoperatorio de los pacientes sometidos a reemplazo de la válvula mitral
| Variable | n (%) |
|---|---|
| 15 | |
| Ventilación mecánica postoperatoria (días) | 2,4±1,8 (0,5-7) |
| Estancia en cuidados intensivos (días) | 5,4±1,9 (3-8) |
| Estancia hospitalaria (días) | 17,9±7,8 (10-38) |
| Complicaciones postoperatorias | |
| Colocación de marcapasos permanente | 1 (7) |
| Fuga paravalvular | 2 (13) |
| Hemorragia por anticoagulante oral | 1 (7) |
| Bloqueo auriculoventricular de primer grado | 1 (7) |
| Reemplazo valvular mitral | 1 (7) |
| Clase funcional (NYHA modificada por Ross) | |
| I | 13 (93) |
| II | 1 (7) |
| Muerte | |
| Operatoria (shock cardiogénico) | 1 (7) |
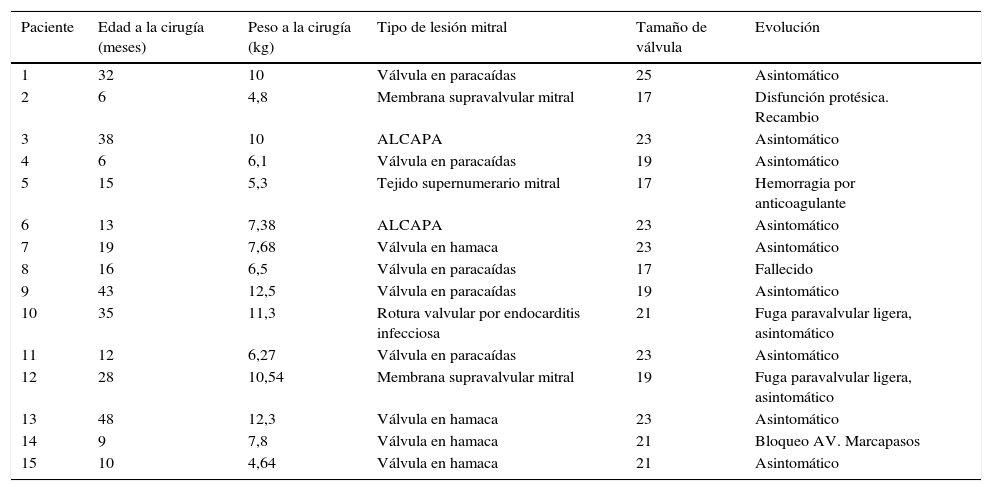
En la tabla 3 se resume el tipo de lesión mitral que presentaba cada uno de los pacientes y su evolución después de la cirugía.
Tipo de lesión mitral y evolución de los pacientes sometidos a cambio valvular mitral
| Paciente | Edad a la cirugía (meses) | Peso a la cirugía (kg) | Tipo de lesión mitral | Tamaño de válvula | Evolución |
|---|---|---|---|---|---|
| 1 | 32 | 10 | Válvula en paracaídas | 25 | Asintomático |
| 2 | 6 | 4,8 | Membrana supravalvular mitral | 17 | Disfunción protésica. Recambio |
| 3 | 38 | 10 | ALCAPA | 23 | Asintomático |
| 4 | 6 | 6,1 | Válvula en paracaídas | 19 | Asintomático |
| 5 | 15 | 5,3 | Tejido supernumerario mitral | 17 | Hemorragia por anticoagulante |
| 6 | 13 | 7,38 | ALCAPA | 23 | Asintomático |
| 7 | 19 | 7,68 | Válvula en hamaca | 23 | Asintomático |
| 8 | 16 | 6,5 | Válvula en paracaídas | 17 | Fallecido |
| 9 | 43 | 12,5 | Válvula en paracaídas | 19 | Asintomático |
| 10 | 35 | 11,3 | Rotura valvular por endocarditis infecciosa | 21 | Fuga paravalvular ligera, asintomático |
| 11 | 12 | 6,27 | Válvula en paracaídas | 23 | Asintomático |
| 12 | 28 | 10,54 | Membrana supravalvular mitral | 19 | Fuga paravalvular ligera, asintomático |
| 13 | 48 | 12,3 | Válvula en hamaca | 23 | Asintomático |
| 14 | 9 | 7,8 | Válvula en hamaca | 21 | Bloqueo AV. Marcapasos |
| 15 | 10 | 4,64 | Válvula en hamaca | 21 | Asintomático |
La realización de un RVM por prótesis mecánica en un niño al cual ya se le ha hecho uno o varios intentos de reparación de la válvula nativa no es una decisión fácil de tomar, pero sí es una opción terapéutica viable a considerar teniendo en cuenta los riesgos que esto conlleva.
Siempre que se decida esta opción quirúrgica, existen 3 aspectos importantes a considerar. El primero es la mortalidad operatoria alta, que oscila entre 10-36%2,3; el segundo es la necesidad de la anticoagulación crónica, y el tercero es la posibilidad de requerir recambio de prótesis debido al crecimiento del paciente.
Se han hecho bastantes publicaciones sobre RVM en menores de 5años. En 2001, Caldarone et al.4 publicaron una de las más grandes: 139 pacientes de 45 centros en un periodo de 17años. Años después, Vohra et al.5 comunicaron una serie de 24 casos en un periodo de 16años de un solo centro hospitalario. En el 2008, Selamet et al.6 presentaron una serie de 118 casos de niños menores de 5años de edad sometidos a RVM en un periodo de 30años. Finalmente, Henaine et al.7 en 2010 publicaron 29 casos en un periodo de 25años.
En todas las series mencionadas, al igual que en la nuestra, se puede apreciar que la cirugía se tuvo que realizar con mayor frecuencia antes de los 2años de edad, situación que incrementa el riesgo quirúrgico y la morbimortalidad4-7.
En nuestro trabajo la mayoría de los casos la lesión valvular mitral fue de origen congénito; solo hubo un caso consecutivo a endocarditis infecciosa, experiencia similar a lo publicado por Brown et al.8, donde el 5% de las operaciones se debieron a endocarditis. Por otra parte, es bien conocida la asociación de insuficiencia mitral por prolapso valvular en la edad pediátrica secundaria a algún síndrome genético. Alsoufi et al.9, publicaron en su serie 2 pacientes con síndrome de Marfan como causante de la insuficiencia valvular que obligó al RVM por prótesis mecánica; en nuestro grupo de estudio no se encontró ningún paciente con síndrome genético asociado.
Se realizó plastia valvular en el 80% de los casos de nuestra serie, ya sea como parte de una cirugía previa o en el mismo acto quirúrgico; este porcentaje es ligeramente superior a lo descrito en la literatura, que oscila del 46 al 78%4,6. Este alto porcentaje refleja la filosofía del equipo en evitar o al menos retrasar el recambio valvular debido a las comorbilidades que conlleva.
La válvula mecánica más utilizada fue la de St. Jude Medical® en el 93% de los casos, y el tamaño de la prótesis valvular osciló entre el n.°17 y el n.°25, con una media de n.°21; hallazgos similares a los comunicados por Henaine et al.7, donde el 100% la válvula utilizada fue la de St. Jude Medical® y el tamaño de la válvula de una media de 19,7±2,7.
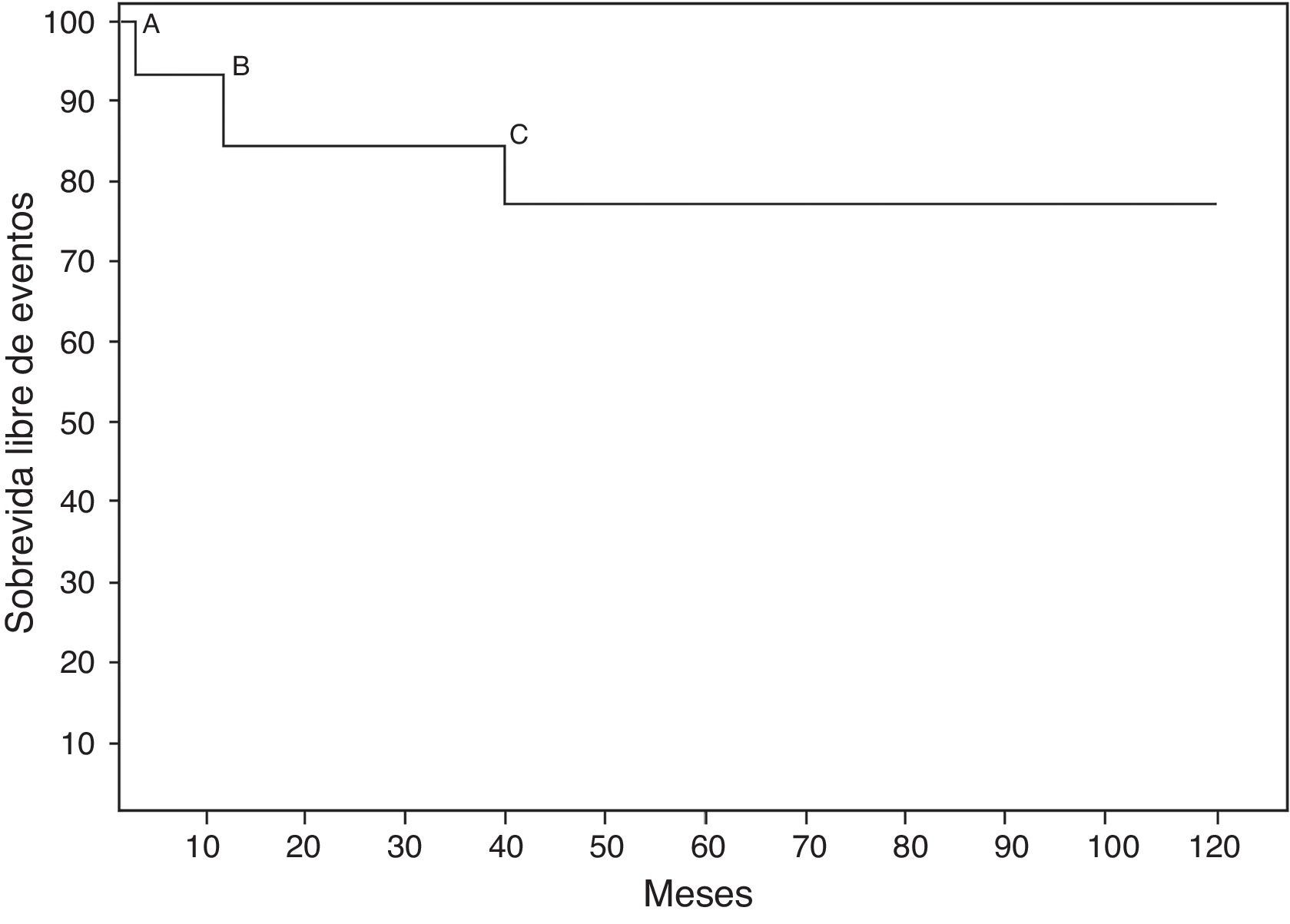
En el seguimiento, 3 pacientes presentaron eventos adversos: un paciente tuvo hemorragia significativa por el tracto gastrointestinal por el uso de anticoagulantes orales; en otro paciente fue necesaria la colocación de un marcapasos definitivo, y finalmente un paciente precisó recambio de la prótesis mitral (fig. 1). Aunque Caldarone et al.4 comunicaron que la anticoagulación crónica no está asociada a mortalidad significativa, existen publicaciones que demuestran lo contrario. Alsoufi et al.9 reportaron hemorragia secundaria al uso de la anticoagulación oral en 5 pacientes: uno del tracto gastrointestinal y 4 con hemorragia intracraneal secundaria a traumatismo craneal, dos de los cuales fallecieron. Vohra et al.5 informaron de la presencia de sangrado digestivo bajo, pancreatitis por warfarina y trombosis de la prótesis que requirió de recambio valvular. Hyung-Tae et al.10 reportaron la presencia de hematuria con un INR mayor de 3,5, hecho que no produjo repercusión hemodinámica y solo requirió vigilancia.
Por otra parte, diversos artículos indican que la necesidad de implantación de un marcapasos definitivo después del RVM oscila entre el 12-16%4-7. Se menciona que la necesidad de la utilización de un marcapasos definitivo es menor si la prótesis se coloca en posición supraanular, ya que no interfiere con el sistema de conducción6,11. En nuestra serie, un paciente requirió de re-RVM, el cual fue realizado 3años y 4meses después de la colocación de la prótesis mecánica; según publicaciones, es un tiempo corto en comparación con lo publicado por Henaine et al.7, donde dicho promedio fue de 12,8±5,7años. En dichas comunicaciones, al igual que en nuestro caso, al realizar el re-RVM se pudo implantar una prótesis mecánica de mayor tamaño que la anterior. En nuestro paciente se colocó una prótesis 2 tamaños mayor a la previa; lo que concuerda con lo descrito por Raghuveer et al.11, que mencionan que el anillo mitral crece a pesar de estar fijado a un anillo protésico.
Diversas publicaciones comunican que la mortalidad operatoria después de RVM por prótesis mecánica puede oscilar entre el 10 y el 36%, y los factores más frecuentemente involucrados con mortalidad son: edad (pacientes ≤2años)12, bajo peso, tamaño de prótesis menor de n.°20 y relación tamaño de la prótesis/peso del paciente alta, >36. En nuestra experiencia, la mortalidad operatoria fue de 6,6%, el paciente que falleció tenía un año y 4meses de edad, con 6,5kg de peso, el tamaño de la válvula implantada fue de n.°17 y la relación tamaño de prótesis/peso era de 2,6. Este paciente cumplía con casi todos los criterios de mal pronóstico descritos en la literatura para este tipo de cirugía.
ConclusiónLa sobrevida de los pacientes sometidos a RVM en menores de 5años en nuestro centro es aceptable con relación a lo publicado por otros autores. En aquellos pacientes donde la plastia mitral falla, como procedimiento primario, somos partidarios de realizar RVM y la colocación de la prótesis mecánica en posición supraanular. Así y todo, continúan siendo un problema las comorbilidades secundarias a la anticoagulación y la necesidad de cambio de prótesis.
Responsabilidades éticasProtección de personas y animalesLos autores declaran que para esta investigación no se han realizado experimentos en seres humanos ni en animales.
Confidencialidad de los datosLos autores declaran que en este artículo no aparecen datos de pacientes.
Derecho a la privacidad y consentimiento informadoLos autores declaran que en este artículo no aparecen datos de pacientes.
Conflicto de interesesLos autores declaran no tener ningún conflicto de intereses.