Introduction. The staging of gastrointestinal tumors is of great importance when planning treatment. Methods of examining the abdominal cavity such as laparoscopic staging and laparoscopic ultrasound are being introduced with increasing frequency into the diagnostic and therapeutic algorithms applied to patients presenting these lesions.
Results. In the authors' experience, laparoscopic staging of gastric cancer prevents unnecessary laparotomy in 40% of cases and its reliability in determining the resectability of the tumor is 98%. In cancer involving the gastric cardia or esophagus and in colorectal cancer, it provides important information concerning the existence of distant dissemination or liver metastases, especially when guided by ultrasound. The utility of the combination of these two techniques is particularly evident in hepatobiliopancreatic surgery, correcting erroneous preoperative tumor staging and preventing 25% of laparotomies in liver tumors. In pancreatic cancer, ultrasound-guided laparoscopic staging leads to changes in the preoperative stage in 35% of cases and prevents unnecessary laparotomy in 20%.
Conclusion. Ultrasound-guided laparoscopic staging is of great utility in the intraoperative staging of gastric tumors and may aid in intraoperative decision-making. In the case of hepatobiliopancreatic tumors, the additional information provided by laparoscopic ultrasound helps to reduce the incidence of unnecessary laparotomies and should be considered an essential preoperative step.
Introducción
Una de las indicaciones mejor aceptadas de la cirugía laparoscópica corresponde a la estadificación laparoscópica (EL) de las neoplasias digestivas. Además, los avances tecnológicos, especialmente en la aplicación de la ecografía intraoperatoria mediante sondas adecuadas a su utilización durante la EL amplían su efectividad. En esta aportación conjunta, Asencio y Escrig analizan las indicaciones y ventajas de la EL en la estadificación de los tumores gastrointestinales, y Cugat, Hoyuela y Marco, las de la EL sumada a la ecolaparoscopia en la evaluación de la resecabilidad del cáncer hepatobiliopancreático (HBP).
Estadificación laparoscópica de los tumores gastrointestinales
"Esta nueva técnica puede revelar metástasis generalizadas o un nódulo secundario en el hígado, haciendo otros procedimientos innecesarios y evitando al paciente una convalecencia prolongada"; con esta frase, de total actualidad, Bernheim definió en 1911 la utilidad de la laparoscopia1. Sin embargo, la "laparoscopia clásica" del internista, realizada generalmente con anestesia local y con el objetivo de observar la superficie visceral, ha sido superada por métodos de imagen más exactos e incruentos.
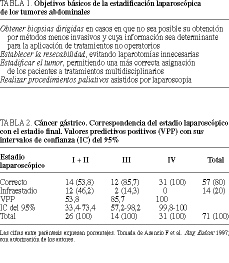
La elevada irresecabilidad de algunos tumores digestivos, junto con los mejores índices de respuesta a la quimioterapia neoadyuvante, exigen métodos objetivos de estadificación. Los métodos de imagen (US, TAC, RNM) carecen de la suficiente exactitud diagnóstica en la evaluación del grado de extensión de este tipo de tumores en los siguientes aspectos2,3: a) diferenciación entre los estadios T2 y T3; b) afectación de las adenopatías peritumorales; c) infiltración de órganos vecinos; d) detección de metástasis hepáticas (< 1 cm), y e) detección de carcinomatosis. Por ello, la cirugía laparoscópica en manos de los cirujanos podría desempeñar un papel importante en la estadificación de tumores abdominales, supliendo los déficit de las técnicas convencionales (tabla 1)4,5.
Estadificación del cáncer gástrico
La mayoría de carcinomas gástricos todavía son diagnosti cados en fases avanzadas, con índices de irresecabilidad del 15-50%6. Por otro lado, el estado actual del tratamiento del adenocarcinoma gástrico incluye métodos terapéuticos multidisciplinarios, como resección quirúrgica (curativa o paliativa), cirugía paliativa sin resección o quimioterapia neoadyuvante o paliativa. Si se añade la posibilidad de nutrición enteral, radiología intervencionista y endoscopia terapéutica, muchos pacientes con enfermedad incurable pueden recibir tratamiento paliativo sin intervención quirúrgica3,7.
La alta morbilidad (13-23%) y mortalidad (10-36%) tras la laparotomía en pacientes no resecables6, añadido a los argumentos anteriores, justifican el interés en evitar laparotomías innecesarias. De ahí que nuestro grupo iniciara en 1992 una investigación multicéntrica en la Comunidad Valenciana con el objetivo de evaluar la eficacia de la EL en la determinación de resecabilidad del carcinoma gástrico, comparándola con la ultrasonografía y la TAC convencional8,9. Nuestra técnica estandarizada de estadificación completa es la que describimos a continuación.
Técnica laparoscópica. Utilizamos anestesia general, lo que permite la continuación ininterrumpida a la cirugía resectiva. El paciente es colocado en decúbito supino con las piernas separadas. El cirujano se sitúa entre las piernas del paciente; la torre se sitúa a la altura del hombro derecho del paciente. Practicamos la exploración colocando una cánula umbilical de 10 mm y óptica de 0 o 30°. Inicialmente se evalúan la superficie hepática, el diafragma, los omentos mayor y menor, el peritoneo parietal y visceral y la cara anterior gástrica. La decisión de realizar una segunda o tercera puertas y su localización viene dictada por los hallazgos encontrados durante esta inspección inicial. A través de una segunda puerta de 5 mm en el vacío izquierdo palparemos la consistencia de los órganos abdominales, lo que nos permite apreciar la extensión macroscópica del tumor. Variando la posición del paciente podremos explorar las diversas áreas anatómicas: en posición de anti-Trendelenburg realizaremos examen y palpación de: a) hígado e hilio hepático: se exploran las superficies superior e inferior hepáticas, valorando la presencia de adenopatías; b) superficie anterior gástrica hasta el hiato, y c) epiplones mayor y menor. En posición de Trendelenburg se examina la cavidad pélvica: el saco de Douglas, el útero y los anexos.
A través de la misma cánula podremos aspirar líquido ascítico no detectado preoperatoriamente para su examen citológico. En caso contrario practicaremos de manera sistemática un lavado peritoneal, con suero salino y aspirado de la pelvis, subfrénicos y subhepático. Posteriormente podremos tomar biopsias de lesiones fácilmente asequibles.
Colocando otra puerta de 10 mm en el vacío derecho abordaremos la transcavidad de los epiplones, siguiendo la técnica descrita por uno de los autores10, para evaluar la pared posterior gástrica, área retrogástrica (pancreática), así como las adenopatías del tronco celíaco. La técnica consiste en la creación de una ventana omental y la introducción de la óptica y un palpador a su través, evaluando la pared posterior gástrica y la relación con estructuras retroperitoneales. No se extirpan adenopatías en pacientes con tumores presumiblemente resecables con fines curativos si éstas se encuentran en el territorio de la linfadenectomía que vayamos a practicar (D1 o D2).
Resultados. Los parámetros evaluados fueron: infiltración de la serosa gástrica, fijación tumoral al retroperitoneo o a órganos vecinos, presencia de metástasis hepáticas y peritoneales y de ascitis maligna. La sensibilidad, especificidad y valores predictivos para estos parámetros se compararon con los obtenidos con ultrasonografía y TAC.
Se evaluaron mediante EL 90 pacientes con tumores presuntamente resecables por US y TAC. Las complicaciones de la EL fueron mínimas, y la mayoría de los pacientes fueron dados de alta en uno o 2 días cuando la exploración se realizó como técnica independiente.
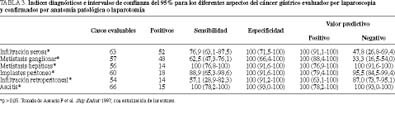
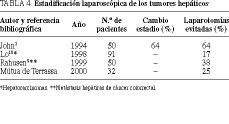
Tras la EL se evitó la laparotomía en un 40% de casos por enfermedad avanzada no evidenciada previamente. La exactitud diagnóstica de la EL en la determinación de la resecabilidad fue del 98%. En la tabla 2 se presenta la correspondencia de la EL global frente al estadio definitivo. La proporción de estadios correctamente diagnosticados fue del 80%. En la ta bla 3 se exponen los índices diagnósticos de la EL y sus intervalos de confianza respecto a los parámetros tumorales usados para la estadificación. La EL demostró una relación estadísticamente significativa con el resultado verdadero para todos los parámetros estudiados de manera independiente (p < 0,05).
En nuestro primer estudio, que incluía a 72 pacientes, la detección de las metástasis hepáticas por la EL obtuvo una especificidad y sensibilidad del 100%. En otro estudio más amplio (90 pacientes) la sensibilidad global descendió al 73% y los falsos negativos fueron en su mayoría por metástasis intraparenquimatosas9.
Para el grupo de pacientes en estadios T3-T4 la laparoscopia obtuvo una sensibilidad en la determinación del tumor del 81% y una especificidad del 100%, con una exactitud diagnóstica del 84%9.
Comentario. Algunos autores dudan de la utilidad real de la EL en el cáncer gástrico, dado que consideran necesaria la práctica de algún tipo de cirugía paliativa independientemente del estadio. Sin embargo, la expectativa media de vida de los pacientes a los que se les encuentran pequeños depósitos metastásicos durante la laparotomía y se someten a resecciones paliativas es de 3-9 meses, y muchos de ellos sin mejoría evidente excepto cuando es necesaria para paliar cuadros de hemorragia u obstrucción2,3.
Analizando nuestros propios resultados, la información aportada por la EL permitió una correcta determinación de la resecabilidad tumoral en el 98% de los casos, apreciable incremento cuando se compara con el 58% utilizando los métodos de imagen convencionales. Otros autores han obtenido porcentajes similares3,7. En nuestra experiencia, la EL tiene un comportamiento excelente para detectar y confirmar la invasión de la serosa (T3) y de órganos vecinos (T4), comparable a los de la ultrasonografía endoscópica.
La técnica resulta óptima en la detección de metástasis hepáticas, peritoneales y de pequeñas cantidades de líquido ascítico. Su valor disminuye en la detección de afectación nodular. Sin embargo, la posibilidad de obtener biopsias guiadas visualmente nos permite una correcta toma de decisiones en aquellos casos que resulten positivos. Las limitaciones de la técnica se deben básicamente a la presencia de adherencias en el área supramesocólica (p. ej., carcinoma de muñón gástrico). La fijación del tumor a estructuras retroperitoneales ha sido uno de los puntos oscuros observados en la EL de tumores gástricos. La técnica aquí descrita permite una correcta determinación de la extensión tumoral retrogástrica.
Aunque la eficacia de la EL debe ser probada frente a las nuevas generaciones de TAC, en un reciente estudio del Anderson3 la EL identificó un 23% más de casos con metástasis intraabdominales que las TAC de última generación, recomendando su realización en todos los pacientes con carcinoma gástrico presumiblemente resecable.
La EL no deja de ser una técnica invasiva y es posible que no sea rentable como método de estadificación en todos los casos de cáncer gástrico. La ultrasonografía endoscópica (USE) se ha descrito recientemente como el método ideal en la determinación del grado de infiltración de la pared gástrica11 y podría ser un elemento importante en el algoritmo de preselección de pacientes para laparoscopia o laparotomía.
La combinación secuencial de técnicas de imagen y mínimamente invasivas, como la punción percutánea y la laparoscopia, son una alternativa razonable en la estadificación del cáncer gástrico. Tras el diagnóstico por gastroscopia y biopsia, las técnicas de imagen (US/TAC) y las biopsias por punción guiadas por dichos métodos podrían representar la primera línea en la estadificación. Aquellos pacientes sin enfermedad obviamente avanzada serían sometidos a ecografía endoscópica. Los pacientes con lesiones ecográficas T1 y T2 serían sometidos directamente a laparotomía. Considerando que los tumores T3 y T4 tienen más de un 80% de posibilidades de ser también N positivos y teniendo en cuenta la frecuencia de diseminación abdominal asociada a ellos, sería en este subgrupo en el que estaría indicada la exploración laparoscópica.
Laparoscopia-toracoscopia en el cáncer esófago-cardial
En el cáncer de esófago y cardias, las áreas a investigar mediante la EL son implantes peritoneales y/o hepáticos de pequeño tamaño o adenopatías en zonas más alejadas de las que se consideran regionales, y que corresponden a aquellas situadas en las cadenas hepática, esplénica, celíaca o más allá de éstas. Para estos tumores, sobre todo para los de tercio superior, este porcentaje quizás no sea tan elevado, pero no por ello es despreciable, dada la morbimortalidad que acompaña a la cirugía exerética: la prevalencia de este tipo de metástasis oscila, según estudios con gran casuística, entre el 612 y el 14%12,13. La mediana de supervivencia es de 4 meses y la disfagia puede paliarse con medios mínimamente invasivos (recanalización con láser o endoprótesis).
En la evaluación del cáncer esofágico y del cardias, la EL podría cumplir los siguientes cometidos: a) valorar la resecabilidad, especialmente tras quimiorradioterapia preoperatoria; b) estadificación ganglionar del tumor como medio de indicar regímenes de tratamientos neoadyuvantes. La toracoscopia practicada desde el lado derecho y con mínima apertura de la pleura mediastínica ofrece una exactitud diagnóstica para el N superior al 80%, llegando a superar el 90% si se asocia a ecografía, y entre el 80-90% en lo que se refiere al diagnóstico de resecabilidad14. Aunque para el diagnóstico del T la mejor prueba es la ecografía endoscópica, cuya utilidad aquí está fuera de toda duda, para la evaluación del estado ganglionar parece que rinde más la EL; c) detección de hipertensión portal, que generalmente contraindica una cirugía agresiva, y d) la esofagectomía mínimamente invasiva, aunque hoy día es motivo de controversia.
Carcinoma colorrectal
La EL de tumores colorrectales, como indicación en sí, es una práctica escasamente utilizada, dada la casi constante necesidad de cirugía resectiva aun en situación de paliación. Sin embargo existen dos situaciones en las que su utilización puede ser beneficiosa: en la evaluación de la posibilidad de resección de metástasis hepáticas y como paso previo a la colectomía laparoscópica.
En cirugía colorrectal, como en toda cirugía oncológica, la evaluación de la presencia de metástasis sincrónicas es un elemento fundamental que puede conllevar importantes modificaciones en la estrategia quirúrgica. Por tanto, la cirugía onco lógica colorrectal con intención curativa realizada por laparoscopia deberá incorporar métodos adecuados de estadificación previa a la toma de decisiones. La EL realizada en el momento de la cirugía curativa permite una valoración adecuada. La técnica posibilita, asimismo, la realización de técnicas paliativas, como la colostomía, o derivaciones internas asistidas por laparoscopia.
Estadificación de tumores hepatobiliopancreáticos
En el futuro, mejorar los resultados del tratamiento de los tumores HBP deberá pasar por la utilización de terapéuticas combinadas. Para ello, es de vital importancia conocer el estadio tumoral. Sin embargo, no es infrecuente que el cirujano, como último eslabón del proceso diagnóstico-terapéutico, se enfrente a una discordancia entre el estadio preoperatorio y los hallazgos intraoperatorios, con lo que el tratamiento quirúrgico puede ser imposible o inadecuado para el paciente.
La estadificación por laparoscopia ha recobrado en los últimos años una especial importancia. Sin embargo, el propio concepto de cirugía de acceso mínimo implica limitaciones en cuanto a la exploración de las vísceras macizas, del retroperitoneo y de los procesos no exteriorizados de las vísceras huecas. La ecografía laparoscópica abre una nueva dimensión en cuanto al diagnóstico y posterior tratamiento de las enfermedades HBP. La EL asociada a la ecolaparoscopia puede aportar información vital para tomar decisiones intraoperatorias, por lo que debe realizarla e interpretarla el propio cirujano15.
Lesiones hepáticas
Para determinar el tipo de resección más apropiada es fundamental conocer el número de lesiones hepáticas a tratar, su localización y sus relaciones con las estructuras vasculares. En la actualidad, la ecografía intraoperatoria es una herramienta imprescindible para obtener esta información16, por lo que la evolución natural ha sido intentar reproducir sus resultados mediante ecolaparoscopia. Si bien la experiencia es limitada, diversos autores han reflejado su capacidad para detectar masas no observadas mediante técnicas de imagen convencionales17. La ecolaparoscopia permite identificar tumores no visualizados durante la EL en un 33% de casos y aportar información complementaria en más del 40%17. En aquellos pacientes en los que las exploraciones previas (incluyendo la EL) no hallaron contraindicación alguna, la ecolaparoscopia demostró la irresecabilidad en el 16%17,18.
Técnica y pacientes. Los aspectos técnicos requieren un mínimo período de aprendizaje, pero para la interpretación de las imágenes la curva de aprendizaje es prolongada. Es necesaria anestesia general y la colocación como mínimo de dos trocares de 10 mm para la cámara y la sonda de ecografía, y en ocasiones un trocar de 5 mm para el instrumental19.
Desde septiembre de 1997 a septiembre de 1999, en el Hospital Mútua de Terrassa se han valorado mediante EL y ecolaparoscopia 32 pacientes con tumores hepáticos y de vía biliar presuntamente resecables. En 17 de ellos se apreciaron metástasis hepáticas de cáncer colorrectal, en 10 hepatomas sobre hígado cirrótico y en cuatro tumores de vías biliares.
De los 17 pacientes con metástasis, en 3 casos fue imposible realizar la ecolaparoscopia por adherencias, y en cinco de los 14 restantes se modificó la estrategia preoperatoria al existir lesiones intrahepáticas insospechadas; en un paciente con metástasis en el lóbulo hepático derecho y con segmentos II-III de pequeño tamaño, la EL descubrió una lesión insospechada en el segmento IV y permitió rescatar al paciente para una resección diferida tras practicar una embolización portal derecha. En 2 casos se descubrió enfermedad irresecable y se evitó la laparotomía.
De los 10 pacientes con hepatocarcinoma, la ecolaparoscopia modificó la actitud establecida en 4 casos: tres por diseminación intrahepática y uno por trombosis portal. En todos se evitó una laparotomía. En los 4 casos con tumores de la vía biliar, la EL modificó el estadio preoperatorio en 2 pacientes por la existencia de adenopatías del tronco celíaco, añadiéndose carcinomatosis en uno.
Del grupo total de 32 pacientes, la estadificación preoperatoria se vio modificada en 11 casos, mientras que se evitó una laparotomía en 8 ocasiones (25%). No existieron complicaciones y la estancia fue de 3 días en el grupo de pacientes en los que sólo se realizó la estadificación laparoscópica.
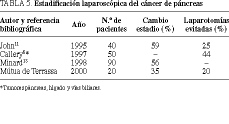
Comentario. El progreso de la cirugía de las metástasis hepáticas se ha reflejado en un importante descenso de la morbimortalidad, lo que ha permitido ampliar las indicaciones de resección. Actualmente, el criterio empleado de mayor relevancia es que exista la posibilidad de tratar todo el tumor20. Jarnagin et al observaron que el 21% de los pacientes que tenían metástasis hepáticas aparentemente resecables en el estudio preoperatorio presentaron enfermedad irresecable tras la laparotomía, y que en la mitad de los casos ésta se localizaba en el hígado21. La posibilidad de realizar EL y ecolaparoscopia permite determinar la extensión real de la enfermedad y evitar una laparotomía innecesaria si es irresecable (tabla 4)22. Por otro lado, la ecolaparoscopia permite obtener un mapa ecográfico hepático exacto y aplicar así diferentes técnicas complementarias (embolización portal, radiofrecuencia, etc.) e incluso recuperar a pacientes para tratamientos quirúrgicos de resección, como se demostró en un paciente de esta serie.
Si bien el tratamiento del hepatocarcinoma mediante resección se utiliza cada vez en un menor número de casos debido a la existencia de otras alternativas terapéuticas, es especialmente importante seleccionar de manera correcta a los pacientes tributarios de cirugía. La ecolaparoscopia es especialmente útil, ya que permite distinguir lesiones no visibles de nódulos de regeneración, así como descartar trombosis portal, satelitosis o multicentricidad23.
Lesiones pancreáticas
La cirugía constituye el único tratamiento curativo del cáncer de páncreas. El 30-40% de los pacientes con tumores teóricamente resecables presentan diseminación tumoral (metástasis hepáticas y/o carcinomatosis) en la intervención24. En los últimos años se han desarrollado técnicas diagnóstico-terapéuticas (colangiopancreatografía retrógrada endoscópica, laparoscopia) que suponen una menor agresión para el paciente y permiten realizar una derivación de la vía biliar y/o gástrica sin la necesidad de una laparotomía. Por tanto, es fundamental establecer correctamente la extensión real de la enfermedad para determinar el tratamiento adecuado para cada paciente. La asociación de EL y ecolaparoscopia cumple este objetivo, ya que permite determinar la extensión local de la tumoración pancreática, detectar carcinomatosis, adenopatías retroperitoneales o metástasis hepáticas desconocidas, e incluso biopsiar las lesiones antes de la laparotomía24.
Técnica y pacientes. La técnica de EL es similar a la descrita. Mediante la ecolaparoscopia se estudian el hígado, el árbol biliar, el páncreas y la estructuras peripancreáticas de una forma estandarizada19. Además de los criterios habituales de irresecabilidad (carcinomatosis, metástasis hepáticas, invasión extrapancreática del tumor, adenopatías del tronco celíaco > 10 mm con biopsia positiva), los criterios ecográficos de invasión vascular son: afectación directa con tumor visible en la luz del vaso, pérdida del plano hiperecogénico que rodea los vasos y/o imposibilidad de definir los vasos, lo que significa obstrucción tumoral.
Entre septiembre de 1997 y septiembre de 1999, en el Hospital Mútua de Terrassa se intervinieron 23 pacientes con cáncer de páncreas potencialmente resecables. De ellos, 20 enfermos fueron estudiados mediante EL y ecolaparoscopia. Ésta no se realizó en un caso por problemas técnicos, y 10 pacientes fueron considerados resecables, lo que se confirmó durante la laparotomía en siete. En un paciente en que la EL demostró resecabilidad, el aspecto macroscópico de la cara lateral de la vena porta durante el acto quirúrgico una vez seccionado el páncreas obligó a una resección parcial de la misma, aunque la histología no demostró infiltración neoplásica y únicamente afectación inflamatoria. En 3 casos el estudio fue dudoso (uno sin ecografía y uno con exploración incompleta por adherencias), aunque la laparotomía demostró con posterioridad crecimiento tumoral extrapancreático en todos ellos.
De los 7 pacientes considerados irresecables mediante EL y ecolaparoscopia (metástasis hepáticas en tres, afectación portal en cuatro y carcinomatosis en dos), dos no recibieron terapéutica añadida, dos fueron tratados con endoprótesis endoscópica y en los tres restantes se realizó una pequeña laparotomía para obtener material histológico y la derivación quirúrgica de la vía biliar. No ha existido morbilidad ni mortalidad relacionadas con el proceso laparoscópico.
Comentario. La EL combinada con ecolaparoscopia modifica en un número considerable de pacientes el estadio del cáncer de páncreas y la actitud terapéutica25. En esta serie, se ha modificado el planteamiento inicial en un 35% de los pacientes, evitando una laparotomía innecesaria en el 20% (tabla 5). No obstante, con el objetivo de no infratratar a pacientes, la definición de irresecabilidad debe ser confirmada histológicamente. Ante la duda, una exploración incompleta o la imposibilidad de obtener material para histología por laparoscopia, debe realizarse una laparotomía exploradora (tres en esta serie). En un futuro, la aplicación de sondas de ecografía con canal de trabajo para toma de muestras, y la progresión en la curva de aprendizaje nos ayudará en estas situaciones.
Por otro lado, en los pacientes no resecables por enfermedad avanzada el abordaje laparoscópico permitiría practicar derivaciones paliativas biliodigestivas26, con lo que, una vez establecido el estadio por EL y ecolaparoscopia, no sería necesario practicar una laparotomía, aunque se deberán tener en cuenta otras alternativas paliativas, como la endoprótesis endoscópica.
La EL-ecolaparoscopia ha demostrado una fiabilidad del 70% de los casos considerados resecables, incluso en un paciente en que el cirujano consideró infiltrada la vena porta. Si bien el "patrón oro" para demostrar la invasión neoplásica de la vena porta ha sido clásicamente la valoración intraoperatoria por parte del cirujano, esta impresión puede ser errónea en un 15-80% de las ocasiones, en que la supuesta afectación portal resultó ser inflamatoria27. La ecografía sería de especial ayuda en el estudio de la encrucijada anatómica del eje espleno-portal y páncreas, ya sea por vía laparoscópica o convencional, evitando descartar a pacientes para una posterior resección.
Inconvenientes de la estadificación ecolaparoscópica. Esta técnica presenta dos inconvenientes: la curva de aprendizaje es dificultosa y prolongada19 y la posible influencia perjudicial de la laparoscopia en la evolución natural de las neoplasias. En los últimos años se ha demostrado el riesgo de diseminación neoplásica en pacientes con cáncer sometidos a procedimientos por laparoscopia, tanto diagnóstica como terapéutica, especialmente por la aparición de implantes en los trocares28. En estas circunstancias nuestro grupo utiliza la EL y ecolaparoscopia como técnica de exploración diagnóstica, evitando en todo momento la manipulación tumoral y la práctica de una punción-citología o una biopsia debe ser realizada únicamente para confirmar el diagnóstico en aquellos pacientes irresecables.