Introducción
La eventración es una complicación frecuente de la laparotomía, sobre todo cuando la incisión interesa a la línea media abdominal, pudiendo aparecer tras el 1-15% de las intervenciones1,2. Cuando el defecto de la pared es mayor de 4-5 cm de diámetro existe una pérdida de sustancia parietal que es preciso reconstruir sin que exista tensión en la línea de sutura3. Las técnicas quirúrgicas que no siguen este principio, como pueden ser las técnicas de sutura directa de los bordes del anillo eventral, se acompañan de unas tasas de recidiva totalmente inaceptables, que alcanzan el 30-40%4-6.
Para corregir la pérdida de sustancia parietal se ha generalizado el uso de prótesis, asociadas o no a algún tipo de plastia en el defecto herniario. Los resultados publicados, en cuanto a la tasa de recidivas, han mejorado de manera sustancial los conseguidos sin la utilización de prótesis, calculándose glo balmente en torno al 6,4%7, aunque pueden variar de forma amplia de unas series a otras, oscilando entre el 0 y más del 18%8-11. De igual forma, también varía el tipo de prótesis utilizada, así como las técnicas de colocación. Estas últimas pueden agruparse en técnicas de sustitución, que son aquellas en las que la prótesis se coloca puenteando o solapando el defecto parietal y actúan como único plano de contención y, por otro lado, en técnicas de refuerzo, donde la prótesis se coloca como un plano más, por encima o por debajo de una reconstrucción plástica musculoaponeurótica.
El objetivo de la actual revisión es conocer si, en nuestra experiencia, hay relación entre la técnica quirúrgica por un lado, y el material protésico por otro, con la aparición de recidivas y/o infección.
Pacientes y método
Pacientes
Hemos revisado la experiencia de dos hospitales que atienden en conjunto a una población de 450.000 habitantes: el Hospital Vega Baja (SVS) durante el período comprendido entre 1990 y 1997, y el Hospital Morales Meseguer (INSALUD) durante el período 1994-1997, es decir, desde la puesta en marcha de ambos hospitales hasta junio de 1997.
Se incluyen todos los pacientes intervenidos por eventración, con un defecto aponeurótico mayor de 5 cm de diámetro y a los que se practicó una corrección quirúrgica con alguna técni ca que implicaba la colocación de una prótesis.
Cumplieron este requisito 175 pacientes, aunque 23 se perdieron durante el seguimiento postoperatorio (seis fallecieron por causas no relacionadas con la intervención y 17 no acudieron a las revisiones), con lo que resulta un total de 152 pacientes, que forman el núcleo de la actual revisión.
La edad media fue de 61 años (rango 43-79). En cuanto al sexo, el 32% de los intervenidos fueron varones y el 68% mujeres.
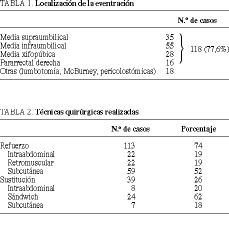
La localización de la eventración se expone en la tabla 1, destacando que en 118 casos (77,6%) se localizó en la línea media.
El 81,5% de los pacientes fueron intervenidos de forma electiva, mientras que el 18,5% fueron operados con carácter urgente ante la presencia de una incarceración de su eventración.
Del total de enfermos, en 28 de ellos la eventración ya había sido intervenida previamente en una o más ocasiones, tratándose pues de una eventración recidivada.
Por último, señalar que, en cuanto al diámetro transverso de orificio herniario, 90 casos fueron clasificados como eventraciones medianas (anillo con diámetro de 6-10 cm), 52 casos como grandes (11-15 cm) y 10 casos como gigantes (16 cm o más).
Método
Dependiendo del tamaño del orificio herniario y de la calidad de la pared muscular adyacente, la prótesis fue colocada bien como un refuerzo al cierre aponeurótico (113 pacientes) o bien como sustitución de la pared abdominal (39 enfermos)12.
En el supuesto de prótesis como refuerzo, las estrategias quirúrgicas usadas fueron la técnica de Usher8, que consiste en la colocación intraabdominal de la prótesis, cubierta por delante por el cierre directo del orificio herniario y separada de las vísceras por un lecho omentoparietal; la técnica de Rives13, con la prótesis en el plano retrorrectal, o bien la técnica de Welti-Eudel14, colocando la malla subcutánea de manera que cubra el defecto aponeurótico anterior creado por el desdoblamiento fascial y su cierre en la línea media.
Las técnicas de sustitución utilizadas fueron: a) la colocación de la malla intraperitoneal sobre un lecho omentoparietal y cubierta por el saco suturado en la línea media; b) prótesis subcutánea sobre el saco suturado en la línea media, y c) prótesis colocada en "sándwich peritoneal", según técnica de Matapurkar15.
En la tabla 2 se exponen los casos realizados según las distintas técnicas quirúrgicas.
El uso de un determinado tipo de prótesis dependió de las preferencias del cirujano y de su disponibilidad en el momento de la intervención, aunque se utilizó preferentemente el par che de politetrafluoroetileno (PTFE) cuando fue preciso ubicarla en la cavidad abdominal. Así, la malla de polipropileno se utilizó en 74 casos, la de PTFE en 53 y la duramadre deshidratada en 25 pacientes.
Se administró profilaxis antibiótica sistemática con 1 g de cefazolina en los pacientes sometidos a cirugía electiva, y 2 g de cefoxitina (Mefoxitin, MSD, S.A.) en los casos de cirugía urgente. Ambas cefalosporinas se utilizaron en una sola dosis, durante la inducción anestésica. Así mismo, se utilizó profilaxis antitrombótica sistemática con enoxaparina (Clexane, Rhône-Poulenc Rorer, S.A.), 20 mg subcutáneos cada 24 h.
Con motivo de la actual revisión se citó a todos los pacientes en consulta externa, donde se estudió su historia clínica en busca de posibles complicaciones surgidas durante el seguimiento, y fueron explorados físicamente por el mismo cirujano para detectar o no la presencia de recidiva. El seguimiento medio ha sido de 40 meses (rango, 8-81).
Para el análisis estadístico se ha utilizado el test de la *2 para la comparación de distribuciones.
Resultados
No ha existido mortalidad postoperatoria. Se detectaron escasas complicaciones de tipo general, que tuvieron poca relevancia clínica.
Infección
Se detectaron 8 casos de infección, lo que supone una tasa de infección de herida quirúrgica del 5,2%.
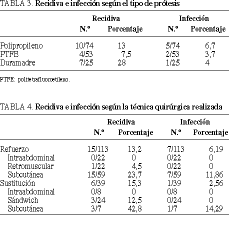
No se ha encontrado asociación estadística entre infección y tipo de prótesis, siendo la tasa de infección para el PTFE del 3,7% (2 de 53 casos), del 4% para la duramadre (1 de 25) y del 6,7% para el polipropileno (5 de 74). Sí hemos encontrado diferencias en cuanto al comportamiento de la prótesis ante la infección: mientras que en el caso de PTFE fue necesario retirar la malla en los 2 pacientes para la resolución de la infección, los pacientes en los que se utilizó duramadre o polipropileno evolucionaron satisfactoriamente con la apertura de la herida y la exposición de la zona, sin precisar la retirada de la malla.
En cuanto a la técnica utilizada, los 8 casos de infección aparecieron en el grupo en el que el plano de colocación de la prótesis fue el subcutáneo (66 pacientes), existiendo diferencias estadísticamente significativas (p < 0,05).
Recidiva
Se detectaron 21 casos de recidiva, lo que supone una tasa global de recurrencia del 13,8%. Estos 21 casos se distribuyen, según la prótesis utilizada, en 4 recidivas en el grupo de 53 pacientes tratados con PTFE (7,5%), 10 recidivas en el grupo de 74 enfermos con polipropileno (13%), y 7 recidivas en los 25 con duramadre (28%). La mayor frecuencia de recidiva en el grupo de duramadre fue estadísticamente significativa al compararla con el grupo de PTFE (p < 0,05) y en el límite de la significación al compararla con el polipropileno (p = 0,09).
En cuanto a la técnica quirúrgica, las recidivas se distribuyeron como se observa en la tabla 4. No se evidenciaron diferencias estadísticamente significativas al comparar las técnicas de sustitución y las de refuerzo. Por el contrario, al comparar el plano de la prótesis, en las técnicas de refuerzo con la prótesis en un plano profundo (intraabdominal o retrorrectal) sólo apareció una recidiva sobre 54 casos (1,8%), mientras que cuando la prótesis se colocó en un plano superficial (subcutáneo) se detectaron 14 recidivas sobre 58 casos (23,7%, p < 0,01).
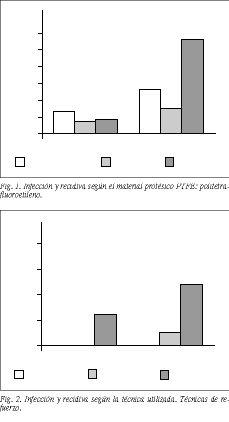
En la figura 1 expone gráficamente la incidencia de infección y recidiva según el tipo de prótesis y en la figura 2 la relación entre recidiva y técnica quirúrgica.
En las tablas 3 y 4 se resumen los datos relativos a la relación entre recidiva e infecciones con el tipo de prótesis y con la técnica quirúrgica, respectivamente.
Discusión
Sobre la infección
Se acepta, en general, que la cirugía de las grandes eventraciones supone un riesgo significativo de infección que justifica el empleo de profilaxis antibiótica de rutina16. De los tres factores de riesgo de infección definidos en el estudio americano National Nosocomial Infection Surveillance17 (ASA mayor de 2, intervención contaminada o sucia y tiempo prolongado de intervención) con frecuencia están presentes en este marco dos o tres.
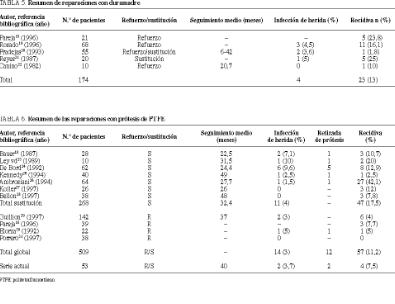
Las tasas de infección publicadas en la bibliografía científica no varían mucho de unas prótesis a otras. En el caso de la malla de polipropileno, el análisis de 16 series, que totalizan 819 pacientes, puso de manifiesto una tasa de infección media del 5,4%7. Las series reunidas en nuestra revisión bibliográfica arrojan, para la prótesis de duramadre (tabla 5) un índice de infección del 4%, y para la de polipropileno (tabla 6) del 3%. Los resultados en nuestra casuística son bastante similares a los referidos anteriormente: un 6,7% para el polipropileno, un 4% con la duramadre y un 3,7% con el PTFE, no existiendo diferencias significativas entre los tres grupos.
Sin embargo, sí se han apreciado diferencias al comparar los distintos planos de colocación de la malla. En nuestra casuística, todos los casos aparecieron en el grupo de pacientes con la prótesis colocada en el plano subcutáneo (8 de 66 casos), con lo que se obtiene una tasa de infección del 12%, mientras que no apareció ningún caso de infección en los restantes 86 casos con prótesis colocadas en planos más profundos. La prótesis en el plano subcutáneo está más expuesta a la contaminación por los gérmenes de la piel del paciente, por lo que es el plano de mayor prevalencia de infección quirúrgica15. Sin embargo, también es cierto que, en estas situaciones, habitualmente la infección se controla bien con medidas locales, sin que sea necesaria la retirada de la prótesis32. Esto sucedió así en nuestra serie cuando la infección asentó sobre una prótesis de polipropileno o de duramadre, pero no con la prótesis de PTFE, ya que en los 2 casos de infección fue precisa su extracción para la resolución del problema. En las series consultadas (tabla 6), de los 14 casos de infección detectados en los que se había utilizado el PTFE fue necesario su retirada en 12 (85,7%). Por este motivo creemos que, en situaciones de alto riesgo de infección, como la cirugía urgente, cuando sea imprescindible usar una prótesis es preferible el polipropileno al PTFE. En situaciones de cirugía electiva, si no existen factores especiales de riesgo de infección (presencia de dermatitis o úlceras tróficas en la piel que recubre la eventración, presencia de focos de supuración durante la disección de la eventración), la probabilidad de aparición de infección local se relaciona más, en nuestra experiencia, con el plano de ubicación de la malla que con el tipo de prótesis. Según nuestros resultados, es más seguro ubicar la prótesis en un plano profundo (intraabdominal, preperitoneal o retromuscular) que en un plano superficial (preaponeurótico o subcutáneo). En los poco frecuentes casos de infección de una prótesis colocada en posición intraperitoneal se recomienda su rápida retirada para impedir la difusión intraabdominal de la sepsis33.
Sobre la recidiva
El aspecto más importante para evaluar los resultados de una técnica de reparación herniaria es la tasa de recidiva. Los resultados de muchos estudios publicados pueden no ser comparables debido a dos factores importantes: el modo de detectar la recidiva y el tiempo de seguimiento. El único procedimiento adecuado para detectar la recidiva es la exploración física en decúbito y en bipedestación realizada por el cirujano, siendo necesaria, por tanto, la revisión en consulta externa. La conversación telefónica o la respuesta a una carta pueden resultar bastantes inexactas en cuanto a la detección de recidivas. En la actual revisión, en algunos de los pacientes que se encontraban asintomáticos y no habían manifestado signos de recidiva, la exploración física demostró su existencia, mientras que en algunos enfermos que tenían dudas al respecto la exploración del cirujano descartó la recidiva. Hallazgos similares han obtenido Hesselink et al6 y McLanahan et al34. En cuanto al tiempo de seguimiento, se recomienda un mínimo de 3 años, pues en este tiempo se calcula que aparecen el 80% de las recidivas6,35. Con motivo de este estudio, todos los pacientes fueron citados y revisados en la consulta por el mismo cirujano, que determinó la presencia o no de recidiva, lo que, unido a un seguimiento promedio de 40 meses, creemos que nos ha permitido reconocer la mayoría de las recidivas.
La tasa global de recidiva del 13,8% obtenida en esta revisión parece bastante realista. Aunque se sitúa en valores intermedios entre los publicados1, y se compara muy favorablemente con el 30-40% de recidiva publicado cuando no se usa prótesis y se practica una sutura simple4-6, creemos que es aún demasiado elevada y puede reducirse. El tipo de prótesis, por un lado, y la técnica quirúrgica, por otro, son factores que han demostrado su importancia en la presente serie. En cuanto al tipo de prótesis, los peores resultados los hemos obtenido con la duramadre, lo que, unido a su elevado precio, nos conduce a desaconsejar su empleo. Nosotros hemos dejado de utilizarla en los últimos años de este estudio. Las tasas de recidiva pu blicadas con esta prótesis (tabla 5) son, en general, bastante elevadas, con la excepción de algún autor22. No encontramos diferencias significativas en la tasa de recidiva entre el polipropileno y el PTFE. Nuestra tasa de recidiva con el PTFE es algo inferior a la media de las series publicadas (tabla 6): el 7,5 frente al 11,2%. Por el contrario, nuestro índice de recidiva con el polipropileno (13%) es superior a la media de las series reunidas por Sitzmann (6,4%)7, aunque alguna de estas series comunicaban un seguimiento inferior a 3 años o desconocido. Sin embargo, las diferencias más llamativas en nuestra serie se encuentran al comparar las distintas técnicas quirúrgicas. Cuando la prótesis se colocó como refuerzo en un plano posterior (intraabdominal o retromuscular), lo que sucedió en 54 casos, sólo se detectó una recidiva (1,8%), mientras que cuando se colocó como refuerzo en el plano subcutáneo, en 59 casos, se detectaron 14 recurrencias (23,7%), es decir, una tasa de recidiva mayor incluso a la de los casos en los que la prótesis se colocó como sustitución (15,3%). Las tasas de recidiva publicadas con prótesis de refuerzo en plano profundo suelen ser bajas. Así, Arnaud36, con prótesis intraperitoneal refiere un 3,6%, Stoppa37 con prótesis preperitoneal, un 2%, McLanahan34, Guillion29 y Flament y Rives32, con prótesis retromuscular, comunican tasas de recidiva del 3,5,4 y del 5,2%, respectivamente. De todos modos, también se han comunicado buenos resultados usando prótesis subcutáneas, como los referidos por Chevrel38, con un índice de recidiva del 5,5%. Incluso algunos autores, como Leber39, ofrecen datos contrarios a los nuestros, con una tasa de recidiva del 19,5% para las mallas subfasciales y del 14,8% para las mallas prefasciales.
En conclusión, en nuestra serie los peores resultados en cuanto a índices de infección y de recidiva se han obtenido con las prótesis colocadas en el plano subcutáneo, por lo que desaconsejamos el uso de esta localización, siempre que sea posible. Dado que algunos autores han obtenido resultados diferentes, creemos que son necesarios más estudios que apoyen una u otra táctica quirúrgica.