El empleo de los dispositivos veno-venosos de oxigenación por membrana extracorpórea (ECMO-vv) en la insuficiencia respiratoria grave de origen traumático ha sido controvertido y no está completamente definido, probablemente debido a su infrautilización en esta población. La ECMO-vv permite una adecuada oxigenación hasta que los pulmones se recuperan. Sin embargo, un aspecto limitante para su generalización ha sido el riesgo hemorrágico por la propia enfermedad traumática y por la anticoagulación necesaria del dispositivo1. En este artículo describimos un caso de hipoxemia traumática refractaria tratada con ECMO sin anticoagulación, reflejando que estos dispositivos pueden ser considerados una medida de rescate una vez optimizadas las opciones terapéuticas previas.
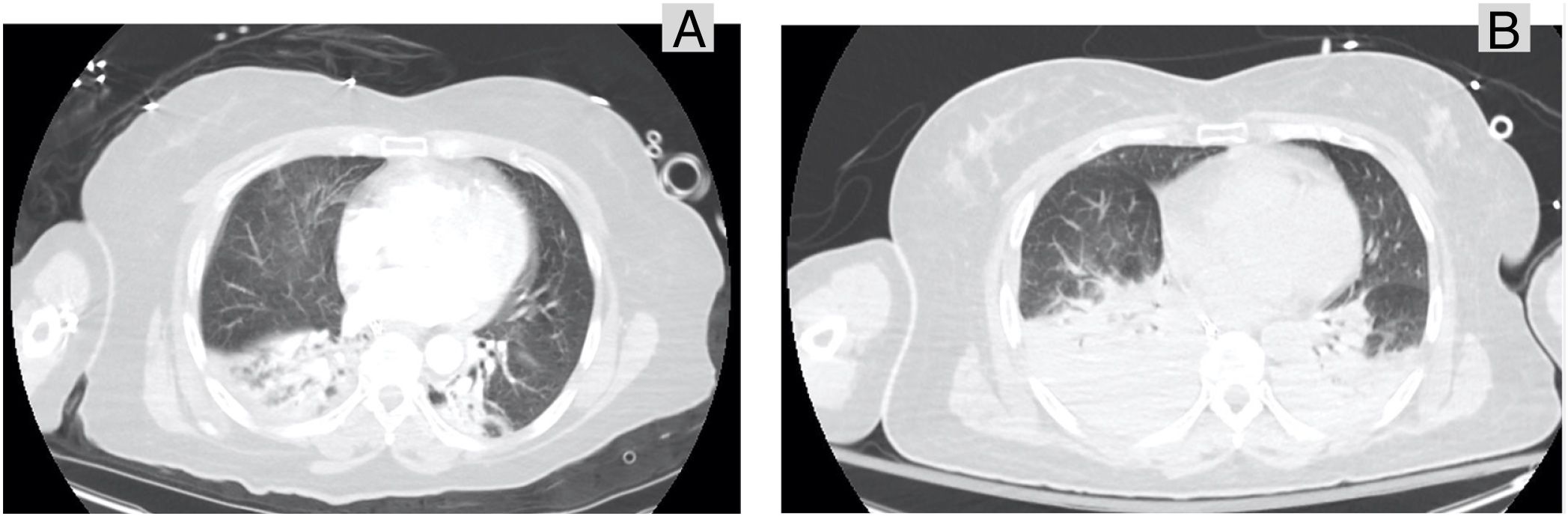
Presentamos el caso de una mujer de 65 años que sufrió un atropello por un coche. A su ingreso en Medicina Intensiva, estaba consciente y sin ninguna focalidad. Presentaba TA 90/60, Fc de 90 lpm y taquipnea de 20 rpm. con SatO2 90%. En la exploración física destacaba hematoma en pómulo izquierdo, hipoventilación en base derecha, discreta defensa abdominal y dolor a la palpación en pelvis. Se efectuó estudio de imagen apreciando fractura de dos costillas unifocales derechas con contusión pulmonar bilateral (fig. 1A), laceración hepática, traumatismo espinal (fractura de cinco apófisis transversas derechas desde T12 hasta L4) y traumatismo esquelético (fracturas en ambas alas sacras, fractura con minuta de pubis izquierdo con fracturas de ambas ramas iliopubiana y ceja cotiloidea anterior derecha). No se apreció lesión intracraneal.
Las primeras horas estuvieron marcadas por shock hemorrágico precisando hemoderivados y drogas vasoactivas (activación de protocolo de hemorragia masiva). Se procedió a intubación orotraqueal y se completó estudio mediante arteriografía. Se identificaron varios focos de extravasación de contraste sugestivos de sangrado que eran dependientes de la arteria hipogástrica y epigástrica izquierda. Se embolizaron y se logró estabilidad hemodinámica.
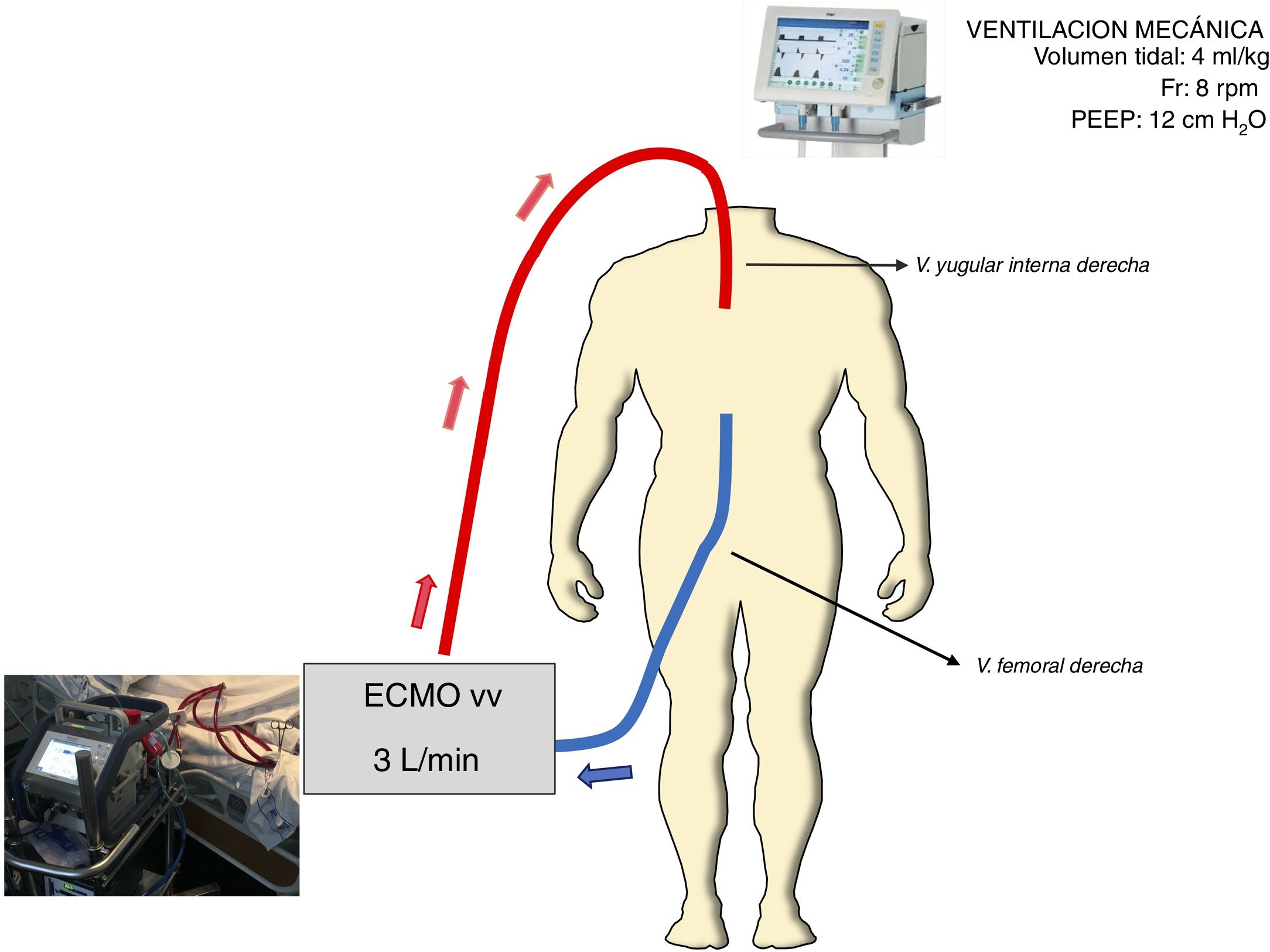
Paralelamente, la insuficiencia respiratoria empeoró. La PaO2/FiO2 era de 65 con PEEP 15. La sedación se mantuvo con midazolam y fentanilo añadiendo puntualmente cisatracurio para optimizar la función ventilatoria. Se repitió prueba de imagen a la hora 16 de ingreso en UCI, objetivando progresión de las contusiones pulmonares (fig. 1B). El estudio de ecocardiograma transtorácico no reveló alteraciones. Entonces se decidió establecer ECMO-vv femoro-yugular (CardioHelp®, Maquet Holding, Alemania) (fig. 2). La ubicación de las cánulas se controló con ecocardiografía transesofágica. Se pautó heparina durante la propia implantación, se pautó un flujo de 3 lpm y se revirtió la anticoagulación con protamina (80 mg) transcurrida una hora de su instauración. Se decidió revertir la anticoagulación ante el riesgo de hemorragia secundaria a la lesión hepática, fracturas pélvicas, hematoma en psoas y la coagulopatía que presentaba secundaria a la hemorragia masiva de las horas previas. La ventilación mecánica fue protectora con PEEP 12 cm de H2O y VT 4 mL/kg, FiO2 45%. Después de la implantación, efectuamos estudio de broncoscopia que no mostró lesiones ni secreciones hemáticas. Con la terapia instaurada se objetivó mejoría en la oxigenación (PO2 medido en arteria radial izquierda), en la hemodinámica y en lactato sérico, logrando preservar diuresis y alcanzar finalmente balance hídrico negativo. Al tercer día se inició el destete de ECMO ante la constatación de mejoría radiológica y gasométrica. Se redujo el flujo de oxígeno en ECMO, se ventiló con FiO2 < 45% y PEEP < 10 cm de H2O y se apreció PaO2/FiO2 > 200. Por todo ello, se retiró la ECMO-vv al cuarto día. No se detectaron complicaciones relacionadas con el dispositivo durante el tratamiento con ECMO. Se efectuó traqueotomía el día séptimo ante la necesidad de soporte respiratorio por polineuropatía. Finalmente, la paciente fue dada de alta a planta de hospitalización.
La insuficiencia respiratoria tras traumatismo grave puede deberse a la propia lesión traumática pulmonar, pero también de modo indirecto por transfusión masiva, broncoaspiración o embolismo graso. Los sistemas ECMO-vv permiten asegurar una correcta oxigenación a los tejidos mientras que, en paralelo, los pulmones se recuperan del daño que ocasionó la insuficiencia respiratoria grave. Su instauración podría plantearse ante la persistencia de hipoxemia grave (PaO2/FiO2 < 120 con FiO2 > 90% y PEEP > 10) tras optimización de medidas terapéuticas menos invasivas (ventilación protectora)2,3.
Los dispositivos ECMO se emplean en las unidades de críticos tanto en situaciones de compromiso cardiorrespiratorio como en los procesos de donación en asistolia4. Sin embargo, la experiencia acumulada en la enfermedad traumática grave ha sido escasa, limitándose a series de casos5,6, debido probablemente al riesgo hemorrágico que implica3. Este riesgo está presente en el momento de la canulación y facilitado por la coagulopatía asociada al traumatismo, así como por la anticoagulación que implican estos sistemas. La necesidad y dosificación de anticoagulación en los dispositivos ECMO-vv ha de individualizarse, valorando en cada caso el riesgo-beneficio. El descarte o dosificación a la baja de la anticoagulación condiciona un seguimiento estrecho de los flujos del dispositivo y no representa una limitación absoluta. En nuestro caso, desestimamos la heparinización por el elevado riesgo de sangrado dadas las lesiones hepáticas y en pelvis. En el traumatismo grave, se ha descrito que la administración inicial de heparina se asoció con mayores complicaciones hemorrágicas. Sin embargo, en nuestro caso, no hubo ninguna incidencia de este tipo, pensamos que tal vez debido a que revertimos la heparina inicial.
El momento de instaurar estas terapias representa otro de los puntos de debate. El caso descrito con un inicio a las 12 horas de ingreso y por un periodo de 80 horas, refrenda el valor de instaurar estos dispositivos de forma precoz, pues se ha asociado con mejores resultados y menor mortalidad7,8. De hecho, en la población traumática la mortalidad asociada al empleo de ECMO ha ocurrido predominantemente en casos con retraso en la instauración y cuando se necesitaba ECMO veno-arterial debido a fallo circulatorio, mientras que el inicio temprano de ECMO-vv por disfunción respiratoria tuvo mejores resultados9. Pensamos que un comienzo precoz puede permitir una recuperación pulmonar más rápida, evitando los potenciales efectos adversos asociados a estos dispositivos. Los resultados iniciales parecen mostrar tasas de supervivencia similares a la población no traumática y convierten a este soporte en una prometedora opción terapéutica para estos pacientes con un nivel elevado de complejidad10.
Los dispositivos ECMO-vv pueden ser considerados una medida de rescate frente a la hipoxemia refractaria en los pacientes con traumatismo grave, una vez optimizadas las opciones terapéuticas previas. La selección de los pacientes y un inicio precoz constituyen dos elementos claves, que se deberían abordar de modo individual en cada caso. El riesgo hemorrágico debe ser evaluado ya que por sí solo no constituye una contraindicación.
Conflicto de interesesLos autores declaran no tener ningún conflicto de intereses.