La paratiroidectomía mínimamente invasiva radioguiada (PMIR)1,2 se ha implementado en el Hospital Universitario de Navarra dentro de un Proyecto de Investigación Prospectivo, autorizado por el Comité de Ética (octubre del 2019), con el objetivo de mejorar nuestra tasa de éxito previa en paratiroidectomía selectiva (94,6%)3.
Desde su incorporación en febrero del 2020, hasta diciembre del 2021, hemos realizado PMIR (MIBI o MAA)2 consecutivamente a todos los pacientes con hiperparatiroidismo primario e indicación de paratiroidectomía mínimamente invasiva (80), edad media 61,1 años (± 11,2), 61 mujeres (76,3%). Los datos clínicos y analíticos se muestran en la tabla 1.
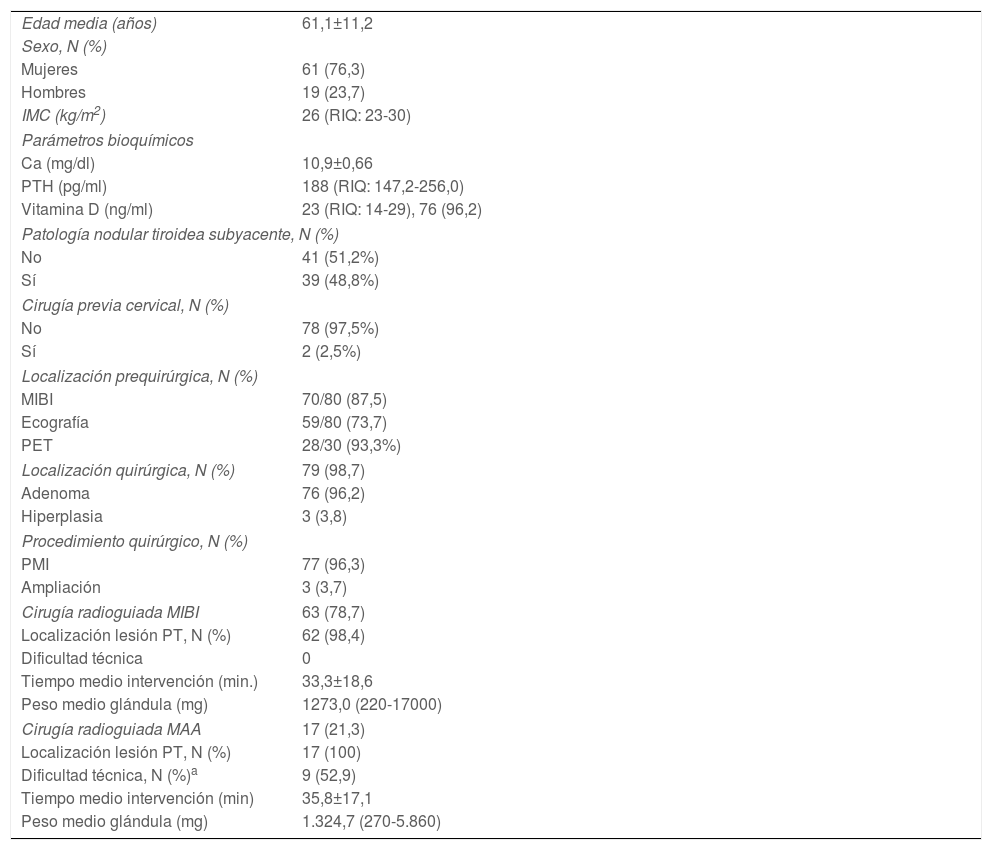
Pacientes con indicación PMIR. Resultados
| Edad media (años) | 61,1±11,2 |
| Sexo, N (%) | |
| Mujeres | 61 (76,3) |
| Hombres | 19 (23,7) |
| IMC (kg/m2) | 26 (RIQ: 23-30) |
| Parámetros bioquímicos | |
| Ca (mg/dl) | 10,9±0,66 |
| PTH (pg/ml) | 188 (RIQ: 147,2-256,0) |
| Vitamina D (ng/ml) | 23 (RIQ: 14-29), 76 (96,2) |
| Patología nodular tiroidea subyacente, N (%) | |
| No | 41 (51,2%) |
| Sí | 39 (48,8%) |
| Cirugía previa cervical, N (%) | |
| No | 78 (97,5%) |
| Sí | 2 (2,5%) |
| Localización prequirúrgica, N (%) | |
| MIBI | 70/80 (87,5) |
| Ecografía | 59/80 (73,7) |
| PET | 28/30 (93,3%) |
| Localización quirúrgica, N (%) | 79 (98,7) |
| Adenoma | 76 (96,2) |
| Hiperplasia | 3 (3,8) |
| Procedimiento quirúrgico, N (%) | |
| PMI | 77 (96,3) |
| Ampliación | 3 (3,7) |
| Cirugía radioguiada MIBI | 63 (78,7) |
| Localización lesión PT, N (%) | 62 (98,4) |
| Dificultad técnica | 0 |
| Tiempo medio intervención (min.) | 33,3±18,6 |
| Peso medio glándula (mg) | 1273,0 (220-17000) |
| Cirugía radioguiada MAA | 17 (21,3) |
| Localización lesión PT, N (%) | 17 (100) |
| Dificultad técnica, N (%)a | 9 (52,9) |
| Tiempo medio intervención (min) | 35,8±17,1 |
| Peso medio glándula (mg) | 1.324,7 (270-5.860) |
a Relacionada con la administración (constatación de la extravasación del radiotrazador que se traduce en la captación intraoperatoria por tejidos distintos a la paratiroides).
Realizamos PMIR-MIBI tras su administración IV (5 mCi 99mTc-MIBI), con adquisición gammagráfica inmediata y procedimiento quirúrgico radioguiado a los 60min, aproximadamente. Para realizar PMIR-MAA se administra intralesional ecoguiado (0,5 mCi 99mTc-macroagregados albúmina) el mismo día de la intervención, con posterior adquisición gammagráfica (SPECT/TC). Intraoperatoriamente empleamos gammasonda Neo2000® (Neoprobe Corporation, Dublin, EE. UU.) con cabezal de 9 mm y gammacámara portátil Sentinella® (Oncovision, Valencia, España).
Las pruebas diagnósticas preoperatorias, MIBI-SPECT/TC y ecografía, habían identificado la glándula patológica en 70 (87,5%) y 59 (73,7%) pacientes, respectivamente, siendo negativos o no concluyentes los restantes (tabla 1). En los 30 casos (37,5%) en que una de las anteriores era negativa o no eran totalmente concordantes se realizó PET-colina o metionina, siendo diagnóstica en 28 (93,3%).
La cirugía radioguiada fue mínimamente invasiva en 77 pacientes (96,3%), incluyendo los 2con antecedente quirúrgico cervical (una tiroidectomía total, una paratiroidectomía selectiva previa fallida). Tres (3,7%) requirieron ampliación de la incisión inicial: 2por afectación de 2glándulas contralaterales y una por la localización ectópica, posterior, del adenoma.
Se consiguió la resección quirúrgica de la lesión en 79 pacientes (98,7%), siendo 76 (96,2%) adenomas y 3(3,8%) hiperplasias (tabla 1). Dos presentaron doble lesión: un adenoma y una hiperplasia. Se registraron complicaciones quirúrgicas leves en 4 (5%): un pequeño hematoma subcutáneo autorresuelto, 2hipocalcemias transitorias y una paresia de cuerda vocal.
Según la valoración previa del estudio de localización4, indicamos PMIR-MAA en 18 pacientes (tabla 1), realizándose finalmente en 17, ya que en uno la gammagrafía demostró extensa contaminación cutánea por fuga del radiotrazador durante su inoculación ecográfica, invalidando el procedimiento. Dado que era una lesión paratiroidea MIBI-positiva, se inyectó a continuación MIBI, extirpándose finalmente. Se resecó la lesión marcada con MAA en los 17 restantes, siendo el tiempo medio del procedimiento quirúrgico 35,8 min. En 9 pacientes objetivamos significativa captación residual en el lecho quirúrgico tras la resección de la glándula radiomarcada (dispersión del radiotrazador a tiroides o musculatura pretiroidea durante su administración). En uno de ellos además se demostró gammagráficamente fijación pulmonar del MAA (administración parcial intravascular, inocua); en otro, un discreto hematoma subcutáneo postinyección, autorresuelto.
Se realizó PMIR-MIBI en 63 pacientes (tabla 1), confirmándose la resección de la lesión paratiroidea en 62 (98,4%). En la única cirugía «fallida» se extirpó una lesión débilmente MIBI-positiva, macroscópicamente indicativa de paratiroides, pero la histopatología demostró una adenopatía, que excepcionalmente puede captar MIBI5. El tiempo medio entre la administración del MIBI y el comienzo de la intervención fue 90 min. La duración media de la PMIR-MIBI fue 33,3 min, inferior al MAA (no significativamente p = 0,349). Tampoco hubo diferencias significativas en el tamaño de la lesión extirpada (p = 0,504).
Se resecaron mediante PMIR-MIBI 22 adenomas ectópicos (27,5%): 9 paraesofágicos, 7 mediastínicos, 3 pretraqueales, 2 prevertebrales y 1 intratímico.
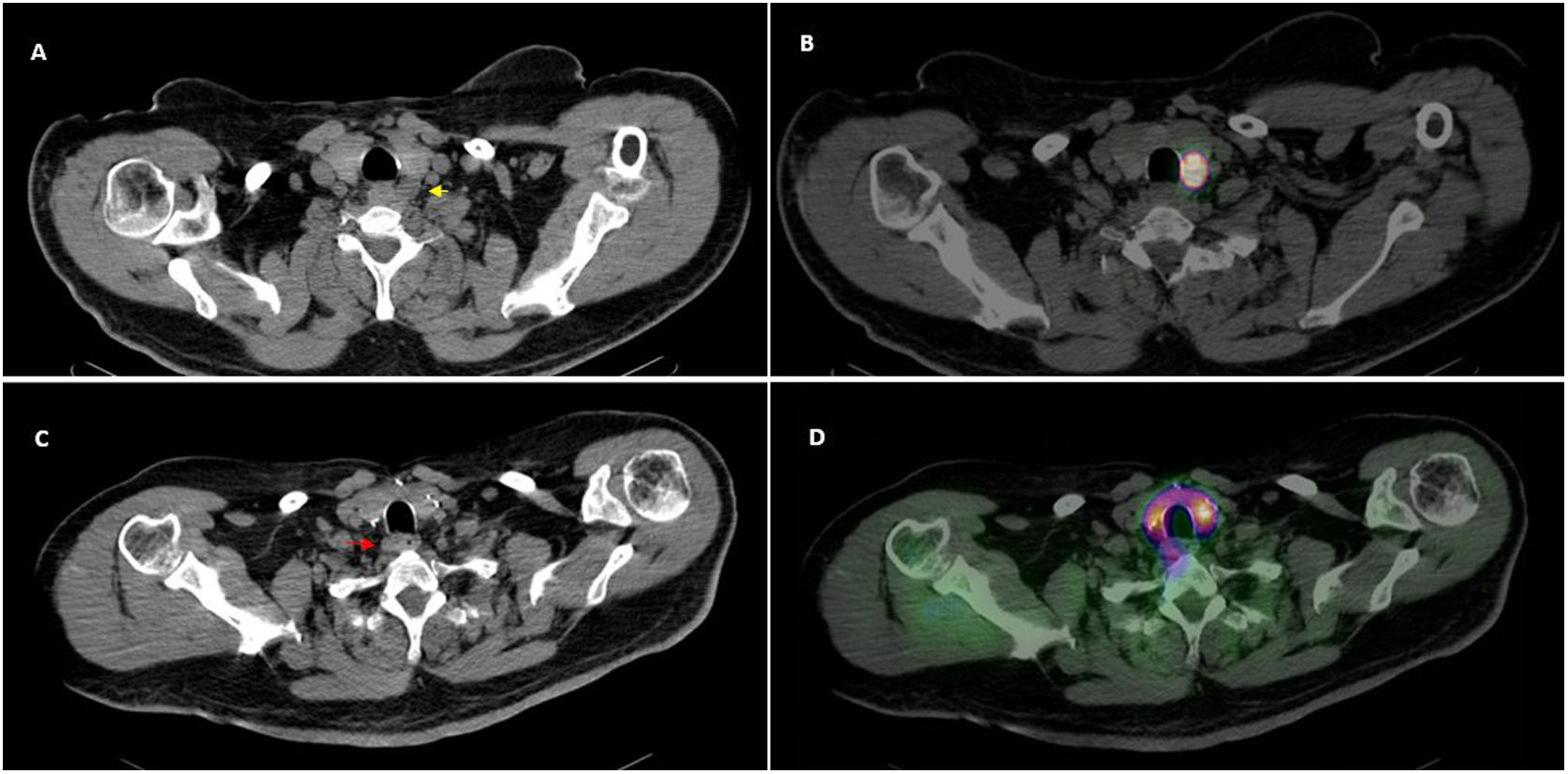
En el seguimiento a 6 meses la única PMIR en la que no se demostró histopatológicamente una glándula paratiroidea patológica, presenta curación bioquímica, circunstancia clínica excepcional6. Dos presentaron hipercalcemia persistente, a pesar de haberse resecado un adenoma; uno ha sido recientemente reintervenido con éxito (fig. 1) tras objetivarse nueva lesión paratiroidea (MIBI y PET-positiva). La tasa de curación provisional es 97,5%.
Paciente con HPP al que se resecó adenoma paratiroideo (flecha amarilla) en localización posterior al polo caudal del LTI (A) mediante PMIR tras la administración ecoguiada de 99mTc-MAA. El corte transaxial de fusión SPECT/TC muestra la correcta localización intralesional de la actividad (B). Al año persiste hipercalcemia, objetivándose una nueva lesión paratiroidea (C) en localización ectópica, más caudal, para-esofágica derecha (flecha roja) que presenta captación significativa de 99mTc-MIBI como muestra la imagen de fusión SPECT/TC (D), por lo que se extirpa satisfactoriamente mediante una segunda cirugía, en esta ocasión radioguiada con MIBI.
La PMIR-MIBI requiere estricta coordinación medicina nuclear-quirófano, que en nuestro ámbito ha sido satisfactoria, aunque el tiempo entre inyección e inicio de cirugía superó el objetivo inicialmente planteado, debido a los traslados intrahospitalarios. La fijación fisiológica del MIBI en tejidos próximos (tiroides, musculatura), puede dificultar la detección quirúrgica, especialmente en caso de glándulas paratiroideas con escasa intensidad de captación7 o «lavado rápido» (estudio preoperatorio). En este sentido, la imagen intraoperatoria (gammacámara portátil) es de gran ayuda, minimizando dicho inconveniente y confirmando la extirpación de la lesión.
La PMIR-MIBI permite la resección mínimamente invasiva de las lesiones ectópicas8.
Aunque el procedimiento quirúrgico con MAA es, en principio, técnicamente más sencillo, no son raras las dificultades en la administración intralesional ecoguiada, probablemente por la profundidad y el pequeño tamaño de las lesiones o la curva de aprendizaje.
En conclusión, la PMIR, tanto MIBI como MAA, se ha implantado en nuestro centro y se desarrolla con fluidez, gracias a la estrecha colaboración de los profesionales implicados. El equipo quirúrgico estima que la PMIR es más sencilla. Consideramos el método adoptado reproductible en cualquier Unidad de Cirugía Endocrina. Aunque la casuística es escasa y el seguimiento limitado (la mayoría de intervenciones en los últimos meses incluidos, debido a la interrupción de actividad quirúrgica por la pandemia de marzo-septiembre del 2020), los favorables resultados nos permiten prescindir del estudio histológico intraoperatorio. No obstante, la inclusión de más pacientes determinará el impacto en el éxito quirúrgico y la tasa de curación, así como la duración de la intervención y la tasa de complicaciones.
Conflicto de interesesLa presente investigación no ha recibido ayudas específicas provenientes de agencias del sector público, sector comercial o entidades sin ánimo de lucro