La miotomía de Heller por vía laparoscópica es el mejor tratamiento que podemos ofertar a los pacientes con acalasia. Al no actuar sobre la causa de la enfermedad sino que únicamente aliviamos la sintomatología la persistencia de los síntomas puede no desaparecer.
ObjetivoAnalizar los resultados de nuestro grupo en el tratamiento de la acalasia por vía laparoscópica.
Material y métodosSe revisan los resultados pre y postoperatorios de una serie de 20 pacientes intervenidos prospectivamente por vía laparoscópica de acalasia durante el período comprendido entre mayo de 2003 y abril de 2010. Para ello se ha utilizado una modificación de la escala de de gradación progresiva de los síntomas pre y postoperatorios descrita por Velanovich para el RGE (escala de 0-5). También se han recogido las complicaciones y estancia hospitalaria.
ResultadosSe ha practicado una miotomía de Heller amplia asociando un mecanismo anti-reflujo tipo Dor en todos los casos. No se han producido perforaciones esofágicas ni complicaciones intraoperatorias. Dos (10%) pacientes han presentado complicaciones postoperatorias. La estancia hospitalaria ha sido de 3,11±2,13 días. Tras un seguimiento medio de 55,8±14,1 meses los síntomas estudiados han disminuido significativamente tras la cirugía. Sólo 3 pacientes (15%) han presentado clínica postoperatoria de RGE. Diecinueve pacientes (95%) refirieron estar satisfechos con el resultado de la intervención.
ConclusionesEl tratamiento laparoscópico de la acalasia es una técnica segura, reproducible y efectiva, que consigue un control de los síntomas de la acalasia muy satisfactorio con una mínima morbilidad.
Heller myotomy using the laparoscopic approach is the best treatment that we can offer to patients with achalasia. On not acting on the cause of the disease, we can only alleviate the persistence of the symptoms, but not make them disappear.
ObjectiveTo analyse the results of our group in the treatment of achalasia by laparoscopy.
Material and methodsThe pre- and post-operative results are analysed of a series of 20 patients intervened prospectively by laparoscopy of achalasia during a period from May 2003 to April 2010. For this we used a modification of the grading scale of pre- and post-operative symptoms described by Velanovich for GER (a scale from 0-5). Data on the complications and the hospital stay were also collected.
ResultsA wide Heller myotomy was performed using a Dor type antireflux mechanism. There were no oesophageal perforations or complications during the surgery. Two (10%) patients had postoperative complications. The mean hospital stay was 3.11±2.13 days. After a mean follow up of 55.8±14.1 months, the symptoms studied had significantly decreased after the surgery. Only 3 (15%) patients had clinical symptoms of GER after surgery. Nineteen patients (95%) said they were satisfied with the operation.
ConclusionsThe laparoscopic treatment of achalasia is a safe technique, reproducible and effective technique, which achieves very satisfactory control of the achalasia symptoms with a minimum of morbidity.
La acalasia es una alteración de la motilidad esofágica poco frecuente, con una incidencia alrededor de un caso cada 100.000 habitantes/año. Se caracteriza por la desaparición de la peristalsis del cuerpo esofágico y la ausencia de relajación del esfínter esofágico inferior (EEI)1–4.
El síntoma más común es la disfagia y en menor grado la regurgitación y el dolor torácico.
La etiología es desconocida y su tratamiento se basa en intentar paliar la disfagia disminuyendo la presión del esfínter esofágico inferior. Para ello existen diversas opciones como son la dilatación neumática, la toxina botulínica o la cirugía, bien convencional por vía torácica o abdominal. En la última década se ha desarrollado y popularizado el acceso laparoscópico, que ha demostrado la misma efectividad que la referida previamente con la cirugía convencional5,6, añadiéndole las ventajas de ser una técnica mínimamente invasiva, con un porcentaje de complicaciones aceptable y buenos resultados a largo plazo1,2,4,7–11.
Presentamos un estudio prospectivo analizando los resultados de nuestro grupo en el tratamiento de la acalasia por vía laparoscópica.
Material y métodosDesde mayo de 2003 hasta abril de 2010 hemos intervenido prospectivamente por vía laparoscópica 20 pacientes con acalasia
Ocho son varones y doce mujeres. La edad media es de 50,5±5,6 años (rango: 21-73).
Dos pacientes (10%) presentaban patología, enfermedad, etc. gastroesofágica asociada: una paciente presentaba una hernia paraesofágica reparada durante la miotomía, asociando reducción herniaria, cierre de pilares y fundoplicatura anterior. En otro caso se evidenció un divertículo esofágico en 1/3 medio que no se trató.
Cinco pacientes habían sido sometidos a dilataciones previas. Otro paciente se trató con toxina botulínica. En 14 casos la cirugía fue el primer tratamiento.
Técnica quirúrgicaEn todos los casos se ha practicado una miotomía de Heller amplia, 8-10cm por encima del EEI y 2cm en la vertiente gástrica. La dislaceración muscular se realiza con tracción-contratracción y tijeras, sin usar instrumentos eléctricos a fin de evitar la perforación mucosa. Hemos realizado sistemáticamente una fibrogastroscopia intraoperatoria. En todos los casos hemos asociado un mecanismo anti-reflujo tipo Dor.
A los 12 meses de la cirugía se ha realizado a todos los pacientes un TEGD y una fibrogastroscopia.
Para poder valorar los resultados de la cirugía, dado que no existe ninguna escala de valoración en acalasia, adecuamos la descrita para el reflujo gastro-esofágico por Velanovich12, consistente en una escala de gradación progresiva de los síntomas pre y postoperatorios de 0-5 (0: nunca y 5: diversas veces al día) (tabla 1).
Escala de Velanovich para el RGE adaptada para este estudio de acalasia.
| 0 = No síntomas |
| 1 = Síntomas leves esporádicamente |
| 2 = Síntomas molestos pero no diariamente |
| 3 = Síntomas molestos cada día |
| 4 = Los síntomas afectan las actividades diarias |
| 5 = Los síntomas son incapacitantes. Impiden realizar las actividades diarias |
Dicho cuestionario fue contestado preoperatoriamente por todos los pacientes. Entre enero de 2010 y abril de 2010 fueron revisados todos los pacientes para este estudio, realizando nuevamente el cuestionario a fin de comparar los resultados y valorar la eficacia terapéutica de la cirugía practicada.
ResultadosLa cirugía se ha completado por vía laparoscópica en todos los casos sin necesidad de conversión.
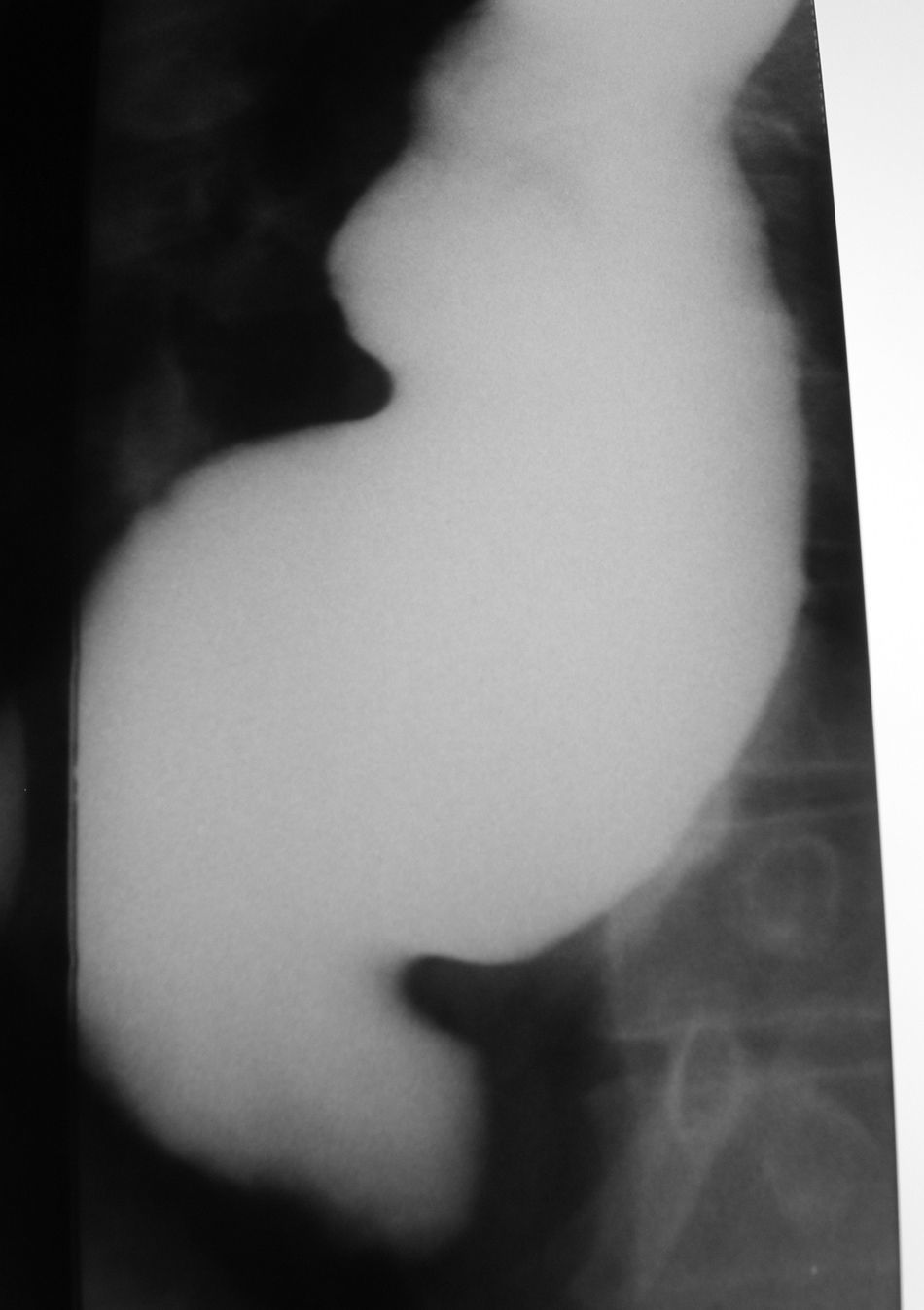
No se han producido perforaciones esofágicas ni complicaciones intraoperatorias. Dos pacientes (10%) han presentado complicaciones postoperatorias. Un paciente con un gran megaesófago (fig. 1) presentó una neumonía postoperatoria presumiblemente por aspiración perianestésica. El otro paciente presentó un hematoma en el lugar de inserción del trocar en epigastrio izdo. que no precisó ningún tratamiento.
La estancia hospitalaria ha sido de 3,11±2,13 días (2-12).
El seguimiento ha sido de 55,8±14,1 meses (4-82). La disfagia se ha controlado en todos los casos, no precisando cirugía de rescate en ningún paciente. Era el síntoma preoperatorio más intenso con 4,15 puntos y, en el seguimiento postoperatorio, su presencia es inferior a otros síntomas con un valor de 0,31 (tabla 2).
La regurgitación y la pirosis presentan un comportamiento muy similar. Preoperatoriamente presentaban valores inferiores a 2 puntos y han disminuido significativamente después de la cirugía por debajo de 1 punto, si bien la pirosis es el síntoma residual más frecuente detectado postoperatoriamente. Únicamente 3 pacientes (15%) han presentado clínica postoperatoria de RGE. En una paciente no se han evidenciado signos endoscópicos de esofagitis y la phmetría ha sido negativa, si bien la clínica se controla con Omeprazol. En los otros 2 casos se ha confirmado la presencia de RGE. Uno de ellos es el paciente con megaesófago y complicaciones respiratorias postoperatorias que presentó una esofagitis erosiva y en otra paciente se objetivó una esofagitis grado I. Ambos casos han mejorado con inhibidores de la bomba de protones.
El dolor torácico también mejora significativamente tras la miotomía de 2,46 puntos a 0,77. A pesar de ser de poca intensidad, llama la atención que 11 de los 20 pacientes lo refieren ocasionalmente en el postoperatorio.
Diecinueve pacientes (95%) refirieron estar satisfechos con el resultado de la intervención.
DiscusiónEl tratamiento de la acalasia no se realiza sobre la causa de la enfermedad sino que únicamente pretende disminuir la presión del esfínter esofágico inferior y favorecer el paso del bolo digestivo a nivel esófago-gástrico. Se trata, únicamente, de aliviar la sintomatología1,9.
¿Cuál es el tratamiento ideal? Se ha escrito mucho sobre ello y, en teoría, sería aquel capaz de disminuir la obstrucción del EII de forma efectiva, duradera y con la menor morbilidad posible1–6. Se ha demostrado que el tratamiento farmacológico con inhibidores del calcio y toxina botulínica es menos efectivo que la dilatación endoscópica, estando indicados únicamente en pacientes pluripatológicos no tributarios de tratamientos más invasivos1,4,13.
La dilatación endoscópica es un procedimiento rápido, que puede realizarse ambulatoriamente, menos doloroso y más barato que la cirugía y fácilmente repetible. En su contra, puede producirse una complicación grave como es la perforación esofágica, descrita entre un 1-10% de casos y, en pacientes jóvenes, es inefectiva en alrededor del 25% de casos13.
¿La cirugía es el tratamiento ideal de la acalasia? Presumiblemente sí, ya que se ha demostrado que la miotomía de Heller proporciona el alivio más favorable y duradero de los síntomas, alrededor del 85-94% a los 10 años, mientras la dilatación endoscópica y la miotomía por toracotomía pierden su eficacia con el paso del tiempo2–6,13.
En cuanto al acceso laparoscópico presenta ventajas sobre el laparotómico en cuanto es menos agresivo, reduciendo el dolor, tiempo de incapacidad y complicaciones postoperatorias, la estancia hospitalaria y, además, ofrece una mejor visión de la sección de las fibras musculares. Por todo ello, la mayoría de autores consideran actualmente la miotomía de Heller por vía laparoscópica el método de elección en el tratamiento de la acalasia1,2,4,7–10,14–16.
Al ser un procedimiento quirúrgico poco prevalente existe gran controversia respecto a detalles técnicos como asociar un mecanismo antirreflujo, el uso de instrumentos eléctricos en la miotomía, la longitud de esta y el uso de endoscopia intraoperatoria. No existe evidencia científica sobre ello pero sí abundante bibliografía.
¿Es necesario añadir un procedimiento antirreflujo? Parece claro que la miotomía puede generar un RGE y que estos pacientes se debaten en la dualidad de presentar acalasia o RGE. Para complicarlo aún más, sabemos que más del 10% de acalasias se acompañan de patología esófago-gástrica concomitante como la hernia hiatal paraesofágica o divertículos esofágicos que plantean dudas de si la clínica es debida a una u otra patología17. Por otro lado, algunos autores creen que puede practicarse una correcta miotomía sin ocasionar RGE y que la fundoplicatura reduce la efectividad de la miotomía, aumentando el tiempo quirúrgico y el riesgo de complicaciones como la disfagia2,3,18. Lyass et al19, en un meta-análisis comparando miotomía con y sin mecanismo antirreflujo, no objetivan diferencias significativas entre ambas en cuanto a incidencia de RGE postoperatorio, que se sitúa alrededor del 10%.
Otra controversia es qué tipo de fundoplicatura realizar. Algunos expertos en acalasia4,6,14,20 son partidarios de realizar una técnica anterior tipo Dor, preservando el mecanismo anatómico antirreflujo posterior y, cubriendo el área de la miotomía lo cual también sería útil en caso de perforación esofágica inadvertida. Otros autores de reconocido prestigio como Millat9, Pellegrini15 y, en nuestro país, el grupo de la Arrixaca5 prefieren una fundoplicatura posterior tipo Toupet, fijada a los bordes de la miotomía, que ayuda a mantenerla abierta. Balaji et al11, en un estudio multicéntrico comparando diferentes fundoplicaturas, objetivaron que la anterior tipo Dor presentaba significativamente menor persistencia de pirosis (24% vs 42%) y disfagia postoperatoria (4 vs 22%) que el Toupet.
Nosotros hemos practicado sistemáticamente una fundoplicatura anterior y sólo en 2 casos (10%) hemos evidenciado RGE en el control endoscópico postoperatorio de nuestros pacientes.
¿Cuál es la longitud adecuada de la miotomía? La distancia de la miotomía proximal es controvertida, entre 5-10cm por encima de la unión esófago-gástrica. Millat9 aconseja adecuarla en función de la sintomatología. Así, cuando el signo preponderante es la disfagia no es necesario superar los 5cm para conseguir una abertura satisfactoria del EEI, mientras cuando el dolor torácico está muy presente en el preoperatorio es partidario de prolongar la miotomía tan alta como sea posible. Más de la mitad de nuestros pacientes refirieron, aunque de forma ocasional, dolor torácico postoperatorio. Probablemente hubiéramos tenido que prolongar cranealmente la miotomía en aquellos pacientes que referían dolor preoperatorio.
Distalmente se recomienda prolongarla 1-3cm por debajo del EEI siendo necesario dividir las fibras musculares oblicuas del estómago, ya que una miotomía incompleta o la fibrosis en la vertiente gástrica son la causa principal de recidiva precoz4,18. A fin de asegurar una correcta miotomía preferimos, al igual que Cowgill et al8, realizar sistemáticamente una endoscopia intraoperatoria que verifique la abertura del EEI y el correcto paso al interior del estómago, visualizando por transiluminación el segmento miotomizado y pudiendo detectar la persistencia de fibras musculares, calibrar la longitud de la miotomía y descartar perforaciones inadvertidas.
Otro elemento de discusión es con qué instrumentos se realiza la miotomía. Nosotros somos partidarios, al igual que Millat9, de dislacerar la musculatura esofágica sin instrumental eléctrico a fin de minimizar el riesgo de perforación. Sin embargo, otros autores prefieren disecar con gancho electrocoagulador y no han referido una mayor morbilidad1,18,19,21.
¿Cómo valorar la efectividad de la miotomía laparoscópica? La acalasia es una enfermedad poco prevalente en la que no existen estudios aleatorizados que clarifiquen la mayoría de las cuestiones aquí expuestas. Además, como refiere Robert et al18, los pacientes asintomáticos son reacios a someterse a controles endoscópicos postoperatorios. Los estudios de calidad de vida específicos para esta patología tampoco son concluyentes22 y la mayoría de series únicamente valoran el control de los síntomas, considerando como éxito de la técnica una remisión de la disfagia superior al 90% y un RGE postoperatorio alrededor del 10% a corto-medio plazo. Sin embargo, tenemos que tener presentes los resultados a largo plazo publicados por grupos expertos en cirugía abierta5,6, que refieren una pérdida de efectividad de la miotomía con el paso del tiempo y cifran el éxito de la cirugía en un 75% a los 15 años de la intervención.
Nuestros resultados en el control de los síntomas son muy similares a los publicados en nuestro país por Trías y Targarona7 y, más recientemente, por Cowgill et al8 que en una amplia serie de 337 pacientes refieren estar satisfechos con el resultado de la intervención un 92% de casos, reportando una disminución postoperatoria significativa de los síntomas, siendo la pirosis el síntoma postoperatorio residual más común, por encima de la disfagia, al igual que presenta nuestro estudio.
La miotomía laparoscópica de Heller es una técnica segura, reproducible y efectiva, que consigue un control de los síntomas de la acalasia muy satisfactorio con una mínima morbilidad. Por ello, consideramos que es el tratamiento de elección en esta enfermedad.
Conflicto de interesesLos autores declaran no tener ningún conflicto de intereses.