Introducción. Los tumores de la ampolla de Vater constituyen el 10% de los cánceres periampulares. Son de crecimiento más lento y tienen mejor pronóstico que los del páncreas, por lo que algunos autores recomiendan ampulectomías en determinados casos. En este trabajo analizamos nuestros resultados en el tratamiento de esta enfermedad, para el que se han utilizado diversas técnicas quirúrgicas.
Pacientes y método. Estudio retrospectivo de datos perioperatorios, morbimortalidad y supervivencia en un grupo de 20 pacientes intervenidos por adenocarcinoma ampular.
Resultados. Fueron intervenidos 14 varones y 6 mujeres, con una edad media de 65 años. El síntoma principal fue la ictericia (75%); la bilirrubina media fue de 7,67 mg%; la prueba diagnóstica más resolutiva fue la colangiopancreatografía retrógrada endoscópica, con un 78,6% de verdaderos positivos. Las intervenciones realizadas fueron: 12 duodenopan createctomías cefálicas, 2 duodenopancreatectomías totales, 3 ampulectomías y 3 derivaciones. La mortalidad fue del 5%. En cuanto a las recidivas se produjeron 1/3 tras ampulectomía a los 10 meses frente a 1/11 tras duodenopancreatectomía cefálica a los 4 años. La supervivencia global fue de 37,11 meses.
Conclusiones. El síntoma más frecuente en estos tumores es la ictericia y la prueba diagnóstica más rentable la colangiopancreatografía retrógrada endoscópica. La técnica de elección sigue siendo la duodenopancreatectomía cefálica.
Introduction. Tumors of the ampolla of Vater constitute 10% of cases of periampullar cancer. Their growth is slow and the prognosis is better than that associated with pancreatic tumors. For this reason, some authors recommend ampullary resection in certain cases. In the present report, we analyze our results in the treatment of these lesions using different surgical techniques.
Patients and methods. We retrospectively reviewed the perioperative data, morbidity and mortality rates and survival in a group of 20 patients who underwent surgery to treat ampullary adenocarcinoma.
Results. The series consisted of 14 men and 6 women with a mean age of 65 years. The most common symptom was jaundice (75%), and the mean bilirubin level was 7.67 mg/dl. The most useful diagnostic test was endoscopic retrograde cholangiopancreatography (ERCP) (78.6% true positives). The following techniques were employed: CPD (n = 12), TPD (n = 2), ampullary resection (n = 3) and diversion (n = 3). The mortality rate was 5%. Recurrences occurred in 1 of 3 patients undergoing ampullary resection (10 months later) versus 1 of 11 patients subjected to CPD (4 years later). The overall survival was 37.11 months.
Conclusions. Jaundice is the most common symptom of these tumors and ERCP the most valuable diagnostic test. CPD continues to be the technique of choice.
Introducción
Los tumores de la ampolla de Vater constituyen el 2% de todos los tumores malignos del tubo digestivo y el 10% de los cánceres periampulares1-3. Su crecimiento es más lento que el del cáncer de la cabeza del páncreas, de forma que hay más casos de tumores resecables en el momento de la intervención y, desde luego, con una mayor supervivencia3. Por esta razón, la UICC los ha clasificado como una entidad aparte4 y, aunque en ocasiones pueda ser difícil diferenciarlos, deben estudiarse siempre de forma independiente. En este trabajo presentamos nuestros resultados en el tratamiento del adenocarcinoma de la ampolla de Vater en los últimos 10 años.
Pacientes y método
Hemos realizado una revisión retrospectiva de las historias clínicas de los pacientes intervenidos por adenocarcinoma ampular en nuestro servicio. El número de historias clínicas fue de 20, correspondientes a pacientes con diagnóstico histológico de adenocarcinoma ampular. Diseñamos un protocolo de recogida de datos en el que se incluyeron datos epidemiológicos, motivo del ingreso y síntomas predominantes, datos de laboratorio, pruebas diagnósticas, estadificación postoperatoria según la clasificación de Martin2,5, intervención realizada, morbimortalidad y supervivencia. Igualmente, se han recogido las posibles complicaciones tardías y reintervenciones, hasta la última revisión en consulta. Todos los registros fueron introducidos en una base de datos y tratados estadísticamente.
Clasificación de Martin
Estadio I: tumores vegetantes papilares o vellosos que no infiltran planos subyacentes.
Estadio II: infiltración de las paredes del esfínter de Oddi, tracto biliar o submucosa duodenal sin llegar al plano muscular.
Estadio III: la infiltración se extiende por la musculatura duodenal.
Estadio IV: existen metástasis linfáticas proximales o distales, invasión periduodenal o del espacio pancreático circundante.
Resultados
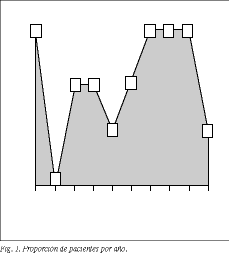
La serie consta de 20 pacientes, 14 varones (70%) con una edad media de 64,9 años (rango 55-76) y 6 mujeres (30%), con edades comprendidas entre 57 y 69 años y una edad media de 62,66 años. La distribución de los pacientes por años de intervención se refleja en la figura 1.
Datos clínicos
Presentaron dolor 11 pacientes (55%), ictericia, 15 (75%), prurito, 8 (40%), pancreatitis, 3 (15%), náuseas y/o vómitos, 4 pacientes (20%) y cuadro de colangitis 2 (10%). La astenia, anorexia y pérdida de peso (síndrome constitucional) apare ció en 8 pacientes (40%). La hiperbilirrubinemia se objetivó en 17 casos (85%).
Diagnóstico de imagen
Se realizaron 16 ecografías con un 56,2% de positividad y 43,8% de falsos negativos; 11 TAC con un 72,7% de diagnósticos correctos y 27,3% de falsos negativos; 14 colangiopancreatografías retrógradas endoscópicas (CPRE) con un 78,6% de verdaderos positivos y 21,4% de falsos negativos y, por último, 2 colangiografías transparietohepáticas (CTPH), ambas con diagnóstico correcto.
Intervención
Fueron intervenidos los 20 pacientes, realizándose 11 duodenopancreatectomías cefálicas (DPC) (55%), una DPC con preservación pilórica (5%), 2 duodenopancreatectomías totales (DPT), en un caso por necrosis pancreática y del colon transverso que hubo que resecar también, y en el otro por pancreatitis aguda con intensa fibrosis, 3 ampulectomías (15%) y 3 derivaciones biliares. Todos los tumores fueron adenocarcinomas, cinco bien diferenciados, siete moderadamente diferenciados y tres pobremente diferenciados. En 5 pacientes no se recoge el grado de diferenciación. Fueron intervenidos 2 pacientes en estadio I (10%), 6 en estadio II (30%), 6 en estadio III (30%) y 3 en estadio IV (15%). Tres pacientes no fueron estadificados (15%). El tipo de intervención en relación a la estadificación postoperatoria se expone en la tabla 1.
Morbimortalidad postoperatoria
Se produjeron 2 fístulas biliares (10%), 3 pancreáticas (15%), una hemorragia, 4 cuadros de peritonitis (20%), una neumonía, un accidente cerebrovascular, un absceso de pared y un cuadro de insuficiencia renal aguda. Precisaron reintervención los 4 pacientes que presentaron un cuadro de peritonitis, uno por peritonitis biliar tras retirada de tubo de Kehr después de una ampulectomía, un paciente con fístula pancreática y hemorragia tras DPC al que se completó la pancreatectomía, un paciente por necrosis de colon derecho tras DPT y colectomía transversa que falleció tras la reintervención y, por último, un paciente con dehiscencia parcial de la anastomosis pancreaticoyeyunal al que se completó la pancreatectomía. La mortalidad postoperatoria fue, por tanto, de un paciente (5%).
Complicaciones tardías
Un paciente presentó estenosis duodenal a los 4 meses de una derivación biliar al que se realizó derivación digestiva, 2 pacientes desarrollaron diabetes, un paciente presentó un absceso hepático al año de una DPC que se drenó por punción bajo control de TAC y un paciente sufrió ictericia al año de una ampulectomía que precisó colocación de endoprótesis biliar.
Recidivas y/o metástasis tardías
Se produjeron una recidiva a los 4 años de DPC, otra a los 10 meses de ampulectomía (paciente al que se colocó una endoprótesis) y metástasis hepáticas en 2 pacientes sometidos a DPT y DPC al año y a los 2 años, respectivamente.
Supervivencia
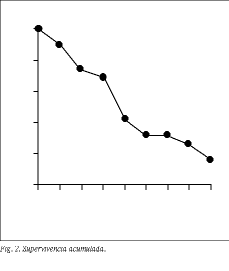
La supervivencia global de los pacientes fue de 37,11 meses (rango 6-74) siendo de 39,5 meses tras duodenopancreatectomía, de 34,33 meses tras ampulectomía y de 18 meses tras derivación. Las diferencias no fueron significativas (p = 0,31, test de rangos logarítmicos). En la actualidad se encuentran vivos 10 pacientes (50%), 6 han fallecido (uno de ellos en el postoperatorio) y 4 no acudieron a la última revisión, por lo que se consideraron perdidos para el seguimiento. La curva de supervivencia global se representa en la figura 2.
En la tabla 2 se recogen los datos de supervivencia según el estadio y el grado de diferenciación.
Discusión
Los carcinomas de la ampolla de Vater constituyen el 2% de todos los tumores malignos del tubo digestivo y el 10% de los cánceres periampulares1-3. Generalmente se trata de adenocarcinomas, siendo excepcionales otros tipos histológicos6. Predominan en el sexo masculino y aparecen hacia la sexta década de la vida (en nuestra serie, un 70% de los pacientes tenía una edad media de 64,2 años), aunque hay autores que encuentran una incidencia similar para ambos sexos2,3. Suelen ser tumores de crecimiento lento y, dado que se desarrollan en torno a la porción final del colédoco, generalmente la manifestación inicial es la ictericia, que puede ser progresiva o recurrente e ir asociada a dolor abdominal y fiebre. Nosotros encontramos ictericia en el 75% de los casos, con un cuadro completo de colangitis en sólo 2 pacientes (10%), datos similares a los descritos en la bibliografía2,7-9. El cuadro clínico de pancreatitis como inicio de la enfermedad se observó en un 15% de los pacientes, siendo destacable un caso con necrosis pancreática y de colon transverso de evolución fatal. No se apreció ningún caso de hemorragia digestiva alta e ictericia asociada con el ampuloma.
La ecografía o la TAC suelen ser las primeras exploraciones que se realizan en pacientes con clínica de dolor abdominal e ictericia y pueden informar de la existencia de dilatación de vías biliares, presencia de cálculos, pancreatitis o tumores pancreáticos y presencia de metástasis, pero la prueba diagnóstica con mayor rentabilidad es la CPRE, que permite la visualización directa de la papila y la toma de biopsia con un alto rendimiento8,10,11, que en nuestra serie fue del 78,6%; sin embargo, una biopsia con resultado de adenoma no siempre excluye la presencia de un adenocarcinoma, e incluso algunos autores lo consideran como una lesión premaligna, por lo que incluso las lesiones benignas deben ser resecadas6,12-14. Cuando no se puede sobrepasar la papila y tomar biopsias, la CTPH ofrece una completa visualización de la vía biliar que permite establecer el diagnóstico con un alto grado de sospecha8,15. Nosotros utilizamos esta prueba en 2 pacientes y en ambos el diagnóstico fue acertado. En la actualidad, la ecoendoscopia está adquiriendo un importante papel no sólo en el diagnóstico y estadificación preoperatoria de los tumores ampulares, sino también de los periampulares y pancreáticos16,17.
Uno de los temas más controvertidos de esta enfermedad es el tipo de intervención que debe realizarse. Hasta ahora, la técnica de elección es la DPC con o sin preservación pilórica, dado que se reseca todo el tumor con un menor índice de recidivas locales y se realiza disección ganglionar, lo que permite la correcta estadificación y tratamiento postoperatorio coadyuvante2,8,18-21. Sin embargo, hay autores que defienden el empleo de técnicas resectivas locales, como la ampulectomía e incluso la ablación tumoral transendoscópica en tumores de pequeño tamaño sin infiltración pancreática, en pacientes con alto riesgo para una cirugía más agresiva e incluso como tratamiento paliativo en algunos casos11,12,22-25. La mortalidad posterior a la ampulectomía es del 0-25%10, y tras DPC del 0-20%1-3,7,8,20,25. En nuestra serie no se ha producido ningún fallecimiento tras ampulectomía ni después de DPC; en este sentido, parece recomendable una resección más radical. Por otra parte, el seguimiento endoscópico posterior a la ampulectomía es obligado en estos pacientes, aun cuando estén libres de síntomas y con analíticas normales, a intervalos de 3-6 meses durante los primeros 2 años y después una al año10. La recurrencia, más frecuente que tras DPC, suele ocurrir en los 3 primeros años10,11,18, lo que podemos corroborar con nuestros propios resultados: una recidiva a los 10 meses de ampulectomía en un paciente en estadio II con adenocarcinoma moderadamente diferenciado, que supone un 30% de recidivas, frente al 7% que hemos observado tras resecciones duodenopancreáticas (un paciente también en estadio II al que se le realizó DPC en el que la recidiva ocurrió a los 53 meses). La supervivencia a los 5 años con ampulectomía es del 7-55%10, 23-26, frente al 35-39% después de DPC3,20,21. Kayahara et al21 aconsejan la DPC con disección ganglionar incluso en tumores ampulares pequeños por no existir relación entre el tamaño tumoral y la afectación ganglionar; sin embargo, la supervivencia a los 5 años en los grupos con o sin afectación ganglionar no ofrece diferencias significativas, al contrario de lo que ocurre en los cánceres de cabeza de páncreas; entonces, ¿para qué realizar la resección radical? A pesar de estas consideraciones, aún no hay series amplias en las que se comparen las dos técnicas para grupos similares. En algunas series en las que se recogen datos de ambas técnicas encontramos sesgos importantes, como la realización de ampulectomía en pacientes con alto riesgo para cirugía más agresiva, pacientes que no aceptaron DPC o casos en los que no se sospechó la presencia de adenocarcinoma, que se determinó en el estudio histopatológico posterior11,24,25. En nuestra serie no hay diferencias significativas de supervivencia media entre la ampulectomía (34,33 meses) y duodenopancreatectomía (39,5 meses) y no tenemos seguimiento a 5 años en los casos de ampulectomía aunque, como hemos comentado anteriormente, la recidiva es más frecuente y precoz después de ésta. Este trabajo no es significativo ni se pueden extraer conclusiones sobre la técnica de elección, pero creemos que, según los datos de la bibliografía consultada, la técnica de elección sigue siendo la DPC, aunque hay un lugar para la ampulectomía sobre todo en pacientes con un deterioro importante de su estado, que presenten un alto riesgo o con tumores menores de 2 cm, si bien es obligado asegurarse de que el margen de resección está libre de tumor. Sin embargo, no creemos que sea una buena técnica paliativa en lugar de la derivación o la endoprótesis, ya que presenta mayor morbilidad.