La terapia con presión negativa (VAC, vacuum assisted closure) es una modalidad poco utilizada aún en nuestro país. Consiste en un sistema de aspiración sobre la herida por medio de una esponja y unos adhesivos plásticos. Permite el tratamiento de heridas complejas incluidas aquellas con fístulas intestinales, aunque este punto es controvertido. Presentamos 3 casos de tratamiento con VAC en esta situación y un resumen de los estudios publicados.
Pacientes y métodoDesde la introducción de la terapia VAC en nuestro centro, hemos tratado a 10 pacientes, 3 de ellos presentaban una fístula en el lecho de la herida quirúrgica. Describimos los datos clínicos de los pacientes y el tratamiento que se siguió en cada uno de los casos.
ResultadosEn los 3 casos se consiguió una significativa mejoría clínica local de la enfermedad, con control de los síntomas. En uno de los pacientes pudimos realizar una nueva cirugía para cierre de la fístula con buena evolución de la herida. En los otros 2 casos se consiguió una mejor calidad de vida, aunque ambos fallecieron por la complejidad de la situación general.
ConclusionesEl tratamiento con VAC, aunque controvertido en las fístulas intestinales, puede ayudar a mejorar la situación local de las heridas, el confort de los enfermos y su situación general.
Negative pressure therapy (VAC, vacuum assisted closure) is a method used still in our country. It consists of a system of aspirating a wound by means of a piece of foam and a few adhesive films. It allows the treatment of complex wounds, included (although this is still controversial) those with intestinal fistulas. We present 3 cases of treatment with VAC in this situation and a review of the published literature.
Patients and methodWe have treated 10 patients, since VAC therapy was introduced into our centre of which 3 of whom had a fistula in the bed of the surgical wound. We describe the clinical information of the patients and the therapy that followed in each of the cases.
ResultsSignificant local clinical improvement of the disease, with control of the symptoms, was achieved in all 3 cases. We were able to re-operate to close the fistula in one of the patients, with subsequent good progression of the wound. In the other two cases it gave them a better quality of life although both died due to the overall complexity of their situation.
ConclusionsVAC therapy, although controversial in the treatment of intestinal fistulas, can help to improve the local situation of the wounds, the comfort of the patients and their general situation.
La terapia con presión negativa (VAC, vacuum assisted closure) se está convirtiendo en un instrumento cada vez más importante para tratar heridas complejas, incluidas heridas infectadas, heridas traumáticas, úlceras por presión, heridas con hueso expuesto, úlceras en pie diabético y por ectasia venosa en extremidades, además de utilizarse para facilitar la viabilidad de los injertos cutáneos. Consiste en aplicar una succión, que puede ser continua o intermitente, sobre una herida en la que se coloca una esponja ajustada a la cavidad y un film plástico adhesivo sobre ella.
El tratamiento de las fístulas enterocutáneas depende de su débito diario, que viene dado por el segmento intestinal afectado, el tamaño de la solución de continuidad, de si hay o no sepsis intraabdominal y de si hay o no obstrucción distal. En general, suele ser conservador, con nutrición parenteral, análogos de la somatostatina para disminuir la secreción, y requiere, con frecuencia, numerosos cambios diarios de apósitos, sobre todo, si es una fístula alta con débito importante (> 500ml/día).
Se han publicado varios trabajos en los que se utiliza este tratamiento aspirativo para las fístulas entéricas, con buenos resultados, según sus autores; aunque este punto resulta controvertido dado que han aparecido varias publicaciones que llaman a la cautela con el uso de este tratamiento en este tipo de pacientes.
Presentamos 3 casos en los que se utilizó presión negativa para el tratamiento de heridas laparotómicas abiertas con fístulas entéricas y revisamos la literatura.
Pacientes y métodoDesde el inicio de la terapia VAC en nuestro centro, en 2005, se ha tratado a 10 pacientes, 3 de ellos con heridas complejas que incluyen fístulas entéricas en el lecho. Presentamos los casos a continuación.
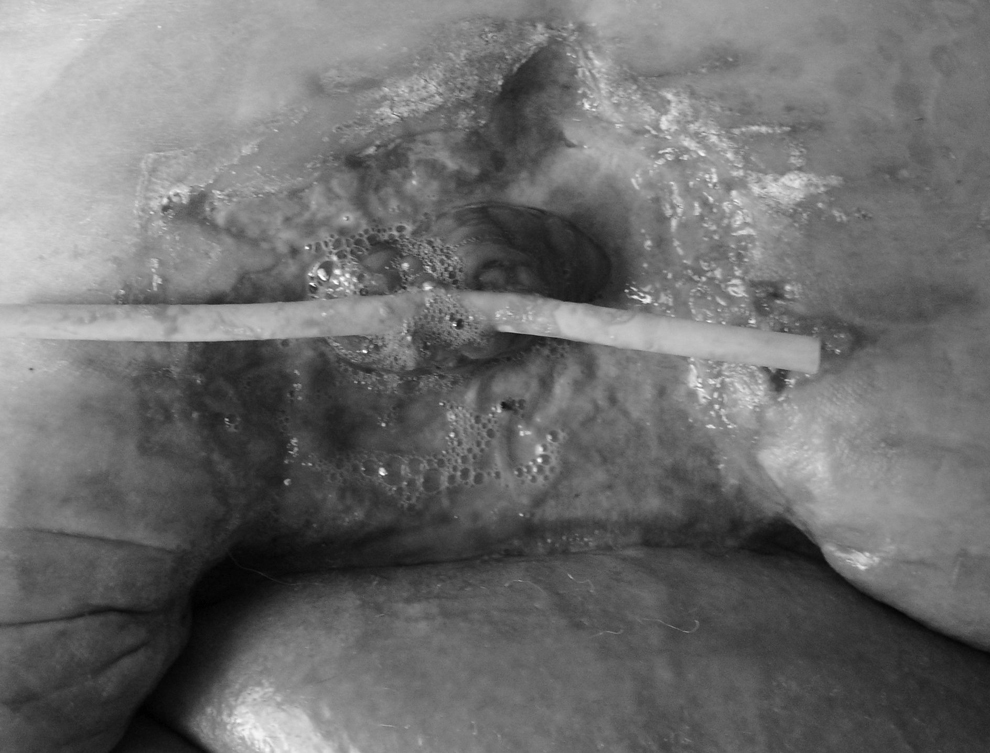
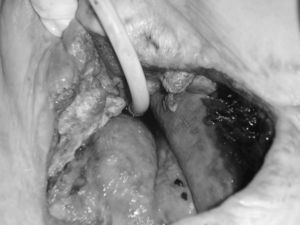
Caso 1Mujer de 67 años con nefropatía crónica por analgésicos, en hemodiálisis, con cardiopatía isquémica y obesidad, intervenida en varias ocasiones por eventración con colocación de malla supraaponeurótica 2 años antes. Acude por herida abierta e infectada por Pseudomonas con exposición de la malla. Se la interviene para extracción de la malla y cierre de la herida. En el postoperatorio inmediato presenta infección de la herida quirúrgica y se evidencia una fístula enteral de alto débito. Tras el mal control de la herida, con curas habituales durante unos 10 días con compresas y cremas protectoras, decidimos aplicar terapia VAC; se deriva el contenido fistuloso mediante sonda de Foley y se aplica esponja blanca alrededor de la sonda de Foley y el resto de la herida, con esponja negra. Este sistema hizo que la herida mejorara lo suficiente para que 1 mes después de la primera intervención pudiésemos reintervenir para resecar el segmento intestinal afectado. Se dejó la piel abierta, para aplicar nuevamente la terapia VAC hasta el alta de la enferma, ya con cultivos negativos para Pseudomonas. La figura 1 muestra la situación de la cura previa a la instauración de VAC.
Figura 1. Situación de la herida antes de iniciar la terapia VAC (vacuum assisted closure), con una sonda Foley se trata de recoger el débito en el fondo de la herida. La piel se protege con pasta de aluminio.
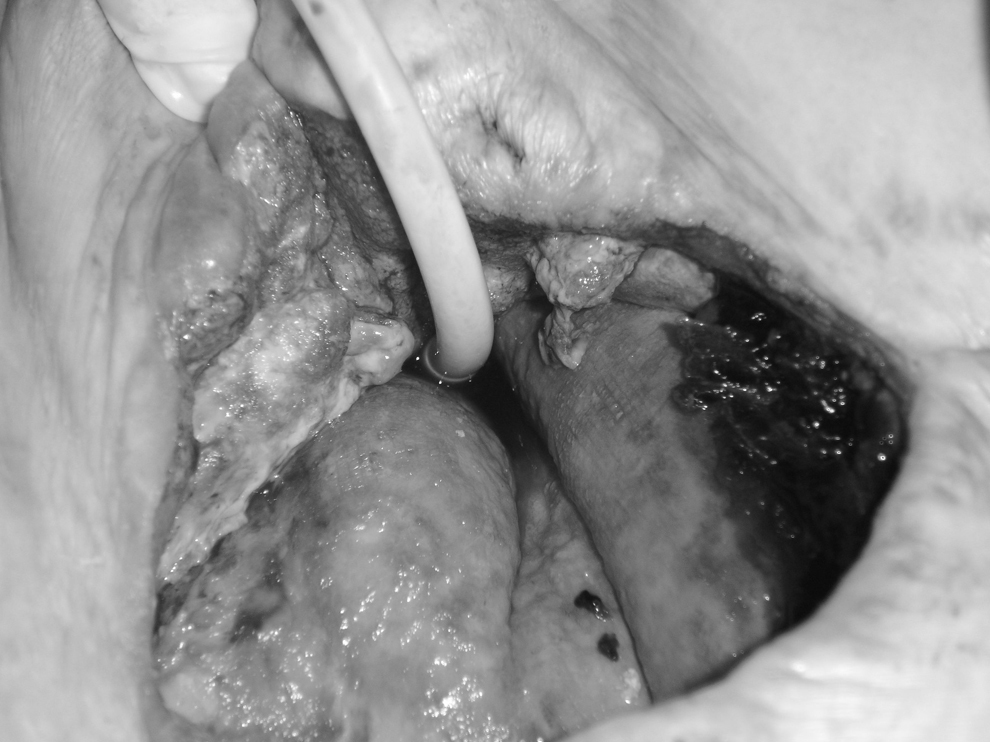
Caso 2Mujer de 75 años con hipertensión arterial, obesidad mórbida y con largo historial de intervenciones quirúrgicas abdominales. Apendicectomía, colecistectomía, cesárea, varias hernias laparotómicas intervenidas, la última de ellas, 12 años antes, con colocación de una malla. Acudió a urgencias por fístula intestinal de bajo débito que no se controló con tratamiento conservador. Se realizó resección intestinal segmentaria y se comprobó el origen de la fístula en un decúbito del intestino sobre la malla. Dehiscencia de sutura en el postoperatorio inmediato y reitervención con resección segmentaria del intestino delgado. Tras esta segunda intervención, nuevamente se produce una dehiscencia de la sutura, apertura de la piel y fístula de alto débito que producía quemazón importante sobre la piel, con continuos cambios de apósitos por parte de enfermería, y un deterioro muy importante de la enferma (figura 2). Tras 1 semana de curas, se decide comenzar terapia VAC, con esponja negra y protección del lecho de la herida con gasas vaselinadas, con intención de mejorar la calidad de vida de la paciente ya que los estudios que se realizan no permiten una nueva reintervención al detectar un intestino ultracorto tras las repetidas cirugías. El resultado es la desaparición de la clínica de quemazón e importante incomodidad de la enferma. Puesto que las curas ahora se realizaban cada 48h, la piel mejoró de forma espectacular en pocos días, el trabajo de enfermería se vio considerablemente aliviado, y la situación de la enferma se estabilizó hasta su fallecimiento por infección respiratoria aproximadamente unos 2 meses después de la última intervención.
Figura 2. Herida expuesta con fístula en su lecho. Con el drenaje de Penrose se trata de derivar la boca proximal y distal de la fístula.
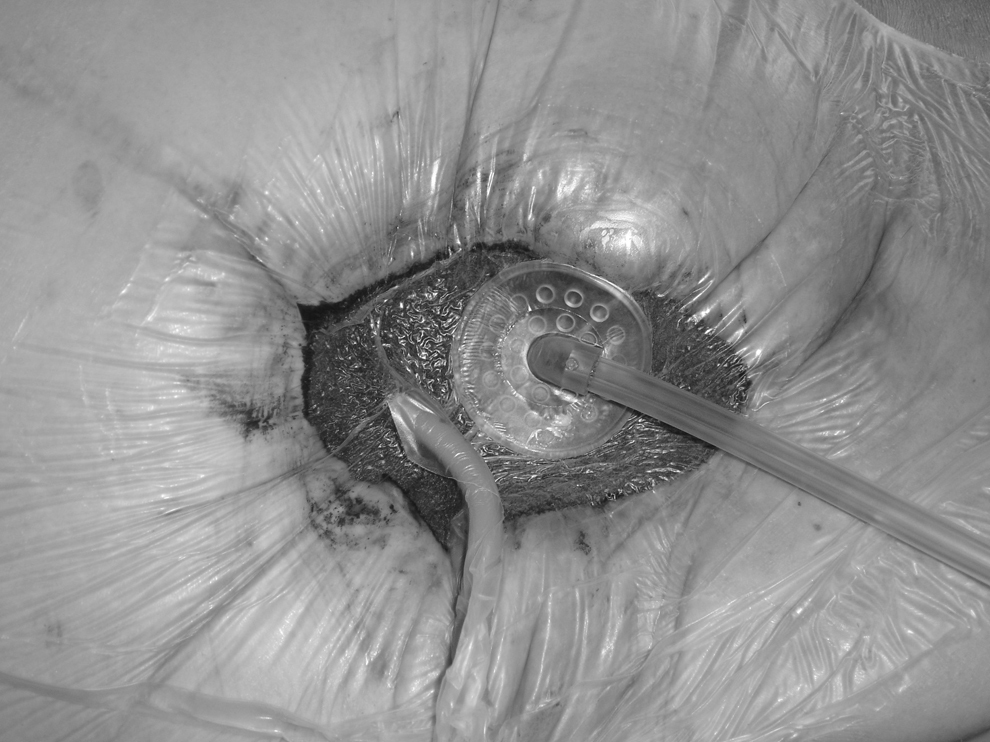
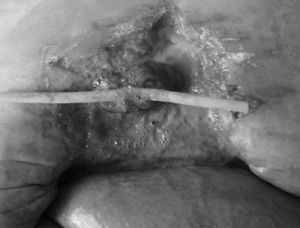
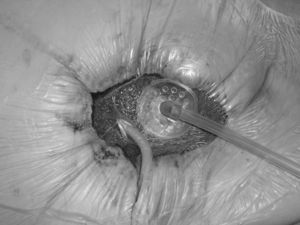
Caso 3Mujer de 69 años de edad, con trasplante hepático por cirrosis secundaria a virus de la hepatitis C, intervenida posteriormente por obstrucción intestinal, se le había realizado ileostomía. Acude por dehiscencia de la sutura, tras la intervención para restaurar el tránsito intestinal, con herida abierta y asas intestinales en el fondo y un orificio fistuloso con alto débito (figura 3). Encontramos una situación de mal control de la herida con cambios continuos de apósitos durante 2 semanas, la piel alrededor de la herida está en muy malas condiciones y la paciente necesita elevadas dosis de analgésicos por quemazón en la herida. Aplicamos terapia VAC con derivación mediante sonda de Foley de la fístula, con esponja negra y protección de las asas del lecho de la herida con gasas vaselinadas y un film plástico (figura 4). El resultado fue una mejora significativa de la situación local de la herida, con lo que requirió menor dosis de analgesia y curas cada 48h, con el beneficio añadido para el personal de enfermería. Posteriormente, la enferma tuvo fallo cardíaco con edema pulmonar y falleció unas 5 semanas después.
Figura 3. Asas intestinales expuestas en el lecho de la herida. La sonda de Foley tutoriza la fístula situada en el fondo de la herida.
Figura 4. Terapia VAC (vacuum assisted closure) aplicada sobre la herida comentada. El sistema de aspiración se colocó protegiendo las asas del fondo y recoge el exudado normal de una herida, a la vez que mantiene fija la sonda de Foley por la que se recoge el débito de la fístula.
DiscusiónEste tipo de terapia se desarrolló a finales de los años ochenta simultáneamente en Estados Unidos y Alemania. Consiste en una aspiración continua o discontinua (habitualmente, entre 75 y 125mmHg) sobre una esponja situada sobre la herida aguda o crónica y mantener el vacío al cubrir todo (herida y esponja) con un adhesivo plástico1,2.
Mantener una presión negativa continua en una herida hace que disminuya el edema perilesional, mejora la vascularización de la herida y moviliza el exceso de secreción, lo que permite una mayor creación de tejido de granulación, facilita la movilización de las bacterias de la herida y aísla la herida de la infección por otro gérmenes3. Al ser un sistema cerrado, mantiene la higiene y evita el mal olor de las heridas infectadas o con fístulas; además, evita el continuo drenaje de exudado a compresas o que se manche la ropa del paciente o la cama.
Es de fácil manejo y disminuye el número de curas a realizar por el equipo de enfermería, se puede pasar, como en los casos presentados, de 7 u 8 curas diarias a curas cada 48 o 72h, con lo que supone un ahorro de tiempo para este personal y comodidad para el paciente. Posibilita la movilización del enfermo, la deambulación (gracias a que el equipo dispone de baterías) e incluso el alta con el equipo ambulatorio. De nuestros casos, sólo la primera paciente se benefició de ello ya que, aunque no deambulaba, sí tenía que asistir en cama a las sesiones de diálisis a días alternos.
Todo ello conlleva la percepción de bienestar del enfermo y la autonomía en su aseo, y puede acortar la estancia hospitalaria.
En un estudio realizado por Joseph et al4, donde comparan este sistema con las clásicas curas con compresas húmedas, se concluye que con el sistema VAC las heridas cicatrizan más rápido y se incrementa el tejido de granulación sano, con lo que se consigue, en grandes heridas crónicas, un 80¿90% de cierre en 3 a 6 semanas. Sin embargo, un metaanálisis publicado recientemente revela que, aunque parece haber una mejoría en la cicatrización de las heridas con esta terapia, no hay evidencia científica al respecto5.
Aunque el coste del equipo y los fungibles (equipo con esponja, adhesivos y catéter de aspirado, por un lado, y colector de secreciones, por otro) es claramente más elevado que unas compresas con suero, parece, según la literatura, en función del número de curas requerido y, fundamentalmente, por la disminución de la estancia hospitalaria que, de manera general, la terapia VAC puede ser coste-efectiva6.
Hay una serie de contraindicaciones para esta terapia, como las fístulas inexploradas o no entéricas, las heridas con tejido necrótico o escaras, células tumorales o en pacientes con osteomielitis no tratada, y una serie de precauciones, como no aplicar el tratamiento sobre tejido con sangrado activo, con terapia anticoagulante, en contacto con vasos sanguíneos expuestos u órganos, y con especial cuidado en vasos u órganos radiados previamente o con suturas.
Rao et al7 y, luego, Fisher8 hacen una llamada de atención sobre el uso de esta terapia en abdomen abierto, en el sentido de considerar que tiene un riesgo elevado de causar fístulas y aumentar la mortalidad. De la serie comentada por Rao et al, de 29 pacientes, 6 desarrollan una fístula y 4 fallecen. Habría que conocer cuántos hubieran fallecido o incluso cuántos hubiesen desarrollado alguna fístula con las curas habituales, dado que eran enfermos graves (el 65,5% requerían cuidados intensivos). Los autores estamos de acuerdo con Rao et al en que hay que ser muy cautelosos en el uso de esta terapia en abdomen abierto o laparostomía, si bien nuestros pacientes ya tenían las fístulas cuando aplicamos el sistema VAC y en ningún caso lo utilizamos para cerrar la fístula.
Podemos pensar que una fístula abierta a la que se aplica una succión continua no hará sino perpetuarse; sin embargo, varias publicaciones1 recogen fístulas tratadas con este sistema con resultados positivos. De 7 publicaciones recogidas, encontramos en total 26 casos tratados; la mayor serie fue la publicada por Nienhuijs et al9 con 10 casos, la media de duración del tratamiento fue 25 días, en 4 casos la fístula cerró, y en otros 5 hubo que intervenirlos para cerrar las fístulas. Todas las publicaciones comunican buenos resultados, bien como cierre completo de la fístula, disminución del débito o bien por la posibilidad de aislar el débito de la fístula de la herida, con lo que la herida mejora en cuanto a excoriación y olor, se puede recoger el contenido completo de la fístula, lo que permite una medición efectiva del débito.
Aunque esta terapia es relativamente novedosa, se usa de forma amplia en ciertos países (Estados Unidos, Alemania) y, de forma progresiva, también en nuestro país; se siguen investigando posibles aplicaciones de la técnica6 y problemas que pudieran ocasionar. Los resultados obtenidos hasta el momento y la literatura publicada nos llevan a tener presente esta terapia, con gran confianza en su utilidad y, en el caso concreto de las fístulas, por la mejora en confort que supone para el paciente.