La dehiscencia de la anastomosis colorrectal es una de las complicaciones más temidas después de una cirugía por cáncer de recto1. Ante esta complicación, debe individualizarse aquella estrategia que nos permita controlar el foco séptico e intentar preservar la continuidad intestinal2,3. El abordaje combinado transanal y transabdominal es un tratamiento emergente para la dehiscencia anastomótica3,4. Los objetivos de asociar una revisión transanal durante la reintervención quirúrgica son valorar el estado de los tejidos, la amplitud del defecto y poder realizar un tratamiento local5. La tendencia actual es intentar reparar el defecto, realizándose en la primera reintervención o en un segundo tiempo tras aplicar terapia de vacío y haber conseguido un mejor control del foco séptico. Esta estrategia tiene el objetivo de reducir la morbimortalidad de esta complicación, preservar y reconstruir las anastomosis viables, reducir la incidencia de sinus anastomótico crónico e identificar con claridad aquellas que deben ser desmontadas.
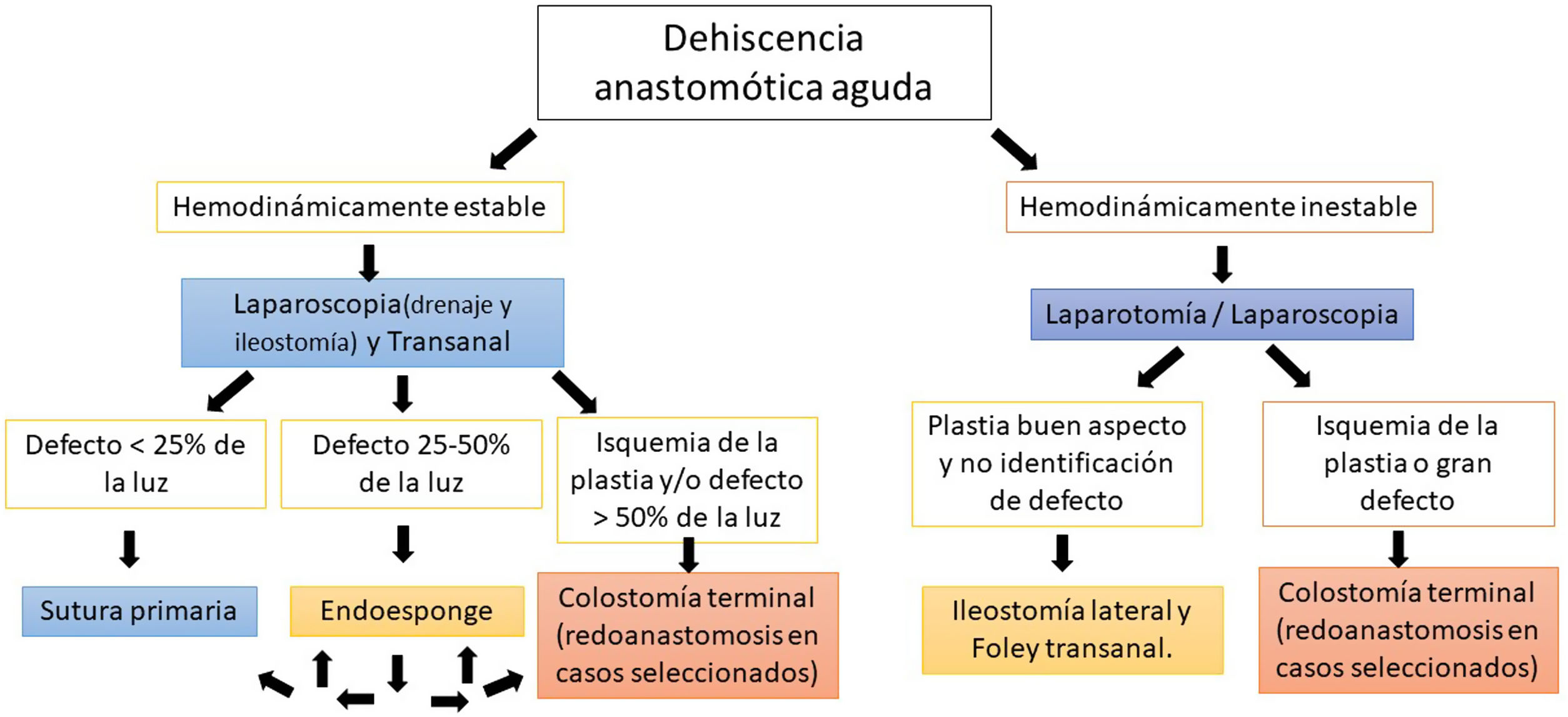
Queremos compartir nuestro algoritmo actual ante una reintervención por dehiscencia anastomótica aguda extraperitoneal (fig. 1).
En nuestro algoritmo, la sutura o cierre del defecto anastomótico podrá efectuarse cuando la dehiscencia sea pequeña (<25%), los tejidos tengan buen estado, el drenaje perianastomótico esté asegurado desde el campo abdominal y se acompañe de una ileostomía lateral con lavado del colon remanente. El sistema de drenaje de vacío (Endo-Sponge, Braun Medical®) se reserva para casos con defectos intermedios y sin isquemia. Se intentará el cierre del defecto después de 2-3 recambios. En caso de defectos mayores o de fracaso de la terapia de vacío se plantean la redoanastomosis o la colostomía terminal6.
En situación de inestabilidad hemodinámica/shock séptico debe primar el drenar el foco séptico y realizar una ostomía (si no tenía). Si no hay isquemia evidente, es mejor una ileostomía lateral a la colostomía7. Posteriormente y según su evolución clínica, se puede plantear una nueva revisión quirúrgica transanal en un segundo tiempo por si la dehiscencia es tributaria de reparar el defecto, aplicar terapia de vacío para mejorar el drenaje o desmontar la anastomosis.
Estos esquemas de tratamiento deben acompañarse de estrategias de rehabilitación multimodal (para que el paciente esté en las mejores condiciones físicas, nutricionales y psicológicas ante un evento adverso)8 y de programas proactivos para la detección precoz de las dehiscencias9.
Nuestra experiencia con la aplicación de algoritmo ha sido progresiva desde el año 2017. Entre enero de 2017 y mayo de 2022 hemos reintervenido 21 pacientes por dehiscencia anastomótica aguda extraperitoneal con una tasa de dehiscencia postoperatoria a 90 días del 7,6%. En 15 ocasiones se ha seguido el protocolo de forma óptima (71%).
De los pacientes que han seguido el protocolo, se han tratado 14 pacientes asociando la cirugía laparoscópica abdominal y revisión transanal. En un caso, debido a la inestabilidad del paciente, se efectuó un abordaje exclusivamente abdominal asociando una ileostomía lateral.
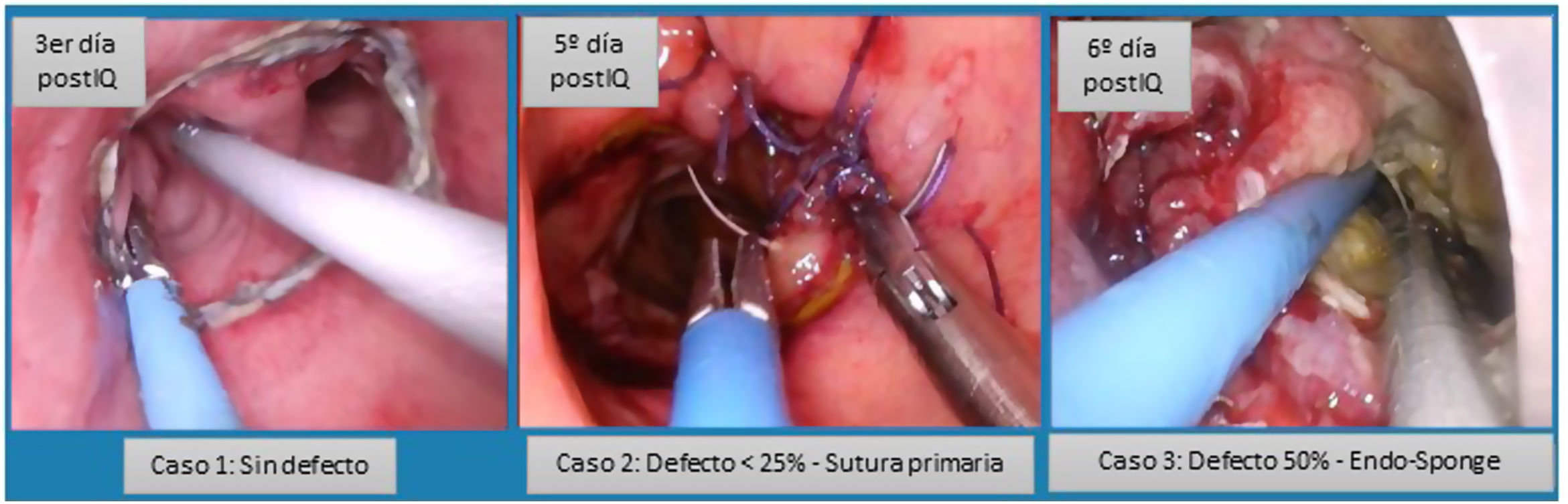
En el 86% el abordaje transanal fue mediante TAMIS y en el 14% (2 casos) con acceso directo transanal, al ser anastomosis ultrabajas. En 12 de los 14 pacientes se pudo realizar una estrategia preservadora de la anastomosis. En 8 se cerró el defecto, en 3 no se identificó ningún defecto anastomótico durante la revisión TAMIS y en uno la evolución fue favorable con terapia de vacío, pero no se pudo cerrar el defecto. En todos los casos se preservó la anastomosis y posteriormente se cerró la ileostomía. En 2 ocasiones los hallazgos transanales indicaron la no viabilidad de la anastomosis con dehiscencia mayor del 50% por isquemia de la plastia. En el primer caso se desmontó la anastomosis y se hizo una colostomía terminal. En el segundo caso se desmontó la anastomosis colorrectal latero-terminal y se realizó una nueva a anastomosis coloanal manual. Este enfermo desarrolló isquemia de la plastia y hubo de ser reintervenido con realización de colostomía terminal y tuvo buena evolución posterior (fig. 2).
De los 6 casos en quienes no se aplicó el protocolo: en 4 ocasiones se trataron por acceso abdominal (2 laparoscopia con conversión, 1 laparoscopia y 1 laparotomía) con 2 ileostomías laterales y 2 colostomías terminales. Los otros 2 casos fueron pacientes con anastomosis coloanales manuales ultrabajas con ileostomía de protección previa y dehiscencias con poca repercusión clínica. Estos pacientes se trataron solamente con drenaje transanal. Estos casos quedan fuera del algoritmo.
En nuestra serie de casos de dehiscencia anastomótica no hemos tenido mortalidad.
El tratamiento ante una dehiscencia debe individualizarse en función del estado clínico del paciente, comorbilidades, nivel de la anastomosis, la presencia o no de estoma derivativo y el tiempo transcurrido entre la cirugía inicial y el diagnóstico de la dehiscencia2,3. El fin de disponer de un algoritmo para el tratamiento de la dehiscencia de la anastomosis es poder sistematizar la actuación ante una de las complicaciones más temidas de la cirugía colorrectal.
El objetivo de compartir el algoritmo es mostrar nuestra evolución en el manejo de la dehiscencia anastomótica, así como la instauración de la revisión transanal sistemática en la dehiscencia extraperitoneal y el uso selectivo de la terapia de vacío. La prioridad ante la dehiscencia es drenar el foco séptico y derivar las heces (si es posible con una ileostomía lateral). Pero actualmente hemos evolucionado en intentar reparar la anastomosis para evitar el sinus crónico10 y así poder aumentar la tasa de cierre de ostomías e identificar con claridad aquellas que deben ser desmontadas. El tiempo nos dirá si además esto mejora la funcionalidad y la calidad de vida de nuestros pacientes.
FinanciaciónNo hay financiación externa para este proyecto.
Conflicto de interesesNo hay conflictos de interés.