El estudio MEMOGAL (NCT04319081) está dirigido a evaluar cambios en la función cognitiva en pacientes tratados con inhibidores de la PCSK9 (iPCSK9). Se realiza primer análisis: 1) discutir el papel de los farmacéuticos hospitalarios durante de la pandemia, así como evaluar el impacto de la misma en el control lipídico; 2) análisis descriptivo; 3) eficacia en reducción de colesterol-LDL (c-LDL) de alirocumab y evolocumab; y 4) reportar seguridad de los iPCSK9.
Material y métodosSe trata de un análisis prospectivo en vida real de pacientes tratados por primera vez con iPCSK9 en la práctica clínica habitual e incluidos en su primera dispensación en las consultas de farmacia de 12 hospitales de Galicia desde mayo de 2020-abril de 2021. Los valores basales de c-LDL son los previos al inicio del tratamiento con iPCSK9 y como seguimiento los valores a los 6 meses.
ResultadosSe incluyeron 89 pacientes. El 86,5% con enfermedad cardiovascular y un 53,9% intolerancia a las estatinas. Un 78,8% de los pacientes fueron tratados con estatinas de alta intensidad. Las estatinas más usadas fueron rosuvastatina (34,1%) y atorvastatina (20,5%). El nivel basal de c-LDL fue 148mg/dl y de 71mg/dl al seguimiento. Los pacientes tratados con alirocumab (n=43) presentaban valores basales de 144mg/dl y de 73mg/dl al seguimiento y con evolocumab (n=46) de 151mg/dl basal y 69mg/dl al seguimiento. La reducción de c-LDL fue para evolocumab 51,21% y alirocumab 51,05%. El 43,1% presentaba a los 6 meses valores>70mg/dl, el 19,4% entre 55 y 69mg/dl y el 37,5%<55mg/dl. Los pacientes que obtuvieron una reducción>50% de c-LDL fueron el 58,3%. Los eventos adversos presentados fueron: reacción en el lugar de inyección (n=2), mialgias (n=1), síntomas pseudogripales (n=1) y deterioro neurocognitivo (n=1).
Conclusiones1) A pesar de haber disminuido el número de prescripciones de iPCSK9 durante la pandemia, el control lipídico de estos pacientes no se ha visto afectado; 2) la mitad de los pacientes tratados con iPSCK9 se debe a intolerancia a estatinas y el 86% es en prevención secundaria; 3) se presentaron valores de reducción similares a los ensayos clínicos pivotales. A pesar de esto, un 39% del total y un 60% en doble terapia no alcanzaron las recomendaciones de las guías ESC/EAS (<55mg/dl y/o reducción>50%). No hubo diferencias significativas entre evolocumab y alirocumab: 51,21% vs. 51,05% (p=0,972); y 4) no se observaron eventos de especial interés con el uso de estos fármacos. El posible deterioro cognitivo será analizado como variable principal una vez completado el estudio MEMOGAL.
MEMOGAL study (NCT04319081) is aimed at evaluating changes in cognitive function in patients treated with PCSK9 inhibitors (PCSK9i). This is the first analysis: (1) discussion about the role of the Hospital Pharmacists during the pandemic, and also the assessment of the impact of COVID-19 in the lipid control; (2) descriptive analysis; (3) effectiveness in LDL cholesterol (LDL-c) reduction of alirocumab and evolocumab; (4) communicate PCSK9i safety.
Material and methodsIt is a prospective Real-World Evidence analysis of patients that take PCSK9i for the first time in the usual clinical practice, and they are included after the first dispensation in the public pharmacy consultations of 12 Hospitals in Galicia from May 2020 to April 2021. Baseline values of LDL-c are the previous values before taking PCSK9 and the follow-up values are in 6 months time.
Results89 patients were included. 86.5% with cardiovascular disease and 53.9% with statin intolerances. 78.8% of the patients were treated with high intensity statins. Statins most used were rosuvastatin (34.1%) and atorvastatin (20.5%). Baseline value of LDL-c was 148mg/dL and the follow-up value was 71mg/dL. The baseline value of patients treated with alirocumab (N=43) was 144mg/dL and 73mg/dL in the follow-up. With evolocumab (N=46) was 151mg/dL in basaline and 69mg/dL in follow-up. The LDLc- reduction was 51.21% with evolocumab and 51.05% with alirocumab. 43.1% of the patients showed values >70mg/dL in six month time; 19.4% between 69mg/dl and 55mg/dL and 37.5% <55mg/dL. 58.3% of the patients achieved a reduction >50% of LDL-c. The adverse events were: injection point reaction (N=2), myalgias (N=1), flu-like symptoms (N=1) and neurocognitive worsening (N=1).
Conclusions(1) Despite the number of prescriptions was reduced because of the pandemic, the lipid control was not affected. (2) Half of the patients treated with PSCK9i is due to statins intolerance and the 86% is for secondary prevention. (2) The reduction results were similar to pivotal clinical trials. Despite this, 39% of the total of the patients and 60% of patients with dual teraphy did not reach the goal of ESC/EAS guidelines (<55mg/dL and/or reduction>50%). There were not significant differences between evolocumab and alirocumab: 51.21% vs 51.05% (P=.972). (3) There were not any adverse events of special interest. The possible neurocognitive worsening will be studied as the primary endpoint once the MEMOGAL study has been completed.
Las lipoproteínas de baja densidad o colesterol LDL (c-LDL) se asocian con aterosclerosis, la primera causa de enfermedad cardiovascular coronaria1. La reducción del c-LDL ha sido fuertemente asociada a una reducción de la incidencia de la enfermedad cardiovascular, y se considera el objetivo principal para la prevención cardiovascular2,3.
La PCSK9 pertenece a la familia de las subtilisinas de las serina-proteasas y se expresa sobre todo en el hígado.? La PCSK9 participa en la regulación de los niveles de proteína del receptor de lipoproteínas de baja densidad (R-LDL). Una vez secretada en el plasma la PCSK9 se une directamente al R-LDL y estimula su degradación lisosómica tras la interiorización. El incremento en la degradación del R-LDL deriva en una menor reducción del c-LDL y, en consecuencia, mayores niveles de c-LDL circulante3,4.
Se han desarollado 2 anticuerpos monoclonales que inhiben la PCSK9 (iPCSK9): alirocumab y evolocumab. Ambos han demostrado reducir los niveles de c-LDL un 50%, así como el riesgo de infarto5,6, motivo por el cual se han autorizado en el tratamiento de hipercolesterolemia familiar (HF) o ateroesclerosis cardiovascular que requiera un mayor descenso del c-LDL, a pesar de recibir estatinas a dosis máximas.
La actual pandemia ocasionada por el virus SARS-CoV-2ha originado mundialmente una enorme crisis económica y social, pero sobre todo sanitaria. Los primeros casos fueron descritos a mediados de diciembre de 2019 y en el primer semestre de 2021 se contabilizaban 180 millones de casos y más de 4 millones de fallecidos7. Una de las principales complicaciones en pacientes hospitalizados por COVID-19 son las enfermedades cardiovasculares, que han mostrado un aumento tanto de las hospitalizaciones, como de las complicaciones intrahospitalarias y la mortalidad8, por lo que el seguimiento de este tipo de pacientes es indispensable a la hora de reducir posibles hospitalizaciones y complicaciones.
Las consultas externas de Farmacia Hospitalaria desempeñan una labor fundamental en el control de este tipo de pacientes. Uno de los objetivos de este artículo es evaluar el papel desempeñado por los farmacéuticos hospitalarios durante la pandemia, para así entender en qué modo la pandemia ha podido influir en la prescripción, dispensación de iPCSK9 y en el manejo de estos pacientes.
El estudio MEMOGAL (NCT04319081) es un estudio observacional, multicéntrico y prospectivo dirigido a evaluar los cambios en la función cognitiva de pacientes tratados con iPCSK99. Este estudio comenzó en mayo de 2020, en plena pandemia, y paralelamente a los objetivos del mismo se definieron una serie de puntos a analizar que se enumeran a continuación:
- 1)
Discutir el papel de los farmacéuticos hopitalarios durante de la pandemia y evaluar el impacto de la misma en el control lipídico.
- 2)
Indicaciones y frecuencia de prescripción de iPCSK9 durante la pandemia de la COVID-19 y análisis descriptivo de pacientes tratados con iPCSK9.
- 3)
Valorar la eficacia en la reducción de c-LDL y diferencias entre alirocumab y evolocumab.
- 4)
Reportar la seguridad de los iPCSK9.
Se trata de un análisis observacional, multicéntrico, prospectivo con un diseño cuasiexperimental con información de vida real (Real-World Evidence) de pacientes tratados por primera vez con iPCSK9 en las condiciones actuales de financiación en las consultas externas de farmacia de 12 hospitales del Sistema Sanitario Público desde mayo de 2020-abril de 2021.
Los sujetos incluidos fueron pacientes con diagnóstico de HF homocigota o heterocigota y/o pacientes con enfermedad cardiovascular establecida (cardiopatía isquémica, enfermedad cerebrovascular isquémica o arteriopatía periférica) en los que se prescribe por práctica clínica habitual y por primera vez evolocumab o alirocumab, que no alcancen c-LDL<100mg/dl tras haber recibido tratamiento con estatinas a la dosis máxima tolerada, o intolerancia a estatinas, y con adherencia terapéutica correcta a las estatinas (≥80% por registro de dispensación).
Los centros participantes fueron: Hospital Clínico Universitario de Santiago, Hospital Universitario de Ourense, Hospital Álvaro Cunqueiro (Vigo), Hospital Provincial de Pontevedra, Hospital Barco de Valdeorras, Hospital Virxe da Xunqueira (Cee), Hospital Arquitecto Macide de Ferrol, Hospital Universitario de A Coruña, Hospital da Costa (Burela), Hospital Universitario Lucus Augusti (Lugo) y Hospital Comacal de Monforte.
Se tomaron como valores basales de c-LDL los previos al inicio del tratamiento con iPCSK9 una vez firmado el consentimiento informado y como seguimiento los valores a los 6 meses. El resto de variables del estudio se tomaron a través de la historia clínica electrónica previa firma de consentimiento informado y a través de entrevista directa con el paciente en las consultas de farmacia hospitalaria.
Análisis estadísticoLas variables cuantitativas son presentadas como media o desviación estándar o mediana y rango intercuartílico, y las cualitativas como frecuencia y porcentaje. Las diferencias entre los niveles de c-LDL se evaluaron mediante el test de Wilcoxon Sign. Además, se calcularon los porcentajes de reducción de c-LDL y se llevó a cabo el test «t» de Student para determinar las diferencias entre los pacientes que tomaban alirocumab y evolocumab.
La significación estadística se aceptó para p<0,05. Todos los análisis fueron realizados con SPSS 19.0 (IBM Corp. Released 2019. IBM SPSS Statistics for Windows, Version 26.0. Armonk, NY: IBM Corp).
ResultadosDespués del período más crítico en España, el primer confinamiento de la pandemia de marzo a abril de 2020, se incluyeron un total de 89 pacientes procedentes de hospitales gallegos durante el período de mayo de 2020 a abril de 2021 (edad media de 60,44 años; el 27% eran mujeres).
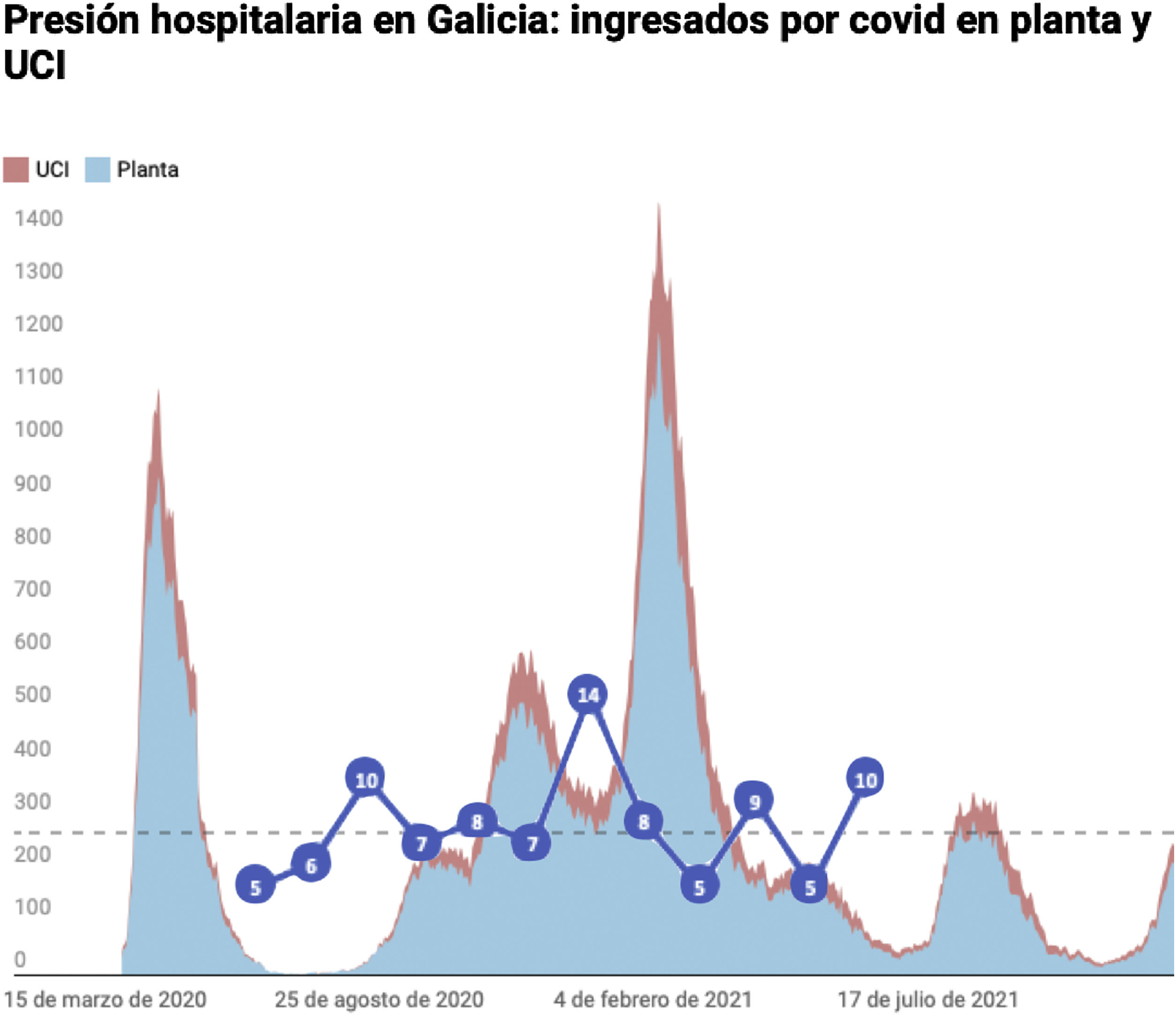
El ritmo de inclusión fue: mayo de 2020 5 pacientes; junio de 2020 6 pacientes; julio de 2020 10 pacientes; agosto de 2020 7 pacientes; septiembre de 2020 8 pacientes; octubre de 2020 7 pacientes; noviembre de 2020 14 pacientes; diciembre de 2020 8 pacientes; enero de 2021 5 pacientes; febrero de 2021 9 pacientes; marzo de 2021 5 pacientes; y abril de 2021 5 pacientes (fig. 1).
En la tabla 1 se describen las características basales y demográficas de los pacientes y cambios en el c-LDL. A continuación se presentan las características más relevantes: el 25,8% presentaban HF, el 86,5% enfermedad cardiovascular y un 53,9% intolerancia a estatinas. Un 78,8% de los pacientes recibía tratamiento con estatinas de alta intensidad, un 19,2% de intensidad media y un 1,9% de baja intensidad. Un 62,9% estaba en tratamiento con ezetimiba.
Características basales y demográficas de los pacientes y cambios en c-LDL
| Variables | Pacientes incluidos, n=89 |
|---|---|
| Características sociodemográficas | |
| Edad (años)a | 60,44±9,973 |
| Sexo (mujer), n(%) | 24 (27,0) |
| IMC (kg/m2)a | 28,47 (±4,531) |
| Historia médica previa, n (%) | |
| Hipercolesterolemia familiar | 23 (25,8) |
| Enfermedad cardiovascular | 77 (86,5) |
| Diabetes mellitus | 18 (20,2) |
| Hipertensión | 52 (58,4) |
| Intolerantes a estatinas | 48 (53,9) |
| Tipo de estatinas, n (%) | |
| Atorvastatina | 18 (20,5) |
| Rosuvastatina | 30 (34,1) |
| Rosuvastatina | 1 (1,1) |
| Piavastatina | 4 (4,5) |
| Sin estatina | 35 (39,8) |
| Potencia | |
| Potencia alta | 41 (78,8) |
| Potencia media | 10 (19,2) |
| Potencia baja | 1 (1,9) |
| Ezetimiba | 56 (62,9) |
| iPCSK9 (n,%) | |
| Evolocumab 140mg | 46 (51,7) |
| Alirocumab 75mg | 33 (37,1) |
| Alirocumab 150mg | 10 (11,2) |
| Niveles de LDL (mg/dl) | |
| LDL basal (mg/dl)a | 148±53 |
| LDL seguimiento (mg/dl)a | 71±4 |
| Reducción de LDL (%) | 51±20 |
| Alirocumab | |
| LDL basal (mg/dl)a | 145±43 |
| LDL seguimiento (mg/dl)a | 73±36 |
| Reducción de LDL (%) | 51±15 |
| Evolocumab | |
| LDL basal (mg/dl)a | 152±62 |
| LDL Seguimiento (mg/dl)a | 69±34 |
| Reducción de LDL (%) | 51±234 |
| Controles de LDL al seguimiento, n (%) | |
| >70mg/dl | 31 (43,1) |
| 55 a 69mg/dl | 14 (19,4) |
| <55mg/dl | 27 (37,5) |
| Reducción>50% basal | 42 (58,3) |
| Pacientes en objetivos LDL, n (%) | 44 (61,1) |
| EST+EZE+iPCSK9 | 26 (59,1) |
| EZE+iPCSK9 | 18 (40,9) |
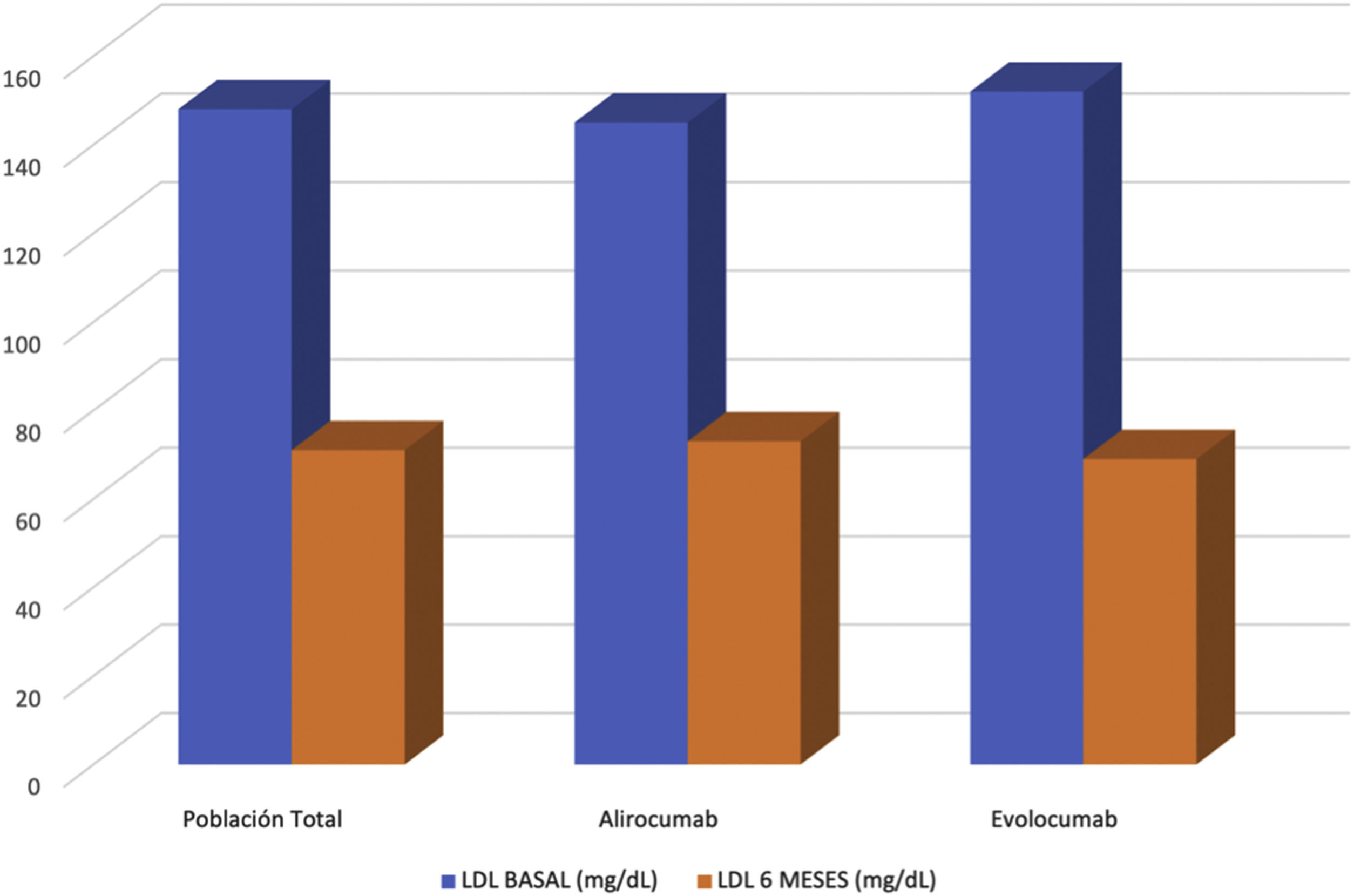
El nivel basal del c-LDL fue 148mg/dl y de 71mg/dl al seguimiento (hasta 6 meses). Cuarenta y seis pacientes fueron tratados con evolocumab (51,7%) y 43 con alirocumab (49,3%). Los pacientes tratados con alirocumab presentaban valores basales de 144mg/dl y de 73mg/dl al seguimiento, y con evolocumab de 151mg/dl basal y 69mg/dl al seguimiento (fig. 2). La reducción de c-LDL fue de 51,14%, siendo para evolocumab 51,21% y alirocumab 51,05% (Figura 3). El 43,1% presentaba a los 6 meses valores>70mg/dl, el 19,4% presentaba valores entre 55 y 69mg/dl y el 37,5% valores<55mg/dl. Los pacientes que obtuvieron una reducción>50% de c-LDL fueron el 58,3%.
Los eventos adversos presentados fueron: reacción en el lugar de inyección (n=2), mialgias (n=1), síntomas pseudogripales (n=1) y deterioro neurocognitivo (n=1).
DiscusiónEn el presente estudio analizamos la prescripción de iPCSK9 y el control lipídico de los pacientes tratados con estos fármacos durante la pandemia por la COVID-19. Probablemente represente el primer estudio en vida real de pacientes tratados con iPCSK9 en este periodo de tiempo. Los resultados apreciados ponen de manifiesto que las prescripciones de iPCSK9 representan una pequeña proporción de pacientes, lo cual pueda ser debido a la disminución de consultas presenciales o a la no implantación de consultas telemáticas. No obstante, teniendo en cuenta también que nuestra población tratada con iPCSK9 es similar a todos los estudios realizados previamente6,10,12,13,20, los resultados en términos de eficacia están acorde con los publicados en los ensayos clínicos pivotales y en vida real en situación de no COVID-195,6,10,11. Estas conclusiones pueden ser de relevancia a la hora de plantear políticas sanitarias en momentos de disminución de la actividad presencial en aras de hacer aplicables los resultados de fármacos con evidencia demostrada.
Pandemia y prescripción iPCSK9Esto puede deberse fundamentalmente a la labor realizada por los profesionales sanitarios y el sistema de dispensación a domicilio14, que ha repercutido en una buena adherencia a todos los tratamientos iniciados en este período, lo que pone de manifiesto que la aplicación de estos recursos sanitarios es efectiva en términos de eficacia y seguridad, y presumiblemente en términos de coste-eficacia15,16.
Por otro lado, cabe destacar que por el número de inclusiones en el estudio por mes se puede intuir que en los períodos con más restricciones sanitarias, en concreto durante el período de mayor ingreso hospitalario, disminuyó el número de prescripciones de iPCSK9. Las curvas de contagios y de inclusiones son totalmente opuestas en ambas gráficas (figs. 1 y 2). Esto se puede deber al hecho de que se hayan suspendido o disminuido el número de consultas médicas presenciales y/o que la teleconsulta no se haya implantado de manera tan eficiente en las diferentes áreas sanitarias a la hora de prescribir estos fármacos17,30 (fig. 1).
Resultados de los iPCSK9En el presente estudio más de la mitad de los pacientes presentaban intolerancia a estatinas y a un 86% se les prescribió los iPCSK9 en prevención secundaria, lo que destaca el gran número de pacientes con enfermedad cardiovascular y la importancia de estos fármacos en esta enfermedad1–3,5,6, en la cual en estos momentos en España tan solo lo reciben un 0,89% de los pacientes a los 12 meses tras un síndrome coronario agudo18. Además, el uso de estatinas en monoterapia ha demostrado en muchos casos no ser suficiente para alcanzar los objetivos en este grupo de pacientes19–21.
Los iPCSK9 reducen en torno al 50% del c-LDL de manera efectiva y segura5,6,10,11. El evolocumab ha demostrado ser efectivo en HF homozigota23. Alirocumab reduce la necesidad de aféresis de c-LDL en este tipo de pacientes, una de las pocas terapias efectivas para el control de c-LDL en HF25. En otros estudios como el OSLER26 y el ODYSSEY Long-term27 también se demostró la eficacia de evolocumab y alirocumab en la reducción de c-LDL y eventos cardiovasculares mayores (MACE). Evolocumab y alirocumab muestran efectos similares en la reducción de c-LDL a dosis equipotentes5,6. Nuestros resultados están en concordancia con estos ensayos pivotales5,6 y muestran que no hay diferencias significativas en la media de porcentaje de reducción de c-LDL entre evolocumab y alirocumab: 51,21% vs. 51,05% (p=0,972).
Las nuevas guías europeas de lípidos (ESC guidelines)21 recomiendan que los pacientes con HF o enfermedad cardiovascular deben reducir un 50% el c-LDL basal o marcar el objetivo<55mg/dl de c-LDL. También en enfermedad cardiovascular tras SCA el perfil lipídico debe de ser revaluado a las 4-6 semanas, y si los objetivos no se han alcanzado debería iniciarse iPCSK9 (nivel de evidencia I, clase B)21.
En el presente análisis los pacientes tratados con estatinas llevaban un 78% de alta intensidad, un 20% de intensidad media y 2% de intensidad baja, un porcentaje similar a la población estudiada en otros estudios previos de uso de estatinas en monoterapia en prevención secundaria, en los cuales se concluye que un 70% de los pacientes no alcanzan objetivos por debajo de 70mg/dl de c-LDL y tan solo un 11% el objetivo de 50mg/dl de c-LDL22,23.
Nuestros resultados de uso de iPCSK9, tanto en monoterapia como en doble o triple terapia (estatinas y/o ezetimiba) fueron que el 43,1% de los pacientes presentaba valores por encima de 70mg/dl de c-LDL en el seguimiento; el 19,4% de los pacientes entre 55mg/dl y 69mg/dl de c-LDL y un 37,5% del total de los pacientes presentaba valores por debajo de 55mg/dl, por lo que hemos pasado de un 30% (en estudios previos22,23) de pacientes que se encuentran por debajo de 70mg/dl a un 60%, y también del 11% de pacientes que se encuentran por debajo de 55mg/dL (en estudios previos22,23) al 37% en esta población a estudio.
Como conclusión vemos cómo la adición de los iPCSK9 mejora los objetivos marcados por las guías, pero a pesar de ello todavía existe en torno a un 40% de los pacientes que no alcanzan la diana de redución>50% de c-LDL o <55mg/dl21. Esto sucede fundamentalmente en triple terapia de tratamiento (estatinas+ezetimibe+iPCSK9), sin embargo en pacientes totalmente intolerantes a estatinas vemos cómo se incrementa el número de sujetos que no alcanzan estos objetivos hasta el 60%, con lo que podemos concluir y destacar la importancia de mantener las estatinas en la medida de lo posible.
El ácido bempedoico, que en el momento de publicar estos datos estaba en proceso de aprobación en España, desempeña un papel fundamental en estos pacientes. Se han publicado varios ensayos clínicos28,29 donde se evaluó la reducción de c-LDL a las 12 semanas. Se observó una reducción del 18% cuando se asocia a estatinas y una reducción del 25% cuando se usaba en monoterapia. La asociación ácido bempedoico más ezetimibe logra una reducción del 38%. Por todo esto, creemos que es una alternativa que podría ser muy eficaz en este tipo de pacientes que no toleran ninguna dosis de estatina y que no alcanzan las recomendaciones de las guías de dislipidemia.
SeguridadEn cuanto a la seguridad de estos fármacos la reducción excesiva de c-LDL se ha relacionado con la hipótesis de posibles cambios en la función cognitiva.
Actualmente no hay evidencias de este posible deterioro cognitivo por lo recogido hasta ahora en una única publicación: el subestudio EBBINGHAUS27. En nuestro estudio los eventos adversos reportados fueron: reacción en el lugar de inyección (n=2), mialgias (n=1), síntomas pseudogripales (n=1) y deterioro neurocognitivo (n=1). El posible deterioro cognitivo está siendo estudiado como variable principal del estudio MEMOGAL9.
Como limitaciones cabe destacar un tamaño de muestra pequeño al tratarse de un análisis realizado en el período de la pandemia, donde posiblemente disminuyó el número de prescripciones de iPCSK9, por eso creemos que nuestros resultados aportarán una información muy importante de la situación actual de estos fármacos durante la pandemia.
Conclusiones- 1)
La pandemia de la COVID-19ha tenido un impacto directo sobre la prescripción de iPCSK9, que se ha visto reducida en la población gallega. Pese a ello, los resultados en términos de eficacia y seguridad son similares a los estudios previos, probablemente por la labor de los profesionales sanitarios.
- 2)
Más de la mitad de los pacientes tratados con iPSCK9 se debe a intolerancia a estatinas, y en el 86% es en prevención secundaria.
- 3)
Estos pacientes presentan valores de reducción similares a los ensayos clínicos pivotales. A pesar de esto, un 39% del total de los pacientes en triple terapia y un 60% de los pacientes en doble terapia no alcanzaron las recomendaciones de las guías ESC/EAS. No hubo diferencias significativas en la media de porcentaje de reducción de c-LDL entre evolocumab y alirocumab: 51,21% vs. 51,05% (p=0,972).
- 4)
No se observaron eventos de especial interés con el uso de estos fármacos.
Este trabajo trata de aportar a la literatura científica datos novedosos e información sobre la situación actual de los pacientes tratados con iPCSK9 durante la pandemia de la COVID-19, en concreto los pacientes que iniciaron iPCSK9 por primera vez. Tratamos de aportar una visión de la situación actual en cuanto a prescripciones, adherencia a los tratamientos en el contexto de las restricciones sanitarias y diferentes estados de alarma y, sobre todo, cómo ha afectado en términos de eficacia y seguridad, y la manera en la que se ajustan estos resultados con las actuales guías de dislipidemias.
Por otro lado, queremos destacar el carácter multicéntrico, multidisciplinar y prospectivo del estudio.
Conflicto de interesesNo existe conflicto de intereses para ninguno de los autores.
24.
Referencia no citada24.
A la Fundación Instituto de Investigación Sanitaria de Santiago de Compostela (FIDIS) y a todos los investigadores principales y subinvestigadores de los centros que participan en el estudio, pertenecientes a las consultas externas de farmacia de los hospitales públicos de Galicia, y al servicio de cardiología de Santiago y Alicante.
Natalia Perez-Rodriguezj, María Anido-Garcíaj, Laura Villaverde-Piñeirok, Concepción Castro-Rubinesl, Yveth Michelle Tajes-Gonzalezl, Karina Lorenzo-Lorenzom, Cristina Casanova-Martinezm, Diego Rodriguez-Penasn, Iria Varela-Reyñ, Luis Margusino-Framiñáno, Carlos Crespo-Dizp, Irene Zarra-Ferroñ, Marisol Rodriguez-Cobosñ, Juan Rojo Valdésñ, Moisés Rodriguez-Mañeron,q, Héctor Mozo-Peñalverr, Esther Espino-Paisánr, Ana Rodriguez-Vazquezs, Jose Luis Rodriguez-Sanchezt, María Jesús García-Verdet, Alberto Cordero-Fortq,u, Jose Ramón Gonzalez-Juanateyn,q
j Servicio de Farmacia, Hospital Lucus Augusti, Lugo, España
k Servicio de Farmacia, Hospital Comarcal de Monforte de Lemos, Monforte de Lemos, España
l Servicio de Farmacia, Hospital da Costa de Burela, Burela, España
m Servicio de Farmacia, Hospital Álvaro Cunqueiro, Vigo, España
n Servicio de Cardiología, Hospital Clínico Universitario de Santiago de Compostela, Santiago de Compostela, España
ñ Servicio de Farmacia, Hospital Clínico Universitario de Santiago de Compostela, Santiago de Compostela, España
o Servicio de Farmacia, Hospital Universitario de A Coruña, A Coruña, España
p Servicio de Farmacia, Complexo Hospitalario Universitario de Pontevedra, Pontevedra, España
q Centro de Investigación Biomédica en Red de Enfermedades Cardiovasculares (CIBERCV), España
r Servicio de Farmacia, Hospital do Barbanza, Ribeira, España
s Servicio de Farmacia, Hospital Comarcal de Valdeorras, O Barco de Valdeorras, España
t Servicio de Farmacia, Hospital Virxe da Xunqueira, Cee, España
u Servicio de Cardiología, Hospital San Juan de Alicante, San Juan de Alicante, España