Las enfermedades endocrinológicas afectan directamente al sistema cardiocirculatorio. Los efectos deletéreos sobre la función cardiovascular pueden ser directos y ligados al incremento o reducción de las hormonas circulantes. Igualmente, los efectos nocivos pueden ser indirectos, por ejemplo los que siguen a la elevación de la presión arterial, el incremento o redistribución de la masa grasa o la elevación de las lipoproteínas plasmáticas. La mejor asistencia sanitaria y la disponibilidad cada vez mayor de pruebas bioquímicas hacen que muchas enfermedades endocrinológicas se diagnostiquen antes de la aparición de la clínica. Esta revisión se va a centrar en mostrar evidencias de alteración funcional o estructural cardiovasculares para casos de hiperparatiroidismo primario, síndrome de Cushing e hipotiroidismo, en sus formas subclínicas, y la reversibilidad de sus complicaciones tras tratamiento adecuado.
Endocrinological diseases directly affect the cardiovascular system. The deleterious effects on cardiovascular function can be direct, and linked to the increase or reduction of circulating hormones. Equally, the adverse effects may be indirect; for example following the rise in blood pressure, increase or redistribution of lean mass, or increased plasma lipoproteins. The best health care and the increasing availability of biochemical tests lead to the diagnosis of many endocrine diseases before the onset of clinical signs. This review will focus on presenting evidence of cardiovascular functional or structural impairment in cases of primary hyperparathyroidism, Cushing's syndrome, and hypothyroidism in their sub-clinical forms, as well as the reversibility of complications after appropriate treatment.
Además de la diabetes mellitus, otras enfermedades endocrinológicas incrementan la probabilidad de padecer enfermedades del sistema circulatorio, bien a nivel del corazón bien a nivel de las grandes arterias. De hecho, muchos trastornos de hipo o hiperfunción glandular tienen como parte del síndrome manifestaciones del sistema circulatorio, como la hipertensión generada en la hiperproducción de hormonas suprarrenales o las manifestaciones cardiacas en los síndromes de hipo e hiperfunción tiroidea.
Los avances en los métodos diagnósticos hacen que con mayor frecuencia en los últimos decenios pocos pacientes se presenten con las manifestaciones completas o clásicas de la enfermedad. Más bien al contrario, en la actualidad es más frecuente diagnosticar un hiperparatiroidismo primario (HPTP) por una discreta elevación del calcio sérico o un hipotiroidismo (HP) por una elevación modesta de la TSH que por el conjunto de los síntomas y signos físicos que caracterizan a la enfermedad.
En este artículo vamos a revisar las principales consecuencias del sistema circulatorio que acompañan al HPTP, al hipercortisolismo y al HP, haciendo hincapié en la potencial reversibilidad de los cambios tras la «curación» del trastorno de base y de las formas subclínicas.
Hiperparatiroidismo primarioDominado por la clínica de la hipercalcemia, el HPTP suele manifestarse por nefrolitiasis, lesión ósea, afectación digestiva, manifestaciones neuropsiquiátricas e hipertensión, aunque la mayoría de pacientes están sintomáticos1,2.
La mortalidad global está incrementada en los pacientes con HPTP, en especial a expensas de la mortalidad cardiovascular; en un estudio que incluyó 4.461 pacientes que fueron tratados con cirugía, la mortalidad global fue un 71% mayor en los casos respecto de los controles, mientras que la cardiovascular lo fue un 85%3. Estos datos fueron confirmados en sendas revisiones de estudios prospectivos adicionales4,5.
Estudios recientes indican que los niveles de parathormona (PTH) son predictores de enfermedad y muerte vascular incidente, incluso en niveles de PTH dentro de los rangos de normalidad e independiente de otros factores de riesgo vascular clásicos6. Es posible que los mecanismos involucrados en este aumento de la incidencia de enfermedad vascular residan en un aumento de la aterogénesis a través del remodelado vascular y de la calcificación de la pared arterial o bien efectos directos a nivel del miocardio, como la hipertrofia o la fibrosis. En este sentido, en un estudio de 49 pacientes con HPTP moderado de ambos sexos, comparados con 991 controles sin la enfermedad, se encontró que el grosor íntimo-medial y la prevalencia de placa de ateroma fueron significativamente más altos en casos que en los controles. Los niveles de PTH, pero no los de calcio, se asociaron de forma significativa con la rigidez y la distensibilidad de la carótida7. Este mismo grupo evaluó a 44 pacientes a los 2años de la paratiroidectomía, observando que de los parámetros estudiados solo se objetivó una discreta mejoría en la rigidez carotídea8. Por el contrario, Carrelli et al.9 no encontraron diferencias respecto de un grupo control en la función endotelial mediada por flujo de la arteria humeral en 45 pacientes con HPTP leve; no obstante, en un subgrupo con una función anormalmente baja, esta mejoró un 35%, normalizándose a los 6meses tras la paratiroidectomía; ninguno de los parámetros analizados en este estudio (calcio, PTH, vitaminaD) se asoció ni con la dilatación medida por flujo basal ni con los cambios post-paratiroidectomía. Datos similares han sido encontrados a nivel de la circulación coronaria. Osto et al.10 estudiaron 100 pacientes con HPTP asintomático y sin enfermedad vascular conocida, y a todos ellos se les midió el flujo de reserva coronario, medido por ecografía transtorácica del flujo de la descendente anterior en estado basal y tras estímulo con adenosina. El flujo de reserva coronario fue menor en pacientes que en controles, mientras que fue mayor significativamente el porcentaje de pacientes con niveles bajos de este parámetro frente a controles (27% vs 4%, p<0,05). Es interesante recalcar que los niveles de PTH fueron significativamente más altos en aquellos pacientes con un flujo de reserva coronario bajo que en los que lo tenían normal, siendo la PTH el único factor asociado con este parámetro en un análisis de regresión logística; curiosamente, en este subgrupo de pacientes el flujo de reserva coronario se normalizó tras la paratiroidectomía, lo que, a juicio de los autores, supone que la PTH juega un papel crucial en la alteración de la función microvascular coronaria.
Es clásico atribuir la enfermedad cardiaca en el HPTP a la suma de hipertrofia ventricular, rigidez de la pared ventricular con la consiguiente disfunción diastólica y calcificación valvular4. Sin embargo, es posible que haya diferencias importantes dependiedo del grado de gravedad del proceso, siendo mayor el impacto en casos sintomáticos que en los leves. En una cohorte de 56 pacientes con HPTP sintomático, respecto de controles sin la enfermedad, se observó una mayor masa ventricular izquierda, del septo interventricular, y mayor disfunción diastólica; igualmente, los pacientes tuvieron mayores niveles séricos de NTproBNP (un marcador de daño miocárdico) y peor función endotelial mediada por flujo; los parámetros de masas ventricular, función diastólica, NTproBNP y función endotelial mejoraron de forma significativa a los 3 y 6meses de la paratiroidectomía; estos resultados no cambiaron al analizar la muestra según el grado de presión arterial11. Por el contrario, en 54 pacientes con HPTP leve, comparados con controles emparejados por edad y sexo, no se encontraron diferencias ni en la masa ventricular izquierda ni en el grado de disfunción diastólica, que incluso fue mejor en los casos que en los controles, aunque los sujetos con mayores niveles de calcio PTH tuvieron peor función diastólica que el resto de pacientes con HPTP12. El mismo grupo no encontró cambios significativos en la masa ventricular, disfunción diastólica o grado de calcificación en 44 pacientes con forma leve de la enfermedad a los 2años de paratiroidectomía8.
En resumen, los pacientes con HPTP sintomáticos muestran hipertensión y cambios funcionales y estructurales en el miocardio que justificarían una mayor incidencia de enfermedad y muerte vascular. Sin embargo, para los pacientes asintomáticos los cambios se circunscriben más a alteraciones funcionales a nivel de la función endotelial periférica y al flujo de reserva coronario, íntimamente ligados a niveles elevados de PTH y que, afortunadamente, parecen reversibles tras la paratiroidectomía.
Síndrome de CushingEl síndrome de Cushing (SC) es el resultado de un exceso prolongado e inapropiado de glucocorticoides circulantes, que en los adultos se caracteriza por la redistribución de la grasa, hipertensión, piel fina con hirsutismo, estrías rojo vinoso, hiperglucemia o diabetes, osteoporosis, trastornos psiquiátricos e hipopotasemia. En el 80% de las ocasiones esta elevación es dependiente de ACTH y a su vez, dentro de estas, el 80% de origen hipofisario13,14. Este síndrome es poco frecuente, ya que solo se registraron 481 pacientes en 2años en un trabajo colaborativo de 36 centros de 23 países europeos15. En el contexto de una consulta de riesgo vascular, el SC debe ser tenido en cuenta en casos de hipertensión o diabetes tipo2, aunque el cribado entre este tipo de pacientes es escasamente rentable16,17.
La mortalidad en el SC es elevada cuando se compara con la población general, en especial durante el primer año, cuando la etiología es indeterminada y en los casos de adenoma suprarrenal18. El riesgo cardiovascular está elevado en los pacientes con SC, no solo por la hipertensión que acarrea la enfermedad sino porque contribuyen otros factores como los caracterizados del síndrome metabólico, hipertrofia ventricular y disfunción diastólica y endotelial y un estado protrombótico19-22. En un estudio retrospectivo de 346 individuos con SC, el sexo masculino, la edad al diagnóstico, la coexistencia de diabetes y la depresión elevaron de forma significativa el riesgo de enfermedad cardiovascular23. En un estudio poblacional desarrollado en el Reino Unido, la mortalidad cardiovascular fue 13 veces superior a la de la población general, siendo los 3 factores más importantes la falta de remisión de la enfermedad, la presencia de diabetes y la hipertensión24. Por todo ello, algunos autores recomiendan, además de la analítica de rutina y un ECG, la práctica de un test de tolerancia oral a la glucosa, un registro de 24h de presión arterial, un ecocardiograma y una ecografía carotídea al objeto de una evaluación más completa de la enfermedad cardiovascular en este síndrome25.
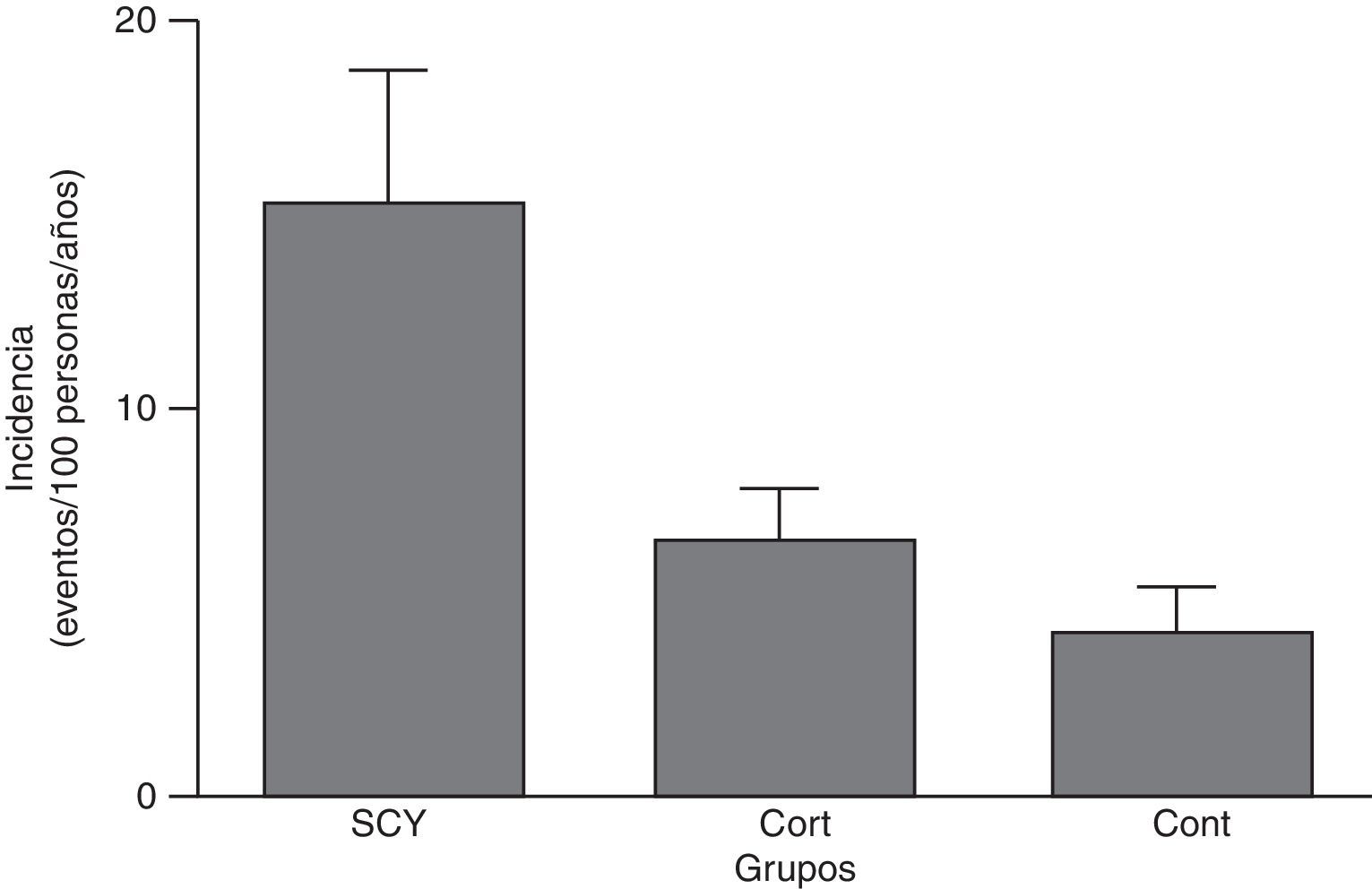
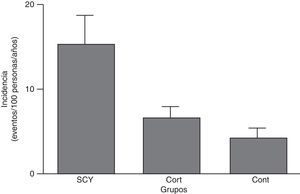
Más frecuente que el SC es el Cushing iatrógeno, ya que se estima que entre el 1-2% ha estado expuesta a glucocorticoides sistémicos. La tasa de incidencia de episodios cardiovasculares (enfermedad coronaria, ictus o insuficiencia cardiaca) fue muy superior en sujetos con SC iatrógeno frente a aquellos que no lo recibieron (fig. 1)26.
Tasa de incidencia de episodios cardiovasculares (coronario, ictus o insuficiencia cardiaca) por 100 pacientes/años (IC al 95%) en pacientes que han recibido corticoides sistémicos y tienen síndrome de Cushing (SCY), aquellos que han recibido corticoides pero no tenían síntomas de síndrome de Cushing (CORT) y aquellos que no recibieron corticoides (CONT).
Tomado de Fardet et al.26.
Los sujetos con SC muestran peor dilatación medida por flujo que controles emparejados por edad y sexo; el grado de disfunción se correlacionó con los niveles matutinos de cortisol sérico y con el cortisol libre urinario; tras la resección quirúrgica y la normalización de los niveles de cortisol se restauró la función endotelial, lo que indica la reversibilidad de este fenómeno27. Otros cambios funcionales parecen igualmente reversibles tras tratamiento. Pereira et al.28 estudiaron varios parámetros de función sistólica y diastólica cardiacas mediante ecografía en 15 pacientes con SC y los compararon con 30 controles apareados por edad, sexo, área de superficie corporal, hipertensión arterial y función sistólica ventricular. Los pacientes no solo tuvieron mayor grado de hipertrofia ventricular y disfunción diastólica que los controles, sino que estos cambios revirtieron tras la normalización del exceso de corticoides.
Por el contrario, otros cambios estructurales a nivel coronario no parecen revertir; tal es el caso de las lesiones coronarias detectadas mediante angiotomografía computarizada (angio-TC) coronaria. Neary et al.29 estudiaron 14 pacientes con SC y 15 controles con al menos un factor de riesgo y emparejados por edad, sexo e índice de masa corporal; los pacientes tuvieron mayor volumen de placa de ateroma y mayor índice Agatston que los controles. De igual modo, Barahona et al.30 publicaron una serie de 29 pacientes curados bioquímicamente de un SC y la compararon con 48 controles emparejados por edad y sexo. Pese a la «curación», los pacientes con SC tenían mayor grado de calcificación (31 vs 21%) y de placas no calcificadas (20 vs 7.8%) cuando se sometieron a un examen por angio-TC coronaria. Respecto de la arteriosclerosis carotídea, en un estudio con 25 sujetos con SC, un 31% de ellos, comparados con un 6% en los controles, presentaron placa en la ecografía31.
Los efectos del hipercortisolismo sobre la dislipidemia han sido menos reportados. La presencia de hipercolesterolemia o hipertrigliceridemia oscilan entre 25-52% y 6-35%, respectivamente32. Faggiano et al.31 estudiaron 25 pacientes con SC, comparándolos con 32 controles emparejados por edad y sexo y otros 32 controles emparejados además por índice de masa corporal. Los niveles de colesterol de LDL mejoraron significativamente al año de la curación del SC, aunque permanecieron elevados significativamente respecto de los grupos control. Mancini et al.33 reportaron la hiperlipidemia en el 37% de 49 pacientes con SC. En este mismo estudio, el 80% de los pacientes con SC presentaban riesgo alto o muy alto, de acuerdo a las recomendaciones de la OMS/Sociedad Internacional de Hipertensión.
HipotiroidismoEl hipotiroidismo (HP) es un trastorno frecuente en nuestro medio que afecta fundamentalmente a mujeres en edades medias de la vida, dado que su etiología fundamental es la autoinmune. El diagnóstico no es difícil cuando se presentan de forma conjunta astenia, edema facial, voz ronca, piel seca, caída del cabello, depresión, somnolencia, estreñimiento e intolerancia al frío34. La generalización de la cuantificación de la TSH y T3 y T4 libres ha permitido que la mayor parte de los nuevos diagnósticos se efectúen antes de que aparezcan los síntomas y, cuando se trata de HP primario, con niveles de TSH entre 4 y 10mU/l. En estudios de prevalencia de HP derivados del consumo hormonal sustitutivo, 2 de 3 pacientes tienen HP subclínico (HPS)35. Cuando se hace un cribado de hormonas tiroideas en pacientes referidos por hipercolesterolemia, solo el 3,7% tuvieron HP (2,4% fue HPS)36.
Los efectos del HP sobre los lípidos séricos son bien conocidos; el HP conduce a elevaciones del colesterol total, del colesterol LDL y de la Lp(a), mientras que reduce la concentración del colesterol HDL37,38. La terapia de sustitución revierte, al menos parcialmente, estas alteraciones39. Los pacientes con HPS, en especial con niveles de TSH>10mU/l, muestran además características típicas de la dislipidemia aterogénica, esto es, elevaciones de triglicéridos, descenso del colesterol de las HDL y un menor tamaño de partículas de LDL, esto es, aumento de partículas LDL pequeñas y densas40.
Para el caso concreto de la asociación entre HPS y enfermedad cardiaca coronaria, se han publicado hasta la fecha 3 metaanálisis. En el primero de ellos, con 14 estudios prospectivos, el HPS elevó el riesgo de enfermedad coronaria, con una OR de 1,65 (IC95%: 1,28-2,12) respecto de los controles41. Cuando en otro metaanálisis se seleccionaron solo las publicaciones de mayor calidad, entonces la OR para enfermedad coronaria en el HPS fue más modesta (1,02-1,08), siendo mayor para aquellos sujetos de edad >65años42. En otro metaanálisis posterior, identificando pacientes con HPS con TSH entre 49-19mU/l, hubo una asociación entre HPS y morbimortalidad coronaria en sujetos con TSH>10,0mU/l43. Resultados similares se han publicado en un estudio prospectivo reciente en población china44. Respecto del riesgo de ictus, el HP eleva el riesgo relativo en 1,6 (IC95%: 1,0-2,6) cuando se compararon con aquellos sin HP45.
Mientras que el tratamiento sustitutivo es obligatorio en el caso del HP clínico, la recomendación para tratar el HPS es muy controvertida. Una revisión de la Chochrane, que incluye ensayos clínicos aleatorizados hasta el año 2007, concluye que la adición de levotiroxina a pacientes con HPS no mejoró la supervivencia ni redujo la incidencia de enfermedad cardiovascular46. Una reciente revisión del tema concluye en la ausencia de evidencia tanto de los beneficios como de los riesgos de la terapia hormonal sustitutiva en el HPS, dado que el único estudio que mostró beneficios sobre eventos cardiovasculares fue observacional y susceptible, por tanto, a sesgos de confusión47.
En conclusión, las enfermedades aquí revisadas se acompañan de alteraciones del sistema circulatorio que al menos parcialmente revierten con la curación bioquímica de la enfermedad, sobre todo las anomalías funcionales. Algunas alteraciones estructurales, como las lesiones ateromatosas coronarias, con o sin calcificación, parecen permanentes. La sustitución hormonal con levotiroxina en pacientes con HP subclínico no ha mostrado reducir la morbilidad vascular, aunque puede ser considerada cuando los niveles de TSH están por encima de 10mU/l.
Responsabilidades éticasProtección de personas y animalesLos autores declaran que para esta investigación no se han realizado experimentos en seres humanos ni en animales.
Confidencialidad de los datosLos autores declaran que en este artículo no aparecen datos de pacientes.
Derecho a la privacidad y consentimiento informadoLos autores declaran que en este artículo no aparecen datos de pacientes.
Conflicto de interesesLos autores declaran no tener conflicto de intereses.