Los seudoaneurismas coronarios son raros, y suelen ocurrir tras procedimientos percutáneos, disecciones espontáneas, bypass aortocoronarios, traumatismos torácicos o perforaciones. Aunque la mayoría de las ocasiones su diagnóstico suele ser casual, otras formas de presentación incluyen el infarto agudo de miocardio, la formación de fístulas o el taponamiento cardiaco. Presentamos el caso de un paciente con seudoaneurisma coronario tras el tratamiento percutáneo de una perforación coronaria.
Coronary pseudoaneurysms are rare and usually occur after percutaneous procedures, spontaneous dissections, aortocoronary bypass, or chest trauma. Although most of the cases are casual, other patients present as acute myocardial infarction, fistula formation or cardiac tamponade. We report the case of a coronary pseudoaneurysm after percutaneous treatment of a coronary perforation.
La etiología más frecuente de los aneurismas coronarios es la aterosclerosis, aunque otras afecciones como la enfermedad de Kawasaki, la arteritis de Takayasu, el lupus eritematoso sistémico, la esclerodermia, las enfermedades del tejido conectivo o la infecciones micóticas pueden producirlos1. Sin embargo, los seudoaneurismas coronarios son extremadamente raros2.
Un seudoaneurisma se define como una dilatación producida por la rotura de la pared de un vaso, que no incluye las 3 capas de la arteria, y que frecuentemente presentan hematoma organizado y fibrosis. Los seudoaneurismas coronarios, mayormente asintomáticos, ocurren principalmente como consecuencia de traumas originados por procedimientos percutáneos, disecciones espontáneas, bypass aortocoronarios, traumatismos torácicos o perforaciones3. Aunque en la época de la angioplastia simple su frecuencia se estimaba en torno a un 4-5% de los casos4, en relación a disecciones iatrogénicas que conllevaban la rotura y el debilitamiento de la pared arterial, tras el uso de los stents coronarios su incidencia ha disminuido drásticamente.
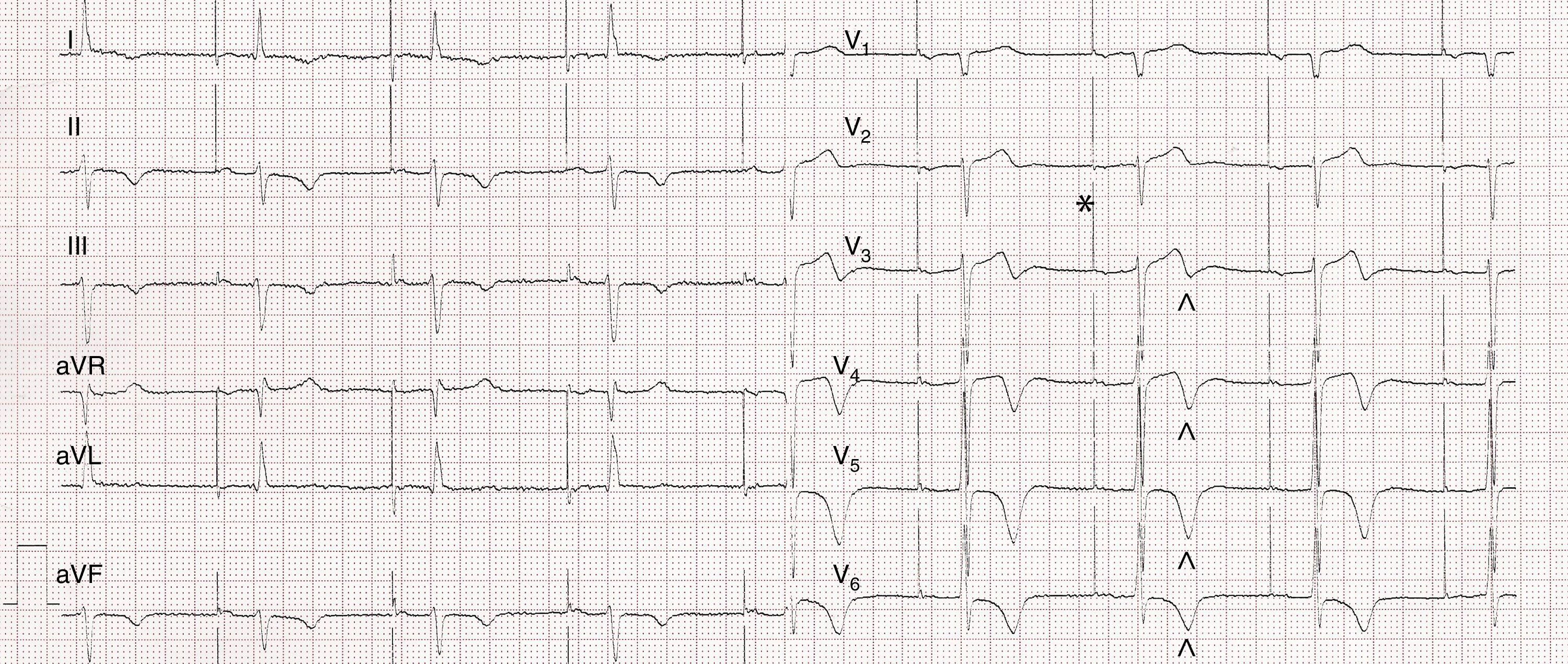
Caso clínicoPaciente varón de 79 años de edad con antecedentes de ateromatosis carotídea, portador de marcapasos definitivo por bloqueo AV de segundo grado, hipertensión arterial sistémica en tratamiento oral con doxazosina (8mg/12h) y verapamilo (180mg/12h) e hipercolesterolemia aislada en tratamiento con rosuvastatina (10mg/24h) y ezetimiba (10mg/24h), que ingresa por dolor torácico retroesternal, irradiado a cuello, de carácter opresivo y progresivo hasta hacerse de mínimos esfuerzos. A la exploración física se evidenciaron tonos cardiacos rítmicos, sin soplos, con murmullo vesicular normal y pulsos periféricos conservados. El electrocardiograma mostró ritmo de estimulación auricular por marcapasos con QRS estrecho y presencia de ondas T negativas profundas en territorio lateral (fig. 1). Las troponinas seriadas fueron normales y el ecocardiograma mostró disfunción ventricular izquierda sistólica moderada con hipocontractilidad generalizada más marcada en la cara inferior. El cateterismo cardiaco, vía arteria radial derecha, evidenció una lesión significativa en tercio medio de la descendente anterior, lesión severa y larga en tercio medio de la circunfleja (fig. 2A) y coronaria derecha, dominante, sin lesiones significativas. Se realizó angioplastia más implante de stents farmacoactivos en tercio medio de la circunfleja (Xience Expeditión® de 3×38mm y 4×12mm, ambos solapados). Tras el implante del stent de mayor diámetro se observó perforación coronaria (fig. 2B), motivo por el que se implantó un stent cubierto (GraftMaster® de 3,5×19mm) a nivel de la zona de extravasación, quedando mínima tinción persistente (fig. 2C) sin datos ecocardiográficos de derrame pericárdico. El paciente evolucionó satisfactoriamente, motivo por el que se decide la revascularización percutánea de la descendente anterior a los 4 días del procedimiento previo. Durante esta se evidencia imagen de seudoaneurisma a nivel de tercio medio de la circunfleja (fig. 2D y E) que se trata con el implante de un nuevo stent cubierto (GraftMaster® de 3,5×19mm) a nivel de tercio medio excluyendo el seudoaneurisma (fig. 2F) además de un stent recubierto farmacoactivo (Biomatrix® 3×28mm) a nivel de tercio medio de la descendente anterior. Buena evolución clínica posterior permaneciendo asintomático, desde el punto de vista cardiológico, a los 4 meses de seguimiento.
A) Coronariografía (oblicua anterior derecha [OAD] con caudo) en la que se evidencia lesión severa y larga a nivel de tercio medio de la circunfleja (Cx) (cabeza de flecha) y lesión significativa en tercio medio de la descendente anterior (DA). B) Proyección en OAD con caudo donde se evidencia extravasación de contrate a pericardio alrededor de la arteria Cx (cabeza de flecha). C) Proyección en OAD con caudo donde se observa imagen lineal peri-stent cubierto (cabeza de flecha) con sellado de la zona perforada. Proyección en OAD con caudo (D) y proyección en oblicua anterior izquierda (OAI) con caudo (E) donde se observa seudoneurisma coronario (cabezas de flecha). F) Inyección final en proyección en OAD con caudo donde se muestra flujo coronario TIMI-III con sellado total de la zona seudoaneurismática.
En la actualidad no hay un tratamiento estándar para el tratamiento de los seudoaneurismas que ocurren tras una perforación en el contexto de una angioplastia coronaria. Algunos autores han optado, según el tamaño del seudoaneurisma, por el tratamiento con stents cubiertos de politetrafluoroetileno, otros por el implante de microcoils, otros por la cirugía de resección, mientras que otros han realizado un seguimiento clínico, hasta de 3 años, sin evidencia de complicaciones5,6.
El implante de un stent cubierto parece ser la opción más aceptada debido a su accesibilidad y eficacia. Sin embargo, debemos tener en cuenta su peor navegabilidad y el mayor riesgo de trombosis y reestenosis y, por tanto, de que aparezca un nuevo evento coronario. Igualmente, debemos prestar atención a la existencia de endofugas ya que, aunque sean mínimas, pueden reflejar la mala posición del stent a la pared arterial o la falta de sellado de la zona perforada lo que puede favorecer la aparición y el crecimiento de seudoaneurismas en pacientes de por sí doblemente antiagregados. A pesar de ello, muchos seudoaneurismas pueden trombosarse espontáneamente o cerrarse una vez que el stent se haya endotelizado. Sin embargo debemos tener en cuenta que a mayor diámetro del seudoaneurisma, probablemente más flujo y presión arterial en su interior y, por tanto, mayor riesgo de crecimiento y rotura, y menor de cierre espontáneo.
En aquellos casos en los que el stent cubierto no progrese adecuadamente hasta la lesión, debido a la tortuosidad o el calcio coronario, podemos optar por el inflado prolongado de balones convencionales a nivel de la zona donde se visualiza la extravasación de contraste, la reversión de la heparina con protamina, la transfusión de plaquetas si el paciente estaba bajo tratamiento con anti-GPIIb/IIIa o el implante de stents convencionales que modifiquen la placa rota y, por tanto, el punto de fuga7,8.
En nuestro caso, debido a que el paciente se encontraba doblemente antiagregado y tenía ya implantado un stent cubierto en la zona del seudoaneurisma, se decidió implantar un nuevo stent cubierto, a altas atmósferas, con el fin de dejar adecuadamente sellada la zona del seudoaneurisma.
Responsabilidades éticasProtección de personas y animalesLos autores declaran que para esta investigación no se han realizado experimentos en seres humanos ni en animales.
Confidencialidad de los datosLos autores declaran que han seguido los protocolos de su centro de trabajo sobre la publicación de datos de pacientes y que todos los pacientes incluidos en el estudio han recibido información suficiente y han dado su consentimiento informado por escrito para participar en dicho estudio.
Derecho a la privacidad y consentimiento informadoLos autores han obtenido el consentimiento informado de los pacientes y/o sujetos referidos en el artículo. Este documento obra en poder del autor de correspondencia.






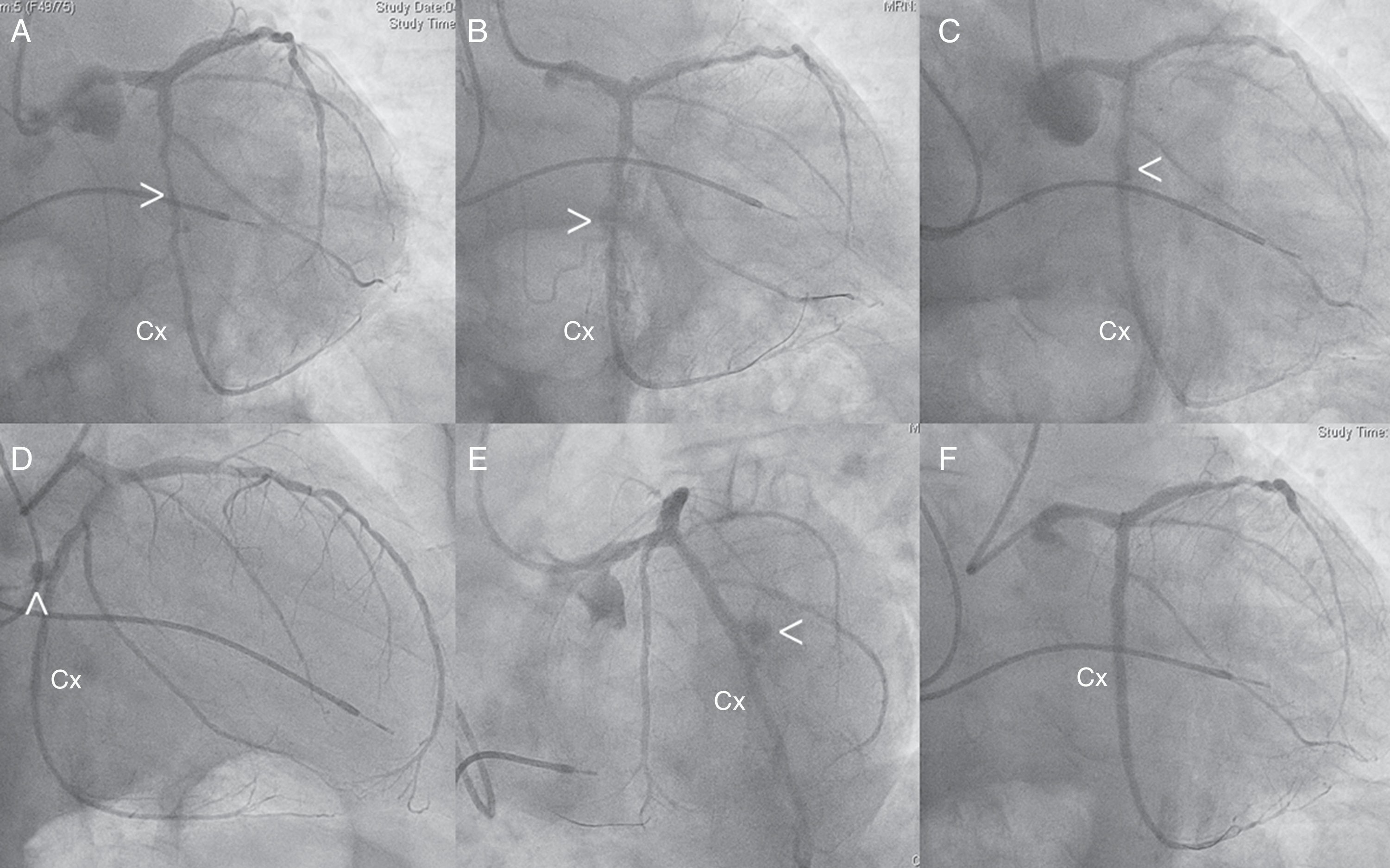
![A) Coronariografía (oblicua anterior derecha [OAD] con caudo) en la que se evidencia lesión severa y larga a nivel de tercio medio de la circunfleja (Cx) (cabeza de flecha) y lesión significativa en tercio medio de la descendente anterior (DA). B) Proyección en OAD con caudo donde se evidencia extravasación de contrate a pericardio alrededor de la arteria Cx (cabeza de flecha). C) Proyección en OAD con caudo donde se observa imagen lineal peri-stent cubierto (cabeza de flecha) con sellado de la zona perforada. Proyección en OAD con caudo (D) y proyección en oblicua anterior izquierda (OAI) con caudo (E) donde se observa seudoneurisma coronario (cabezas de flecha). F) Inyección final en proyección en OAD con caudo donde se muestra flujo coronario TIMI-III con sellado total de la zona seudoaneurismática. A) Coronariografía (oblicua anterior derecha [OAD] con caudo) en la que se evidencia lesión severa y larga a nivel de tercio medio de la circunfleja (Cx) (cabeza de flecha) y lesión significativa en tercio medio de la descendente anterior (DA). B) Proyección en OAD con caudo donde se evidencia extravasación de contrate a pericardio alrededor de la arteria Cx (cabeza de flecha). C) Proyección en OAD con caudo donde se observa imagen lineal peri-stent cubierto (cabeza de flecha) con sellado de la zona perforada. Proyección en OAD con caudo (D) y proyección en oblicua anterior izquierda (OAI) con caudo (E) donde se observa seudoneurisma coronario (cabezas de flecha). F) Inyección final en proyección en OAD con caudo donde se muestra flujo coronario TIMI-III con sellado total de la zona seudoaneurismática.](https://static.elsevier.es/multimedia/02149168/0000002700000006/v1_201511100033/S0214916815000364/v1_201511100033/es/main.assets/thumbnail/gr2.jpeg?xkr=ue/ImdikoIMrsJoerZ+w96p5LBcBpyJTqfwgorxm+Ow=)